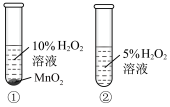
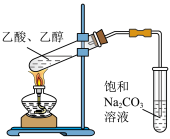
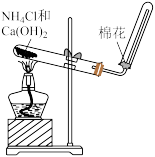
1 . 下列装置及操作能达到实验目的的是
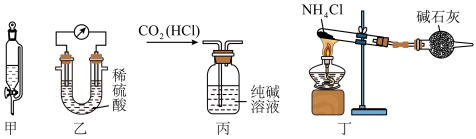
| A.利用甲装置用四氯化碳萃取碘水中的碘 | B.利用乙装置验证金属镁、铝的活泼性 |
C.利用丙装置除去 气体中混有的少量HCl 气体中混有的少量HCl | D.利用丁装置制备少量 |
您最近一年使用:0次
名校
解题方法
2 . 三氯化磷(PCl3)是一种重要的有机合成催化剂。实验室常用红磷与干燥的Cl2制取PCl3,装置如下图所示。
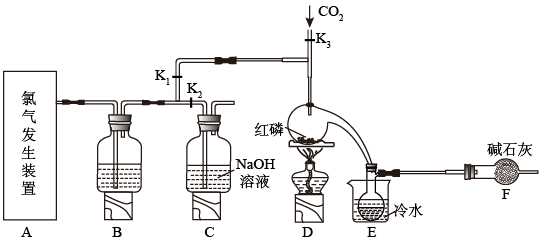
已知:红磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5。PCl3遇O2会生成POCl3(三氯氧磷),POCl3溶于PCl3,PCl3遇水会强烈水解生成H3PO3和HCl。PCl3、POCl3的熔沸点见下表。
请答下面问题:
(1)B中所装试剂是______ ,F中碱石灰的作用是_______ 。
(2)实验时,检查装置气密性后,向D装置的曲颈甑中加入红磷,打开K3通入干燥的CO2,一段时间后,关闭K 3,加热曲颈甑至上部有黄色升华物出现时通入氯气,反应立即进行。通干燥CO2的作用是___________ ;
(3)实验制得的粗产品中常含有POCl3、PCl5等。加入红磷加热除去PCl5后,通过_____ (填实验操作名称),即可得到较纯净的PCl 3。
(4)C装置中的K1、K2的设计也出于类似的目的,为了达到这一实验目的,实验时与K1、K2有关的操作是___________ 。
(5)实验后期关闭K1,打开K2,将气体通入C装置中发生反应,反应后的溶液为X。某同学设计实验来确定溶液X中含有的某些离子,请补充完成实验步骤和现象。

已知:红磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5。PCl3遇O2会生成POCl3(三氯氧磷),POCl3溶于PCl3,PCl3遇水会强烈水解生成H3PO3和HCl。PCl3、POCl3的熔沸点见下表。
| 物质 | 熔点/℃ | 沸点/℃ |
| 的PCl 3 | -112 | 75.5 |
| 三氯氧磷3 | 2 | 105.3 |
(1)B中所装试剂是
(2)实验时,检查装置气密性后,向D装置的曲颈甑中加入红磷,打开K3通入干燥的CO2,一段时间后,关闭K 3,加热曲颈甑至上部有黄色升华物出现时通入氯气,反应立即进行。通干燥CO2的作用是
(3)实验制得的粗产品中常含有POCl3、PCl5等。加入红磷加热除去PCl5后,通过
(4)C装置中的K1、K2的设计也出于类似的目的,为了达到这一实验目的,实验时与K1、K2有关的操作是
(5)实验后期关闭K1,打开K2,将气体通入C装置中发生反应,反应后的溶液为X。某同学设计实验来确定溶液X中含有的某些离子,请补充完成实验步骤和现象。
| 实验步骤 | 实验现象 | 实验结论 |
| ① | 溶液X中含有Na+ | |
| ② | 溶液X中含有Cl- |
您最近一年使用:0次
名校
3 . 用下列仪器或装置进行相应实验,可以达到实验目的的是
|
|
| A.证明MnO2是H2O2分解的催化剂 | B.制备并收集乙酸乙酯 |
|
|
| C.收集NO2气体 | D.实验室制NH3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-07-12更新
|
368次组卷
|
4卷引用: 青海省西宁市2022-2023学年高一下学期期末考试化学试题
解题方法
4 . 用下列实验装置(部分夹持装置略去),能达到实验目的的是
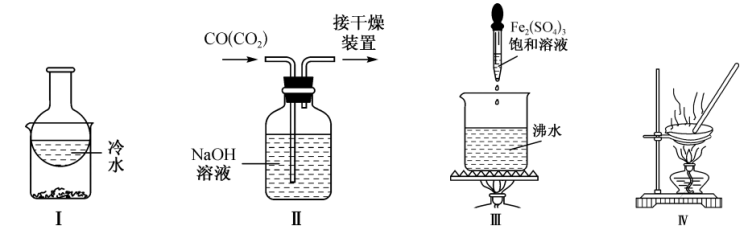

| A.加热装置I中的烧杯,分离I2和高锰酸钾固体 |
| B.利用装置II除去CO中的CO2 |
| C.利用装置III制备Fe(OH)3胶体 |
| D.利用装置IV蒸干AlCl3溶液制无水AlCl3固体 |
您最近一年使用:0次
名校
解题方法
5 . 利用下列装置进行实验(夹持仪器已省略),能达到实验目的的是
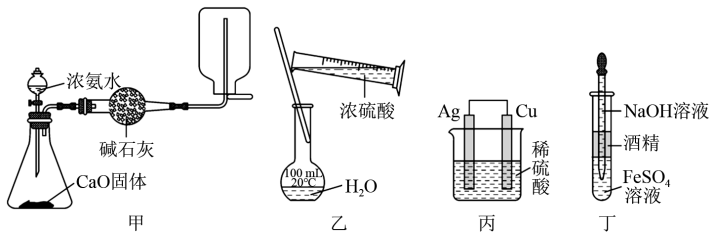

| A.图甲制取并收集干燥纯净的NH3 |
| B.图乙用于配制100mL一定浓度H2SO4溶液 |
| C.用图丙装置实现Cu+H2SO4=CuSO4+H2↑ |
| D.用图丁装置制备Fe(OH)2并能较长时间观察到白色 |
您最近一年使用:0次
2021-07-13更新
|
647次组卷
|
4卷引用:青海省西宁市大通回族土族自治县2021届高三下学期高考二模化学试题
青海省西宁市大通回族土族自治县2021届高三下学期高考二模化学试题安徽省六安市第一中学2022届高三第二次月考化学试题(已下线)2020年山东卷化学高考真题变式题1-10(已下线)微专题14 氢氧化亚铁、高铁酸盐的制备实验探究-备战2023年高考化学一轮复习考点微专题
解题方法
6 . 下列装置不能达到实验目的的是
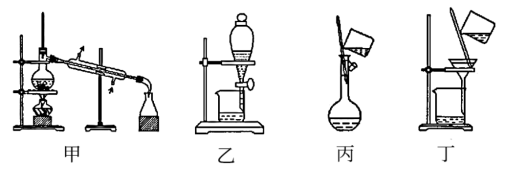

| A.图甲用于制备蒸馏水 |
| B.图乙用于分离苯和水 |
| C.图丙用于配制一定物质的量浓度的溶液 |
| D.图丁用于分离硫酸铜溶液和氢氧化铁胶体 |
您最近一年使用:0次
2021-01-30更新
|
51次组卷
|
2卷引用:青海省海东市2020-2021学年高一上学期期末考试化学试题
名校
解题方法
7 . 下列装置或操作能达到实验目的的是( )






| A.装置甲可用于实验室制备乙烯 |
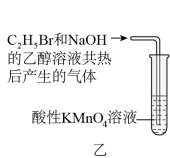
B.操作乙可用于检验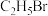 与 与 的乙醇溶液反应生成的气体中含有乙烯 的乙醇溶液反应生成的气体中含有乙烯 |
| C.操作丙可用于比较乙醇中羟基的氢原子和水分子中氢原子的活泼性 |
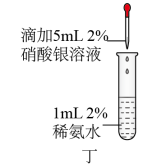
| D.操作丁可用于配制银氨溶液 |
您最近一年使用:0次
2020-07-15更新
|
177次组卷
|
5卷引用:青海省海东市2019-2020学年高二下学期期末联考化学试题
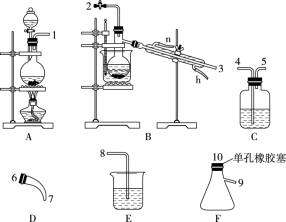
8 . 氯气用于自来水的杀菌消毒,但在消毒时会产生一些负面影响,因此人们开始研究一些新型自来水消毒剂。某学习小组查阅资料发现NCl3可作为杀菌消毒剂,该小组利用如图所示的装置制备NCl3,并探究NCl3的漂白性。NCl3的相关性质如下:
回答下列问题:
(1)根据实验目的,接口连接的顺序为1-________ -________ -2-3-6-7-________ -________ -____ 。
(2)C装置中盛放的试剂为饱和食盐水,E装置中盛放的试剂为____________________ 。
(3)A装置中发生反应的离子方程式为_________________________________________ 。
(4)B装置中发生反应的化学方程式为___________________________________ ,当B装置蒸馏烧瓶中出现较多油状液体后,关闭接口2处的活塞,控制水浴加热的温度为 __________________ 。
(5)当E装置的锥形瓶内有黄色油状液体出现时,用干燥、洁净的玻璃棒蘸取该液体滴到干燥的红色石蕊试纸上,不褪色;若取该液体滴入热水中,片刻后取该热水再滴到干燥的红色石蕊试纸上,先变蓝后褪色,结合反应方程式解释该现象:_____________________________________________________________ 。
| 物理性质 | 制备原理 | 化学性质 |
| 黄色油状液体,熔点为-40 ℃,沸点为 71 ℃,不溶于冷水,易溶于有机溶剂,密度为 1.65 g·mL-1 | Cl2与NH4Cl水溶液在低温下反应 | 95 ℃ 爆炸,热水中发生水解 |
回答下列问题:
(1)根据实验目的,接口连接的顺序为1-
(2)C装置中盛放的试剂为饱和食盐水,E装置中盛放的试剂为
(3)A装置中发生反应的离子方程式为
(4)B装置中发生反应的化学方程式为
(5)当E装置的锥形瓶内有黄色油状液体出现时,用干燥、洁净的玻璃棒蘸取该液体滴到干燥的红色石蕊试纸上,不褪色;若取该液体滴入热水中,片刻后取该热水再滴到干燥的红色石蕊试纸上,先变蓝后褪色,结合反应方程式解释该现象:
您最近一年使用:0次
9 . 实验室用白磷和浓硝酸反应制备磷酸并探究产物的性质,装置如图所示。回答下列问题:
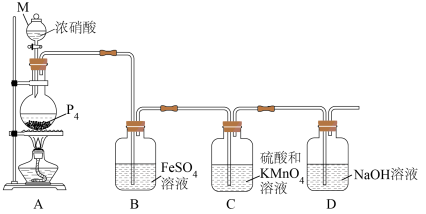
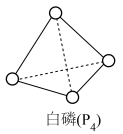
(1)白磷呈正四面体形结构(如图), 含
含_____  共价键;实验室中少量
共价键;实验室中少量 保存在
保存在________ 。
(2)仪器 的名称是
的名称是_________ ,仪器 在使用前应该先
在使用前应该先_________ 。
(3)已知 和浓硝酸反应生成
和浓硝酸反应生成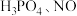 和
和 ,经检测产物中
,经检测产物中 和
和 的物质的量之比为
的物质的量之比为 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(4) 装置中溶液褪色,氧化产物的阴离子为
装置中溶液褪色,氧化产物的阴离子为 ,写出
,写出 装置中发生反应的离子方程式:
装置中发生反应的离子方程式:________ 。
(5) 不能与
不能与 溶液反应,利用
溶液反应,利用 装置吸收尾气中的
装置吸收尾气中的 时,需要同时通入某种模拟空气
时,需要同时通入某种模拟空气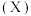 。若
。若 恰好完全被吸收,且氧化产物只有
恰好完全被吸收,且氧化产物只有 ,则同温同压下,
,则同温同压下,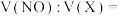
______ 。(设该模拟空气中氧气的体积分数为 )
)
(6)探究 装置中溶液呈棕黄色的原因,一课题小组提出如下猜想:
装置中溶液呈棕黄色的原因,一课题小组提出如下猜想:
猜想1:存在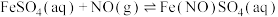 (棕黄色);
(棕黄色);
猜想2:生成了 。
。
针对猜想2设计实验:_________ (写出步骤、现象),猜想2成立。

(1)白磷呈正四面体形结构(如图),
 含
含 共价键;实验室中少量
共价键;实验室中少量 保存在
保存在
(2)仪器
 的名称是
的名称是 在使用前应该先
在使用前应该先(3)已知
 和浓硝酸反应生成
和浓硝酸反应生成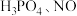 和
和 ,经检测产物中
,经检测产物中 和
和 的物质的量之比为
的物质的量之比为 ,该反应的化学方程式为
,该反应的化学方程式为(4)
 装置中溶液褪色,氧化产物的阴离子为
装置中溶液褪色,氧化产物的阴离子为 ,写出
,写出 装置中发生反应的离子方程式:
装置中发生反应的离子方程式:(5)
 不能与
不能与 溶液反应,利用
溶液反应,利用 装置吸收尾气中的
装置吸收尾气中的 时,需要同时通入某种模拟空气
时,需要同时通入某种模拟空气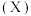 。若
。若 恰好完全被吸收,且氧化产物只有
恰好完全被吸收,且氧化产物只有 ,则同温同压下,
,则同温同压下,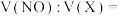
 )
)(6)探究
 装置中溶液呈棕黄色的原因,一课题小组提出如下猜想:
装置中溶液呈棕黄色的原因,一课题小组提出如下猜想:猜想1:存在
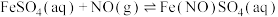 (棕黄色);
(棕黄色);猜想2:生成了
 。
。针对猜想2设计实验:
您最近一年使用:0次
10 . 三草酸合铁酸钾晶体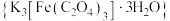 为翠绿色的晶体,易溶于水,难溶于乙醇,是一种重要的光敏材料和有机催化剂。某化学兴趣小组设计如下实验对
为翠绿色的晶体,易溶于水,难溶于乙醇,是一种重要的光敏材料和有机催化剂。某化学兴趣小组设计如下实验对 进行探究。
进行探究。
请回答下列问题:
I. 的制备
的制备
主要试剂为 、
、 溶液、
溶液、 饱和溶液、
饱和溶液、 饱和溶液、
饱和溶液、 溶液、
溶液、 乙醇。经过下列三步合成:
乙醇。经过下列三步合成:
沉淀:
氧化配位: (过量)
(过量) (未配平)
(未配平)
酸溶配位: (未配平)
(未配平)
(1)配平“酸溶配位”中制备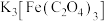 反应的化学方程式:
反应的化学方程式:_____ 。
(2)制备过程中乙醇的作用是_____ 。分离出晶体时需减压抽滤,装置如图所示,抽滤的优点是_____ ;抽滤完毕需进行下列操作,从实验安全角度考虑,你认为接下来最合理的第一步操作为_____ (填标号)。
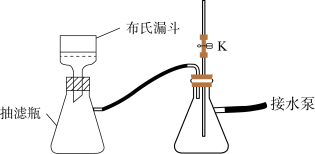
①取下布氏漏斗②关闭水泵开关③打开活塞K④拔下抽滤瓶处橡皮管
Ⅱ.探究 热分解的气体产物组成
热分解的气体产物组成
(3)某研究小组将 在一定条件下加热分解,利用如图装置(可重复使用)验证所得气体产物中含有
在一定条件下加热分解,利用如图装置(可重复使用)验证所得气体产物中含有 和
和 。
。
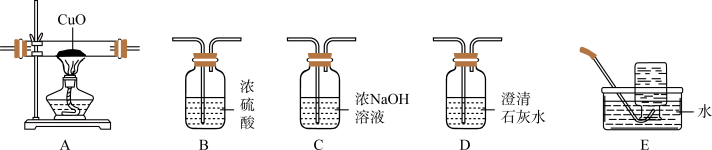
①按气流从左到右的方向,合理的装置连接顺序为_____ 。
_____→_____→D→B→_____→D→E(填装置标号,装置可重复使用)。
②当观察到第一个D装置中出现浑浊现象时,确认气体产物中含有_____ (填化学式);当观察到A装置中有红色固体物质生成且_____ 时,确认气体产物中含有CO。
Ⅲ.阴离子所带电荷数目的测定
(4)测定晶体中阴离子所带电荷数目可以利用离子交换法,步骤如下:
步骤1:准确称取一定质量晶体,完全溶解于一定量水中。
步骤2:使溶液通过阴离子交换柱,并用蒸馏水冲洗交换柱,收集所有过柱液体。{已知离子交换反应: }
}
步骤3:以甲基橙为指示剂,用盐酸标准溶液滴定过柱液体至终点。
①滴定终点的现象为_____ 。
②步骤2中未用蒸馏水冲洗交换柱,则对测得阴离子所带电荷数目的影响是_____ (填“偏大”“偏小”或“无影响”)。
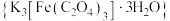 为翠绿色的晶体,易溶于水,难溶于乙醇,是一种重要的光敏材料和有机催化剂。某化学兴趣小组设计如下实验对
为翠绿色的晶体,易溶于水,难溶于乙醇,是一种重要的光敏材料和有机催化剂。某化学兴趣小组设计如下实验对 进行探究。
进行探究。请回答下列问题:
I.
 的制备
的制备主要试剂为
 、
、 溶液、
溶液、 饱和溶液、
饱和溶液、 饱和溶液、
饱和溶液、 溶液、
溶液、 乙醇。经过下列三步合成:
乙醇。经过下列三步合成:沉淀:

氧化配位:
 (过量)
(过量) (未配平)
(未配平)酸溶配位:
 (未配平)
(未配平)(1)配平“酸溶配位”中制备
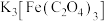 反应的化学方程式:
反应的化学方程式:(2)制备过程中乙醇的作用是

①取下布氏漏斗②关闭水泵开关③打开活塞K④拔下抽滤瓶处橡皮管
Ⅱ.探究
 热分解的气体产物组成
热分解的气体产物组成(3)某研究小组将
 在一定条件下加热分解,利用如图装置(可重复使用)验证所得气体产物中含有
在一定条件下加热分解,利用如图装置(可重复使用)验证所得气体产物中含有 和
和 。
。
①按气流从左到右的方向,合理的装置连接顺序为
_____→_____→D→B→_____→D→E(填装置标号,装置可重复使用)。
②当观察到第一个D装置中出现浑浊现象时,确认气体产物中含有
Ⅲ.阴离子所带电荷数目的测定
(4)测定晶体中阴离子所带电荷数目可以利用离子交换法,步骤如下:
步骤1:准确称取一定质量晶体,完全溶解于一定量水中。
步骤2:使溶液通过阴离子交换柱,并用蒸馏水冲洗交换柱,收集所有过柱液体。{已知离子交换反应:
 }
}步骤3:以甲基橙为指示剂,用盐酸标准溶液滴定过柱液体至终点。
①滴定终点的现象为
②步骤2中未用蒸馏水冲洗交换柱,则对测得阴离子所带电荷数目的影响是
您最近一年使用:0次