名校
解题方法
1 . 氯元素可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备 (
( 与KOH溶液加热条件下制得)和NaClO,并探究其氧化、还原性质。
与KOH溶液加热条件下制得)和NaClO,并探究其氧化、还原性质。
(1)盛放 粉末的仪器名称是
粉末的仪器名称是______ ,a中的试剂为_______ 。
(2)b中采用的加热方式是_______ ,c中化学反应的离子方程式是_____ ,采用冰水浴冷却的目的是_____ 。
(3)d的作用是____ ,可选用试剂____ (填标号)。
A. B.NaCl C.NaOH D.
B.NaCl C.NaOH D.
(4)反应结束后,取出b中试管,经冷却结晶,_______ ,______ ,干燥,得到 晶体。
晶体。
(5)取少量 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显
层显____ 色。可知该条件下 的氧化能力
的氧化能力_____ NaClO(填“大于”或“小于”)。
 (
( 与KOH溶液加热条件下制得)和NaClO,并探究其氧化、还原性质。
与KOH溶液加热条件下制得)和NaClO,并探究其氧化、还原性质。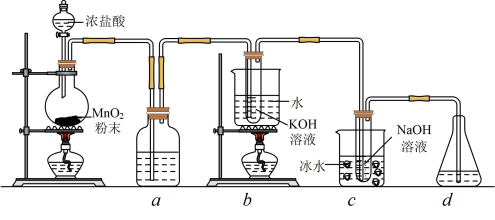
(1)盛放
 粉末的仪器名称是
粉末的仪器名称是(2)b中采用的加热方式是
(3)d的作用是
A.
 B.NaCl C.NaOH D.
B.NaCl C.NaOH D.
(4)反应结束后,取出b中试管,经冷却结晶,
 晶体。
晶体。(5)取少量
 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显
层显 的氧化能力
的氧化能力
您最近一年使用:0次
名校
解题方法
2 . 硫酸铁铵[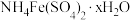 ]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:下列各项说法错误的是
]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:下列各项说法错误的是
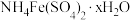 ]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:下列各项说法错误的是
]是一种重要铁盐。为充分利用资源,变废为宝,在实验室中探究采用废铁屑来制备硫酸铁铵,具体流程如下:下列各项说法错误的是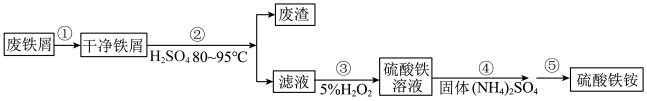
| A.①为去油污,可采用稀碱液浸泡、清水淋洗方式除去 |
| B.②为浸泡并过滤,过程中保持溶液温度80—95℃有利于提高浸取效率,得到较高浓度硫酸亚铁溶液 |
| C.④⑤过程中包含了蒸发浓缩、冷却结晶、洗涤、晾干等步骤 |
D.③中可改用 氧化二价铁离子 氧化二价铁离子 |
您最近一年使用:0次
3 . 藿香蓟具有清热解毒功效,其有效成分结构如下。下列有关该物质的说法错误的是

| A.可以和NaOH溶液发生反应 | B.有四种不同的官能团 |
| C.可以使酸性高锰酸钾溶液和溴水褪色 | D.分子中所有碳原子不可能共面 |
您最近一年使用:0次
名校
解题方法
4 . 主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。W、X、Y最外层电子数之和为11,W与Y同族且都是复合化肥的营养元素,Z的氢化物遇水可产生最轻的气体。下列说法正确的是
| A.X的氧化物所含化学键类型相同 |
| B.Y和W最高价氧化物水化物的酸性:Y>W |
| C.Z的金属性比X弱 |
| D.简单离子半径最大的是Y |
您最近一年使用:0次
5 .  为阿伏伽德罗常数的值。下列叙述正确的是
为阿伏伽德罗常数的值。下列叙述正确的是
 为阿伏伽德罗常数的值。下列叙述正确的是
为阿伏伽德罗常数的值。下列叙述正确的是A.16g 和 和 的混合物含有的电子数一定是8 的混合物含有的电子数一定是8 |
B.48g正丁烷和10g异丁烷的混合物中共价键数目为12 |
C.标准状况下22.4L甲烷与 发生取代反应,生成的 发生取代反应,生成的 分子数一定是 分子数一定是 |
D.0.1mol 和0.1mol 和0.1mol 于密闭容器中充分反应后,容器中的分子总数小于0.2 于密闭容器中充分反应后,容器中的分子总数小于0.2 |
您最近一年使用:0次
6 . 化学与生产、生活和社会发展密切相关,下列叙述正确的是
| A.“雷雨发庄稼”说明有铵盐生成 |
| B.宣纸的主要成分是一种天然的高分子化合物 |
| C.太阳能电池与原电池的原理相同 |
D. 可以作止血剂是因为 可以作止血剂是因为 具有较强的氧化性 具有较强的氧化性 |
您最近一年使用:0次
7 .  为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.标准状况下,2.24L 或2.24LHF含有的分子数都大于0.1 或2.24LHF含有的分子数都大于0.1 |
| B.0.1mol/L的NaOH溶液中氢原子数和氧原子数相等 |
C.标准状况下,2.24L 与1.12L 与1.12L 充分反应,生成2.24L 充分反应,生成2.24L 分子 分子 |
D.0.1mol/L的NaCl溶液中 的浓度为0.1mol/L 的浓度为0.1mol/L |
您最近一年使用:0次
名校
解题方法
8 . 下列反应的离子方程式或电离方程式正确的是
A. 溶液中加足量 溶液中加足量 溶液: 溶液: |
B.用 溶液吸收 溶液吸收 制石膏乳( 制石膏乳( ): ): |
C.向 溶液中通入 溶液中通入 : :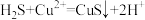 |
D.向澄清石灰水中滴加足量的碳酸氢钠溶液: |
您最近一年使用:0次
名校
解题方法
9 . 化学与生活、科技、社会发展息息相关。下列有关说法正确的是
| A.侯氏制碱法生产纯碱的主要原料有:氯化钠、氨气、二氧化碳、水 |
| B.医疗上采用75%的酒精溶液消毒,而不使用95%的工业酒精目的是节约酒精,降低成本,增加经济效益 |
| C.氢氟酸(HF)可腐蚀玻璃,只能用陶瓷试剂瓶盛装 |
| D.试管上附着的硫单质不溶于水,但可用酒精洗涤 |
您最近一年使用:0次
解题方法
10 . (一)某研究性学习小组为探究 Fe3+与 Ag 反应,进行如下实验:按下图连接装置并加入药品(盐桥中的物质不参与反应)。_______________ (填“正极”或“负极”)。
(2)盐桥中装有含有 KNO3饱和溶液的琼脂,K 闭合时,K+移向_______________ 溶液。
(3)结合上述实验,写出本原电池装置的负极反应:_______________ 。
(二)某研究性学习小组利用草酸(H2C2O4)溶液和酸性 KMnO4溶液之间的反应
来探究“外界条件改变对化学反应速率的影响”,实验设计如下:(假设溶液混合
时体积可以加和)
(4)写出草酸与酸性 KMnO4溶液反应的离子方程式:_______ 。
(5)乙同学欲通过实验①、②探究反应物浓度对该反应速率的影响,则a=_______ ,T=_______ 。若 t1<8 s,可以得出的结论是:_______ 。
(6)通过比较实验②、③的结果,可以探究_______ 变化对化学反应速率的影响。
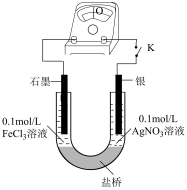
(2)盐桥中装有含有 KNO3饱和溶液的琼脂,K 闭合时,K+移向
(3)结合上述实验,写出本原电池装置的负极反应:
(二)某研究性学习小组利用草酸(H2C2O4)溶液和酸性 KMnO4溶液之间的反应
来探究“外界条件改变对化学反应速率的影响”,实验设计如下:(假设溶液混合
时体积可以加和)
| 实验序号 | 实验温度(K) | 酸性KMnO4溶液 | 草酸溶液 | 蒸馏水 | 褪色时间 | ||
| c(mol/L) | V(mL) | c(mol/L) | V(mL) | V(mL) | t(s) | ||
| ① | 298 | 0.02 | 2.0 | 0.10 | 4.0 | 0 | t1 |
| ② | T | 0.02 | 2.0 | 0.10 | 3.0 | a | 8.0 |
| ③ | 343 | 0.02 | 2.0 | 0.10 | 3.0 | a | t2 |
| ④ | 373 | 0.02 | 2.0 | 0.10 | 3.0 | a | t3 |
(4)写出草酸与酸性 KMnO4溶液反应的离子方程式:
(5)乙同学欲通过实验①、②探究反应物浓度对该反应速率的影响,则a=
(6)通过比较实验②、③的结果,可以探究
您最近一年使用:0次



