名校
1 . 几种含硫物质的转化如下图(部分反应条件略去),下列判断不正确的是
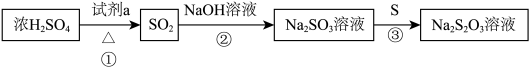
| A.①中,试剂a可以是Na2SO3固体 |
| B.②中,需要确保NaOH溶液足量,否则将得到NaHSO3溶液 |
C.③中,将S换为 ,氧化产物为 ,氧化产物为 |
D.③中,生成1mol  时,转移4mol电子 时,转移4mol电子 |
您最近一年使用:0次
昨日更新
|
52次组卷
|
2卷引用:云南省泸西县第一中学2023-2024学年高一下学期期中考试化学试题
名校
2 . 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.0.1mol/L  溶液中含有的 溶液中含有的 数目为0.1 数目为0.1 |
B.1mol  与足量 与足量 反应时,转移电子数为 反应时,转移电子数为 |
C.1 个 个 分子占有的体积为22.4L 分子占有的体积为22.4L |
D.20g 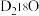 含有的中子数目为10 含有的中子数目为10 |
您最近一年使用:0次
名校
解题方法
3 . 下列实验中物质的颜色变化与氧化还原反应无关的是
| A.苯酚空气中显粉红色 |
B.向 酸性溶液中加入乙醇,溶液由橙色变为绿色 酸性溶液中加入乙醇,溶液由橙色变为绿色 |
| C.向AgCl悬浊液中滴加KI溶液,固体由白色变为黄色 |
D.向新制的 中加入乙醛溶液,加热,有砖红色沉淀生成 中加入乙醛溶液,加热,有砖红色沉淀生成 |
您最近一年使用:0次
名校
4 . 下列除去杂质的实验方法正确的是
A.除去 中的少量HCl:通过饱和 中的少量HCl:通过饱和 溶液,收集气体 溶液,收集气体 |
B.除去NaCl溶液中少量 :加入过量 :加入过量 ,过滤 ,过滤 |
| C.铁粉(铝粉):加入过量的烧碱溶液,过滤、洗涤、干燥 |
D. 固体( 固体( 固体):加热 固体):加热 |
您最近一年使用:0次
名校
解题方法
5 . 下列实验操作、现象与结论的对应关系均正确的是
| 选项 | 实验操作 | 实验现象与结论 |
| A | 常温下,将铁片浸入足量浓硫酸中 | 铁片不溶解,常温下,铁与浓硫酸一定没有发生化学反应 |
| B | 向样品溶液中先滴加过量的稀硝酸,再滴加 溶液 溶液 | 滴加稀硝酸无现象,滴加 溶液后出现白色沉淀,说明样品溶液中一定含有 溶液后出现白色沉淀,说明样品溶液中一定含有 |
| C | 将氯气通入淀粉碘化钾溶液中,溶液由无色变为蓝色 | 氯气的氧化性强于碘单质 |
| D | 某溶液先加KSCN溶液无现象,再通氯气溶液变为血红色 | 该溶液中一定含有 , , |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 下列指定反应的离子方程式书写正确的是
A.向 溶液中通入 溶液中通入 气体出现白色沉淀: 气体出现白色沉淀: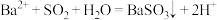 |
B.过氧化钠与水反应: |
C.室温下用稀 溶解铜: 溶解铜: |
D.向饱和 溶液中通入足量 溶液中通入足量 : : |
您最近一年使用:0次
名校
7 . 下列化学用语表述错误的是
A.基态铜原子价层电子的轨道表示式: |
B.中子数为10的氧原子: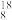 O O |
| C.NH3分子的空间结构为三角锥形 |
D.基态N原子的价层电子排布图: |
您最近一年使用:0次
名校
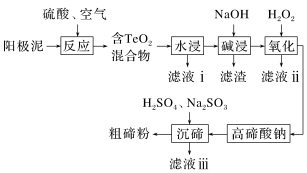
8 . 碲(Te)广泛应用于冶金、航空航天、电子等领域。从精炼钢的阳极泥(主要成分为Cu2Te,还含有金、银、铂等)中回收碲的工艺流程如图:
(1)为提高“反应”效率,可采取的措施为_______ (任答一条)。
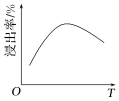
(2)滤液i的主要成分是_______ (写化学式)。滤液i中溶质的浸出率与温度的关系如图所示,解释浸出率随温度变化的可能原因_______ 。_______ 。滤液ii可循环使用,应将其导入到_______ (写操作单元名称)操作中。
(4)“沉碲”过程中发生反应的化学方程式为_______ 。
(5)粗碲粉中碲质量分数的测定步骤如下:取mg粗碲粉,加入酸使其转化为亚碲酸(H2TeO3),配制成100mL溶液,取25.00mL于锥形瓶中。向锥形瓶中加入V1mLc1mol•L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为碲酸(H6TeO6)。用c2mol•L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]标准溶液滴定剩余的酸性K2Cr2O7溶液,消耗V2mL硫酸亚铁铵标准溶液。该粗碲粉中碲的质量分数为_______ 。
(1)为提高“反应”效率,可采取的措施为
(2)滤液i的主要成分是
(4)“沉碲”过程中发生反应的化学方程式为
(5)粗碲粉中碲质量分数的测定步骤如下:取mg粗碲粉,加入酸使其转化为亚碲酸(H2TeO3),配制成100mL溶液,取25.00mL于锥形瓶中。向锥形瓶中加入V1mLc1mol•L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为碲酸(H6TeO6)。用c2mol•L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]标准溶液滴定剩余的酸性K2Cr2O7溶液,消耗V2mL硫酸亚铁铵标准溶液。该粗碲粉中碲的质量分数为
您最近一年使用:0次
名校
9 . I.某化学自主实验小组利用如图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。_______ 。E装置发生的化学反应方程式为________ 。
(2)甲、乙分别是___________ (填标号)。
a.硫酸、浓硫酸 b.碱石灰、无水氯化钙
c.碱石灰、碱石灰 d.五氧化二磷、五氧化二磷
(3)若NO2能够被NH3还原,写出发生反应的化学方程式:___________ 。
(4)此实验装置存在一个明显的缺陷是___________ 。
(5)NH3分子中的一个氢原子被羟基(-OH)取代后生成的物质为羟胺,羟胺的性质与氨气相似。请写出羟胺与HCl反应的化学方程式:___________ 。
II.硫酸可用于生产化肥、农药、炸药、染料和盐类等。工业生产硫酸的流程图如下:_________ 。
(7)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨,请写出硫酸工业吸收尾气的离子方程式___________ 。
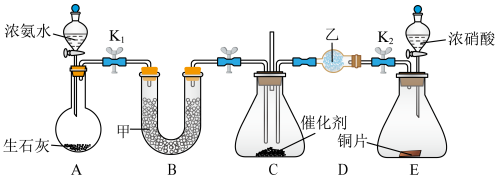
(2)甲、乙分别是
a.硫酸、浓硫酸 b.碱石灰、无水氯化钙
c.碱石灰、碱石灰 d.五氧化二磷、五氧化二磷
(3)若NO2能够被NH3还原,写出发生反应的化学方程式:
(4)此实验装置存在一个明显的缺陷是
(5)NH3分子中的一个氢原子被羟基(-OH)取代后生成的物质为羟胺,羟胺的性质与氨气相似。请写出羟胺与HCl反应的化学方程式:
II.硫酸可用于生产化肥、农药、炸药、染料和盐类等。工业生产硫酸的流程图如下:
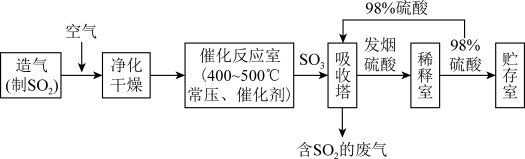
(7)硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨,请写出硫酸工业吸收尾气的离子方程式
您最近一年使用:0次
名校
10 . 在如图所示的转化关系中,A是最常见的金属单质,D是一种黄绿色的气体(图中部分产物和反应条件未标出)。
(1)写出下列物质的化学式:B___________ 、F___________ 。
(2)D的电子式为___________ 。
(3)写出反应⑤的离子方程式:___________ 。
(4)写出反应⑧的化学方程式:___________ 。
(5)将饱和G溶液滴加到沸水中,继续加热煮沸,得到的分散系属于___________ 。

(1)写出下列物质的化学式:B
(2)D的电子式为
(3)写出反应⑤的离子方程式:
(4)写出反应⑧的化学方程式:
(5)将饱和G溶液滴加到沸水中,继续加热煮沸,得到的分散系属于
您最近一年使用:0次



