解题方法
1 . 2023年11月23日,我国在西昌卫星发射中心使用长征二号丁运载火箭,成功将卫星互联网技术试验卫星发射升空,其中火箭推进剂的研究功不可没。
(1)火箭推进剂可用 (1)作燃料,
(1)作燃料,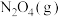 作氧化剂,
作氧化剂, (1)与
(1)与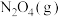 反应生成
反应生成 的热化学方程式为
的热化学方程式为___________ 。(已知:一定温度下,以元素的最稳定单质生成 纯物质的热效应为该物质的摩尔生成焓,以
纯物质的热效应为该物质的摩尔生成焓,以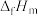 表示,单质的摩尔生成焓为
表示,单质的摩尔生成焓为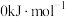 ,相关物质的摩尔生成焓如下表所示,焓变
,相关物质的摩尔生成焓如下表所示,焓变 生成物的总摩尔生成焓-反应物的总摩尔生成焓)
生成物的总摩尔生成焓-反应物的总摩尔生成焓)
(2)结合化学反应原理, (1)作推进剂燃料,(1)中反应可自发进行的原因是
(1)作推进剂燃料,(1)中反应可自发进行的原因是___________ 。
(3)氢燃料也是常用的火箭推进剂燃料,工业上可通过“一碳化学”技术实现氢气的制备,其主要涉及的反应如下。
反应Ⅰ:
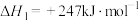
反应Ⅱ:
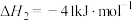
①反应Ⅰ、Ⅱ的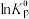 随
随 的变化如图所示(
的变化如图所示(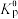 为反应的标准压强平衡常数,物质的标准压强等于物质的分压与标准压力
为反应的标准压强平衡常数,物质的标准压强等于物质的分压与标准压力 的比值)。
的比值)。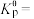
___________ (用各物质的分压 和标准压力
和标准压力 表示);图中表示反应Ⅱ的
表示);图中表示反应Ⅱ的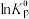 随
随 的变化的曲线为
的变化的曲线为___________ (填“a”或“b”)。
② 时,向恒容密闭容器中通入按照
时,向恒容密闭容器中通入按照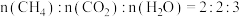 混合的气体,发生反应Ⅰ、Ⅱ,若初始时压强为
混合的气体,发生反应Ⅰ、Ⅱ,若初始时压强为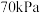 ,达到平衡时体系的压强为
,达到平衡时体系的压强为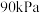 。该温度下
。该温度下 的平衡转化率为
的平衡转化率为___________ , 的平衡分压为
的平衡分压为___________ 。
③火箭推进器内氢氧燃烧的简化反应历程如下图所示。___________ 步进行,其中氢氧燃烧决速步骤对应反应的化学方程式为___________ 。
④体系中 的平衡含量随温度的变化如下图所示,请解释
的平衡含量随温度的变化如下图所示,请解释 的含量随温度变化的原因:
的含量随温度变化的原因:___________ 。
(1)火箭推进剂可用
 (1)作燃料,
(1)作燃料,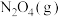 作氧化剂,
作氧化剂, (1)与
(1)与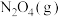 反应生成
反应生成 的热化学方程式为
的热化学方程式为 纯物质的热效应为该物质的摩尔生成焓,以
纯物质的热效应为该物质的摩尔生成焓,以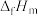 表示,单质的摩尔生成焓为
表示,单质的摩尔生成焓为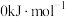 ,相关物质的摩尔生成焓如下表所示,焓变
,相关物质的摩尔生成焓如下表所示,焓变 生成物的总摩尔生成焓-反应物的总摩尔生成焓)
生成物的总摩尔生成焓-反应物的总摩尔生成焓)| 物质 | 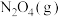 | 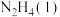 |  |
摩尔生成焓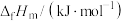 | 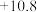 | 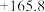 | 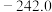 |
(2)结合化学反应原理,
 (1)作推进剂燃料,(1)中反应可自发进行的原因是
(1)作推进剂燃料,(1)中反应可自发进行的原因是(3)氢燃料也是常用的火箭推进剂燃料,工业上可通过“一碳化学”技术实现氢气的制备,其主要涉及的反应如下。
反应Ⅰ:

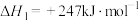
反应Ⅱ:

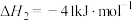
①反应Ⅰ、Ⅱ的
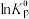 随
随 的变化如图所示(
的变化如图所示(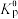 为反应的标准压强平衡常数,物质的标准压强等于物质的分压与标准压力
为反应的标准压强平衡常数,物质的标准压强等于物质的分压与标准压力 的比值)。
的比值)。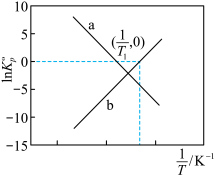
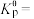
 和标准压力
和标准压力 表示);图中表示反应Ⅱ的
表示);图中表示反应Ⅱ的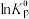 随
随 的变化的曲线为
的变化的曲线为②
 时,向恒容密闭容器中通入按照
时,向恒容密闭容器中通入按照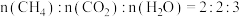 混合的气体,发生反应Ⅰ、Ⅱ,若初始时压强为
混合的气体,发生反应Ⅰ、Ⅱ,若初始时压强为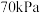 ,达到平衡时体系的压强为
,达到平衡时体系的压强为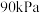 。该温度下
。该温度下 的平衡转化率为
的平衡转化率为 的平衡分压为
的平衡分压为③火箭推进器内氢氧燃烧的简化反应历程如下图所示。
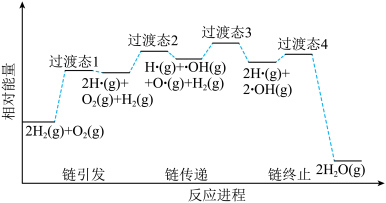
④体系中
 的平衡含量随温度的变化如下图所示,请解释
的平衡含量随温度的变化如下图所示,请解释 的含量随温度变化的原因:
的含量随温度变化的原因: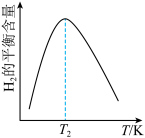
您最近一年使用:0次
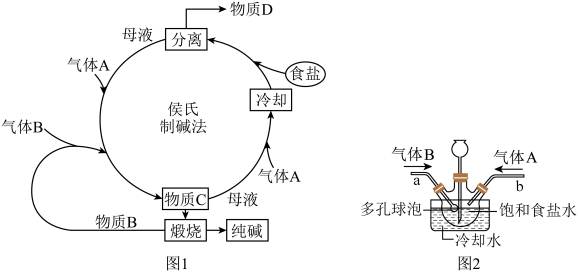
2 . 侯氏制碱法为世界制碱技术谱写了新的篇章。某实验小组模拟侯氏制碱法,其实验流程如图1所示,实验装置如图2所示。 为
为___________ ,物质D为___________ ,a导管末端多孔球泡的作用是___________ 。
(2)侯德榜制碱法的原理是___________ (用化学方程式表示)。
(3)“冷却”后又加入食盐细粉的目的是___________ 。
(4)产品杂质含量的测定。若搬烧时间短,纯碱产品中常含有 杂质,实验小组通过滴定法确定产品的纯度。
杂质,实验小组通过滴定法确定产品的纯度。
ⅰ.称取 产品,用蒸馏水溶解,定容于
产品,用蒸馏水溶解,定容于 容量瓶中;
容量瓶中;
ⅱ.移取 上述溶液于锥形瓶中,用
上述溶液于锥形瓶中,用 盐酸标准溶液滴定,溶液
盐酸标准溶液滴定,溶液 随滴加
随滴加 溶液体积变化关系如图所示(混合后溶液体积变化忽略不计)。
溶液体积变化关系如图所示(混合后溶液体积变化忽略不计)。 的质量分数为
的质量分数为___________ ;若产品中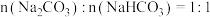 ,则溶液中离子浓度大小顺序为
,则溶液中离子浓度大小顺序为___________ 。
②若分别用酚酞、甲基橙作指示剂,到达第二滴定终点时的现象是___________ 。第一滴定终点时,某同学仰视读数,其他操作均正确,则 的质量分数的计算结果
的质量分数的计算结果___________ (填“偏大”“偏小”或“无影响”)。
(5)通过电解纯碱溶液可制得 和
和 ,其电解装置如图所示。
,其电解装置如图所示。 为
为___________ 极,离子交换膜为膜___________ (填“阴”或“阳”)。
(2)制备 的原理为
的原理为___________ (用电极反应式表示)。
 为
为(2)侯德榜制碱法的原理是
(3)“冷却”后又加入食盐细粉的目的是
(4)产品杂质含量的测定。若搬烧时间短,纯碱产品中常含有
 杂质,实验小组通过滴定法确定产品的纯度。
杂质,实验小组通过滴定法确定产品的纯度。ⅰ.称取
 产品,用蒸馏水溶解,定容于
产品,用蒸馏水溶解,定容于 容量瓶中;
容量瓶中;ⅱ.移取
 上述溶液于锥形瓶中,用
上述溶液于锥形瓶中,用 盐酸标准溶液滴定,溶液
盐酸标准溶液滴定,溶液 随滴加
随滴加 溶液体积变化关系如图所示(混合后溶液体积变化忽略不计)。
溶液体积变化关系如图所示(混合后溶液体积变化忽略不计)。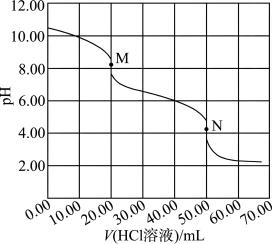
 的质量分数为
的质量分数为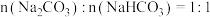 ,则溶液中离子浓度大小顺序为
,则溶液中离子浓度大小顺序为②若分别用酚酞、甲基橙作指示剂,到达第二滴定终点时的现象是
 的质量分数的计算结果
的质量分数的计算结果(5)通过电解纯碱溶液可制得
 和
和 ,其电解装置如图所示。
,其电解装置如图所示。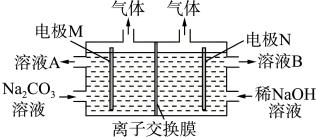
 为
为(2)制备
 的原理为
的原理为
您最近一年使用:0次
3 . 铬、钥在工业生产中具有重要的应用,从红铬矿渣(主要含有 和
和 ,还含有少量铁、铝、硅等氧化物)中分离提取铬和钒的一种流程如图所示:
,还含有少量铁、铝、硅等氧化物)中分离提取铬和钒的一种流程如图所示: 范围如下表。
范围如下表。
回答下列问题:
(1)“焙烧”前需要研磨的目的是___________ ,若焙烧后铬与钒均生成其最高价含氧酸盐,请写出 焙烧生成
焙烧生成 的化学方程式:
的化学方程式:___________ 。
(2)“溶浸渣”的主要成分是___________ (写化学式),第一次“调 ”的范围为
”的范围为___________ 。
(3)在实验室中模拟“除硅”后的分离操作中所用到的玻璃仪器有___________ 、___________ 和烧杯。
(4)已知焙烧后钒以 形式存在,“提取钒”步骤中,将溶液
形式存在,“提取钒”步骤中,将溶液 调到1.8左右得到
调到1.8左右得到 沉淀,该反应的离子方程式为
沉淀,该反应的离子方程式为___________ ,此时铬元素的主要存在形式为___________ 。
(5)若最终得到氢氧化铬的沉淀质量为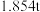 ,第三次“调
,第三次“调 ”时铬元素只有
”时铬元素只有 的沉淀分离出来,则“还原”步骤理论上转移的电子数为
的沉淀分离出来,则“还原”步骤理论上转移的电子数为___________ (设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(6)一种含钒的氧化物晶胞结构如图所示,已知 表示阿伏加德罗常数的值,则该晶体的密度为
表示阿伏加德罗常数的值,则该晶体的密度为___________  (列出计算式即可)。
(列出计算式即可)。
 和
和 ,还含有少量铁、铝、硅等氧化物)中分离提取铬和钒的一种流程如图所示:
,还含有少量铁、铝、硅等氧化物)中分离提取铬和钒的一种流程如图所示: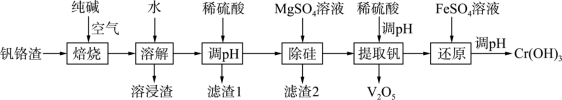
 范围如下表。
范围如下表。| 物质 |  |  |  |  |  |
开始沉淀的 | 4.6 | 7.5 | 1.9 | 4.1 |  |
完全沉淀的 | 5.9 | 9.0 | 3.2 | 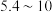 |
(1)“焙烧”前需要研磨的目的是
 焙烧生成
焙烧生成 的化学方程式:
的化学方程式:(2)“溶浸渣”的主要成分是
 ”的范围为
”的范围为(3)在实验室中模拟“除硅”后的分离操作中所用到的玻璃仪器有
(4)已知焙烧后钒以
 形式存在,“提取钒”步骤中,将溶液
形式存在,“提取钒”步骤中,将溶液 调到1.8左右得到
调到1.8左右得到 沉淀,该反应的离子方程式为
沉淀,该反应的离子方程式为(5)若最终得到氢氧化铬的沉淀质量为
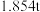 ,第三次“调
,第三次“调 ”时铬元素只有
”时铬元素只有 的沉淀分离出来,则“还原”步骤理论上转移的电子数为
的沉淀分离出来,则“还原”步骤理论上转移的电子数为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。(6)一种含钒的氧化物晶胞结构如图所示,已知
 表示阿伏加德罗常数的值,则该晶体的密度为
表示阿伏加德罗常数的值,则该晶体的密度为 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
4 . 以辉锑矿(主要成分为 ,还含有
,还含有 )为原料提取金属
)为原料提取金属 的部分流程如下图所示:
的部分流程如下图所示: ;“水解”最终产物为
;“水解”最终产物为 固体;
固体;
②难溶物的部分数值如下:
下列有关说法正确的是
 ,还含有
,还含有 )为原料提取金属
)为原料提取金属 的部分流程如下图所示:
的部分流程如下图所示: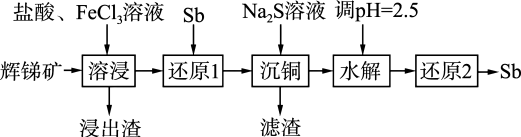
 ;“水解”最终产物为
;“水解”最终产物为 固体;
固体;②难溶物的部分数值如下:
| 物质 |  |  |  | 物质 |  |  |
开始沉淀 | 1.9 | 7.5 | 4.2 |  | 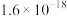 |  |
完全沉淀 | 3.2 | 9.0 | 6.7 |
A.“浸出渣”为 ,“滤渣”为 ,“滤渣”为 |
B.“还原1”发生反应的离子方程式为 |
C.“沉铜”时,若溶液中的阳离子的浓度均为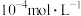 ,为保证只有铜离子沉出,则溶液中 ,为保证只有铜离子沉出,则溶液中 最大为 最大为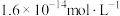 |
D.为了使“水解”时产物的纯度高,可通入 气体 气体 |
您最近一年使用:0次
5 . 下列离子方程式的书写正确的是
A.联氨 为二元弱碱,在水中的电离方式与氨相似,其一级电离方程式为: 为二元弱碱,在水中的电离方式与氨相似,其一级电离方程式为: |
B.往碳酸钡中滴加稀盐酸: |
C.实验室制备 胶体: 胶体: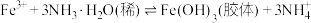 |
D. 与足量的氯气反应: 与足量的氯气反应: |
您最近一年使用:0次
6 . 下列化学用语正确的是
A.聚丙烯腈的结构简式: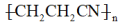 |
B. 的水解方程式: 的水解方程式: |
C.基态铬原子的价电子轨道表示式: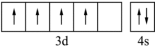 |
D.乙烯的空间填充模型: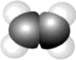 |
您最近一年使用:0次
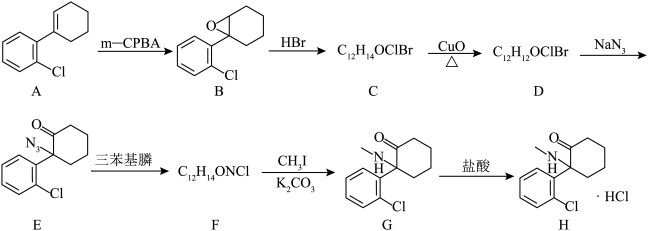
7 . 2024年8月浙江大学胡海岚教授在国际顶尖期刊《科学》上发表文章,揭示了氯胺酮作为快速抗抑郁剂的脑区特异性功能。一种合成盐酸氯胺酮的路线如图所示:_______ ,C→D转化过程的反应类型为_______ 。
(2)若三苯基膦在E→F的转化过程中起到还原剂的作用,则有机物F的结构简式为_______ 。
(3)写出B→C过程的化学方程式_______ 。
(4)在F→G的转化过程中,加入少量 固体可提高G的产量。试解释原因
固体可提高G的产量。试解释原因_______ 。
(5)有机物G能与盐酸反应生成盐酸氯胺酮的原因是_______ 。
(6)同时满足下列条件的B的同分异构体(不考虑立体异构)有_______ 种。
①遇 溶液显色 ②苯环上有3个取代基且其中1个为六元环状结构
溶液显色 ②苯环上有3个取代基且其中1个为六元环状结构
(7)有机物G与 完全加成的产物中含有
完全加成的产物中含有_______ 个手性碳原子。
(2)若三苯基膦在E→F的转化过程中起到还原剂的作用,则有机物F的结构简式为
(3)写出B→C过程的化学方程式
(4)在F→G的转化过程中,加入少量
 固体可提高G的产量。试解释原因
固体可提高G的产量。试解释原因(5)有机物G能与盐酸反应生成盐酸氯胺酮的原因是
(6)同时满足下列条件的B的同分异构体(不考虑立体异构)有
①遇
 溶液显色 ②苯环上有3个取代基且其中1个为六元环状结构
溶液显色 ②苯环上有3个取代基且其中1个为六元环状结构(7)有机物G与
 完全加成的产物中含有
完全加成的产物中含有
您最近一年使用:0次
昨日更新
|
49次组卷
|
2卷引用:河北省唐山市2024-2025学年高三上学期摸底演练化学试题
解题方法
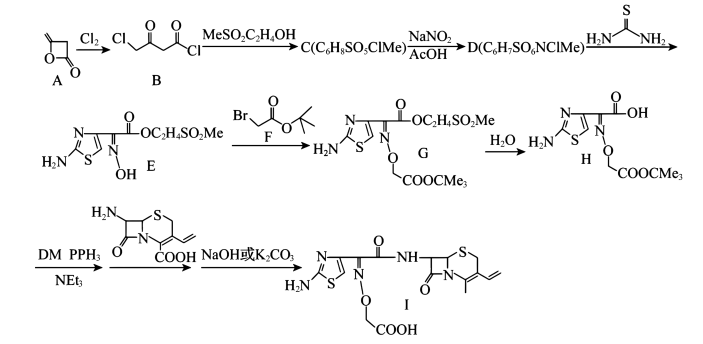
8 . 头孢克肟作为广谱的第三代头孢菌素,具有许多突出的特点,其合成路线如图所示。
(1)A的分子式为_______ 。
(2)F中含有的无氧官能团的名称为_______ 。
(3)B→C的反应类型为_______ ;C的结构简式为_______ 。
(4)D→E的化学方程式为_______ 。
(5)F的同分异构体中满足下列条件的有_______ 种(不考虑立体异构)。
A.属于能发生银镜反应的酯类物质;B.含有两个甲基
(6)结合上述流程,以二氯乙酸酐(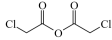 )为原料制备
)为原料制备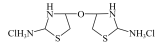 的合成路线为
的合成路线为_______ 。(无机试剂任选)
(1)A的分子式为
(2)F中含有的无氧官能团的名称为
(3)B→C的反应类型为
(4)D→E的化学方程式为
(5)F的同分异构体中满足下列条件的有
A.属于能发生银镜反应的酯类物质;B.含有两个甲基
(6)结合上述流程,以二氯乙酸酐(
 )为原料制备
)为原料制备 的合成路线为
的合成路线为
您最近一年使用:0次
9 . 智能手机因其集成的高清摄像头和智能传感器而常被应用于化学实验。某实验小组利用实验室中的废铁屑(久置但未生锈)制备硝酸铁,并利用配制的硝酸铁标准溶液对“硫酸亚铁补铁剂”中铁元素的含量进行测定。实验过程如下:
实验Ⅰ: 的制备
的制备 溶液并小火加热的目的是:
溶液并小火加热的目的是:___________ 。
(2)逐氮过程中使用氢氧化钠溶液吸收 ,写出该反应的化学方程式:
,写出该反应的化学方程式:___________ 。
(3)操作A包含的实验步骤有:___________ 、___________ 、___________ 、洗涤、干燥。
实验Ⅱ:标准硝酸铁溶液的配制
准确称取0.8080g的 按如图步骤配成100mL溶液。
按如图步骤配成100mL溶液。___________ (填“偏高”“偏低”或“无影响”)。 溶液与灰度值的标准曲线
溶液与灰度值的标准曲线
①分别向7个100mL容量瓶中加入0、0.5、1.0、2.0、3.0、4.0、5.0mL实验Ⅱ中标定的浓度为 的
的 标准溶液,然后分别加入1.5mL某浓度
标准溶液,然后分别加入1.5mL某浓度 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。
②将配好的溶液加入到10mL比色皿中,如图进行放置,在相同条件下用智能手机进行拍照,后用软件确定照片中各溶液相同位置的灰度数值,所得数据如下表所示:

___________ (保留1位有效数字)。
实验Ⅳ:“硫酸亚铁补铁剂”中铁元素含量的测定
①取补铁剂样品2.0g,加入10mL蒸馏水完全溶解,再加入足量 溶液,充分反应后配成100mL溶液。
溶液,充分反应后配成100mL溶液。
②取1.0mL①中所配溶液于100mL容量瓶中,加入1.5mL某浓度 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。
将最终配好的溶液加入到10mL比色皿中,在与实验Ⅲ步骤②中相同条件下拍照,软件处理获得溶液图片的灰度值为97.32。
(6)“硫酸亚铁补铁剂”中铁元素的质量分数为___________ %(保留2位有效数字)。
(7)下列操作中有利于更准确测得“硫酸亚铁补铁剂”中的铁元素含量的有___________。
实验Ⅰ:
 的制备
的制备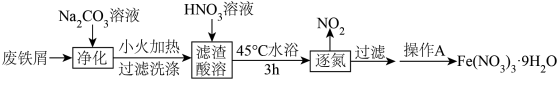
 溶液并小火加热的目的是:
溶液并小火加热的目的是:(2)逐氮过程中使用氢氧化钠溶液吸收
 ,写出该反应的化学方程式:
,写出该反应的化学方程式:(3)操作A包含的实验步骤有:
实验Ⅱ:标准硝酸铁溶液的配制
准确称取0.8080g的
 按如图步骤配成100mL溶液。
按如图步骤配成100mL溶液。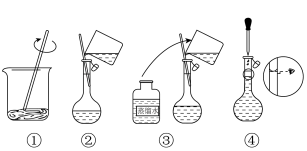
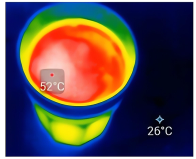
 溶液与灰度值的标准曲线
溶液与灰度值的标准曲线①分别向7个100mL容量瓶中加入0、0.5、1.0、2.0、3.0、4.0、5.0mL实验Ⅱ中标定的浓度为
 的
的 标准溶液,然后分别加入1.5mL某浓度
标准溶液,然后分别加入1.5mL某浓度 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。②将配好的溶液加入到10mL比色皿中,如图进行放置,在相同条件下用智能手机进行拍照,后用软件确定照片中各溶液相同位置的灰度数值,所得数据如下表所示:
| 比色管编号 | S0 | S1 | S2 | S3 | S4 | S5 | S6 |
 溶液(mL) 溶液(mL) | 0 | 0.5 | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 |
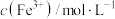 | 0 | 0.0001 | 0.0002 | 0.0004 | 0.0006 | 0.0008 | 0.001 |
| 灰度值 | 127.3 | 119.4 | 107.1 | 87.3 | 65.3 | 47.2 | 29.2 |
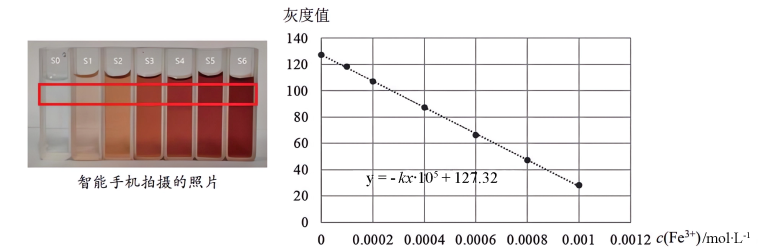

实验Ⅳ:“硫酸亚铁补铁剂”中铁元素含量的测定
①取补铁剂样品2.0g,加入10mL蒸馏水完全溶解,再加入足量
 溶液,充分反应后配成100mL溶液。
溶液,充分反应后配成100mL溶液。②取1.0mL①中所配溶液于100mL容量瓶中,加入1.5mL某浓度
 溶液,用蒸馏水定容。
溶液,用蒸馏水定容。将最终配好的溶液加入到10mL比色皿中,在与实验Ⅲ步骤②中相同条件下拍照,软件处理获得溶液图片的灰度值为97.32。
(6)“硫酸亚铁补铁剂”中铁元素的质量分数为
(7)下列操作中有利于更准确测得“硫酸亚铁补铁剂”中的铁元素含量的有___________。
A.提前除去实验Ⅰ溶解铁屑所用硝酸中的 杂质 杂质 |
B.用浓硝酸溶液代替实验Ⅳ中所用的 溶液 溶液 |
C.整个实验中所用的 溶液均采用相同浓度的溶液 溶液均采用相同浓度的溶液 |
| D.将配制的样品溶液和7个标准溶液放在一起在相同条件下同时拍照,再统一进行数据处理 |
您最近一年使用:0次
10 . 阿司匹林(结构如图所示)是一种历史悠久的解热镇痛药,能抑制血小板聚集。下列关于阿司匹林的说法正确的是
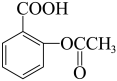
| A.第一电离能:C>O | B.含有极性共价键和非极性共价键 |
| C.沸点:H2O<CH4 | D.最多能与5molH2发生加成反应 |
您最近一年使用:0次



