名校
1 . 化合物 是一种重要中间体,其合成路线如下:
是一种重要中间体,其合成路线如下:_______ 。
(2) 的分子式为C11H14O2,则
的分子式为C11H14O2,则 的结构简式:
的结构简式:_______ 。
(3)1mol 中sp3杂化的原子数目为
中sp3杂化的原子数目为_______ 。
(4)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式_______ 。
①能发生银镜反应;
②能与FeCl3溶液发生显色反应;
③分子中只有4种不同化学环境的氢。
(5)已知: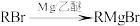
 是一种重要中间体,其合成路线如下:
是一种重要中间体,其合成路线如下:
(2)
 的分子式为C11H14O2,则
的分子式为C11H14O2,则 的结构简式:
的结构简式:(3)1mol
 中sp3杂化的原子数目为
中sp3杂化的原子数目为(4)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式
①能发生银镜反应;
②能与FeCl3溶液发生显色反应;
③分子中只有4种不同化学环境的氢。
(5)已知:
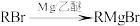
设计以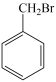 为原料制备
为原料制备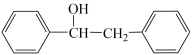 的合成路线(无机试剂和有机溶剂任用,合成路线示例见本题题干)。
的合成路线(无机试剂和有机溶剂任用,合成路线示例见本题题干)。
您最近一年使用:0次
名校
解题方法
2 . CO2的捕获是实现资源利用的重要途径。
(1)烟气中CO2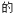 捕集可通过如下所示的物质转化实现。
捕集可通过如下所示的物质转化实现。_______ 。
(2)CO2和H2催化合成CH4。
主要发生反应为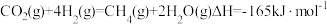 ,一定温度和压强下,将一定比例CO2和H2分别通过装有两种不同催化剂的反应器,反应相同时间,测得CO2转化率随温度变化情况如图1所示。
,一定温度和压强下,将一定比例CO2和H2分别通过装有两种不同催化剂的反应器,反应相同时间,测得CO2转化率随温度变化情况如图1所示。_______ 。
②高于320℃后,用Ni-CeO2作催化剂,CO2转化率略有下降,可能原因是_______ 。
(3)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原CO2的装置示意图如图2所示。控制其他条件相同,将一定量的CO2通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图3所示。_______ 。
②b电极生成HCOOH的电极反应式为_______ 。
③科研小组利用13CO2代替原有的CO2进行研究,其目的是_______ 。
④控制电压为0.8V,电解时转移电子的物质的量为_______ mol。
(1)烟气中CO2
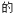 捕集可通过如下所示的物质转化实现。
捕集可通过如下所示的物质转化实现。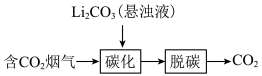
(2)CO2和H2催化合成CH4。
主要发生反应为
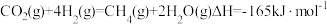 ,一定温度和压强下,将一定比例CO2和H2分别通过装有两种不同催化剂的反应器,反应相同时间,测得CO2转化率随温度变化情况如图1所示。
,一定温度和压强下,将一定比例CO2和H2分别通过装有两种不同催化剂的反应器,反应相同时间,测得CO2转化率随温度变化情况如图1所示。
②高于320℃后,用Ni-CeO2作催化剂,CO2转化率略有下降,可能原因是
(3)一种有机多孔电极材料(铜粉沉积在一种有机物的骨架上)电催化还原CO2的装置示意图如图2所示。控制其他条件相同,将一定量的CO2通入该电催化装置中,阴极所得产物及其物质的量与电压的关系如图3所示。
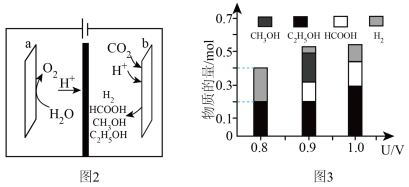
②b电极生成HCOOH的电极反应式为
③科研小组利用13CO2代替原有的CO2进行研究,其目的是
④控制电压为0.8V,电解时转移电子的物质的量为
您最近一年使用:0次
名校
解题方法
3 . 利用含锌废料(主要成分是氧化锌,含有少量铁、铝、铜、锰等金属氧化物或盐)制备氯化锌的一种工艺流程如下:_______ 。(写出任意两点)
(2)为优化工艺流程,盐酸浸取后直接进行高锰酸钾氧化除杂。结合下列图表选择浸取工艺最佳pH范围为_______ ,理由是_______ 。
A.1.5~2.0 B.2.0~3.0 C.3.0~4.0 D.4.5~5.0
(3)滤渣的主要成分有Fe(OH)3、_______ 和MnO2,该工艺中去除锰的离子方程式为_______ 。
(4)最适宜使用的还原剂是_______ 。
(5)氯化锌溶液在蒸发浓缩过程中如操作不当将有碱式盐Zn(OH)Cl生成,该反应方程式为_______ 。
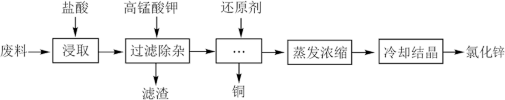
(2)为优化工艺流程,盐酸浸取后直接进行高锰酸钾氧化除杂。结合下列图表选择浸取工艺最佳pH范围为
A.1.5~2.0 B.2.0~3.0 C.3.0~4.0 D.4.5~5.0
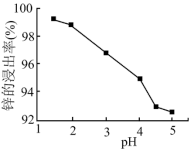
| 金属离子 | Fe2+ | Al3+ | Fe3+ | Cu2+ | Mn2+ | Zn2+ |
| 开始沉淀的pH c=0.01mol·L-1 | 6.8 | 3.7 | 1.8 | 5.2 | 8.6 | 6.7 |
| 沉淀完全的pH c=1.0×10-5mol·L-1 | 8.3 | 4.7 | 2.8 | 6.7 | 10.1 | 8.2 |
(4)最适宜使用的还原剂是
(5)氯化锌溶液在蒸发浓缩过程中如操作不当将有碱式盐Zn(OH)Cl生成,该反应方程式为
您最近一年使用:0次
名校
4 . 下列设计的实验方案不能 达到实验目的是
| 选项 | 实验现象和操作 | 实验目的 |
| A | 向2 mL 0.1mol·L-1 Na2S溶液中滴加0.1 mol·L-1 ZnSO4溶液至不再有沉淀产生,再滴加几滴0.1 mol·L-1 CuSO4溶液,出现黑色沉淀 | 验证Ksp(ZnS)>Ksp(CuS) |
| B | 向装有电石的圆底烧瓶中逐滴加入适量饱和NaCl溶液,将产生的气体通入酸性高锰酸钾溶液中,溶液紫色褪去 | 检验乙炔中含有碳碳三键 |
| C | 以Zn、Fe为电极,以酸化的3% NaCl 溶液作电解质溶液,连接成原电池装置。过一段时间,从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴K3[Fe(CN)6]溶液,观察现象 | 探究金属的牺牲阳极保护法 |
| D | 取5mL0.1 mol·L-1 KI溶液和1mL 0.1mol·L-1 FeCl3溶液充分反应后,加2 mL CCl4振荡、静置后取上层清液滴加少量KSCN溶液,溶液变为红色 | Fe3+与I-的化学反应存在一定限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
5 . 胍(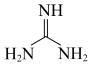 )的盐是病毒核酸保存液的重要成分。下列说法正确的是
)的盐是病毒核酸保存液的重要成分。下列说法正确的是
A.中子数为8的N原子可表示为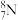 | B.胍中σ键与π键的数目之比为3∶1 |
C.氨基(-NH2)的电子式为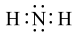 | D.胍分子间能够形成氢键 |
您最近一年使用:0次
名校
6 . 根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 将Al(OH)3固体粉末加入过量NaOH溶液中,充分搅拌,溶解得到无色溶液 | 既体现碱性又体现酸性 |
| B | 向盛有铜片的试管中加入少量硝酸,一段时间后观察到试管口有红色气体逸出 | 实验所用为浓硝酸 |
| C | 向盛有某溶液的试管中滴加稀氢氧化钠溶液,将湿润的红色石蕊试纸靠近试管口,试纸未变蓝 | 该溶液中不存在NH |
| D | 向a、b两试管中同时加入4mL0.01mol·L-1KMnO4溶液和2mL0.1mol·L-1H2C2O4溶液,再向a试管内加入少量MnSO4,a试管中溶液褪色较快 | MnSO4是KMnO4和H2C2O4反应的催化剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 有机物A( )具有兰花香味,可用作香皂、洗发香波的芳香赋予剂。部分相关物质的转化如下图:
)具有兰花香味,可用作香皂、洗发香波的芳香赋予剂。部分相关物质的转化如下图:
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被氯取代,其一氯代物只有一种。
④F可以使溴的四氯化碳溶液褪色。
回答下列问题:
(1)A的结构简式为_______________ ,B可以发生的反应有__________ (填序号)。
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D、F分子所含的官能团的名称分别是_______________ 、_______________ 。
(3)写出与D、E具有相同官能团的同分异构体的可能结构简式:_______________ 、_______________ 。
(4)E可用于生产氨苄青霉素等。已知E的制备方法不同于其常见的同系物,据报道,可由2-甲基-1-丙醇和甲酸在一定条件下制取E。该反应的化学方程式是________________ 。
 )具有兰花香味,可用作香皂、洗发香波的芳香赋予剂。部分相关物质的转化如下图:
)具有兰花香味,可用作香皂、洗发香波的芳香赋予剂。部分相关物质的转化如下图: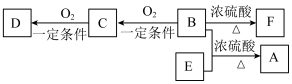
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被氯取代,其一氯代物只有一种。
④F可以使溴的四氯化碳溶液褪色。
回答下列问题:
(1)A的结构简式为
①取代反应 ②消去反应 ③加聚反应 ④氧化反应
(2)D、F分子所含的官能团的名称分别是
(3)写出与D、E具有相同官能团的同分异构体的可能结构简式:
(4)E可用于生产氨苄青霉素等。已知E的制备方法不同于其常见的同系物,据报道,可由2-甲基-1-丙醇和甲酸在一定条件下制取E。该反应的化学方程式是
您最近一年使用:0次
名校
解题方法
8 . 在工业上用辉铜矿(主要成分为(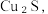 含少量Fe₂O₃、SiO₂等杂质)来制备碱式碳酸铜的工艺流程如下图:
含少量Fe₂O₃、SiO₂等杂质)来制备碱式碳酸铜的工艺流程如下图:_____ 。(填字母)
A.适当增大硫酸浓度 B.将辉铜矿粉碎 C.延长浸取时间
(2)“浸取”过程中,会加入软锰矿(主要成分为 氧化
氧化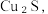 并生成一种黄色沉淀,该沉淀为:
并生成一种黄色沉淀,该沉淀为:_____ 。
(3)“除铁”时将溶液从强酸性调至pH约为3,A物质宜选用_____ 。
(4)为了保证产品纯度,请设计实验确认 是否除尽
是否除尽_____ 。
(5)“沉锰”(除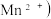 过程中有关反应的离子方程式为
过程中有关反应的离子方程式为_____ 。
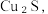 含少量Fe₂O₃、SiO₂等杂质)来制备碱式碳酸铜的工艺流程如下图:
含少量Fe₂O₃、SiO₂等杂质)来制备碱式碳酸铜的工艺流程如下图: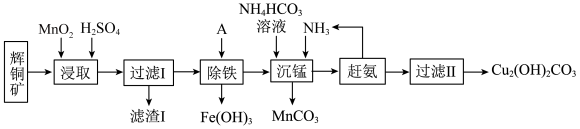
A.适当增大硫酸浓度 B.将辉铜矿粉碎 C.延长浸取时间
(2)“浸取”过程中,会加入软锰矿(主要成分为
 氧化
氧化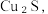 并生成一种黄色沉淀,该沉淀为:
并生成一种黄色沉淀,该沉淀为:(3)“除铁”时将溶液从强酸性调至pH约为3,A物质宜选用
(4)为了保证产品纯度,请设计实验确认
 是否除尽
是否除尽(5)“沉锰”(除
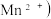 过程中有关反应的离子方程式为
过程中有关反应的离子方程式为
您最近一年使用:0次
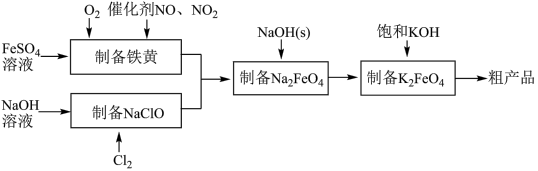
9 . 工业上,以钛白副产品硫酸亚铁制备的铁黄(FeOOH)代替硝酸铁等可溶性铁盐制备高铁酸钾,可降低生产工艺成本且产品质量好。工艺流程如图所示:
(1)制备铁黄的离子方程式为_____ 。
(2)已知K₂FeO₄难溶于乙醇,可溶于水,故洗涤K₂FeO₄晶体时,先使用冷水洗涤,再使用乙醇洗涤,简述用乙醇洗涤K₂FeO₄晶体的操作_____ 。
(3)制备铁黄时,温度高于40°C时,铁黄的产量下降的原因是_____ 。
(4)向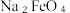 溶液中加入饱和KOH溶液可以制备K₂FeO₄晶体的原因是
溶液中加入饱和KOH溶液可以制备K₂FeO₄晶体的原因是_____ 。
(5)实验室测定含少量杂质的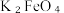 样品的纯度:称取
样品的纯度:称取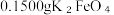 样品溶于碱性KI溶液中,调节pH至弱酸性使混合液充分反应。用(
样品溶于碱性KI溶液中,调节pH至弱酸性使混合液充分反应。用(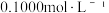 的
的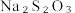 标准溶液进行滴定,消耗
标准溶液进行滴定,消耗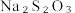 标准溶液25.00mL。滴定时,发生反应的离子方程式:
标准溶液25.00mL。滴定时,发生反应的离子方程式: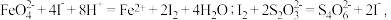 已知:
已知: 试计算K₂FeO₄样品的纯度:
试计算K₂FeO₄样品的纯度:_____ (写出计算过程)。
(1)制备铁黄的离子方程式为
(2)已知K₂FeO₄难溶于乙醇,可溶于水,故洗涤K₂FeO₄晶体时,先使用冷水洗涤,再使用乙醇洗涤,简述用乙醇洗涤K₂FeO₄晶体的操作
(3)制备铁黄时,温度高于40°C时,铁黄的产量下降的原因是
(4)向
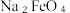 溶液中加入饱和KOH溶液可以制备K₂FeO₄晶体的原因是
溶液中加入饱和KOH溶液可以制备K₂FeO₄晶体的原因是(5)实验室测定含少量杂质的
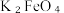 样品的纯度:称取
样品的纯度:称取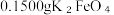 样品溶于碱性KI溶液中,调节pH至弱酸性使混合液充分反应。用(
样品溶于碱性KI溶液中,调节pH至弱酸性使混合液充分反应。用(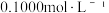 的
的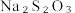 标准溶液进行滴定,消耗
标准溶液进行滴定,消耗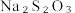 标准溶液25.00mL。滴定时,发生反应的离子方程式:
标准溶液25.00mL。滴定时,发生反应的离子方程式: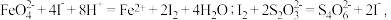 已知:
已知: 试计算K₂FeO₄样品的纯度:
试计算K₂FeO₄样品的纯度:
您最近一年使用:0次
名校
解题方法
10 . 以高硫铝土矿(主要成分为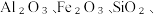 少量
少量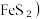 为原料,生产
为原料,生产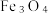 的部分工艺如下:
的部分工艺如下: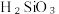 酸性比碳酸弱,难溶于水。下列说法正确的是
酸性比碳酸弱,难溶于水。下列说法正确的是
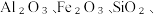 少量
少量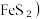 为原料,生产
为原料,生产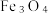 的部分工艺如下:
的部分工艺如下: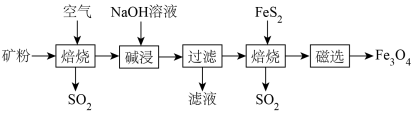
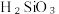 酸性比碳酸弱,难溶于水。下列说法正确的是
酸性比碳酸弱,难溶于水。下列说法正确的是A.“焙烧”时 做氧化剂 做氧化剂 |
B.碱浸过程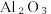 发生的反应:Al2O3+OH-= 发生的反应:Al2O3+OH-=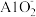 +H2O +H2O |
C.向过滤后得到的滤液中通入过量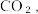 得到的沉淀为 得到的沉淀为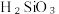 |
D.若由 与 与 在无氧条件下焙烧制得 在无氧条件下焙烧制得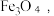 则两者物质的量之比为16:1 则两者物质的量之比为16:1 |
您最近一年使用:0次



