名校
1 . 酚类化合物在医疗、环保、工业等方面有着广泛的用途。

已知部分弱酸的电离平衡常数如下表所示:
(1)室温下,0.1mol/L苯酚钠溶液的pH___________ 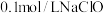 溶液的pH。
溶液的pH。
a.大于 b.小于 c.等于
(2)向苯酚钠水溶液中通入少量SO2,写出反应的离子方程式___________ 。
Ⅱ.石油加工、造纸等企业易产生含有苯酚的工业废水,可通过 氧化法进行处理,其原理为
氧化法进行处理,其原理为 (非可逆反应,反应未配平)。在
(非可逆反应,反应未配平)。在 和
和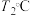 时,分别向含有苯酚的水样中加入等量的
时,分别向含有苯酚的水样中加入等量的 溶液,再以相同的流速向水样中通入
溶液,再以相同的流速向水样中通入 ,测得水样中苯酚的含量随时间变化的曲线如图所示。
,测得水样中苯酚的含量随时间变化的曲线如图所示。 时,
时,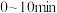 内,
内, 的平均反应速率为
的平均反应速率为___________ 。
(4)请判断 和
和 的大小:
的大小:
___________  。
。
a.大于 b.小于 c.等于
(5) 时对工业废水中苯酚的去除率低于
时对工业废水中苯酚的去除率低于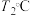 时的原因可能是
时的原因可能是___________ (写一种即可)。
(6)利用 溶液与苯酚的显色反应,可定性检测工业废水中的苯酚,其反应原理为
溶液与苯酚的显色反应,可定性检测工业废水中的苯酚,其反应原理为 。反应到达平衡时,下列说法正确的有___________。
。反应到达平衡时,下列说法正确的有___________。
Ⅲ.绿原酸是一种新型高效的酚型天然抗氧化剂,在食品行业有着广泛的用途。 发生反应,则绿原酸的分子式为
发生反应,则绿原酸的分子式为___________ 。
(8)1mol化合物Ⅰ与足量金属钠反应生成标准状况下氢气体积为___________ 。
(9)化合物Ⅲ有如下特点:①与化合物Ⅱ互为同分异构体;②遇 溶液显色;③1mol化合物Ⅲ与足量银氨溶液反应生成
溶液显色;③1mol化合物Ⅲ与足量银氨溶液反应生成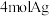 ;④苯环上的一卤代物只有一种。写出化合物Ⅲ的一种可能的结构简式:
;④苯环上的一卤代物只有一种。写出化合物Ⅲ的一种可能的结构简式:___________ 。

已知部分弱酸的电离平衡常数如下表所示:
| 弱酸 | 次氯酸 | 亚硫酸 | 苯酚 |
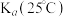 | 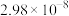 | 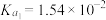  |  |
(1)室温下,0.1mol/L苯酚钠溶液的pH
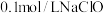 溶液的pH。
溶液的pH。a.大于 b.小于 c.等于
(2)向苯酚钠水溶液中通入少量SO2,写出反应的离子方程式
Ⅱ.石油加工、造纸等企业易产生含有苯酚的工业废水,可通过
 氧化法进行处理,其原理为
氧化法进行处理,其原理为 (非可逆反应,反应未配平)。在
(非可逆反应,反应未配平)。在 和
和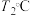 时,分别向含有苯酚的水样中加入等量的
时,分别向含有苯酚的水样中加入等量的 溶液,再以相同的流速向水样中通入
溶液,再以相同的流速向水样中通入 ,测得水样中苯酚的含量随时间变化的曲线如图所示。
,测得水样中苯酚的含量随时间变化的曲线如图所示。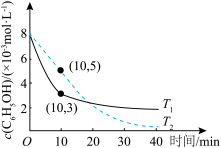
 时,
时,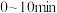 内,
内, 的平均反应速率为
的平均反应速率为(4)请判断
 和
和 的大小:
的大小:
 。
。a.大于 b.小于 c.等于
(5)
 时对工业废水中苯酚的去除率低于
时对工业废水中苯酚的去除率低于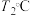 时的原因可能是
时的原因可能是(6)利用
 溶液与苯酚的显色反应,可定性检测工业废水中的苯酚,其反应原理为
溶液与苯酚的显色反应,可定性检测工业废水中的苯酚,其反应原理为 。反应到达平衡时,下列说法正确的有___________。
。反应到达平衡时,下列说法正确的有___________。| A.加水稀释,溶液pH减小 |
B.滴入几滴浓盐酸,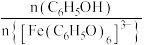 增大 增大 |
| C.加入少量NaOH固体,反应平衡常数增大 |
| D.加入少量Cu粉,溶液紫色变浅 |
Ⅲ.绿原酸是一种新型高效的酚型天然抗氧化剂,在食品行业有着广泛的用途。

 发生反应,则绿原酸的分子式为
发生反应,则绿原酸的分子式为(8)1mol化合物Ⅰ与足量金属钠反应生成标准状况下氢气体积为
(9)化合物Ⅲ有如下特点:①与化合物Ⅱ互为同分异构体;②遇
 溶液显色;③1mol化合物Ⅲ与足量银氨溶液反应生成
溶液显色;③1mol化合物Ⅲ与足量银氨溶液反应生成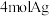 ;④苯环上的一卤代物只有一种。写出化合物Ⅲ的一种可能的结构简式:
;④苯环上的一卤代物只有一种。写出化合物Ⅲ的一种可能的结构简式:
您最近一年使用:0次
名校
2 . 亚氯酸钠(NaClO2)是高效氧化剂和漂白剂。实验室制备NaClO2的装置图如图所示。 2NaClO3+2NaCl。
2NaClO3+2NaCl。
(1)仪器a的名称为______ 。
(2)补全并配平下列反应的化学方程式______ 。
_______H2O2+_______ +_______NaOH=_______NaClO2+_______
+_______NaOH=_______NaClO2+_______ +_______H2O
+_______H2O
(3)冷水浴的作用不包括______ 。
(4)当试管中有大量晶体析出时,停止反应。获得该晶体所需要操作方法为______ 。
(5)若获得的晶体纯度不符合要求,欲提高其纯度的实验方法为_______ 。
(6)某小组同学欲测定亚氯酸钠晶体(NaClO2•3H2O)中结晶水的数目。甲同学指出NaClO2会分解而无法完成实验,但乙同学却认为可行。简述你的观点和理由_______ 。
(7)上述NaClO2产品的纯度测定实验为:称取mg样品溶解后,加入稍过量的KI,再滴加适量的稀硫酸,充分反应后,稀释为100mL溶液。最后移取25.00mL上述溶液,恰好消耗VmLcmol•L-1Na2S2O3溶液。
有关反应原理如下:ClO +4I-+4H+=2H2O+2I2+Cl-
+4I-+4H+=2H2O+2I2+Cl-
I2+2S2O =2I-+S4O
=2I-+S4O
计算该NaClO2产品的纯度______ 。(用含m、C、V的代数式表示,写出计算过程)。
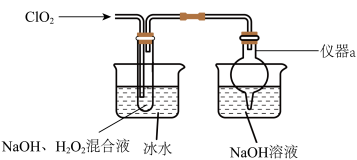
 2NaClO3+2NaCl。
2NaClO3+2NaCl。(1)仪器a的名称为
(2)补全并配平下列反应的化学方程式
_______H2O2+_______
 +_______NaOH=_______NaClO2+_______
+_______NaOH=_______NaClO2+_______ +_______H2O
+_______H2O(3)冷水浴的作用不包括
| A.防止NaClO2分解 | B.防止H2O2分解 |
| C.促进NaClO2析出 | D.提高反应速率 |
(4)当试管中有大量晶体析出时,停止反应。获得该晶体所需要操作方法为
| A.过滤 | B.结晶 | C.蒸馏 | D.分液 |
(5)若获得的晶体纯度不符合要求,欲提高其纯度的实验方法为
(6)某小组同学欲测定亚氯酸钠晶体(NaClO2•3H2O)中结晶水的数目。甲同学指出NaClO2会分解而无法完成实验,但乙同学却认为可行。简述你的观点和理由
(7)上述NaClO2产品的纯度测定实验为:称取mg样品溶解后,加入稍过量的KI,再滴加适量的稀硫酸,充分反应后,稀释为100mL溶液。最后移取25.00mL上述溶液,恰好消耗VmLcmol•L-1Na2S2O3溶液。
有关反应原理如下:ClO
 +4I-+4H+=2H2O+2I2+Cl-
+4I-+4H+=2H2O+2I2+Cl-I2+2S2O
 =2I-+S4O
=2I-+S4O
计算该NaClO2产品的纯度
您最近一年使用:0次
名校
解题方法
3 . 油酸熔点为14℃,沸点为360℃,不溶于水,密度为0.89g•cm-3,其摩尔质量为282g•mol-1。其分子结构如图所示。_______ 。
(2)油酸分子式为_______ 。
(3)常温下,欲分离油酸和水的混合物,除烧杯、铁架台外,还需_______ 。
利用油膜法能近似测定分子直径和阿伏加德罗常数。先取0.5mL的油酸溶解于酒精中形成1L溶液。再取0.020mL上述溶液滴入水中,测得油酸分散的面积约为1.0×10-2m2。假设在水面上油酸呈单分子紧密排列,如图所示。_______ m。
(5)若把油酸分子近似为球体,根据球体的体积计算公式:V=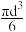 。计算本实验测定的阿伏加德罗常数(NA)约为
。计算本实验测定的阿伏加德罗常数(NA)约为_______ 。

| A.电子式 | B.结构式 | C.球棍模型 | D.空间填充模型 |
| A.C18H34O2 | B.C18H36O2 | C.C19H38O | D.C19H36O |
A. | B. | C. | D. |
利用油膜法能近似测定分子直径和阿伏加德罗常数。先取0.5mL的油酸溶解于酒精中形成1L溶液。再取0.020mL上述溶液滴入水中,测得油酸分散的面积约为1.0×10-2m2。假设在水面上油酸呈单分子紧密排列,如图所示。

| A.10-3 | B.10-6 | C.10-9 | D.10-12 |
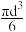 。计算本实验测定的阿伏加德罗常数(NA)约为
。计算本实验测定的阿伏加德罗常数(NA)约为
您最近一年使用:0次
4 . 下列事实能证明氮元素的非金属性强于磷元素的是
| A.沸点:NH3>PH3 |
| B.酸性:HNO3>H3PO4 |
| C.P4与浓硝酸反应生成H3PO4与NO2 |
D. 中N—P共用电子对偏向N 中N—P共用电子对偏向N |
您最近一年使用:0次
名校
5 . Ⅰ.提取碘。高分子树脂吸附法是工业提取碘的方法之一,其流程如图: 只能将
只能将 氧化为
氧化为 ,同时生成NO气体;
,同时生成NO气体;
(1)步骤④“洗脱”反应的离子方程式为___________ 。
(2)经步骤①和④所得溶液中的 :①
:①___________ ④。(选填“>”、“<”“=”)
(3)步骤⑤“氧化”的离子方程式为___________ 。
(4)步骤⑤“氧化”没有选择氯气,而是选择了价格较高的 ,原因是
,原因是___________ 。
(5)高分子树脂上吸附的 还能用浓
还能用浓 溶液洗脱,该反应的离子方程式是
溶液洗脱,该反应的离子方程式是___________ 。
Ⅱ.利用海水可以缓解煤燃烧过程中排放的 造成的环境问题,其工艺流程如图所示:
造成的环境问题,其工艺流程如图所示: 、
、 等分子或离子,需要用氧气进行“氧化”处理,写出
等分子或离子,需要用氧气进行“氧化”处理,写出 参加反应的离子方程式:
参加反应的离子方程式:___________ 。
(7)“氧化”后的海水需用大量天然海水与之混合后才能排放。该操作的主要目的是___________ 。
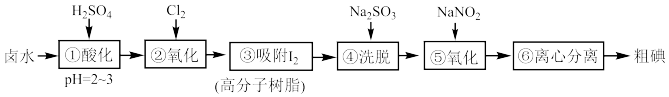
 只能将
只能将 氧化为
氧化为 ,同时生成NO气体;
,同时生成NO气体;(1)步骤④“洗脱”反应的离子方程式为
(2)经步骤①和④所得溶液中的
 :①
:①(3)步骤⑤“氧化”的离子方程式为
(4)步骤⑤“氧化”没有选择氯气,而是选择了价格较高的
 ,原因是
,原因是(5)高分子树脂上吸附的
 还能用浓
还能用浓 溶液洗脱,该反应的离子方程式是
溶液洗脱,该反应的离子方程式是Ⅱ.利用海水可以缓解煤燃烧过程中排放的
 造成的环境问题,其工艺流程如图所示:
造成的环境问题,其工艺流程如图所示: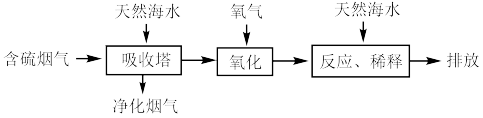
 、
、 等分子或离子,需要用氧气进行“氧化”处理,写出
等分子或离子,需要用氧气进行“氧化”处理,写出 参加反应的离子方程式:
参加反应的离子方程式:(7)“氧化”后的海水需用大量天然海水与之混合后才能排放。该操作的主要目的是
您最近一年使用:0次
名校
6 . 下面描述了 的一些化学性质,其中
的一些化学性质,其中 作氧化剂的是
作氧化剂的是
 的一些化学性质,其中
的一些化学性质,其中 作氧化剂的是
作氧化剂的是A.溶于水形成不稳定的 |
B.在一定条件下与 反应生成 反应生成 |
C.通入到 溶液中,溶液的棕黄色褪去 溶液中,溶液的棕黄色褪去 |
D.与 气体混合出现淡黄色固体 气体混合出现淡黄色固体 |
您最近一年使用:0次
名校
解题方法
7 . 下列物质中不含有硫元素的是
| A.重晶石 | B.蛋白质 | C.尿素 | D.明矾 |
您最近一年使用:0次
解题方法
8 . 氯碱工业的生产原理是_____ (写化学方程式)。检验阳极产物的方法是_____ 。
您最近一年使用:0次
9 . 2023年诺贝尔化学奖授予三位在发现和合成量子点方面做出重要贡献的科学家。量子点是一种纳米级别的半导体,其直径常在2~20nm之间,例如碳量子点、砷化镓(GaAs)量子点等。
(1)我国化学家研究的一种新型复微合光催化剂[碳量子点/氮化碳(纳米复合物)]可以利用太阳光实现高效分解水,其原理如图1所示。下列说法正确的是 ___________。
(2)Ga在元素周期表中的位置___________ 。
(3)N、P、As的气态氢化物沸点由高到低的顺序是___________ (用氢化物分子式表示)。
(4)砷化镓可由(CH3)3Ga和AsH3在700℃时制得。(CH3)3Ga中镓原子的杂化方式为___________ 。AsH3分子的VSEPR模型为 ___________ 。
(5)砷化镓(GaAs)的晶胞结构如图2所示。将Mn掺杂到晶体中得到稀磁性半导体材料,其晶胞结构如图3所示。下列说法错误的是 ___________。
(6)已知砷化镓晶胞的边长为0.565nm,NA为阿伏加德罗常数的数值,则GaAs晶体的密度为___________ g/cm3。
(1)我国化学家研究的一种新型复微合光催化剂[碳量子点/氮化碳(纳米复合物)]可以利用太阳光实现高效分解水,其原理如图1所示。下列说法正确的是 ___________。

| A.总反应为H2O2=H2+O2 |
| B.水分解过程中,H2O2作催化剂 |
| C.复合光催化剂中两种纳米材料均属于共价化合物 |
| D.若反应Ⅱ是放热反应,则反应Ⅰ一定是吸热反应 |
(2)Ga在元素周期表中的位置
(3)N、P、As的气态氢化物沸点由高到低的顺序是
(4)砷化镓可由(CH3)3Ga和AsH3在700℃时制得。(CH3)3Ga中镓原子的杂化方式为
(5)砷化镓(GaAs)的晶胞结构如图2所示。将Mn掺杂到晶体中得到稀磁性半导体材料,其晶胞结构如图3所示。下列说法错误的是 ___________。

| A.图2中,与Ga原子直接连接的As原子构成的几何形状为正四面体形 |
| B.图2中,与Ga原子等距离的Ga原子个数为12个 |
| C.Ga的第一电离能小于As |
| D.稀磁性半导体材料中,Mn、As的原子个数比为1:2 |
(6)已知砷化镓晶胞的边长为0.565nm,NA为阿伏加德罗常数的数值,则GaAs晶体的密度为
您最近一年使用:0次
10 . 砷的一些化合物常用作半导体、除草剂、杀鼠药等。As4O6分子的结构如图所示,下列说法正确的是

| A.该分子中As和O的杂化方式均为sp3 |
| B.稳定性:AsH3>H2O |
| C.As4O6分子中只存在非极性共价键 |
| D.As位于元素周期表中第四周期第ⅤB族 |
您最近一年使用:0次



