1 . 钴在新能源、新材料领域具有重要用途。某炼锌废渣含有锌、铅、铜、铁、钴、锰的 价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。 ,其他金属离子不沉淀,即认为完全分离。
,其他金属离子不沉淀,即认为完全分离。
已知:①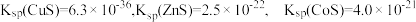 。
。
②以氢氧化物形式沉淀时,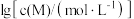 和溶液
和溶液 的关系如图所示。
的关系如图所示。
(1)“酸浸”前,需将废渣磨碎,其目的是_____ 。
(2)“酸浸”步骤中, 发生反应的化学方程式是
发生反应的化学方程式是_____ 。
(3)假设“沉铜”后得到的滤液中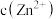 和
和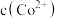 均为
均为 ,向其中加入
,向其中加入 至
至 沉淀完全,此时溶液中
沉淀完全,此时溶液中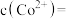
_____  ,据此判断能否实现
,据此判断能否实现 和
和 的完全分离
的完全分离_____ (填“能”或“不能”)。
(4)“沉锰”步骤中,生成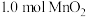 ,产生
,产生 的物质的量为
的物质的量为_____ 。
(5)“沉淀”步骤中,用 调
调 ,分离出的滤渣是
,分离出的滤渣是_____ 。
(6)“沉钴”步骤中,控制溶液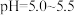 ,加入适量的
,加入适量的 氧化
氧化 ,其反应的离子方程式为
,其反应的离子方程式为_____ 。
(7)根据题中给出的信息,从“沉钴”后的滤液中回收氢氧化锌的方法是_____ 。
 价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
价氧化物及锌和铜的单质。从该废渣中提取钴的一种流程如下。
 ,其他金属离子不沉淀,即认为完全分离。
,其他金属离子不沉淀,即认为完全分离。已知:①
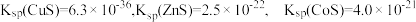 。
。②以氢氧化物形式沉淀时,
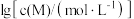 和溶液
和溶液 的关系如图所示。
的关系如图所示。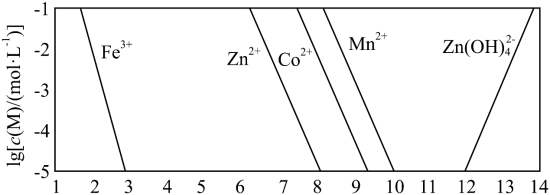
(1)“酸浸”前,需将废渣磨碎,其目的是
(2)“酸浸”步骤中,
 发生反应的化学方程式是
发生反应的化学方程式是(3)假设“沉铜”后得到的滤液中
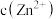 和
和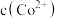 均为
均为 ,向其中加入
,向其中加入 至
至 沉淀完全,此时溶液中
沉淀完全,此时溶液中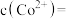
 ,据此判断能否实现
,据此判断能否实现 和
和 的完全分离
的完全分离(4)“沉锰”步骤中,生成
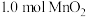 ,产生
,产生 的物质的量为
的物质的量为(5)“沉淀”步骤中,用
 调
调 ,分离出的滤渣是
,分离出的滤渣是(6)“沉钴”步骤中,控制溶液
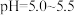 ,加入适量的
,加入适量的 氧化
氧化 ,其反应的离子方程式为
,其反应的离子方程式为(7)根据题中给出的信息,从“沉钴”后的滤液中回收氢氧化锌的方法是
您最近一年使用:0次
2024高三·上海·专题练习
2 . PtF6是极强的氧化剂,Xe和PtF6可制稀有气体离子化合物。
六氟合铂酸氙([XeF]+[Pt2F11]-)的制备方式如图所示:
2.上述过程中属于氧化还原反应的是_______。
3.氟气通入氙(Xe)会产生XeF2、XeF4、XeF6三种氟化物气体。现将1 mol的Xe和9 mol的F2同时通入50 L的容器中,反应10 min后,测得容器内共有8.9 mol气体,且三种氟化物的比例为XeF2∶XeF4∶XeF6 = 1∶6∶3,则10 min内XeF4的速率v(XeF4) = _______ 。
六氟合铂酸氙([XeF]+[Pt2F11]-)的制备方式如图所示:
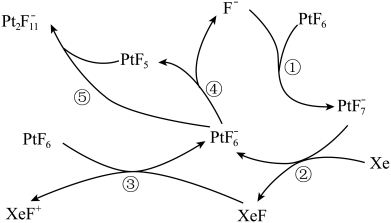
| A.PtF6 | B.PtF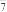 | C.F- | D.XeF+ |
| A.② | B.③ | C.④ | D.⑤ |
您最近一年使用:0次
真题
解题方法
3 . 精炼铜产生的铜阳极泥富含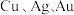 等多种元素。研究人员设计了一种从铜阳极泥中分离提收金和银的流程,如下图所示。
等多种元素。研究人员设计了一种从铜阳极泥中分离提收金和银的流程,如下图所示。
(1) 位于元素周期表第
位于元素周期表第_______ 周期第_______ 族。
(2)“浸出液1”中含有的金属离子主要是_______ 。
(3)“浸取2”步骤中,单质金转化为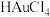 的化学方程式为
的化学方程式为_______ 。
(4)“浸取3”步骤中,“浸渣2”中的_______ (填化学式)转化为 。
。
(5)“电沉积”步骤中阴极的电极反应式为_______ 。“电沉积”步骤完成后,阴极区溶液中可循环利用的物质为_______ (填化学式)。
(6)“还原”步骤中,被氧化的 与产物
与产物 的物质的量之比为
的物质的量之比为_______ 。
(7) 可被
可被 氧化为
氧化为 。从物质结构的角度分析
。从物质结构的角度分析 的结构为(a)而不是(b)的原因:
的结构为(a)而不是(b)的原因:_______ 。
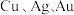 等多种元素。研究人员设计了一种从铜阳极泥中分离提收金和银的流程,如下图所示。
等多种元素。研究人员设计了一种从铜阳极泥中分离提收金和银的流程,如下图所示。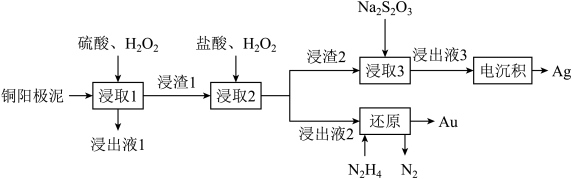
(1)
 位于元素周期表第
位于元素周期表第(2)“浸出液1”中含有的金属离子主要是
(3)“浸取2”步骤中,单质金转化为
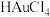 的化学方程式为
的化学方程式为(4)“浸取3”步骤中,“浸渣2”中的
 。
。(5)“电沉积”步骤中阴极的电极反应式为
(6)“还原”步骤中,被氧化的
 与产物
与产物 的物质的量之比为
的物质的量之比为(7)
 可被
可被 氧化为
氧化为 。从物质结构的角度分析
。从物质结构的角度分析 的结构为(a)而不是(b)的原因:
的结构为(a)而不是(b)的原因: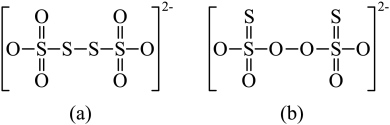
您最近一年使用:0次
真题
4 . 研究人员制备了一种具有锂离子通道的导电氧化物(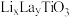 ),其立方晶胞和导电时
),其立方晶胞和导电时 迁移过程如下图所示。已知该氧化物中
迁移过程如下图所示。已知该氧化物中 为
为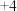 价,
价, 为
为 价。下列说法错误的是
价。下列说法错误的是
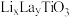 ),其立方晶胞和导电时
),其立方晶胞和导电时 迁移过程如下图所示。已知该氧化物中
迁移过程如下图所示。已知该氧化物中 为
为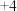 价,
价, 为
为 价。下列说法错误的是
价。下列说法错误的是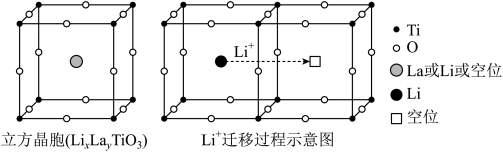
A.导电时, 和 和 的价态不变 的价态不变 | B.若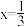 , , 与空位的数目相等 与空位的数目相等 |
| C.与体心最邻近的O原子数为12 | D.导电时、空位移动方向与电流方向相反 |
您最近一年使用:0次
名校
5 . 下列实验操作正确且能达到相应实验目的的是
选项 | 实验目的 | 实验操作 |
A | 比较室温下 、 、 溶度积的大小 溶度积的大小 | 向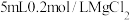 溶液中滴加少量NaOH溶液,振荡充分后,再滴加几滴 溶液中滴加少量NaOH溶液,振荡充分后,再滴加几滴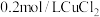 溶液 溶液 |
B | 证明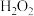 具有氧化性 具有氧化性 | 将一定浓度的双氧水与 溶液混合 溶液混合 |
C | 除去乙烷中混有的乙烯 | 一定条件下向混合气体中通入一定量的 |
D | 证明葡萄糖具有还原性 | 在试管中加入2mL5%的 溶液,再加5滴稀NaOH溶液,混匀后加入0.5mL葡萄糖溶液,加热 溶液,再加5滴稀NaOH溶液,混匀后加入0.5mL葡萄糖溶液,加热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
6 . 2-溴戊二酸二甲酯(相对分子质量为239)是某抗癌药物的重要中间体,其制备的反应原理如图所示:
步骤一:制备
将10.0g戊二酸(固态,相对分子质量为132)加入到三颈烧瓶中,再向其中加入三氯甲烷25mL,搅拌均匀,保持78℃条件下,依次缓慢滴加12mL氯化亚砜、3滴催化剂、10ml液溴,随后回流;回流完毕后,将三颈烧瓶置于冰盐浴中,将溶液温度降到-10℃后,缓慢滴加25mL甲醇(沸点64.7℃)保持滴加过程中温度不超过0℃。
步骤二:除杂
向三颈烧瓶中加入25mL饱和碳酸氢钠溶液进行洗涤,分液除去上层水相,下层有机相再用25mL饱和氯化钠溶液洗涤3次,洗涤完毕,“用无水硫酸镁干燥,过滤。
步骤三:提纯
过滤后的液体置于热浴容器中(外温170℃),接上精馏装置,进行减压蒸馏。
步骤四:收集
收集100—110℃的馏分,得到10.86g无色透明油状液体。
回答下列问题:
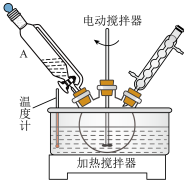
(1)使用装置A的优点是_____________ ,三颈烧瓶宜选择的规格是__________ (填标号)。
A.50mL B.150mL C.200mL D.500mL
(2)步骤一中采取“温度降到-10℃”“缓慢滴加”这些措施的可能原因有_____________ 。
a.减缓反应速率
b.防止高温下发生复杂的有机副反应
c.避免原料挥发,使反应物充分反应
(3)步骤二中用饱和氯化钠溶液洗涤的目的是_______________ 。
(4)步骤三中使用减压蒸馏的目的是______________ 。
(5)中间产物Ⅰ比戊二酸的沸点低很多的原因是_______________ ,反应中生成中间产物1(戊二酰氯)的同时得到两种有刺激性气味的气体,该反应的化学方程式为________________ 。
(6)从环保角度分析,该实验装置存在明显不足之处,解决的办法是_____________ 。
(7)本实验的产率约是 。

步骤一:制备
将10.0g戊二酸(固态,相对分子质量为132)加入到三颈烧瓶中,再向其中加入三氯甲烷25mL,搅拌均匀,保持78℃条件下,依次缓慢滴加12mL氯化亚砜、3滴催化剂、10ml液溴,随后回流;回流完毕后,将三颈烧瓶置于冰盐浴中,将溶液温度降到-10℃后,缓慢滴加25mL甲醇(沸点64.7℃)保持滴加过程中温度不超过0℃。
步骤二:除杂
向三颈烧瓶中加入25mL饱和碳酸氢钠溶液进行洗涤,分液除去上层水相,下层有机相再用25mL饱和氯化钠溶液洗涤3次,洗涤完毕,“用无水硫酸镁干燥,过滤。
步骤三:提纯
过滤后的液体置于热浴容器中(外温170℃),接上精馏装置,进行减压蒸馏。
步骤四:收集
收集100—110℃的馏分,得到10.86g无色透明油状液体。
回答下列问题:
(1)使用装置A的优点是
A.50mL B.150mL C.200mL D.500mL
(2)步骤一中采取“温度降到-10℃”“缓慢滴加”这些措施的可能原因有
a.减缓反应速率
b.防止高温下发生复杂的有机副反应
c.避免原料挥发,使反应物充分反应
(3)步骤二中用饱和氯化钠溶液洗涤的目的是
(4)步骤三中使用减压蒸馏的目的是
(5)中间产物Ⅰ比戊二酸的沸点低很多的原因是
(6)从环保角度分析,该实验装置存在明显不足之处,解决的办法是
(7)本实验的产率约是 。
| A.30% | B.50% | C.60% | D.80% |
您最近一年使用:0次
7 . 萘哌地尔是一种常用的肾上腺素受体阻滞药,可由以下工艺合成:
i.合成中间体 :
:
① ;
;
(1)②的反应类型为___________ ,D中含有的官能团名称为___________ 。
(2) 的化学方程式为
的化学方程式为___________ 。可用 溶液检验
溶液检验 中是否混有
中是否混有 ,其现象为
,其现象为___________ 。
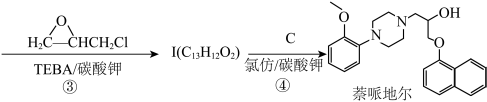
(3)D的同分异构体中,能使 溶液变色的有
溶液变色的有___________ 种;I的结构简式为___________ 。
(4)根据上述信息,写出以1,1-二苯乙烷和苯胺为主要原料制备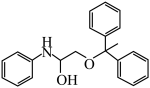 的路线
的路线___________ 。
i.合成中间体
 :
: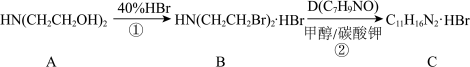
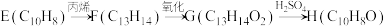
①
 ;
;②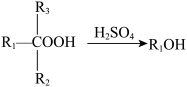 。
。
(1)②的反应类型为
(2)
 的化学方程式为
的化学方程式为 溶液检验
溶液检验 中是否混有
中是否混有 ,其现象为
,其现象为(3)D的同分异构体中,能使
 溶液变色的有
溶液变色的有(4)根据上述信息,写出以1,1-二苯乙烷和苯胺为主要原料制备
 的路线
的路线
您最近一年使用:0次
8 . 卡维地洛类药物(丁)可用于治疗原发性高血压、有症状的充血性心力衰竭。以甲为原料合成丁的方法如下图所示。下列说法正确的是

| A.试剂X可以是足量的NaOH溶液 |
| B.乙、丙、丁均能与盐酸反应 |
| C.丙、丁互为同系物 |
| D.戊的同分异构体有3种 |
您最近一年使用:0次
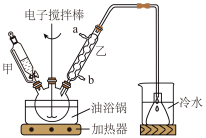
9 . 清凉茶酸乙酯(CH2CH=CHCH=CHCOOCH2CH3)是一种消毒杀菌剂,对细菌霉菌等有灭活作用。通过酯化反应制备清凉茶酸乙酯的方法如图,实验装置(部分夹持装置省略)如图所示。
Ⅱ.油浴加热,控制温度为110℃,并不断搅拌,一段时间之后停止加热和搅拌。
Ⅲ.反应混合物冷却至室温,进行操作X。
Ⅳ.在滤液中加入5%的小苏打溶液,洗涤,至混合液pH=7左右,再用蒸馏水洗涤。
V.将洗涤后混合液加入分液漏斗,进行分液。
Ⅵ.在分液后的有机层加入干燥剂,振荡,静置,过滤。
Ⅶ.对滤液进行蒸馏,收集一定温度的馏分,得到5.4mL纯净的清凉茶酸乙酯。
已知部分物质的性质如表:
(1)仪器甲的名称为______ 。
(2)写出实验中三颈烧瓶中发生的主要反应______ ,其中环己烷的作用是______ 。
(3)加热搅拌过程中忘加沸石,正确的操作是______ 。
(4)下列有关该实验过程,正确的是______ 。
(5)计算该制备实验的产率:______ (保留三位有效数字)。
Ⅱ.油浴加热,控制温度为110℃,并不断搅拌,一段时间之后停止加热和搅拌。
Ⅲ.反应混合物冷却至室温,进行操作X。
Ⅳ.在滤液中加入5%的小苏打溶液,洗涤,至混合液pH=7左右,再用蒸馏水洗涤。
V.将洗涤后混合液加入分液漏斗,进行分液。
Ⅵ.在分液后的有机层加入干燥剂,振荡,静置,过滤。
Ⅶ.对滤液进行蒸馏,收集一定温度的馏分,得到5.4mL纯净的清凉茶酸乙酯。
已知部分物质的性质如表:
| 沸点/℃ | 密度/(g•cm-3) | 水溶性 | 备注 | |
| 乙醇 | 78 | 0.789 | 混溶 | |
| 清凉茶酸 | 228 | 1.204 | 易溶 | |
| 清凉茶酸乙酯 | 195 | 0.926 | 难溶 | |
| 环己烷 | 80.7 | 0.780 | 难溶 | 挥发过程中可带出较多的水 |
(2)写出实验中三颈烧瓶中发生的主要反应
(3)加热搅拌过程中忘加沸石,正确的操作是
(4)下列有关该实验过程,正确的是
| A.乙中的进水口为a |
| B.操作X使用的玻璃仪器有玻璃棒,漏斗,烧杯 |
| C.加入小苏打是为了中和混合物中的酸性物质 |
| D.分液后的有机层加入碱石灰干燥 |
您最近一年使用:0次
真题
解题方法
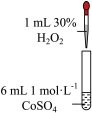
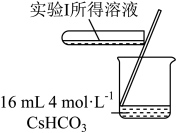
10 . 学习小组为探究 、
、 能否催化
能否催化 的分解及相关性质,室温下进行了实验I~Ⅳ。
的分解及相关性质,室温下进行了实验I~Ⅳ。
已知: 为粉红色、
为粉红色、 为蓝色、
为蓝色、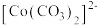 为红色、
为红色、 为墨绿色。回答下列问题:
为墨绿色。回答下列问题:
(1)配制 的
的 溶液,需要用到下列仪器中的
溶液,需要用到下列仪器中的_______ (填标号)。
_______ (填“能”或“不能”)催化 的分解。实验Ⅱ中
的分解。实验Ⅱ中 大大过量的原因是
大大过量的原因是_______ 。实验Ⅲ初步表明 能催化
能催化 的分解,写出
的分解,写出 在实验Ⅲ中所发生反应的离子方程式
在实验Ⅲ中所发生反应的离子方程式_______ 、_______ 。
(3)实验I表明,反应 难以正向进行,利用化学平衡移动原理,分析
难以正向进行,利用化学平衡移动原理,分析 、
、 分别与
分别与 配位后,正向反应能够进行的原因
配位后,正向反应能够进行的原因_______ 。_______ 、_______ 。
 、
、 能否催化
能否催化 的分解及相关性质,室温下进行了实验I~Ⅳ。
的分解及相关性质,室温下进行了实验I~Ⅳ。| 实验I | 实验Ⅱ | 实验Ⅲ |
|
|
|
| 无明显变化 | 溶液变为红色,伴有气泡产生 | 溶液变为墨绿色,并持续产生能使带火星木条复燃的气体 |
 为粉红色、
为粉红色、 为蓝色、
为蓝色、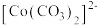 为红色、
为红色、 为墨绿色。回答下列问题:
为墨绿色。回答下列问题:(1)配制
 的
的 溶液,需要用到下列仪器中的
溶液,需要用到下列仪器中的a.  b.
b. 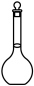 c.
c.  d.
d.

 的分解。实验Ⅱ中
的分解。实验Ⅱ中 大大过量的原因是
大大过量的原因是 能催化
能催化 的分解,写出
的分解,写出 在实验Ⅲ中所发生反应的离子方程式
在实验Ⅲ中所发生反应的离子方程式(3)实验I表明,反应
 难以正向进行,利用化学平衡移动原理,分析
难以正向进行,利用化学平衡移动原理,分析 、
、 分别与
分别与 配位后,正向反应能够进行的原因
配位后,正向反应能够进行的原因实验Ⅳ:
您最近一年使用:0次