1 . 完成下列问题。
(1)某温度下,纯水中的c(OH-)=1×10-6 mol/L,则此时c(H+)为_____ mol/L。若在温度不变时,往其中滴加盐酸使 c(H+)=1×10-4mol/L,则溶液中c(OH-)为_____ mol/L。若将此盐酸稀释 1 000 倍,则溶液的c(H+)约为______ mol/L。
(2)已知:Cu(OH)2(s) Cu2+(aq)+2OH-(aq),Ksp=2×10-20。
Cu2+(aq)+2OH-(aq),Ksp=2×10-20。
①某CuSO4溶液里c(Cu2+)=0.02 mol·L-1,如果要使其生成 Cu(OH)2沉淀,应调整溶液的pH,使之大于_____ 。
②要使0.2 mol·L-1CuSO4溶液中的Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为_____ 。
(3)重金属离子会对河流和海洋造成严重污染。某化工厂废水(pH=2.0)中含有Ag+、Pb2+等重金属离子,其浓度约为0.01 mol/L,排放前拟用沉淀法除去这两种离子,查找有关数据如下:
①你认为往废水中加入_____ (填字母),沉淀效果最好。
A.NaOH B.Na2S C.KI D.Ca(OH)2
②如果用生石灰处理上述废水,使溶液的pH=8,处理后废水中c(Pb2+)=_____ 。
(1)某温度下,纯水中的c(OH-)=1×10-6 mol/L,则此时c(H+)为
(2)已知:Cu(OH)2(s)
 Cu2+(aq)+2OH-(aq),Ksp=2×10-20。
Cu2+(aq)+2OH-(aq),Ksp=2×10-20。①某CuSO4溶液里c(Cu2+)=0.02 mol·L-1,如果要使其生成 Cu(OH)2沉淀,应调整溶液的pH,使之大于
②要使0.2 mol·L-1CuSO4溶液中的Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为
(3)重金属离子会对河流和海洋造成严重污染。某化工厂废水(pH=2.0)中含有Ag+、Pb2+等重金属离子,其浓度约为0.01 mol/L,排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S |
| Ksp | 8.3×10-12 | 5.6×10-8 | 6.3×10-50 |
| 难溶电解质 | PbI2 | Pb(OH)2 | PbS |
| Ksp | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
A.NaOH B.Na2S C.KI D.Ca(OH)2
②如果用生石灰处理上述废水,使溶液的pH=8,处理后废水中c(Pb2+)=
您最近一年使用:0次
2 . 完成下列问题。
(1)化学键的键能是形成(或断裂)1 mol化学键时释放(或吸收)的能量。以下是部分共价键键能的数据:H-S:364 kJ·mol-1,S-S:266 kJ·mol-1,S=O:522 kJ·mol-1,H-O:463 kJ·mol-1,试根据这些数据计算下列反应的反应热:2H2S(g)+SO2(g)= 3S(s)+2H2O(l) ΔH=-Q kJ·mol-1,反应产物中的S实为S8,实际分子是一个八元环状分子(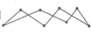 ),则Q=
),则Q=______ 。
(2)已知反应aA(g)+bB(g) cC(g),某温度下,在2 L的密闭容器中投入一定量的A、B,两种气体的物的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2 L的密闭容器中投入一定量的A、B,两种气体的物的量浓度随时间变化的曲线如图所示。_____ 。
②经测定,前4 s内v(C)=0.05 mol·L-1·s-1,则该反应的化学方程式为______ 。
③若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:v(A)=0.3 mol·L-1·s-1,乙:v(B)=0.12 mol·L-1·s-1,丙:v(C)=9.6 mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为_______ 。
(3)向某容积不变的密闭容器中充入一定量的NO2,发生反应2NO2(g) N2O4(g) ΔH<0,达到平衡后,若分别单独改变下列条件,下列判断正确的是_____。
N2O4(g) ΔH<0,达到平衡后,若分别单独改变下列条件,下列判断正确的是_____。
(4)工业上常用甲烷水蒸气重整制备氢气,体系中发生如下反应:
Ⅰ.CH4(g)+H2O(g) CO(g)+3H2(g) Ⅱ.CO(g)+H2O(g)
CO(g)+3H2(g) Ⅱ.CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)
①下列操作中,能提高CH4(g)平衡转化率的是____ (填标号)。
A.增加CH4 (g)用量 B.恒温恒压下通入惰性气体
C.移除CO(g) D.加入催化剂
②恒温恒压条件下,1 mol CH4 (g)和1 mol H2O(g)反应达平衡时,CH4 (g)的转化率为α,CO2(g)的物质的量为b mol,则反应Ⅰ的平衡常数Kx=____ [写出含有α、b的计算式;对于反应mA(g)+nB(g) pC(g)+qD(g),Kx=
pC(g)+qD(g),Kx=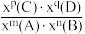 ,x为物质的量分数]。
,x为物质的量分数]。
(1)化学键的键能是形成(或断裂)1 mol化学键时释放(或吸收)的能量。以下是部分共价键键能的数据:H-S:364 kJ·mol-1,S-S:266 kJ·mol-1,S=O:522 kJ·mol-1,H-O:463 kJ·mol-1,试根据这些数据计算下列反应的反应热:2H2S(g)+SO2(g)= 3S(s)+2H2O(l) ΔH=-Q kJ·mol-1,反应产物中的S实为S8,实际分子是一个八元环状分子(
 ),则Q=
),则Q=(2)已知反应aA(g)+bB(g)
 cC(g),某温度下,在2 L的密闭容器中投入一定量的A、B,两种气体的物的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2 L的密闭容器中投入一定量的A、B,两种气体的物的量浓度随时间变化的曲线如图所示。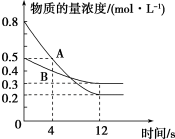
②经测定,前4 s内v(C)=0.05 mol·L-1·s-1,则该反应的化学方程式为
③若上述反应分别在甲、乙、丙三个相同的密闭容器中进行,经同一段时间后,测得三个容器中的反应速率分别为甲:v(A)=0.3 mol·L-1·s-1,乙:v(B)=0.12 mol·L-1·s-1,丙:v(C)=9.6 mol·L-1·min-1,则甲、乙、丙三个容器中反应速率由快到慢的顺序为
(3)向某容积不变的密闭容器中充入一定量的NO2,发生反应2NO2(g)
 N2O4(g) ΔH<0,达到平衡后,若分别单独改变下列条件,下列判断正确的是_____。
N2O4(g) ΔH<0,达到平衡后,若分别单独改变下列条件,下列判断正确的是_____。| A.升高温度,混合气体的颜色变浅 |
| B.通入NO2,化学平衡常数增大 |
| C.通入NO2,重新达到平衡后混合气体的平均相对分子质量增大 |
| D.增大压强,平衡向正反应方向移动,混合气体的颜色变浅 |
Ⅰ.CH4(g)+H2O(g)
 CO(g)+3H2(g) Ⅱ.CO(g)+H2O(g)
CO(g)+3H2(g) Ⅱ.CO(g)+H2O(g)  CO2(g)+H2(g)
CO2(g)+H2(g)①下列操作中,能提高CH4(g)平衡转化率的是
A.增加CH4 (g)用量 B.恒温恒压下通入惰性气体
C.移除CO(g) D.加入催化剂
②恒温恒压条件下,1 mol CH4 (g)和1 mol H2O(g)反应达平衡时,CH4 (g)的转化率为α,CO2(g)的物质的量为b mol,则反应Ⅰ的平衡常数Kx=
 pC(g)+qD(g),Kx=
pC(g)+qD(g),Kx=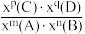 ,x为物质的量分数]。
,x为物质的量分数]。
您最近一年使用:0次
名校
解题方法
3 . 配平下列方程式或完成下列问题
(1)______ClO-+______Fe(OH)3+_______OH-=______Cl-+______FeO +______H2O。
+______H2O。________ 。
(2)______FeS2+______O2 ______Fe2O3+______SO2。
______Fe2O3+______SO2。________ 。
(3)____KI+____KIO3+____H2SO4=____I2+____K2SO4+____H2O。________ 。
(4)____S+____KOH=____K2S+____K2SO3+____H2O。________ 。
(5)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:
KOCN+______Cl2+______ =______K2CO3+______N2+______KCl+______
=______K2CO3+______N2+______KCl+______ 。
。________ 。
(6)在酸性条件下,NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为_____________ 。
(7)黑火药的成分是硝酸钾、硫磺、木炭。当加热或点燃时会发生剧烈反应而爆炸。生成物中硫元素变为最低价,碳、氮两元素均变成空气中常见的气体。
写出有关反应的化学方程式:___________________________ 。
(8)以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”,将烟气中的 、NO转化为:
、NO转化为: 、
、 。当烟气中
。当烟气中 和NO的体积比为2:1时,其离子方程式为
和NO的体积比为2:1时,其离子方程式为___________ 。
(9)研究发现钼酸钠可减缓金属的腐蚀速率。工业上利用钼精矿(主要成分是不溶于水的MoS2,含少量重金属化合物)制备钼酸钠晶体(Na2MoO4·2H2O)的途径如图所示:
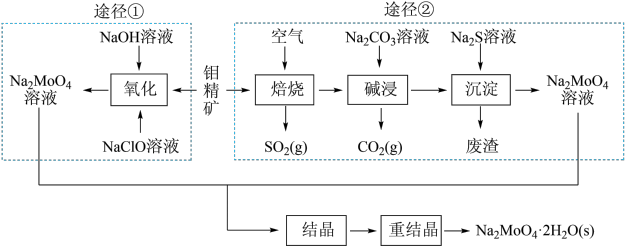
回答下列问题:
途径①制备钼酸钠溶液,同时有SO 生成,该反应的离子方程式为
生成,该反应的离子方程式为_____________ 。
(1)______ClO-+______Fe(OH)3+_______OH-=______Cl-+______FeO
 +______H2O。
+______H2O。(2)______FeS2+______O2
 ______Fe2O3+______SO2。
______Fe2O3+______SO2。(3)____KI+____KIO3+____H2SO4=____I2+____K2SO4+____H2O。
(4)____S+____KOH=____K2S+____K2SO3+____H2O。
(5)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平下列化学方程式:
KOCN+______Cl2+______
 =______K2CO3+______N2+______KCl+______
=______K2CO3+______N2+______KCl+______ 。
。(6)在酸性条件下,NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为
(7)黑火药的成分是硝酸钾、硫磺、木炭。当加热或点燃时会发生剧烈反应而爆炸。生成物中硫元素变为最低价,碳、氮两元素均变成空气中常见的气体。
写出有关反应的化学方程式:
(8)以NaClO溶液作为吸收剂进行一体化“脱硫”、“脱硝”,将烟气中的
 、NO转化为:
、NO转化为: 、
、 。当烟气中
。当烟气中 和NO的体积比为2:1时,其离子方程式为
和NO的体积比为2:1时,其离子方程式为(9)研究发现钼酸钠可减缓金属的腐蚀速率。工业上利用钼精矿(主要成分是不溶于水的MoS2,含少量重金属化合物)制备钼酸钠晶体(Na2MoO4·2H2O)的途径如图所示:

回答下列问题:
途径①制备钼酸钠溶液,同时有SO
 生成,该反应的离子方程式为
生成,该反应的离子方程式为
您最近一年使用:0次
名校
4 . ①现有 铜镁合金与一定量浓硝酸恰好完全反应,得到
铜镁合金与一定量浓硝酸恰好完全反应,得到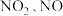 的混合气体(不考虑
的混合气体(不考虑 等其它气体)体积为
等其它气体)体积为 (本题气体体积均为标准状况下):②这些气体与一定体积氧气混合后通入水中,所有气体完全被水吸收生成硝酸。若向①所得溶液中加入
(本题气体体积均为标准状况下):②这些气体与一定体积氧气混合后通入水中,所有气体完全被水吸收生成硝酸。若向①所得溶液中加入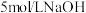 溶液至金属离子恰好完全沉淀,消耗
溶液至金属离子恰好完全沉淀,消耗 溶液的体积是
溶液的体积是 。下列说法不正确的是
。下列说法不正确的是
 铜镁合金与一定量浓硝酸恰好完全反应,得到
铜镁合金与一定量浓硝酸恰好完全反应,得到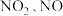 的混合气体(不考虑
的混合气体(不考虑 等其它气体)体积为
等其它气体)体积为 (本题气体体积均为标准状况下):②这些气体与一定体积氧气混合后通入水中,所有气体完全被水吸收生成硝酸。若向①所得溶液中加入
(本题气体体积均为标准状况下):②这些气体与一定体积氧气混合后通入水中,所有气体完全被水吸收生成硝酸。若向①所得溶液中加入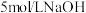 溶液至金属离子恰好完全沉淀,消耗
溶液至金属离子恰好完全沉淀,消耗 溶液的体积是
溶液的体积是 。下列说法不正确的是
。下列说法不正确的是A.①中参加反应的硝酸是 | B.②中消耗氧气的体积是 |
C.铜镁合金中镁的质量为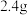 | D.混合气体中 体积为 体积为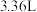 |
您最近一年使用:0次
2023-05-11更新
|
875次组卷
|
5卷引用:宁夏石嘴山市第三中学2023-2024学年高三上学期开学检测化学试题
5 . 铁是人类较早使用的金属之一,回答下列问题。
(1)下列所含铁元素只有还原性的物质是_______ (填字母)。
A.Fe B. C.
C.
(2)血红蛋白(Hb)中的铁元素呈正二价,能与 分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。
分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。 因具有氧化性能使血红蛋白丧失与
因具有氧化性能使血红蛋白丧失与 结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是
结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是_______ (填字母)。
A.药品美蓝发生还原反应 B.药品美蓝是还原剂 C.药品美蓝被还原
(3)电子工业常用30%的 溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出
溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出 溶液与铜发生反应的离子方程式
溶液与铜发生反应的离子方程式_______ ,若向 和
和 的混合溶液中加入一定量铁粉,最终有固体剩余,则下列有关说法中正确的是
的混合溶液中加入一定量铁粉,最终有固体剩余,则下列有关说法中正确的是_______ (填字母)。
A.固体中一定有铜 B.固体中一定有铁 C.溶液中一定有 D.溶液中一定有
D.溶液中一定有
(4)高铁酸钾( )是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒:
)是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平该反应的离子方程式
。写出并配平该反应的离子方程式_______ ;若反应过程中转移了0.3mol电子,则还原产物的物质的量为_______ mol。
(5)某“铁基脱氧剂”的主要成分是还原Fe粉,使用一段时间后会部分变质为 。将一包使用过一段时间后的脱氧剂用稀盐酸浸泡,浸泡过程中粉末表面有大量细小无色气泡产生。
。将一包使用过一段时间后的脱氧剂用稀盐酸浸泡,浸泡过程中粉末表面有大量细小无色气泡产生。
①溶液中的反应有: 、
、 、
、_______ (写离子方程式)。
②甲同学用如下方法验证了溶液中 的存在:取少量上层清液,加入氨水,出现白色沉淀,并很快变为灰绿色,将沉淀倾倒在滤纸上,沉淀逐渐变为红褐色。出现白色沉淀的离子反应方程式为
的存在:取少量上层清液,加入氨水,出现白色沉淀,并很快变为灰绿色,将沉淀倾倒在滤纸上,沉淀逐渐变为红褐色。出现白色沉淀的离子反应方程式为_____ ;滤纸上沉淀变化的反应方程式为_______ 。
③乙同学另取少量上层溶液,滴加氯水后溶液呈黄色,再滴加KSCN溶液,溶液变红。滴加氯水后溶液变黄的离子方程式为_______ 。
(1)下列所含铁元素只有还原性的物质是
A.Fe B.
 C.
C.
(2)血红蛋白(Hb)中的铁元素呈正二价,能与
 分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。
分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。 因具有氧化性能使血红蛋白丧失与
因具有氧化性能使血红蛋白丧失与 结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是
结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是A.药品美蓝发生还原反应 B.药品美蓝是还原剂 C.药品美蓝被还原
(3)电子工业常用30%的
 溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出
溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出 溶液与铜发生反应的离子方程式
溶液与铜发生反应的离子方程式 和
和 的混合溶液中加入一定量铁粉,最终有固体剩余,则下列有关说法中正确的是
的混合溶液中加入一定量铁粉,最终有固体剩余,则下列有关说法中正确的是A.固体中一定有铜 B.固体中一定有铁 C.溶液中一定有
 D.溶液中一定有
D.溶液中一定有
(4)高铁酸钾(
 )是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒:
)是一种新型、高效、多功能绿色水处理剂。工业上湿法制备高铁酸钾的反应体系中有六种微粒: 、
、 、
、 、
、 、
、 、
、 。写出并配平该反应的离子方程式
。写出并配平该反应的离子方程式(5)某“铁基脱氧剂”的主要成分是还原Fe粉,使用一段时间后会部分变质为
 。将一包使用过一段时间后的脱氧剂用稀盐酸浸泡,浸泡过程中粉末表面有大量细小无色气泡产生。
。将一包使用过一段时间后的脱氧剂用稀盐酸浸泡,浸泡过程中粉末表面有大量细小无色气泡产生。①溶液中的反应有:
 、
、 、
、②甲同学用如下方法验证了溶液中
 的存在:取少量上层清液,加入氨水,出现白色沉淀,并很快变为灰绿色,将沉淀倾倒在滤纸上,沉淀逐渐变为红褐色。出现白色沉淀的离子反应方程式为
的存在:取少量上层清液,加入氨水,出现白色沉淀,并很快变为灰绿色,将沉淀倾倒在滤纸上,沉淀逐渐变为红褐色。出现白色沉淀的离子反应方程式为③乙同学另取少量上层溶液,滴加氯水后溶液呈黄色,再滴加KSCN溶液,溶液变红。滴加氯水后溶液变黄的离子方程式为
您最近一年使用:0次
名校
解题方法
6 . 向一定量的CuO、 的混合物中加入200mL,2mol/L的盐酸,恰好使混合物完全溶解,若用过量CO在高温下还原相同质量的原混合物,固体减少的质量为
的混合物中加入200mL,2mol/L的盐酸,恰好使混合物完全溶解,若用过量CO在高温下还原相同质量的原混合物,固体减少的质量为
 的混合物中加入200mL,2mol/L的盐酸,恰好使混合物完全溶解,若用过量CO在高温下还原相同质量的原混合物,固体减少的质量为
的混合物中加入200mL,2mol/L的盐酸,恰好使混合物完全溶解,若用过量CO在高温下还原相同质量的原混合物,固体减少的质量为| A.6.4g | B.3.2g | C.1.6g | D.0.8g |
您最近一年使用:0次
2023-02-20更新
|
296次组卷
|
2卷引用:宁夏银川市第二中学2022-2023学年高一下学期开学教学质量检测化学试题
名校
解题方法
7 . 高分子树脂M具有较好的吸水性,其合成路线如图:
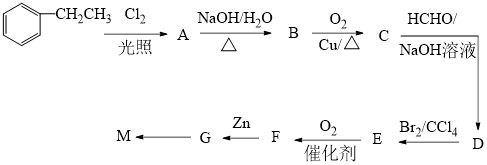
已知:i、—CHO+—CH2CHO
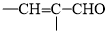 ;
;
ii、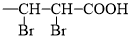
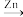 —CH=CH—COOH
—CH=CH—COOH
(1)C的名称为___ ,D中的官能团名称为___ ,M的结构简式为___ 。
(2)由A生成B的化学方程式为___ 。
(3)上述合成路线中,D→E转化在合成M中的作用为___ 。
(4)下列叙述正确的是____ (填序号)。
(5)H是G的同系物,且与G相差一个碳原子,则同时满足下列条件的H的同分异构体共有___ 种。(不考虑立体异构)
①与G具有相同的官能团②苯环上只有两个取代基
(6)根据上述合成路线和信息,以苯乙醛为原料(其他无机试剂任选)设计制备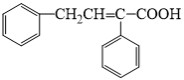 的合成路线:
的合成路线:___ 。

已知:i、—CHO+—CH2CHO

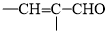 ;
;ii、
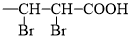
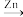 —CH=CH—COOH
—CH=CH—COOH(1)C的名称为
(2)由A生成B的化学方程式为
(3)上述合成路线中,D→E转化在合成M中的作用为
(4)下列叙述正确的是
| A.F能与NaHCO3反应生成CO2 |
| B.F能发生水解反应和消去反应 |
| C.F能聚合成高分子化合物 |
| D.1molF最多消耗2molNaOH |
①与G具有相同的官能团②苯环上只有两个取代基
(6)根据上述合成路线和信息,以苯乙醛为原料(其他无机试剂任选)设计制备
 的合成路线:
的合成路线:
您最近一年使用:0次
名校
解题方法
8 . 下列各组离子能大量共存的是( )
①“84”消毒液的水溶液中:Fe2+、Cl-、Ca2+、Na+
②加入KSCN显红色的溶液:K+、NH 、Cl-、S2-
、Cl-、S2-
③常温下能够与金属Cu反应放出NO气体的溶液:Fe3+、Al3+、SO 、K+
、K+
④pH=2的溶液中:NH 、Na+、Cl-、Cu2+
、Na+、Cl-、Cu2+
⑤无色溶液中:K+、CH3COO-、HCO 、MnO
、MnO
①“84”消毒液的水溶液中:Fe2+、Cl-、Ca2+、Na+
②加入KSCN显红色的溶液:K+、NH
 、Cl-、S2-
、Cl-、S2-③常温下能够与金属Cu反应放出NO气体的溶液:Fe3+、Al3+、SO
 、K+
、K+④pH=2的溶液中:NH
 、Na+、Cl-、Cu2+
、Na+、Cl-、Cu2+⑤无色溶液中:K+、CH3COO-、HCO
 、MnO
、MnO
| A.③④ | B.①③ | C.①⑤ | D.②③ |
您最近一年使用:0次
2020-08-24更新
|
439次组卷
|
2卷引用:宁夏吴忠市吴忠中学2020-2021学年高二上学期开学分科考试化学试题
11-12高一上·辽宁沈阳·期中
名校
解题方法
9 . 有一真空瓶质量为m1,该瓶充入空气后质量为m2。在相同状况下,若改为充入某气体A时,总质量为m3。则A的相对分子质量是
| A.29 m2/m1 | B.29 m3/m1 |
| C.29(m2-m1)/(m3-m1) | D.29(m3-m1)/(m2-m1) |
您最近一年使用:0次
2020-05-09更新
|
2260次组卷
|
12卷引用:2016-2017学年宁夏吴忠中学高二上学期开学考试化学试卷
2016-2017学年宁夏吴忠中学高二上学期开学考试化学试卷(已下线)2011-2012学年辽宁省沈阳同泽女中高一上学期期中考试化学试卷(已下线)2011-2012学年山东省微山一中高一上学期期中考试化学试卷【全国百强校】四川省雅安市雅安中学2018-2019学年高一上学期期中考试化学试题四川省雅安中学2019-2020学年高一上学期期中考试化学试题江西省南昌市进贤一中2019-2020学年高一上学期期中考试化学试题福建省莆田第一中学2019-2020学年高一上学期第一次月考化学试题湖北省黄梅一中2019--2020学年高一下学期期中考试化学试题人教版(2019)高一必修第一册 模块综合测评-B卷吉林省白城市洮南一中2020-2021学年高一上学期期中考试化学试题河北省沧州市第一中学2020-2021学年高一上学期第一次月考化学试题四川省成都市第十二中学2020-2021学年高一上学期十月月考化学试题
14-15高三上·上海黄浦·期末
名校
解题方法
10 . 向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5 L,固体物质完全反应,生成NO和Cu(NO3)2。在所得溶液中加入1.0 mol/L的NaOH溶液1.0 L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2g,下列说法不正确的是
| A.Cu与Cu2O的物质的量之比为1:2 |
| B.硝酸的物质的量浓度为2.4 mol/L |
| C.产生的NO在标准状况下的体积为4.48 L |
| D.Cu、Cu2O与硝酸反应后剩余HNO3的物质的量为0.2 mol |
您最近一年使用:0次
2020-03-24更新
|
223次组卷
|
3卷引用:宁夏吴忠中学2023-2024学年高三上学期开学第一次月考化学试题



