名校
解题方法
1 . 某固体混合物可能由 、
、 、FeS、
、FeS、 、
、 、
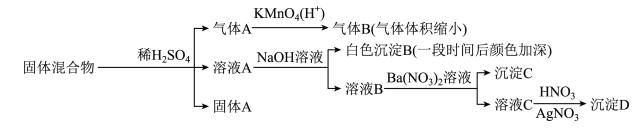
、 中的若干种物质组成,设计部分实验方案探究该固体混合物的成分,所加试剂均过量,下列说法正确的是
中的若干种物质组成,设计部分实验方案探究该固体混合物的成分,所加试剂均过量,下列说法正确的是
 、
、 、FeS、
、FeS、 、
、 、
、 中的若干种物质组成,设计部分实验方案探究该固体混合物的成分,所加试剂均过量,下列说法正确的是
中的若干种物质组成,设计部分实验方案探究该固体混合物的成分,所加试剂均过量,下列说法正确的是
A.气体A中一定含有 | B.固体A中一定含有S和 |
C.该固体混合物至少含 和FeS中的一种 和FeS中的一种 | D.该固体混合物中一定含有 、 、 、 、 |
您最近一年使用:0次
2023-09-27更新
|
734次组卷
|
5卷引用:吉林省四平市第一高级中学2023-2024学年高三上学期10月月考化学试题
名校
2 . T℃时,在密闭容器中进行的反应:COCl2(g) ⇌ CO(g)+Cl2(g) △H=+108KJ/mol,在4min、10min、14min时均只改变影响平衡的一个条件,各物质的浓度变化如图所示,下列说法正确的是
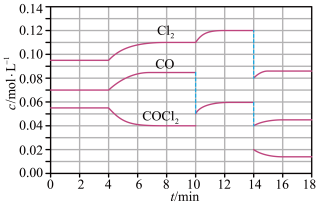

| A.4min时降低温度,10min时充入Cl2,14min时增大容器的体积 |
| B.平衡常数K2min<K9min<K13min |
| C.4min~8min COCl2平均反应速率为0.01mol(L·min) |
| D.若T℃时,起始向2L的恒容密闭容器中充入COCl2、Cl2、CO均为0.20 mol,则达到平衡前,v正>v逆 |
您最近一年使用:0次
2020-08-14更新
|
1923次组卷
|
4卷引用:吉林省四平市普通高中2021-2022学年高二上学期期中考试化学试题
3 . 钕铁硼磁铁是目前为止具有最强磁力的永久磁铁。生产钕铁硼磁铁的主要原材料有稀土金属钕、高纯铁、铝、硼等。回答下列问题:
(1)钕(Nd)为60号元素,在周期表中位于第_________ 周期。基态硼原子中占据最高能级的电子,电子云轮廓图形状为_______ 。铁离子的电子排布式__________________
(2)实验测得AlCl3的实际存在形式为Al2Cl6,其分子的球棍模型如下图所示:

①分子中A1原子采取____ 杂化。Al2Cl6属于____ 分子(填“极性”或“非极性”)。
②AlCl3与过量NaOH溶液反应生成Na[Al(OH)4],[A1(OH)4]-中存在的化学键有_________ (填选项字母)。
A.离子键 B.共价键 C.配位键 D.金属键 E.氢键
(3)工业上可用电解熔融的FeO、Fe2O3冶炼高纯铁。基态Fe2+的价电子排布图(轨道表达式)为______________ ;用物质结构知识说明Fe2+容易被氧化成Fe3+的原因:________________________ 。
(4)氮化铁晶体的晶胞结构如图1所示。该晶体中铁、氮的微粒个数之比为_____ 。

(5)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm—3,NA代表阿伏加 德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为_________ ;Fe2+与O2—的最短核间距为_____________ pm。
(1)钕(Nd)为60号元素,在周期表中位于第
(2)实验测得AlCl3的实际存在形式为Al2Cl6,其分子的球棍模型如下图所示:

①分子中A1原子采取
②AlCl3与过量NaOH溶液反应生成Na[Al(OH)4],[A1(OH)4]-中存在的化学键有
A.离子键 B.共价键 C.配位键 D.金属键 E.氢键
(3)工业上可用电解熔融的FeO、Fe2O3冶炼高纯铁。基态Fe2+的价电子排布图(轨道表达式)为
(4)氮化铁晶体的晶胞结构如图1所示。该晶体中铁、氮的微粒个数之比为

(5)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm—3,NA代表阿伏加 德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为
您最近一年使用:0次



