1 . 某实验小组欲通过加热蒸发KNO3溶液的方法获得KNO3固体。已知KNO3固体在一定温度下能够发生反应:2KNO3 2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
【查阅资料】
ⅰ.AgNO2是微溶于水的白色(略带黄色)固体
ⅱ.KNO2能在酸性条件下与KI反应,生成I2
【实验过程】
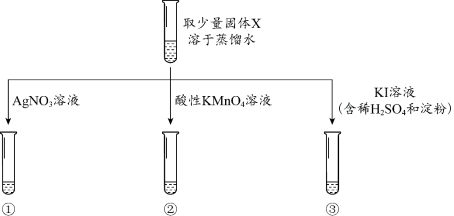
【分析解释】
(1)实验①中,观察到有少量白色沉淀生成,该白色沉淀是_______ 。
(2)实验②中,观察到酸性KMnO4溶液紫红色褪去,利用对比实验排除了稀释对溶液颜色变化的影响。补全该反应的离子方程式:2MnO + 5NO
+ 5NO + 6H+ = 2Mn2+ +
+ 6H+ = 2Mn2+ +_______ + 3H2O
(3)实验③中,观察到溶液变为蓝色。实验③中选择KI溶液的依据是_______ (填字母)。
a.KNO2具有氧化性,KI具有还原性
b.KNO2具有还原性,KI具有氧化性
【反思评价】
(4)综合上述实验,甲同学认为,实验①、②、③均可以证明固体X中含有KNO2;乙同学认为,通过实验③不能证明固体X中含有KNO2。乙同学的理由是_______ 。
 2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。
2KNO2 + O2↑。为了探究加热蒸发所得固体X中是否含有KNO2,小组同学分别设计并完成了以下实验。【查阅资料】
ⅰ.AgNO2是微溶于水的白色(略带黄色)固体
ⅱ.KNO2能在酸性条件下与KI反应,生成I2
【实验过程】

【分析解释】
(1)实验①中,观察到有少量白色沉淀生成,该白色沉淀是
(2)实验②中,观察到酸性KMnO4溶液紫红色褪去,利用对比实验排除了稀释对溶液颜色变化的影响。补全该反应的离子方程式:2MnO
 + 5NO
+ 5NO + 6H+ = 2Mn2+ +
+ 6H+ = 2Mn2+ +(3)实验③中,观察到溶液变为蓝色。实验③中选择KI溶液的依据是
a.KNO2具有氧化性,KI具有还原性
b.KNO2具有还原性,KI具有氧化性
【反思评价】
(4)综合上述实验,甲同学认为,实验①、②、③均可以证明固体X中含有KNO2;乙同学认为,通过实验③不能证明固体X中含有KNO2。乙同学的理由是
您最近一年使用:0次
2022-04-15更新
|
290次组卷
|
2卷引用:北京市2021-2022学年高三年级下学期合格考(第一次)化学试题
名校
2 . 某化学兴趣小组利用如图装置制取并探究二氧化疏的性质。
(已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,部分夹持仪器已略去)
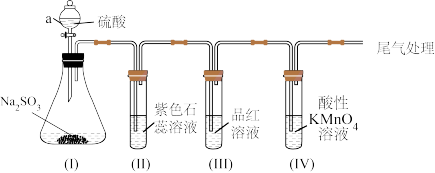
【实验探究】
(1)装置(I)仪器a的名称是___ 。
(2)实验进行一段时间后:
①装置(II)中观察到紫色石蕊试液颜色变为____ ,原因是SO2和水反应生成____ (填“H2SO3”或“H2SO4”)。
②装置(III)中品红溶液褪色,原因是____ 。
③装置(IV)中酸性KMnO4溶液褪色,证明SO2具有___ (填“氧化性”或“还原性”)。
(3)为防止SO2污染空气,尾气可用____ (填“NaOH溶液”或“稀硫酸”)吸收。
(4)用12.6gNa2SO3固体与足量硫酸反应,理论上可生成标准状况下SO2的体积为___ L。(已知Na2SO3的摩尔质量为126g•mol-1)
【实验拓展】
(5)将装置(IV)中酸性KMnO4溶液换成Na2S溶液,可观察到溶液中出现____ (填“白色”或“淡黄色”)浑浊,补充完整下面的离子方程式:____ 。
SO2+2S2-+4_____=3S↓+2H2O
【知识应用】
(6)二氧化硫可作为食品添加剂。查阅资料:
国家食品添加剂使用标准中二氧化硫最大使用量
说明在严格控制用量的情况下,二氧化硫可被添加到食品中作为漂白剂、防腐剂和____ (填“氧化剂”或“抗氧化剂”)。
(已知:Na2SO3+H2SO4=Na2SO4+SO2↑+H2O,部分夹持仪器已略去)

【实验探究】
(1)装置(I)仪器a的名称是
(2)实验进行一段时间后:
①装置(II)中观察到紫色石蕊试液颜色变为
②装置(III)中品红溶液褪色,原因是
③装置(IV)中酸性KMnO4溶液褪色,证明SO2具有
(3)为防止SO2污染空气,尾气可用
(4)用12.6gNa2SO3固体与足量硫酸反应,理论上可生成标准状况下SO2的体积为
【实验拓展】
(5)将装置(IV)中酸性KMnO4溶液换成Na2S溶液,可观察到溶液中出现
SO2+2S2-+4_____=3S↓+2H2O
【知识应用】
(6)二氧化硫可作为食品添加剂。查阅资料:
国家食品添加剂使用标准中二氧化硫最大使用量
| 食品名称 | 食糖 | 葡萄酒 | 水果干类 |
| SO2最大使用量 | 0.1g•kg-1 | 0.25g•kg-1 | 1g•kg-1 |
您最近一年使用:0次
2022-07-11更新
|
403次组卷
|
2卷引用:2022年01月福建省普通高中高一学业水平合格性考试真题化学试题
3 . 硫及其化合物广泛存在于自然界中,硫的部分化合物相互转化关系如图所示。回答下列问题: 与NaOH溶液反应可实现转化
与NaOH溶液反应可实现转化______ (填图中的序号),由该反应推断。 属于
属于______ (填“酸性”或“碱性”)氧化物。
(2)在转化②中,硫元素的化合价由+4价变成+6价,这表明 具有
具有______ (填“氧化性”或“还原性”)。
(3) 还具有氧化性,
还具有氧化性, 与
与 反应可生成
反应可生成______ (填化学式)和 ,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。
,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。
(4)在加热条件下,Cu与浓硫酸反应可实现转化③,该反应中 被Cu
被Cu______ (填“氧化”或“还原”)成 。
。 能使
能使______ (填试剂名称)溶液褪色,说明 具有漂白性,因此可用作草帽、纸张等的漂白剂。
具有漂白性,因此可用作草帽、纸张等的漂白剂。
(5)为检验Cu与浓硫酸反应后溶液中的 ,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴
,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴______ (填化学式)溶液,振荡,生成______ 色沉淀,则证明溶液中含有 ,生成该沉淀的离子反应方程式为
,生成该沉淀的离子反应方程式为______ 。
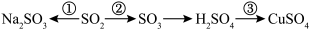
 与NaOH溶液反应可实现转化
与NaOH溶液反应可实现转化 属于
属于(2)在转化②中,硫元素的化合价由+4价变成+6价,这表明
 具有
具有(3)
 还具有氧化性,
还具有氧化性, 与
与 反应可生成
反应可生成 ,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。
,该反应可发生在火山口附近的大气中,这是自然界中硫单质存在于火山口附近的原因之一。(4)在加热条件下,Cu与浓硫酸反应可实现转化③,该反应中
 被Cu
被Cu 。
。 能使
能使 具有漂白性,因此可用作草帽、纸张等的漂白剂。
具有漂白性,因此可用作草帽、纸张等的漂白剂。(5)为检验Cu与浓硫酸反应后溶液中的
 ,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴
,取少量稀释后的溶液,加入少量稀盐酸,再滴加几滴 ,生成该沉淀的离子反应方程式为
,生成该沉淀的离子反应方程式为
您最近一年使用:0次
4 . 一种酒驾检测仪的工作原理是:人体呼出的气体若含有乙醇,将使检测仪中的 转化为+3价Cr的化合物,发生颜色变化。这一过程说明乙醇具有
转化为+3价Cr的化合物,发生颜色变化。这一过程说明乙醇具有
 转化为+3价Cr的化合物,发生颜色变化。这一过程说明乙醇具有
转化为+3价Cr的化合物,发生颜色变化。这一过程说明乙醇具有| A.碱性 | B.酸性 | C.氧化性 | D.还原性 |
您最近一年使用:0次
5 . 化学实验是研究和学习物质及其变化的基本方法,是科学探究的一种重要途径。浓硫酸与木炭在加热条件下可发生化学反应: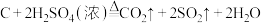 。为检验反应的产物,设计了如下图所示的实验。请基于实验事实回答下列问题:
。为检验反应的产物,设计了如下图所示的实验。请基于实验事实回答下列问题:
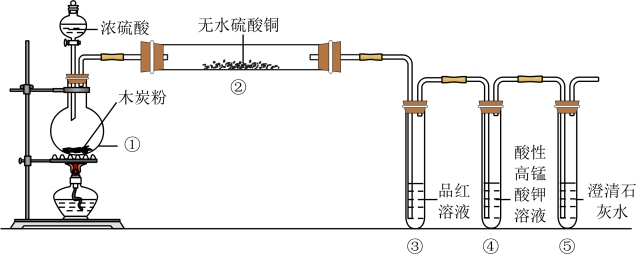
(1)装置中仪器①的名称是
(2)在浓硫酸与木炭的反应中,硫元素化合价的变化是
(3)装置②中的实验现象是白色粉末变蓝,这证明了产物中有
(4)装置③中的实验现象是品红溶液褪色,体现了二氧化硫的性质是
(5)装置④中酸性高锰酸钾溶液的作用是
(6)装置⑤中可观察到的实验现象是
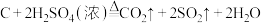 。为检验反应的产物,设计了如下图所示的实验。请基于实验事实回答下列问题:
。为检验反应的产物,设计了如下图所示的实验。请基于实验事实回答下列问题:
(1)装置中仪器①的名称是
| A.锥形瓶 | B.圆底烧瓶 | C.酒精灯 | D.分液漏斗 |
| A.升高 | B.降低 | C.不变 | D.无法判断 |
A. | B. | C. | D. 和 和 |
| A.酸性 | B.还原性 | C.氧化性 | D.漂白性 |
A.吸收 | B.吸收 | C.吸收 | D.检验 |
| A.澄清石灰水变蓝 | B.澄清石灰水变红 | C.澄清石灰水变浑浊 | D.澄清石灰水无现象 |
您最近一年使用:0次
6 . 为探究 的相关性质,某课外小组的同学设计如图所示装置进行实验(省略部分夹持装置)。下列实验事实与结论正确的是
的相关性质,某课外小组的同学设计如图所示装置进行实验(省略部分夹持装置)。下列实验事实与结论正确的是
 的相关性质,某课外小组的同学设计如图所示装置进行实验(省略部分夹持装置)。下列实验事实与结论正确的是
的相关性质,某课外小组的同学设计如图所示装置进行实验(省略部分夹持装置)。下列实验事实与结论正确的是
| 选项 | 实验事实 | 解释 |
| A | K处试管中有白色沉淀生成 | 白色沉淀为 |
| B | L处蘸有酸性 溶液的棉花褪色 溶液的棉花褪色 |  具有漂白性 具有漂白性 |
| C | M处蘸有 溶液的棉花上出现黄色固体 溶液的棉花上出现黄色固体 |  具有氧化性 具有氧化性 |
| D | N中滴有酚酞的NaOH溶液褪色 |  具有还原性 具有还原性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . “鱼浮灵”又称固态双氧水,主要成分为2Na2CO3·3H2O2,是水产品运输过程中常用的化学增氧剂。某小组为探究溶液酸碱性对H2O2溶液中溶解氧含量的影响,进行了如下实验。
[查阅资料]
i.Na2SO4 溶液显中性。
ii.pH<7时, pH越小,溶液的酸性越强; pH>7时,pH越大,溶液的碱性越强。
[进行实验]
向3个均盛有80 mL 4% H2O2溶液的烧杯中,依次加入20 mL的稀硫酸、Na2SO4 溶液、NaOH溶液,分别测定溶液的pH和溶解氧含量。实验记录如下表。
[分析解释]
(1)H2O2发生分解反应的产物是___________ 。
(2)由实验②可知,H2O2 溶液显___________ ( 填字母)。
a.酸性 b.碱性
(3)综合上述实验数据,可以得出的结论是____________ 。
[应用实践]
(4)结合上述实验分析,“鱼浮灵”可以提高水中溶解氧含量的可能原因有___________ 。
[查阅资料]
i.Na2SO4 溶液显中性。
ii.pH<7时, pH越小,溶液的酸性越强; pH>7时,pH越大,溶液的碱性越强。
[进行实验]
向3个均盛有80 mL 4% H2O2溶液的烧杯中,依次加入20 mL的稀硫酸、Na2SO4 溶液、NaOH溶液,分别测定溶液的pH和溶解氧含量。实验记录如下表。
| 实验编号 | ① | ② | ③ |
| 加入的试剂 | 稀硫酸 | Na2SO4溶液 | NaOH溶液 |
| pH | 0.44 | 5.97 | 11.74 |
| 溶解氧含量/ (mg·L-1) | 5.9 | 6.5 | 13.1 |
[分析解释]
(1)H2O2发生分解反应的产物是
(2)由实验②可知,H2O2 溶液显
a.酸性 b.碱性
(3)综合上述实验数据,可以得出的结论是
[应用实践]
(4)结合上述实验分析,“鱼浮灵”可以提高水中溶解氧含量的可能原因有
您最近一年使用:0次
解题方法
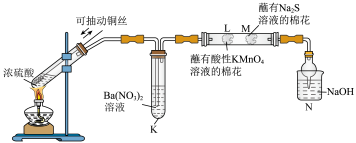
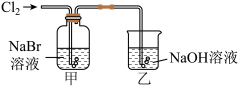
8 . 探究是创新的源泉,某化学兴趣小组进行了制备氯气并探究卤素性质的实验。
(1)用二氧化锰与浓盐酸制备氯气,应选择的发生装置是_______ (填字母代号),该反应体现了浓盐酸的酸性和_______ (填“氧化性”或“还原性”)。
①甲中反应的离子方程式为_______ ,向反应后的橙黄色溶液中滴加 KI-淀粉溶液,溶液变为蓝色,通过上述实验_______ (填“能”或“不能”)得出氧化性:Cl2>Br2>I2。
②乙装置中 NaOH 溶液的作用为_______ ,其主要反应的化学方程式为_______ 。
(1)用二氧化锰与浓盐酸制备氯气,应选择的发生装置是
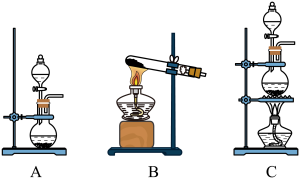
①甲中反应的离子方程式为
②乙装置中 NaOH 溶液的作用为
您最近一年使用:0次
9 . 黑木耳是常见食品,可以补充人体所必需的微量元素铁。某兴趣小组设计实验,检验黑木耳中的铁元素,实验流程如图:
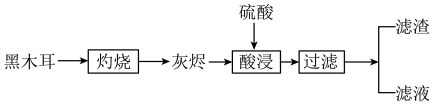
(1)灼烧黑木耳必须用到下列仪器中的___ (填字母)。
A.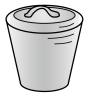 B.
B.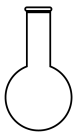 C.
C.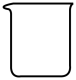 D.
D.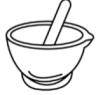
(2)灰烬中含有铁的氧化物以及钾、钙、硅等元素的化合物,酸浸的目的是___ 。
(3)取少许滤液于试管中,滴入几滴KSCN溶液,显红色,说明滤液中含有___ ;另取滤液检验,滤液能使KMnO4溶液紫色褪去,说明滤液中存在具有___ (填“氧化性”或“还原性”)的粒子。
(4)为进一步探究Fe3+和Fe2+的氧化性和还原性,该兴趣小组设计并进行如下实验,记录现象,完成实验报告。
(5)实验结束,离开实验室之前,下列做法正确的是___ (填字母)。
A.废弃药品直接倒入水池冲走 B.药品仪器归放
C.清洁实验仪器,打扫实验室卫生 D.关闭水电、门窗

(1)灼烧黑木耳必须用到下列仪器中的
A.
 B.
B. C.
C. D.
D.
(2)灰烬中含有铁的氧化物以及钾、钙、硅等元素的化合物,酸浸的目的是
(3)取少许滤液于试管中,滴入几滴KSCN溶液,显红色,说明滤液中含有
(4)为进一步探究Fe3+和Fe2+的氧化性和还原性,该兴趣小组设计并进行如下实验,记录现象,完成实验报告。
| 实验操作 | 实验现象 | 离子方程式 | 实验结论 |
| 向FeCl2溶液中添加新制氯水 | 溶液由浅绿色变为棕黄色 | 2Fe2++Cl2=2Fe3++2Cl- | ① |
| 向FeCl3溶液加入足量的铁粉 | 铁粉逐渐溶解,溶液由棕黄色变为浅绿色 | ② | Fe3+具有氧化性 |
A.废弃药品直接倒入水池冲走 B.药品仪器归放
C.清洁实验仪器,打扫实验室卫生 D.关闭水电、门窗
您最近一年使用:0次
2021-05-23更新
|
767次组卷
|
5卷引用:2021年1月广东省普通高中学业水平合格性考试化学试题
2021年1月广东省普通高中学业水平合格性考试化学试题(已下线)第12讲 铁、亚铁盐和铁盐-【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)(已下线)考点14 铁及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)广东省深圳市南头中学2021~2022学年下学期期中考试化学试题 (学考科目)(已下线)考点14 铁及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
10 . 化学是一门以实验为基础的自然科学,实验是科学探究的重要途径。请填写下列空白:
(1)下图是实验室制取气体的常用发生装置。
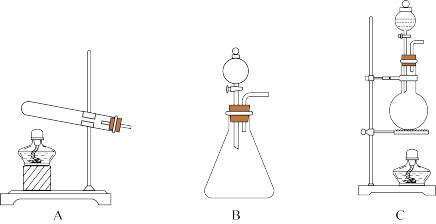
选用加热氯化铵和氢氧化钙固体混合物的方法制取氨气时,应选择的装置是___________ (填字母代号):反应的化学方程式为___________ :收集氨气时,常采用___________ 填“向上”或“向下”)排空气法。
(2)下图是探究二氧化硫性质的实验装置图。
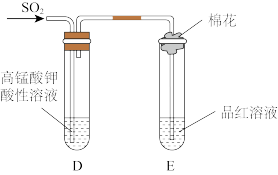
通入二氧化硫气体后,装置D中可观察到紫色的酸性高锰酸钾溶液颜色褪去,这体现了二氧化硫的___________ (填“氧化性”、“还原性”或“漂白性”);装置E中试管口放置的棉花中浸有NaOH溶液,其作用是___________ ;实验过程中装置E中可观察到的现象为___________ 。
(1)下图是实验室制取气体的常用发生装置。

选用加热氯化铵和氢氧化钙固体混合物的方法制取氨气时,应选择的装置是
(2)下图是探究二氧化硫性质的实验装置图。

通入二氧化硫气体后,装置D中可观察到紫色的酸性高锰酸钾溶液颜色褪去,这体现了二氧化硫的
您最近一年使用:0次



