名校
1 . 羟基自由基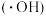 具有很强的氧化性,能将苯酚氧化为
具有很强的氧化性,能将苯酚氧化为 和
和 。我国科学家开发出如图所示装置,能实现制备氢气、处理含苯酚废水二位一体。下列说法正确的是
。我国科学家开发出如图所示装置,能实现制备氢气、处理含苯酚废水二位一体。下列说法正确的是
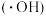 具有很强的氧化性,能将苯酚氧化为
具有很强的氧化性,能将苯酚氧化为 和
和 。我国科学家开发出如图所示装置,能实现制备氢气、处理含苯酚废水二位一体。下列说法正确的是
。我国科学家开发出如图所示装置,能实现制备氢气、处理含苯酚废水二位一体。下列说法正确的是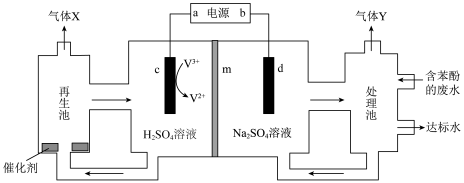
A.d电极的电极反应式: |
B.再生池中发生的反应: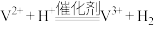 |
C.a为电源负极,m为阴离子交换膜, 能增强导电性 能增强导电性 |
D.气体X与Y在相同条件下的体积比为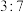 |
您最近一年使用:0次
2024-06-04更新
|
588次组卷
|
5卷引用:选择题11-14
(已下线)选择题11-142024届黑龙江省哈尔滨师范大学附属中学高三下学期三模化学试题东北三省三校2024届高三下学期5月第三次联合模拟考试化学试卷 (已下线)江苏省南京师范大学附属中学2024届高三下学期5月模拟化学试题福建省泉州第五中学2024届高三下学期适应性检测化学试题
名校
解题方法
2 . 氮气电解催化装置可以实现同时制备铵盐和硝酸盐,利用双极膜(M、N)将水解离成 、
、 ,还可以浓缩溶液(图中进、出气通道及部分反应均省略)。下列说法正确的是
,还可以浓缩溶液(图中进、出气通道及部分反应均省略)。下列说法正确的是

 、
、 ,还可以浓缩溶液(图中进、出气通道及部分反应均省略)。下列说法正确的是
,还可以浓缩溶液(图中进、出气通道及部分反应均省略)。下列说法正确的是
| A.a端的电势比b端高 |
| B.M、N分别为阴、阳离子交换膜 |
| C.相同时间内X、Y电极上消耗的氮气质量比为5∶3 |
D.阴极室的总反应为 |
您最近一年使用:0次
2024-06-04更新
|
186次组卷
|
4卷引用:选择题11-14
3 . 纯碱是一种重要的化工原料,具有广泛的用途。实验室利用氯化钠和碳酸氢铵制备纯碱并测定产品中碳酸氢钠的含量,具体步骤如下:
步骤i.精制氯化钠
取饱和粗盐水并加热,向其中加入饱和 溶液调节pH至11,有大量胶状沉淀析出;继续加热至沸,趁热过滤,滤液用盐酸调节pH至7。
溶液调节pH至11,有大量胶状沉淀析出;继续加热至沸,趁热过滤,滤液用盐酸调节pH至7。
步骤ⅱ.制备纯碱
在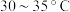 水浴条件下,向上述滤液中加入碳酸氢铵粉末,搅拌至反应完全;冷却后过滤得到碳酸氢钠晶体;用碳酸氢钠饱和过的酒精水溶液洗涤晶体;加热使其分解得到产品。
水浴条件下,向上述滤液中加入碳酸氢铵粉末,搅拌至反应完全;冷却后过滤得到碳酸氢钠晶体;用碳酸氢钠饱和过的酒精水溶液洗涤晶体;加热使其分解得到产品。
步骤ⅲ.产品中碳酸氢钠含量的测定
称取a g产品加水溶解,滴加指示剂M,用 盐酸逐滴滴定,并不断振荡,到达终点时消耗盐酸
盐酸逐滴滴定,并不断振荡,到达终点时消耗盐酸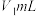 ;滴加指示剂N,继续用上述盐酸滴定,到达终点时消耗盐酸总体积
;滴加指示剂N,继续用上述盐酸滴定,到达终点时消耗盐酸总体积 。
。
已知:相关物质的溶解度如下
说明:“—”表示该物质在相应温度下已开始分解。
回答下列问题:
(1)步骤ⅰ中,胶状沉淀的成分为 ,生成该沉淀的离子方程式为
,生成该沉淀的离子方程式为________________ ;
(2)步骤ⅰ中,沉淀析出后需继续加热煮沸一段时间,其目的为________________ ;
(3)步骤ⅱ中,选择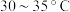 水浴的原因为
水浴的原因为________________ ;
(4)步骤ⅱ中,用碳酸氢钠饱和过的酒精水溶液洗涤晶体可除去的杂质为________________ ;
(5)步骤ⅲ中,用到的玻璃仪器除胶头滴管外还需要下列仪器中的________ (填仪器名称);________ ;滴定过程中,盐酸需要逐滴加入并不断振荡的原因为________________ ;选择指示剂N时,滴定终点溶液颜色变化为________________ ;
(7)产品中碳酸氢钠的质量分数为________ (用含字母的代数式表示)。
步骤i.精制氯化钠
取饱和粗盐水并加热,向其中加入饱和
 溶液调节pH至11,有大量胶状沉淀析出;继续加热至沸,趁热过滤,滤液用盐酸调节pH至7。
溶液调节pH至11,有大量胶状沉淀析出;继续加热至沸,趁热过滤,滤液用盐酸调节pH至7。步骤ⅱ.制备纯碱
在
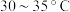 水浴条件下,向上述滤液中加入碳酸氢铵粉末,搅拌至反应完全;冷却后过滤得到碳酸氢钠晶体;用碳酸氢钠饱和过的酒精水溶液洗涤晶体;加热使其分解得到产品。
水浴条件下,向上述滤液中加入碳酸氢铵粉末,搅拌至反应完全;冷却后过滤得到碳酸氢钠晶体;用碳酸氢钠饱和过的酒精水溶液洗涤晶体;加热使其分解得到产品。步骤ⅲ.产品中碳酸氢钠含量的测定
称取a g产品加水溶解,滴加指示剂M,用
 盐酸逐滴滴定,并不断振荡,到达终点时消耗盐酸
盐酸逐滴滴定,并不断振荡,到达终点时消耗盐酸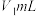 ;滴加指示剂N,继续用上述盐酸滴定,到达终点时消耗盐酸总体积
;滴加指示剂N,继续用上述盐酸滴定,到达终点时消耗盐酸总体积 。
。已知:相关物质的溶解度如下
温度 | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| 15.8 | 21.0 | 27.0 | — | — | — | — |
| 8.15 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | — |
| 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 |
回答下列问题:
(1)步骤ⅰ中,胶状沉淀的成分为
 ,生成该沉淀的离子方程式为
,生成该沉淀的离子方程式为(2)步骤ⅰ中,沉淀析出后需继续加热煮沸一段时间,其目的为
(3)步骤ⅱ中,选择
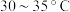 水浴的原因为
水浴的原因为(4)步骤ⅱ中,用碳酸氢钠饱和过的酒精水溶液洗涤晶体可除去的杂质为
(5)步骤ⅲ中,用到的玻璃仪器除胶头滴管外还需要下列仪器中的
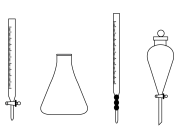
(7)产品中碳酸氢钠的质量分数为
您最近一年使用:0次
2024-06-01更新
|
159次组卷
|
3卷引用:T15-实验综合题
解题方法
4 . Be是一种重要的战略性金属,以铍矿石、方解石( )为原料制备硫酸铝铵和铍的工艺流程如下:
)为原料制备硫酸铝铵和铍的工艺流程如下: ,还含有
,还含有 ;铍玻璃体为混合物,主要成分为
;铍玻璃体为混合物,主要成分为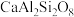 、
、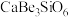 、
、 ,还含有
,还含有 和
和 .
.
(2) 具有两性;
具有两性; 时,
时,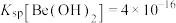 (已知:常温下,溶液中离子浓度低于
(已知:常温下,溶液中离子浓度低于 即可认为该离子被除尽);
即可认为该离子被除尽); .
.
回答下列问题:
(1)“配料熔化”时, 发生反应的化学方程式为
发生反应的化学方程式为________________ ;铍玻璃体属于________ (“晶体”或“非晶体”);
(2)“酸溶”时,从铍玻璃体进入到滤渣1中的元素为________ (填元素符号);
(3)“调pH”时,发生氧化还原反应的离子方程式为________________ ;
(4)“沉铍”时,需控制溶液的pH不低于________ 才能将 沉淀完全;若将氨水换成
沉淀完全;若将氨水换成 溶液也可沉铍,但需控制溶液的pH不能过高,否则会因生成
溶液也可沉铍,但需控制溶液的pH不能过高,否则会因生成________ (填化学式)导致铍的产率降低;
(5)“电解”时的工作原理如图所示,其中燃料电池负极的电极反应式为________________ ;该制铍工艺的缺点除能耗高外,还有________________ ;
 )为原料制备硫酸铝铵和铍的工艺流程如下:
)为原料制备硫酸铝铵和铍的工艺流程如下:
 ,还含有
,还含有 ;铍玻璃体为混合物,主要成分为
;铍玻璃体为混合物,主要成分为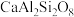 、
、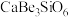 、
、 ,还含有
,还含有 和
和 .
.(2)
 具有两性;
具有两性; 时,
时,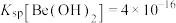 (已知:常温下,溶液中离子浓度低于
(已知:常温下,溶液中离子浓度低于 即可认为该离子被除尽);
即可认为该离子被除尽); .
.回答下列问题:
(1)“配料熔化”时,
 发生反应的化学方程式为
发生反应的化学方程式为(2)“酸溶”时,从铍玻璃体进入到滤渣1中的元素为
(3)“调pH”时,发生氧化还原反应的离子方程式为
(4)“沉铍”时,需控制溶液的pH不低于
 沉淀完全;若将氨水换成
沉淀完全;若将氨水换成 溶液也可沉铍,但需控制溶液的pH不能过高,否则会因生成
溶液也可沉铍,但需控制溶液的pH不能过高,否则会因生成(5)“电解”时的工作原理如图所示,其中燃料电池负极的电极反应式为

您最近一年使用:0次
2024-06-01更新
|
232次组卷
|
3卷引用:T16-工业流程题
名校
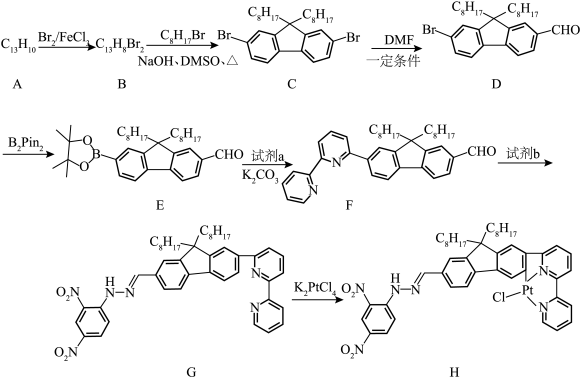
5 . 二联吡啶铂(Ⅱ)配合物(H)在传感器中有重要应用,一种合成路线如图。回答下列问题: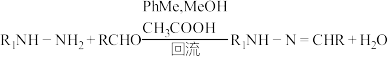
(1)有机物 的官能团的名称为
的官能团的名称为__________ 。
(2)写出 的反应方程式:
的反应方程式:______________ ,该反应的反应类型为__________ 。
(3)试剂 的结构简式为
的结构简式为__________ 。
(4)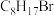 的同分异构体有多种,其中含有两个甲基的结构有
的同分异构体有多种,其中含有两个甲基的结构有__________ 种。
(5)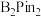 的结构为
的结构为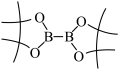 ,可由频哪醇(
,可由频哪醇(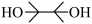 )和四(二甲氨基)二硼合成制得,频哪醇在浓硫酸作用下,加热,可制得分子式为
)和四(二甲氨基)二硼合成制得,频哪醇在浓硫酸作用下,加热,可制得分子式为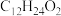 的物质,写出其结构:
的物质,写出其结构:__________ 。
(6)请从物质结构角度分析有机物 能与
能与 反应的原因:
反应的原因:______________ 。
(7)下列关于有机物 的说法错误的是__________(填标号)。
的说法错误的是__________(填标号)。
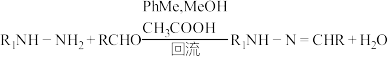
(1)有机物
 的官能团的名称为
的官能团的名称为(2)写出
 的反应方程式:
的反应方程式:(3)试剂
 的结构简式为
的结构简式为(4)
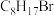 的同分异构体有多种,其中含有两个甲基的结构有
的同分异构体有多种,其中含有两个甲基的结构有(5)
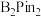 的结构为
的结构为 ,可由频哪醇(
,可由频哪醇( )和四(二甲氨基)二硼合成制得,频哪醇在浓硫酸作用下,加热,可制得分子式为
)和四(二甲氨基)二硼合成制得,频哪醇在浓硫酸作用下,加热,可制得分子式为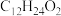 的物质,写出其结构:
的物质,写出其结构:(6)请从物质结构角度分析有机物
 能与
能与 反应的原因:
反应的原因:(7)下列关于有机物
 的说法错误的是__________(填标号)。
的说法错误的是__________(填标号)。A. 的配位数为4 的配位数为4 | B.含有手性碳原子 |
C. 原子的杂化方式为 原子的杂化方式为 | D.存在由 轨道“头碰头”形成的 轨道“头碰头”形成的 键 键 |
您最近一年使用:0次
2024-05-30更新
|
183次组卷
|
4卷引用:T18-有机推断题
名校
6 .  时,用氨水分别滴定浓度均为
时,用氨水分别滴定浓度均为 的
的 、
、 、
、 三种溶液,
三种溶液,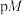 随
随 的变化关系如图所示[
的变化关系如图所示[ 表示负对数,
表示负对数, 表示
表示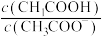 、
、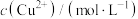 、
、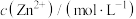 等],已知
等],已知 ,溶液中离子浓度小于
,溶液中离子浓度小于 可以认为已经除去。下列有关分析错误的是
可以认为已经除去。下列有关分析错误的是
 时,用氨水分别滴定浓度均为
时,用氨水分别滴定浓度均为 的
的 、
、 、
、 三种溶液,
三种溶液,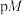 随
随 的变化关系如图所示[
的变化关系如图所示[ 表示负对数,
表示负对数, 表示
表示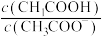 、
、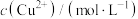 、
、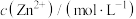 等],已知
等],已知 ,溶液中离子浓度小于
,溶液中离子浓度小于 可以认为已经除去。下列有关分析错误的是
可以认为已经除去。下列有关分析错误的是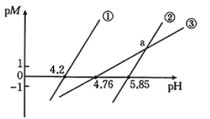
A. 时, 时, |
B. 点对应的 点对应的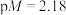 |
C.可通过调节 的方法除尽 的方法除尽 溶液(浓度为 溶液(浓度为 )中含有的 )中含有的 |
D.氨水过量时,均可形成 ( ( 表示 表示 或 或 ) ) |
您最近一年使用:0次
2024-05-30更新
|
175次组卷
|
4卷引用:选择题11-14
名校
7 . 常温下,二甲基亚砜( )为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸点为189℃。实验室模拟“
)为无色无臭且能与水混溶的透明液体,熔点为18.4℃,沸点为189℃。实验室模拟“ 氧化法”制备二甲基亚砜的装置如图所示(加热装置及夹持装置已省略)。
氧化法”制备二甲基亚砜的装置如图所示(加热装置及夹持装置已省略)。

①制备二甲基亚砜的反应原理为
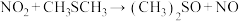 。
。②二甲基硫醚和二甲基亚砜的密度分别为
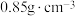 和
和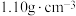 。
。③
 微热易分解为NO、
微热易分解为NO、 和
和 。
。实验过程:将仪器A中制得的气体通入15.00mL二甲基硫醚中,控制温度为60∼80℃,反应一段时间得到二甲基亚砜粗品,粗品经减压蒸馏后共收集到11.10mL二甲基亚砜纯品。回答下列问题:
(1)通入
 的目的是
的目的是a.碱石灰 b.
 c.硅胶
c.硅胶(2)冷凝管进出水的方向
(3)二甲基亚砜能与水混溶的原因可能为
(4)NaOH溶液吸收尾气中NO和
 生成亚硝酸盐的化学方程式为
生成亚硝酸盐的化学方程式为(5)本实验的产率是
您最近一年使用:0次
2024-05-29更新
|
257次组卷
|
6卷引用:T15-实验综合题
8 . 以天青石 (主要成分: 和炭粉焙烧后的水浸液为原料制备
和炭粉焙烧后的水浸液为原料制备  的流程如图所示。
的流程如图所示。 其中。
其中。  约为
约为  。
。
ii.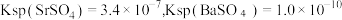 。
。
iii. Sr、Ba分别位于第5、6周期 A族。
A族。
下列说法错误的是
 和炭粉焙烧后的水浸液为原料制备
和炭粉焙烧后的水浸液为原料制备  的流程如图所示。
的流程如图所示。
 其中。
其中。  约为
约为  。
。ii.
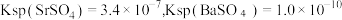 。
。iii. Sr、Ba分别位于第5、6周期
 A族。
A族。下列说法错误的是
A.“焙烧”烟气中可能含有CO和 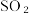 |
| B.“沉钡”后的滤液呈酸性 |
C.“沉钡”过程若  降到 降到  滤渣中混有 滤渣中混有  |
| D.硫酸锶的熔点高于硫酸钡 |
您最近一年使用:0次
名校
解题方法
9 . 由原子序数依次增大的短周期元素X、Y、Z、W、R组成的一种离子液体(其阳离子中五元环上5个原子共面),其结构如图。Z的最简单氢化物易液化,可用作制冷剂。W的氢化物的水溶液能腐蚀玻璃,Z、R为同一主族元素。下列说法错误的是
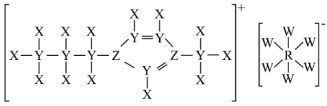
| A.电负性:W>Z>Y |
| B.该离子液体中的Z原子的杂化方式均为sp2 |
C.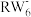 空间结构为正八面体形 空间结构为正八面体形 |
| D.最简单氢化物的沸点:Z<R |
您最近一年使用:0次
10 . 三氯化铝在有机催化、金属冶炼中应用广泛。某小组以铝土矿为原料制备无水 并测定其纯度,设计了如下实验方案。回答下列问题:
并测定其纯度,设计了如下实验方案。回答下列问题:
I. 的制备
的制备_______ 。
(2)步骤②通入 时用多孔球泡的目的是
时用多孔球泡的目的是_______ 。
(3)步骤④的操作为:在不断滴加_______ (填试剂名称)的条件下蒸发、结晶、过滤洗涤。
Ⅱ.无水 的制备
的制备
以 晶体制备无水
晶体制备无水 的装置如下图。已知
的装置如下图。已知 熔点为
熔点为 ,沸点为
,沸点为 ,遇水极易生成两种酸性气体。
,遇水极易生成两种酸性气体。 ,一段时间后,先加热装置
,一段时间后,先加热装置_______ (填“A”或“B”);装置B内发生反应的化学方程式为_______ 。
(5)装置E中碱石灰的作用有_______ 。
Ⅲ. 纯度的测定
纯度的测定
称取 产品,配成
产品,配成 溶液,取
溶液,取 于锥形瓶中,滴入
于锥形瓶中,滴入 溶液
溶液 滴(作指示剂),然后用
滴(作指示剂),然后用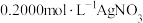 标准溶液滴定,经三次实验,平均消耗标准溶液
标准溶液滴定,经三次实验,平均消耗标准溶液 。
。
(6)产品的纯度为_______ (保留3位有效数字)。
(7)下列操作,会使测量结果偏低的是_______ 。
a.滴定过程中往锥形瓶中加入
b.达到滴定终点时俯视读数
c.滴定后滴定管尖嘴处有一液滴悬而未落
 并测定其纯度,设计了如下实验方案。回答下列问题:
并测定其纯度,设计了如下实验方案。回答下列问题:I.
 的制备
的制备
(2)步骤②通入
 时用多孔球泡的目的是
时用多孔球泡的目的是(3)步骤④的操作为:在不断滴加
Ⅱ.无水
 的制备
的制备以
 晶体制备无水
晶体制备无水 的装置如下图。已知
的装置如下图。已知 熔点为
熔点为 ,沸点为
,沸点为 ,遇水极易生成两种酸性气体。
,遇水极易生成两种酸性气体。
 ,一段时间后,先加热装置
,一段时间后,先加热装置(5)装置E中碱石灰的作用有
Ⅲ.
 纯度的测定
纯度的测定称取
 产品,配成
产品,配成 溶液,取
溶液,取 于锥形瓶中,滴入
于锥形瓶中,滴入 溶液
溶液 滴(作指示剂),然后用
滴(作指示剂),然后用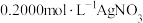 标准溶液滴定,经三次实验,平均消耗标准溶液
标准溶液滴定,经三次实验,平均消耗标准溶液 。
。(6)产品的纯度为
(7)下列操作,会使测量结果偏低的是
a.滴定过程中往锥形瓶中加入

b.达到滴定终点时俯视读数
c.滴定后滴定管尖嘴处有一液滴悬而未落
您最近一年使用:0次








