真题
名校
1 . 常温下 水溶液体系中存在反应:
水溶液体系中存在反应: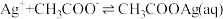 ,平衡常数为K。已初始浓度
,平衡常数为K。已初始浓度 ,所有含碳物种的摩尔分数与
,所有含碳物种的摩尔分数与 变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
 水溶液体系中存在反应:
水溶液体系中存在反应: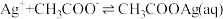 ,平衡常数为K。已初始浓度
,平衡常数为K。已初始浓度 ,所有含碳物种的摩尔分数与
,所有含碳物种的摩尔分数与 变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
变化关系如图所示(忽略溶液体积变化)。下列说法正确的是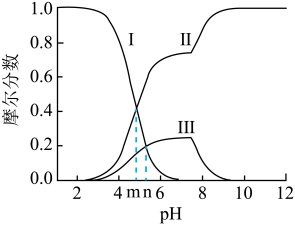
A.线Ⅱ表示 的变化情况 的变化情况 |
B. 的电离平衡常数 的电离平衡常数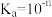 |
C. 时, 时,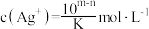 |
D. 时, 时, |
您最近一年使用:0次
昨日更新
|
530次组卷
|
3卷引用:2024年高考化学真题完全解读(山东卷)
2 . 以不同材料修饰的 为电极,一定浓度的
为电极,一定浓度的 溶液为电解液,采用电解和催化相结合的循环方式,可实现高效制
溶液为电解液,采用电解和催化相结合的循环方式,可实现高效制 和
和 ,装置如图所示。下列说法错误的是
,装置如图所示。下列说法错误的是
 为电极,一定浓度的
为电极,一定浓度的 溶液为电解液,采用电解和催化相结合的循环方式,可实现高效制
溶液为电解液,采用电解和催化相结合的循环方式,可实现高效制 和
和 ,装置如图所示。下列说法错误的是
,装置如图所示。下列说法错误的是
| A.电极a连接电源负极 |
B.加入Y的目的是补充 |
C.电解总反应式为 |
D.催化阶段反应产物物质的量之比 |
您最近一年使用:0次
昨日更新
|
560次组卷
|
3卷引用:2024年高考化学真题完全解读(山东卷)
真题
解题方法
3 . 下列化学用语或图示正确的是
A.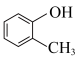 的系统命名:2-甲基苯酚 的系统命名:2-甲基苯酚 |
B. 分子的球棍模型: 分子的球棍模型: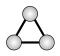 |
C.激发态H原子的轨道表示式: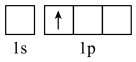 |
D.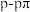 键形成的轨道重叠示意图: 键形成的轨道重叠示意图: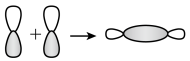 |
您最近一年使用:0次
4 . 化学品在食品工业中也有重要应用,下列说法错误的是
| A.活性炭可用作食品脱色剂 | B.铁粉可用作食品脱氧剂 |
| C.谷氨酸钠可用作食品增味剂 | D.五氧化二磷可用作食品干燥剂 |
您最近一年使用:0次
真题
解题方法
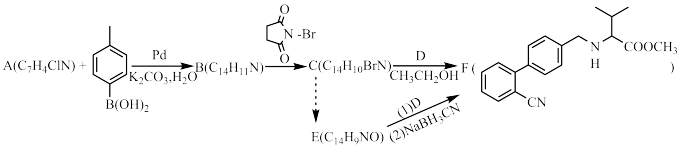
5 . 心血管药物缬沙坦中间体(F)的两条合成路线如下:
回答下列问题:
(1)A结构简式为_______ ;B→C反应类型为_______ 。
(2)C+D→F化学方程式为_______ 。
(3)E中含氧官能团名称为_______ ;F中手性碳原子有_______ 个。
(4)D的一种同分异构体含硝基和3种不同化学环境的氢原子(个数此为 ),其结构简式为
),其结构简式为_______ 。
(5)C→E的合成路线设计如下:
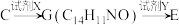
试剂X为_______ (填化学式);试剂Y不能选用 ,原因是
,原因是_______ 。
I.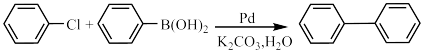

回答下列问题:
(1)A结构简式为
(2)C+D→F化学方程式为
(3)E中含氧官能团名称为
(4)D的一种同分异构体含硝基和3种不同化学环境的氢原子(个数此为
 ),其结构简式为
),其结构简式为(5)C→E的合成路线设计如下:
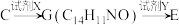
试剂X为
 ,原因是
,原因是
您最近一年使用:0次
真题
解题方法
6 . 以铅精矿(含 ,
, 等)为主要原料提取金属
等)为主要原料提取金属 和
和 的工艺流程如下:
的工艺流程如下:
(1)“热浸”时,难溶的 和
和 转化为
转化为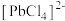 和
和 及单质硫。溶解等物质的量的
及单质硫。溶解等物质的量的 和
和 时,消耗
时,消耗 物质的量之比为
物质的量之比为_______ ;溶液中盐酸浓度不宜过大,除防止“热浸”时 挥发外,另一目的是防止产生
挥发外,另一目的是防止产生_______ (填化学式)。
(2)将“过滤Ⅱ”得到的 沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属
沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属 “电解I”阳极产物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为
“电解I”阳极产物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为_______ 。
(3)“还原”中加入铅精矿的目的是_______ 。
(4)“置换”中可选用的试剂X为_______ (填标号)。
A. B.
B. C.
C. D.
D.
“置换”反应的离子方程式为_______ 。
(5)“电解II”中将富银铅泥制成电极板,用作_______ (填“阴极”或“阳极”)。
 ,
, 等)为主要原料提取金属
等)为主要原料提取金属 和
和 的工艺流程如下:
的工艺流程如下: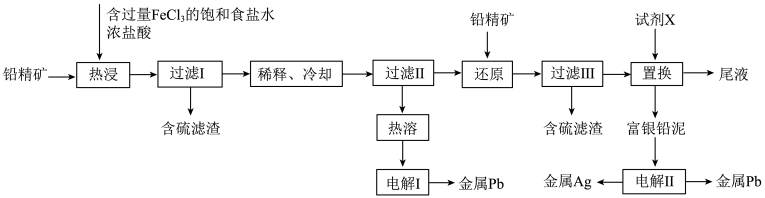
(1)“热浸”时,难溶的
 和
和 转化为
转化为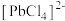 和
和 及单质硫。溶解等物质的量的
及单质硫。溶解等物质的量的 和
和 时,消耗
时,消耗 物质的量之比为
物质的量之比为 挥发外,另一目的是防止产生
挥发外,另一目的是防止产生(2)将“过滤Ⅱ”得到的
 沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属
沉淀反复用饱和食盐水热溶,电解所得溶液可制备金属 “电解I”阳极产物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为
“电解I”阳极产物用尾液吸收后在工艺中循环使用,利用该吸收液的操作单元为(3)“还原”中加入铅精矿的目的是
(4)“置换”中可选用的试剂X为
A.
 B.
B. C.
C. D.
D.
“置换”反应的离子方程式为
(5)“电解II”中将富银铅泥制成电极板,用作
您最近一年使用:0次
真题
7 . 逆水气变换反应: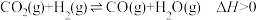 。一定压力下,按
。一定压力下,按 ,
, 物质的量之比
物质的量之比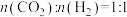 投料,
投料, ,
, 温度时反应物摩尔分数随时间变化关系如图所示。已知该反应的速率方程为
温度时反应物摩尔分数随时间变化关系如图所示。已知该反应的速率方程为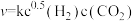 ,
, ,
, 温度时反应速率常数k分别为
温度时反应速率常数k分别为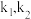 。下列说法错误的是
。下列说法错误的是
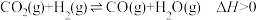 。一定压力下,按
。一定压力下,按 ,
, 物质的量之比
物质的量之比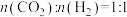 投料,
投料, ,
, 温度时反应物摩尔分数随时间变化关系如图所示。已知该反应的速率方程为
温度时反应物摩尔分数随时间变化关系如图所示。已知该反应的速率方程为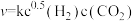 ,
, ,
, 温度时反应速率常数k分别为
温度时反应速率常数k分别为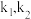 。下列说法错误的是
。下列说法错误的是
A.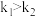 |
B.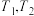 温度下达平衡时反应速率的比值: 温度下达平衡时反应速率的比值: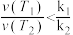 |
| C.温度不变,仅改变体系初始压力,反应物摩尔分数随时间的变化曲线不变 |
D. 温度下,改变初始投料比例,可使平衡时各组分摩尔分数与 温度下,改变初始投料比例,可使平衡时各组分摩尔分数与 温度时相同 温度时相同 |
您最近一年使用:0次
真题
8 . 水煤气是 的主要来源,研究
的主要来源,研究 对
对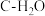 体系制
体系制 的影响,涉及主要反应如下:
的影响,涉及主要反应如下:
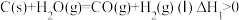

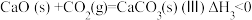
回答列问题:
(1)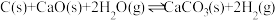 的焓变
的焓变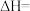
_______ (用代数式表示)。
(2)压力p下,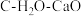 体系达平衡后,图示温度范围内
体系达平衡后,图示温度范围内 已完全反应,
已完全反应, 在
在 温度时完全分解。气相中
温度时完全分解。气相中 ,
, 和
和 摩尔分数随温度的变化关系如图所示,则a线对应物种为
摩尔分数随温度的变化关系如图所示,则a线对应物种为_______ (填化学式)。当温度高于 时,随温度升高c线对应物种摩尔分数逐渐降低的原因是
时,随温度升高c线对应物种摩尔分数逐渐降低的原因是_______ 。 时,图示三种气体的摩尔分数分别为0.50,0.15,0.05,则反应
时,图示三种气体的摩尔分数分别为0.50,0.15,0.05,则反应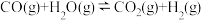 的平衡常数
的平衡常数
_______ ;此时气体总物质的量为 ,则
,则 的物质的量为
的物质的量为_______  ;若向平衡体系中通入少量
;若向平衡体系中通入少量 ,重新达平衡后,分压
,重新达平衡后,分压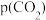 将
将_______ (填“增大”“减小”或“不变”),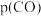 将
将_______ (填“增大”“减小”或“不变”)。
 的主要来源,研究
的主要来源,研究 对
对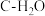 体系制
体系制 的影响,涉及主要反应如下:
的影响,涉及主要反应如下: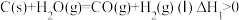

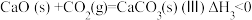
回答列问题:
(1)
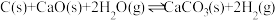 的焓变
的焓变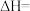
(2)压力p下,
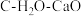 体系达平衡后,图示温度范围内
体系达平衡后,图示温度范围内 已完全反应,
已完全反应, 在
在 温度时完全分解。气相中
温度时完全分解。气相中 ,
, 和
和 摩尔分数随温度的变化关系如图所示,则a线对应物种为
摩尔分数随温度的变化关系如图所示,则a线对应物种为 时,随温度升高c线对应物种摩尔分数逐渐降低的原因是
时,随温度升高c线对应物种摩尔分数逐渐降低的原因是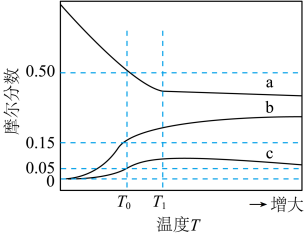
 时,图示三种气体的摩尔分数分别为0.50,0.15,0.05,则反应
时,图示三种气体的摩尔分数分别为0.50,0.15,0.05,则反应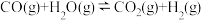 的平衡常数
的平衡常数
 ,则
,则 的物质的量为
的物质的量为 ;若向平衡体系中通入少量
;若向平衡体系中通入少量 ,重新达平衡后,分压
,重新达平衡后,分压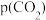 将
将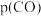 将
将
您最近一年使用:0次
真题
解题方法
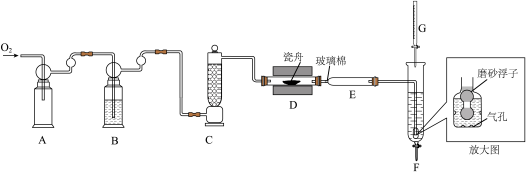
9 . 利用“燃烧—碘酸钾滴定法”测定钢铁中硫含量的实验装置如下图所示(夹持装置略)。
①加样,将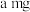 样品加入管式炉内瓷舟中(瓷舟两端带有气孔且有盖),聚四氟乙烯活塞滴定管G内预装
样品加入管式炉内瓷舟中(瓷舟两端带有气孔且有盖),聚四氟乙烯活塞滴定管G内预装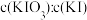 略小于
略小于 的
的 碱性标准溶液,吸收管F内盛有盐酸酸化的淀粉水溶液。向F内滴入适量
碱性标准溶液,吸收管F内盛有盐酸酸化的淀粉水溶液。向F内滴入适量 碱性标准溶液,发生反应:
碱性标准溶液,发生反应: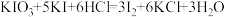 ,使溶液显浅蓝色。
,使溶液显浅蓝色。
②燃烧:按一定流速通入 ,一段时间后,加热并使样品燃烧。
,一段时间后,加热并使样品燃烧。
③滴定:当F内溶液浅蓝色消退时(发生反应: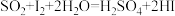 ),立即用
),立即用 碱性标准溶液滴定至浅蓝色复现。随
碱性标准溶液滴定至浅蓝色复现。随 不断进入F,滴定过程中溶液颜色“消退-变蓝”不断变换,直至终点。
不断进入F,滴定过程中溶液颜色“消退-变蓝”不断变换,直至终点。
回答下列问题:
(1)取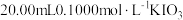 的碱性溶液和一定量的
的碱性溶液和一定量的 固体,配制
固体,配制
 碱性标准溶液,下列仪器必须用到的是_______(填标号)。
碱性标准溶液,下列仪器必须用到的是_______(填标号)。
(2)装置B和C的作用是充分干燥 ,B中的试剂为
,B中的试剂为_______ 。装置F中通气管末端多孔玻璃泡内置一密度小于水的磨砂浮子(见放大图),目的是_______ 。
(3)该滴定实验达终点的现象是_______ ;滴定消耗 碱性标准溶液
碱性标准溶液 ,样品中硫的质量分数是
,样品中硫的质量分数是_______ (用代数式表示)。
(4)若装置D中瓷舟未加盖,会因燃烧时产生粉尘而促进 的生成,粉尘在该过程中的作用是
的生成,粉尘在该过程中的作用是_______ ;若装置E冷却气体不充分,可能导致测定结果偏大,原因是_______ ;若滴定过程中,有少量 不经
不经 直接将
直接将 氧化成
氧化成 ,测定结果会
,测定结果会_______ (填“偏大”“偏小”或“不变”)。
①加样,将
 样品加入管式炉内瓷舟中(瓷舟两端带有气孔且有盖),聚四氟乙烯活塞滴定管G内预装
样品加入管式炉内瓷舟中(瓷舟两端带有气孔且有盖),聚四氟乙烯活塞滴定管G内预装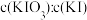 略小于
略小于 的
的 碱性标准溶液,吸收管F内盛有盐酸酸化的淀粉水溶液。向F内滴入适量
碱性标准溶液,吸收管F内盛有盐酸酸化的淀粉水溶液。向F内滴入适量 碱性标准溶液,发生反应:
碱性标准溶液,发生反应: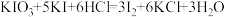 ,使溶液显浅蓝色。
,使溶液显浅蓝色。②燃烧:按一定流速通入
 ,一段时间后,加热并使样品燃烧。
,一段时间后,加热并使样品燃烧。③滴定:当F内溶液浅蓝色消退时(发生反应:
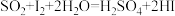 ),立即用
),立即用 碱性标准溶液滴定至浅蓝色复现。随
碱性标准溶液滴定至浅蓝色复现。随 不断进入F,滴定过程中溶液颜色“消退-变蓝”不断变换,直至终点。
不断进入F,滴定过程中溶液颜色“消退-变蓝”不断变换,直至终点。回答下列问题:
(1)取
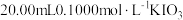 的碱性溶液和一定量的
的碱性溶液和一定量的 固体,配制
固体,配制
 碱性标准溶液,下列仪器必须用到的是_______(填标号)。
碱性标准溶液,下列仪器必须用到的是_______(填标号)。| A.玻璃棒 | B. 锥形瓶 锥形瓶 | C.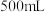 容量瓶 容量瓶 | D.胶头滴管 |
(2)装置B和C的作用是充分干燥
 ,B中的试剂为
,B中的试剂为(3)该滴定实验达终点的现象是
 碱性标准溶液
碱性标准溶液 ,样品中硫的质量分数是
,样品中硫的质量分数是(4)若装置D中瓷舟未加盖,会因燃烧时产生粉尘而促进
 的生成,粉尘在该过程中的作用是
的生成,粉尘在该过程中的作用是 不经
不经 直接将
直接将 氧化成
氧化成 ,测定结果会
,测定结果会
您最近一年使用:0次
真题
解题方法
10 . 锰氧化物具有较大应用价值,回答下列问题:
(1) 在元素周期表中位于第
在元素周期表中位于第_______ 周期_______ 族;同周期中,基态原子未成对电子数比 多的元素是
多的元素是_______ (填元素符号)。
(2) 如某种氧化物
如某种氧化物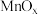 的四方晶胞及其在xy平面的投影如图所示,该氧化物化学式为
的四方晶胞及其在xy平面的投影如图所示,该氧化物化学式为_______ 。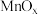 晶体有O原子脱出时,出现O空位,
晶体有O原子脱出时,出现O空位, 的化合价
的化合价_______ (填“升高”“降低”或“不变”),O空位的产生使晶体具有半导体性质。下列氧化物晶体难以通过该方式获有半导体性质的是_______ (填标号)。
A. B.
B. C.
C. D.
D.
(3)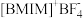 (见图)是
(见图)是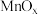 晶型转变的诱导剂。
晶型转变的诱导剂。 的空间构型为
的空间构型为_______ ;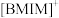 中咪唑环存在
中咪唑环存在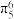 大
大 键,则N原子采取的轨道杂化方式为
键,则N原子采取的轨道杂化方式为_______ 。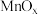 可作
可作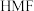 转化为
转化为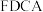 的催化剂(见下图)。
的催化剂(见下图)。 的熔点远大于
的熔点远大于 ,除相对分子质量存在差异外,另一重要原因是
,除相对分子质量存在差异外,另一重要原因是_______ 。
(1)
 在元素周期表中位于第
在元素周期表中位于第 多的元素是
多的元素是(2)
 如某种氧化物
如某种氧化物 的四方晶胞及其在xy平面的投影如图所示,该氧化物化学式为
的四方晶胞及其在xy平面的投影如图所示,该氧化物化学式为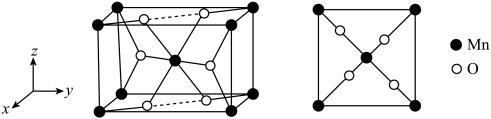
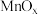 晶体有O原子脱出时,出现O空位,
晶体有O原子脱出时,出现O空位, 的化合价
的化合价A.
 B.
B. C.
C. D.
D.
(3)
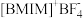 (见图)是
(见图)是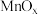 晶型转变的诱导剂。
晶型转变的诱导剂。 的空间构型为
的空间构型为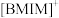 中咪唑环存在
中咪唑环存在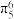 大
大 键,则N原子采取的轨道杂化方式为
键,则N原子采取的轨道杂化方式为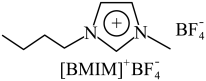
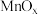 可作
可作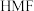 转化为
转化为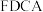 的催化剂(见下图)。
的催化剂(见下图)。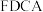 的熔点远大于
的熔点远大于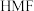 ,除相对分子质量存在差异外,另一重要原因是
,除相对分子质量存在差异外,另一重要原因是
您最近一年使用:0次



