解题方法
1 .  是锂离子电池的活性材料。某小组以含锰矿料(主要成分是
是锂离子电池的活性材料。某小组以含锰矿料(主要成分是 ,含少量
,含少量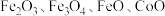 和
和 )为原料制备
)为原料制备 的工艺流程如图所示(部分条件和产物省略)。
的工艺流程如图所示(部分条件和产物省略)。 如表所示:
如表所示:
回答下列问题:
(1)写出一条提高“酸浸”速率的措施:_______ 。
(2)“除杂1”时,加入 的作用是
的作用是_______ (用离子方程式表示)。
(3)“固体1”的主要成分是_______ (写化学式),“除杂1”过程调节 范围为
范围为_______ 。
(4)在高温下“合成” ,反应的化学方程式为
,反应的化学方程式为_______ 。
(5)已知:常温下,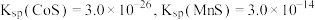 。若除杂后所得溶液中
。若除杂后所得溶液中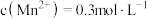 ,则此时
,则此时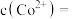
_______ 。
(6)“浸渣”中含少量锰元素,其含量测定方法如下:
第1步:称取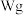 “浸渣”,加酸将铦元素以
“浸渣”,加酸将铦元素以 形式全部溶出,过泥,将滵液加入
形式全部溶出,过泥,将滵液加入 容量瓶中,定容;
容量瓶中,定容;
第2步:取 上述定容后的溶液于锥形瓶中,加入少量催化剂和过量
上述定容后的溶液于锥形瓶中,加入少量催化剂和过量 溶液,加热,充分反应后,煮沸溶液;
溶液,加热,充分反应后,煮沸溶液;
第3步:用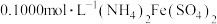 溶液滴定至终点,消耗滴定液
溶液滴定至终点,消耗滴定液 ,使
,使 重新变为
重新变为 。
。
已知: 具有强氧化性,受热易分解。
具有强氧化性,受热易分解。
①“浸渣”中锰元素的质量分数为_______ (用含W、V的代数式表示)。
②如果省略第2步“煮沸溶液”,测得结果将_______ (填“偏高”、“偏低”或“无影响”)。
 是锂离子电池的活性材料。某小组以含锰矿料(主要成分是
是锂离子电池的活性材料。某小组以含锰矿料(主要成分是 ,含少量
,含少量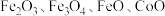 和
和 )为原料制备
)为原料制备 的工艺流程如图所示(部分条件和产物省略)。
的工艺流程如图所示(部分条件和产物省略)。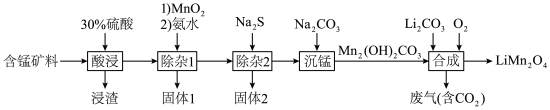
 如表所示:
如表所示:| 金属氢氧化物 |  |  |  |  |
开始沉淀的 | 2.7 | 7.6 | 7.6 | 7.7 |
完全沉淀的 | 3.7 | 9.1 | 9.1 | 9.2 |
(1)写出一条提高“酸浸”速率的措施:
(2)“除杂1”时,加入
 的作用是
的作用是(3)“固体1”的主要成分是
 范围为
范围为(4)在高温下“合成”
 ,反应的化学方程式为
,反应的化学方程式为(5)已知:常温下,
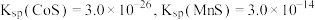 。若除杂后所得溶液中
。若除杂后所得溶液中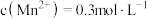 ,则此时
,则此时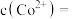
(6)“浸渣”中含少量锰元素,其含量测定方法如下:
第1步:称取
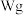 “浸渣”,加酸将铦元素以
“浸渣”,加酸将铦元素以 形式全部溶出,过泥,将滵液加入
形式全部溶出,过泥,将滵液加入 容量瓶中,定容;
容量瓶中,定容;第2步:取
 上述定容后的溶液于锥形瓶中,加入少量催化剂和过量
上述定容后的溶液于锥形瓶中,加入少量催化剂和过量 溶液,加热,充分反应后,煮沸溶液;
溶液,加热,充分反应后,煮沸溶液;第3步:用
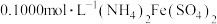 溶液滴定至终点,消耗滴定液
溶液滴定至终点,消耗滴定液 ,使
,使 重新变为
重新变为 。
。已知:
 具有强氧化性,受热易分解。
具有强氧化性,受热易分解。①“浸渣”中锰元素的质量分数为
②如果省略第2步“煮沸溶液”,测得结果将
您最近一年使用:0次
解题方法
2 . 我国航空航天技术走在世界前列,其中化学材料起着重要作用。下列说法错误的是
| A.神舟十七号载人飞船使用的可充电镉镍电池属于二次电池 |
| B.中国空间站核心舱使用的半导体砷化镓是太阳能电池材料 |
| C.航天员航天服制作材料中的涤纶属于天然有机高分子材料 |
D.国产飞机 用到的氮化硅陶瓷属于新型无机非金属材料 用到的氮化硅陶瓷属于新型无机非金属材料 |
您最近一年使用:0次
3 . 药物贝诺酯由乙酰水杨酸和对乙酰氨基酚制备,其原理为
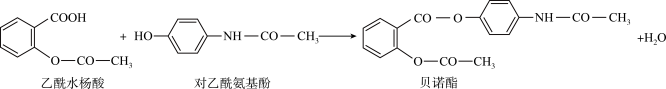
| A.乙酰水杨酸分子中所有碳原子可共平面 |
| B.对乙酰氨基酚的核磁共振碳谱有6组峰 |
| C.对乙酰氨基酚在一定条件下可与甲醛反应 |
| D.贝诺酯在酸性条件下充分水解可得到3种产物 |
您最近一年使用:0次
解题方法
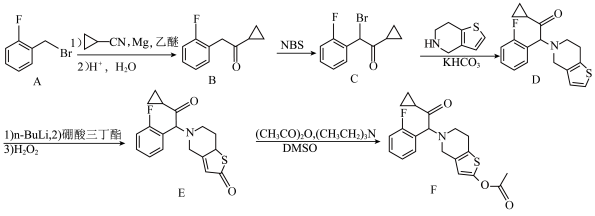
4 . F是一种抗血小板凝聚的药物,其人工合成路线如图:
(1)B中官能团的名称是_______ 。
(2)A的芳香族同分异构体中,与其具有相同官能团的有_______ 种(不考虑立体异构)。
(3)E→F中有一种相对分子质量为60的产物生成,该产物的结构简式为_______ ,实验室中如需确定此产物中的官能团,通常使用的分析仪器的名称是_______ 。
(4)A→B的反应需经历三步反应:_______ ;Z的分子式为 ,其结构简式为
,其结构简式为_______ ;
(5)已知: ,
, 也可以由某多酮结构在碱性溶液中发生分子内缩合生成,则此多酮的结构简式为
也可以由某多酮结构在碱性溶液中发生分子内缩合生成,则此多酮的结构简式为_______ (填标号)。
(1)B中官能团的名称是
(2)A的芳香族同分异构体中,与其具有相同官能团的有
(3)E→F中有一种相对分子质量为60的产物生成,该产物的结构简式为
(4)A→B的反应需经历三步反应:
第一步: (制备格氏试剂)
(制备格氏试剂)
第二步: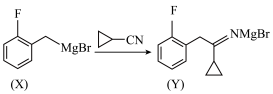
第三步: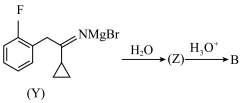 (水解反应)
(水解反应)
 ,其结构简式为
,其结构简式为(5)已知:
 ,
, 也可以由某多酮结构在碱性溶液中发生分子内缩合生成,则此多酮的结构简式为
也可以由某多酮结构在碱性溶液中发生分子内缩合生成,则此多酮的结构简式为a.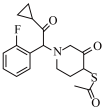 b.
b.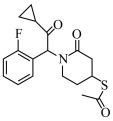
您最近一年使用:0次
5 . 一定条件下,1-苯基丙炔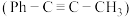 可与
可与 发生催化加成,反应过程的能量变化如图1,反应体系中三种有机物的百分占比随时间变化如图2。
发生催化加成,反应过程的能量变化如图1,反应体系中三种有机物的百分占比随时间变化如图2。
(1)反应Ⅲ: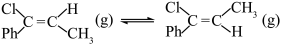

_______ 。
(2)分析产物A占比呈先变大后减小的原因_______ 。
(3)下列关于该反应的说法正确的是_______ 。
a.选择较短的反应时间,及时分离可获得高产率产物A
b.选择对产物A选择性较好的催化剂,能有效提高A的平衡产率
c.将普通固体催化剂换成纳米级颗粒,产物A的浓度峰值点可能变成图示点a
d.升高温度,1-苯基丙炔的转化率和A的选择性均增大
(4)为研究上述反应体系的平衡关系,在一定温度下,向某刚性密闭容器中加入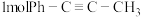 和
和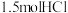 ,容器内总压强为
,容器内总压强为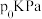 ,反应5分钟达平衡。平衡时测得
,反应5分钟达平衡。平衡时测得 的转化率为α。已知反应Ⅲ的平衡常数
的转化率为α。已知反应Ⅲ的平衡常数 ,则平衡时反应体系的总压强为
,则平衡时反应体系的总压强为_______ 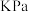 ,反应前5分钟A的反应速率为
,反应前5分钟A的反应速率为_______ 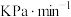 ,该温度下反应Ⅰ的压强平衡常数
,该温度下反应Ⅰ的压强平衡常数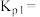
_______ (用含有α的代数式表示)。
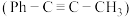 可与
可与 发生催化加成,反应过程的能量变化如图1,反应体系中三种有机物的百分占比随时间变化如图2。
发生催化加成,反应过程的能量变化如图1,反应体系中三种有机物的百分占比随时间变化如图2。
(1)反应Ⅲ:
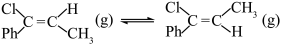

(2)分析产物A占比呈先变大后减小的原因
(3)下列关于该反应的说法正确的是
a.选择较短的反应时间,及时分离可获得高产率产物A
b.选择对产物A选择性较好的催化剂,能有效提高A的平衡产率
c.将普通固体催化剂换成纳米级颗粒,产物A的浓度峰值点可能变成图示点a
d.升高温度,1-苯基丙炔的转化率和A的选择性均增大
(4)为研究上述反应体系的平衡关系,在一定温度下,向某刚性密闭容器中加入
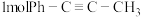 和
和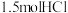 ,容器内总压强为
,容器内总压强为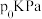 ,反应5分钟达平衡。平衡时测得
,反应5分钟达平衡。平衡时测得 的转化率为α。已知反应Ⅲ的平衡常数
的转化率为α。已知反应Ⅲ的平衡常数 ,则平衡时反应体系的总压强为
,则平衡时反应体系的总压强为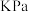 ,反应前5分钟A的反应速率为
,反应前5分钟A的反应速率为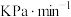 ,该温度下反应Ⅰ的压强平衡常数
,该温度下反应Ⅰ的压强平衡常数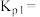
您最近一年使用:0次
解题方法
6 . 利用平衡移动原理,分析常温下金属 在不同
在不同 的
的 体系中的可能产物。已知:图1中曲线表示
体系中的可能产物。已知:图1中曲线表示 体系中各含碳粒子的物质的量分数与
体系中各含碳粒子的物质的量分数与 的关系;图2中曲线I的离子浓度关系符合
的关系;图2中曲线I的离子浓度关系符合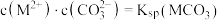 ;曲线II的离子浓度关系符合
;曲线II的离子浓度关系符合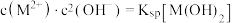 ;[注:起始
;[注:起始 体系中
体系中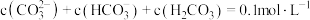 ;不同
;不同 下
下 由图1得到]。下列说法正确的是
由图1得到]。下列说法正确的是
 在不同
在不同 的
的 体系中的可能产物。已知:图1中曲线表示
体系中的可能产物。已知:图1中曲线表示 体系中各含碳粒子的物质的量分数与
体系中各含碳粒子的物质的量分数与 的关系;图2中曲线I的离子浓度关系符合
的关系;图2中曲线I的离子浓度关系符合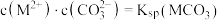 ;曲线II的离子浓度关系符合
;曲线II的离子浓度关系符合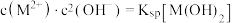 ;[注:起始
;[注:起始 体系中
体系中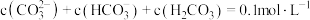 ;不同
;不同 下
下 由图1得到]。下列说法正确的是
由图1得到]。下列说法正确的是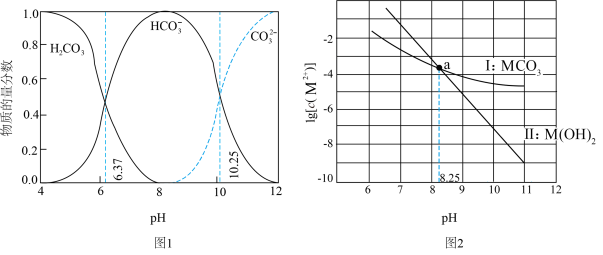
A. 时,碳酸钠溶液体系中存在: 时,碳酸钠溶液体系中存在: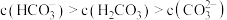 |
B.图2中, 点时溶液中存在: 点时溶液中存在: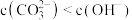 |
C.起始状态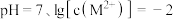 ,平衡后溶液中存在: ,平衡后溶液中存在: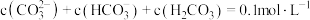 |
D.沉淀 制备 制备 时,选用 时,选用 溶液比 溶液比 溶液效果好 溶液效果好 |
您最近一年使用:0次
7 . 从制钕铁硼合金的废料中提取氧化钕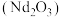 的工艺流程如图所示。
的工艺流程如图所示。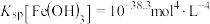
下列说法错误的是
 的工艺流程如图所示。
的工艺流程如图所示。
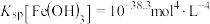
下列说法错误的是
A.反应I所得气体的主要成分是 ,滤渣是硼和其他不溶于酸的杂质 ,滤渣是硼和其他不溶于酸的杂质 |
B.为完全除去滤液1中铁元素,反应II应调节 的最小值为2.9 的最小值为2.9 |
| C.温度越高,越有利于反应II的进行 |
| D.反应III中适当增大草酸的浓度,有利于草酸钕晶体的析出 |
您最近一年使用:0次
8 . 某化学学习小组设计实验制备SO2并探究SO2的化学性质,过程设计如下图所示:
(1)仪器a的名称为_____ ;按图连接好装置后,实验开始前依次进行的操作是______ (填字母)。
a.加入足量70%浓硫酸 b.加入 粉末 c.检查装置的气密性
粉末 c.检查装置的气密性
(2)实验结束后观察③中颜色无变化,加入少量蒸馏水红色褪去。该实验的目的是_______ 。足量碱石灰的作用是_______ 。由此得出的实验结论是_______ 。
(3)④中溶液变为绿色(含 ),写出该反应的离子反应方程式
),写出该反应的离子反应方程式_______ 。
(4)小组成员进一步进行定量实验:取⑤中溶液 于锥形瓶中,滴入稀硫酸使溶液呈酸性,并加入几滴淀粉溶液。用
于锥形瓶中,滴入稀硫酸使溶液呈酸性,并加入几滴淀粉溶液。用 的
的 溶液滴定,以测定溶液浓度,三次平行实验测得标准液的平均体积为
溶液滴定,以测定溶液浓度,三次平行实验测得标准液的平均体积为 。滴定终点时锥形㼛中的现象为
。滴定终点时锥形㼛中的现象为_______ ,所测⑤中 的质量浓度(以溶液中
的质量浓度(以溶液中 的质量浓度计算)为
的质量浓度计算)为_______  。
。

(1)仪器a的名称为
a.加入足量70%浓硫酸 b.加入
 粉末 c.检查装置的气密性
粉末 c.检查装置的气密性(2)实验结束后观察③中颜色无变化,加入少量蒸馏水红色褪去。该实验的目的是
(3)④中溶液变为绿色(含
 ),写出该反应的离子反应方程式
),写出该反应的离子反应方程式(4)小组成员进一步进行定量实验:取⑤中溶液
 于锥形瓶中,滴入稀硫酸使溶液呈酸性,并加入几滴淀粉溶液。用
于锥形瓶中,滴入稀硫酸使溶液呈酸性,并加入几滴淀粉溶液。用 的
的 溶液滴定,以测定溶液浓度,三次平行实验测得标准液的平均体积为
溶液滴定,以测定溶液浓度,三次平行实验测得标准液的平均体积为 。滴定终点时锥形㼛中的现象为
。滴定终点时锥形㼛中的现象为 的质量浓度(以溶液中
的质量浓度(以溶液中 的质量浓度计算)为
的质量浓度计算)为 。
。
您最近一年使用:0次
解题方法
9 . 碱土金属(ⅡA族)元素单质及其相关化合物的性质一直以来是化学界研究的重点。回答下列问题:
(1)对于碱土金属元素 ,随着原子序数的增加,以下性质呈单调递减变化的是
,随着原子序数的增加,以下性质呈单调递减变化的是_______ 。
a.原子半径 b.单质的硬度 c.第一电离能
(2)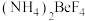 是工业制备金属铍过程中的重要中间产物,其阳离子含有的化学键类型为
是工业制备金属铍过程中的重要中间产物,其阳离子含有的化学键类型为_______ ,阴离子中心原子杂化方式为_______ 。
(3) 是人体必需的矿物元素。
是人体必需的矿物元素。 的电子排布式为
的电子排布式为_______ 。判断 的热分解温度
的热分解温度_______ (填“大于”或“小于”) 的热分解温度,理由是
的热分解温度,理由是_______ 。
(4) 和金属
和金属 在一定条件下用球磨机研磨,可制得化学式为
在一定条件下用球磨机研磨,可制得化学式为 的储氢化合物,其立方晶胞结构如图所示:
的储氢化合物,其立方晶胞结构如图所示: 原子周围距离最近且相等的
原子周围距离最近且相等的 原子有
原子有_______ 个,若唱胞边长为 ,则
,则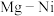 核间距为
核间距为_______  。
。
②若以晶胞中氢的密度与液态氢密度之比定义储氢材料的储氢能力,则该化合物的储氢能力为_______ (列出计算式即可。假定该化合物中所有的 可以全部放出,液氢密度为
可以全部放出,液氢密度为 ;设
;设 代表阿伏加德罗常数的值)。
代表阿伏加德罗常数的值)。
(1)对于碱土金属元素
 ,随着原子序数的增加,以下性质呈单调递减变化的是
,随着原子序数的增加,以下性质呈单调递减变化的是a.原子半径 b.单质的硬度 c.第一电离能
(2)
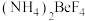 是工业制备金属铍过程中的重要中间产物,其阳离子含有的化学键类型为
是工业制备金属铍过程中的重要中间产物,其阳离子含有的化学键类型为(3)
 是人体必需的矿物元素。
是人体必需的矿物元素。 的电子排布式为
的电子排布式为 的热分解温度
的热分解温度 的热分解温度,理由是
的热分解温度,理由是(4)
 和金属
和金属 在一定条件下用球磨机研磨,可制得化学式为
在一定条件下用球磨机研磨,可制得化学式为 的储氢化合物,其立方晶胞结构如图所示:
的储氢化合物,其立方晶胞结构如图所示:
 原子周围距离最近且相等的
原子周围距离最近且相等的 原子有
原子有 ,则
,则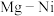 核间距为
核间距为 。
。②若以晶胞中氢的密度与液态氢密度之比定义储氢材料的储氢能力,则该化合物的储氢能力为
 可以全部放出,液氢密度为
可以全部放出,液氢密度为 ;设
;设 代表阿伏加德罗常数的值)。
代表阿伏加德罗常数的值)。
您最近一年使用:0次
解题方法
10 . 一定条件下, 与
与 在活性
在活性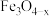 表面转化为
表面转化为 ,其部分反应机理如图所示。已知:
,其部分反应机理如图所示。已知: 在催化剂不同离子表面会出现电性差异。下列说法正确的是
在催化剂不同离子表面会出现电性差异。下列说法正确的是
 与
与 在活性
在活性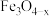 表面转化为
表面转化为 ,其部分反应机理如图所示。已知:
,其部分反应机理如图所示。已知: 在催化剂不同离子表面会出现电性差异。下列说法正确的是
在催化剂不同离子表面会出现电性差异。下列说法正确的是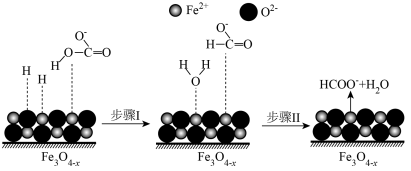
A. 的空间构型是三角锥形 的空间构型是三角锥形 |
B.生成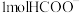 理论上转移 理论上转移 |
| C.反应过程中只有极性键的断裂与生成 |
D.步骤I中吸附在 上的 上的 与 与 中的碳结合 中的碳结合 |
您最近一年使用:0次



