名校
解题方法
1 . 2023年化学诺贝尔奖授予了三位研究量子点的科学家。量子点又称“人造原子”、“超原子”,是一种纳米级的半导体材料,在医疗,科技等多个领域有广泛的应用。
(1)聚多巴胺量子点具有广泛的光学吸收和荧光特性,可直接用于体内成像。多巴胺结构如下图所示。___________ ,其最高能层上有___________ 种运动状态不同的电子。
②多巴胺分子中碳原子的杂化方式为___________ ,1mol多巴胺中含有 键的数目为
键的数目为___________ 。
③多巴胺易溶于水,原因是___________ 。
(2)聚多巴胺量子点还可以通过吸附金属离子如 ,
, ,
, 等用于核磁共振成像(MRI)。
等用于核磁共振成像(MRI)。
① 中含有
中含有 ,其阴离子空间构型为
,其阴离子空间构型为___________ 。
②Mn的第三电离能大于Fe的第三电离能,原因是___________ 。
(3)CdS量子点是一种常见的量子点。某种CdS晶体的立方晶胞如下图所示。 的配位数为
的配位数为___________ 。
②若CdS晶体的密度为 ,则晶胞中
,则晶胞中 和
和 间的最短距离为
间的最短距离为___________ pm(列出计算式即可)。
(1)聚多巴胺量子点具有广泛的光学吸收和荧光特性,可直接用于体内成像。多巴胺结构如下图所示。
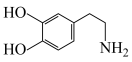
②多巴胺分子中碳原子的杂化方式为
 键的数目为
键的数目为③多巴胺易溶于水,原因是
(2)聚多巴胺量子点还可以通过吸附金属离子如
 ,
, ,
, 等用于核磁共振成像(MRI)。
等用于核磁共振成像(MRI)。①
 中含有
中含有 ,其阴离子空间构型为
,其阴离子空间构型为②Mn的第三电离能大于Fe的第三电离能,原因是
(3)CdS量子点是一种常见的量子点。某种CdS晶体的立方晶胞如下图所示。

 的配位数为
的配位数为②若CdS晶体的密度为
 ,则晶胞中
,则晶胞中 和
和 间的最短距离为
间的最短距离为
您最近一年使用:0次
2024-06-11更新
|
199次组卷
|
3卷引用:T35-结构与性质
2 . 常温下向 饱和溶液(始终有
饱和溶液(始终有 固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中
固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中 浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知
浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知 的电离常数的负对数:
的电离常数的负对数: ,
, ;下列说法正确的是
;下列说法正确的是
 饱和溶液(始终有
饱和溶液(始终有 固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中
固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中 浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知
浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知 的电离常数的负对数:
的电离常数的负对数: ,
, ;下列说法正确的是
;下列说法正确的是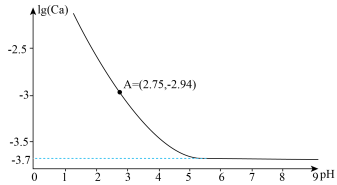
A.溶液中始终存在: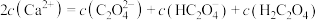 |
B.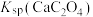 的数量级为 的数量级为 |
C.pH=7时,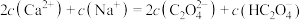 |
D.A点时,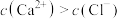 |
您最近一年使用:0次
解题方法
3 . 我国在政府工作报告中提出力争于2030年前做到碳达峰,2060年前实现碳中和。因此,研发二氧化碳转化利用技术,成为当下研究热点。
 .
. 与
与 重整是
重整是 再利用的研究热点之一。该重整反应体系主要涉及以下反应:
再利用的研究热点之一。该重整反应体系主要涉及以下反应:
①

②
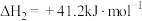
③
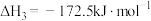
(1)已知反应①低温无法自发进行,只能在高温下自发进行,则
___________ 0(填“>”或“<”)。
(2)某温度下,在体积 的密闭容器中加入
的密闭容器中加入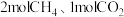 及催化剂仅发生反应①,经过
及催化剂仅发生反应①,经过 达到平衡状态时
达到平衡状态时 的转化率为
的转化率为 。则用
。则用 表示的平均化学反应速率为
表示的平均化学反应速率为___________ ,平衡常数的值为___________ ;达到平衡后,其他条件不变时向容器中充入 与
与 各
各 ,则化学平衡
,则化学平衡___________ 移动(选填“正向”、“逆向”或“不”)。
(3) 下,将
下,将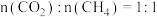 的混合气体置于密闭容器中,不同温度下重整体系中
的混合气体置于密闭容器中,不同温度下重整体系中 和
和 的平衡转化率如图所示。
的平衡转化率如图所示。 时
时 的平衡转化率远大于
的平衡转化率远大于 时
时 的平衡转化率。原因是
的平衡转化率。原因是___________ 。 .
. 在催化剂作用下,通过电催化还原为
在催化剂作用下,通过电催化还原为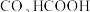 是一种具有前景的利用
是一种具有前景的利用 的方式。在催化剂表面,
的方式。在催化剂表面, 还原生成
还原生成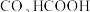 通过两种平行的反应途径进行,各自途径的关键中间体分别为
通过两种平行的反应途径进行,各自途径的关键中间体分别为 。催化剂催化
。催化剂催化 转化为
转化为 和
和 的反应历程如图1(*表示吸附在催化剂表面)。
的反应历程如图1(*表示吸附在催化剂表面)。 催化剂表面更利于生成
催化剂表面更利于生成___________ 。
(5)在m和n两种催化剂作用下,反应①的阿伦尼乌斯经验公式实验数据如图2所示,已知阿伦尼乌斯经验公式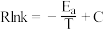 (
( 为活化能,k为速率常数,R和C为常数),m和n两种催化剂中对该反应催化效果较高的是
为活化能,k为速率常数,R和C为常数),m和n两种催化剂中对该反应催化效果较高的是___________ (填“m”或“n”)。
 .
. 与
与 重整是
重整是 再利用的研究热点之一。该重整反应体系主要涉及以下反应:
再利用的研究热点之一。该重整反应体系主要涉及以下反应:①


②

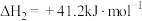
③

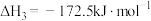
(1)已知反应①低温无法自发进行,只能在高温下自发进行,则

(2)某温度下,在体积
 的密闭容器中加入
的密闭容器中加入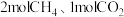 及催化剂仅发生反应①,经过
及催化剂仅发生反应①,经过 达到平衡状态时
达到平衡状态时 的转化率为
的转化率为 。则用
。则用 表示的平均化学反应速率为
表示的平均化学反应速率为 与
与 各
各 ,则化学平衡
,则化学平衡(3)
 下,将
下,将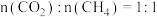 的混合气体置于密闭容器中,不同温度下重整体系中
的混合气体置于密闭容器中,不同温度下重整体系中 和
和 的平衡转化率如图所示。
的平衡转化率如图所示。 时
时 的平衡转化率远大于
的平衡转化率远大于 时
时 的平衡转化率。原因是
的平衡转化率。原因是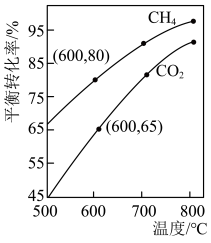
 .
. 在催化剂作用下,通过电催化还原为
在催化剂作用下,通过电催化还原为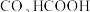 是一种具有前景的利用
是一种具有前景的利用 的方式。在催化剂表面,
的方式。在催化剂表面, 还原生成
还原生成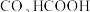 通过两种平行的反应途径进行,各自途径的关键中间体分别为
通过两种平行的反应途径进行,各自途径的关键中间体分别为 。催化剂催化
。催化剂催化 转化为
转化为 和
和 的反应历程如图1(*表示吸附在催化剂表面)。
的反应历程如图1(*表示吸附在催化剂表面)。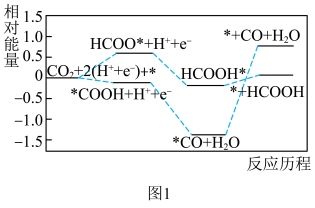
 催化剂表面更利于生成
催化剂表面更利于生成(5)在m和n两种催化剂作用下,反应①的阿伦尼乌斯经验公式实验数据如图2所示,已知阿伦尼乌斯经验公式
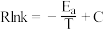 (
( 为活化能,k为速率常数,R和C为常数),m和n两种催化剂中对该反应催化效果较高的是
为活化能,k为速率常数,R和C为常数),m和n两种催化剂中对该反应催化效果较高的是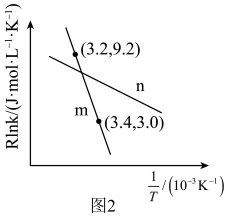
您最近一年使用:0次
名校
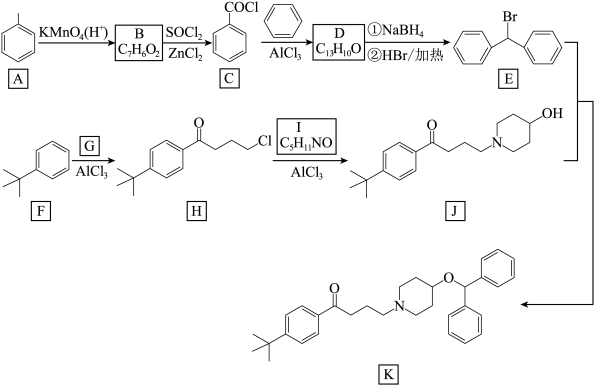
4 . 现代有机化学的发展,为药学的进步提供了充足的动力。化合物K(C32H39NO2)在临床上用于变应性疾病,包括儿童变应性鼻炎、成人的终年鼻炎、季节性鼻炎、枯草热和慢性荨麻疹等。其一种合成路线如下(部分反应条件已简化,忽略立体化学):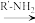 R-NH-R′
R-NH-R′
回答下列问题:
(1)B的化学名称是_______ 。
(2)由D生成E涉及两步反应,第二步反应的反应类型为_______ ,并写出②的化学方程式_______ 。
(3)G的分子式为_______ 。
(4)I的结构简式为_______ 。
(5)J中含氧官能团的名称是_______ 。
(6)有机物M的分子组成比B(C7H6O2)多2个“CH2”,M中能与碳酸氢钠溶液反应生成无色气体且具有芳香性的同分异构体有_______ 种(不考虑立体异构,填标号)。
a.12 b.13 c.14 d.15
其中,核磁共振氢谱显示4组峰,且峰面积比为1:1:2:6的同分异构体结构简式为_______ 。
已知:i.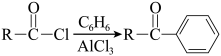
ii.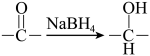
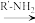 R-NH-R′
R-NH-R′回答下列问题:
(1)B的化学名称是
(2)由D生成E涉及两步反应,第二步反应的反应类型为
(3)G的分子式为
(4)I的结构简式为
(5)J中含氧官能团的名称是
(6)有机物M的分子组成比B(C7H6O2)多2个“CH2”,M中能与碳酸氢钠溶液反应生成无色气体且具有芳香性的同分异构体有
a.12 b.13 c.14 d.15
其中,核磁共振氢谱显示4组峰,且峰面积比为1:1:2:6的同分异构体结构简式为
您最近一年使用:0次
解题方法
5 . 副族元素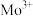 、
、 等元素较
等元素较 更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液
更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液_______ ;锰在周期表中的_______ 区。
(2)“超分子”中各元素(除H外)电负性由大到小的顺序为_______ 。
(3)副族元素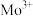 、
、 等元素比
等元素比 更易形成配合物,其原因是
更易形成配合物,其原因是_______ ; 与配体
与配体 形成共价键,提供孤电子对的原子是
形成共价键,提供孤电子对的原子是_______ (填元素符号),其中配体中C原子的杂化方式为_______ , 结合1个O和1个
结合1个O和1个 得到一种常见微粒,其空间构型为
得到一种常见微粒,其空间构型为_______ 。
(4)冠醚能够提升高锰酸钾氧化己烯的速率的原因是_______ 。
(5)氮化钼晶胞结构如图所示,N原子填充Mo围成的八面体空隙中,填充率为100%。_______ ;
② 的熔点
的熔点_______ (填“>”、“<”或“=”) ;
;
③若该八面体边长为 ,则晶胞的密度为
,则晶胞的密度为
_______  (
( 表示啊伏伽德罗常数)。
表示啊伏伽德罗常数)。
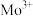 、
、 等元素较
等元素较 更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液
更易形成配合物,但是二环己烷并—18—冠(醚)—6在高锰酸钾溶液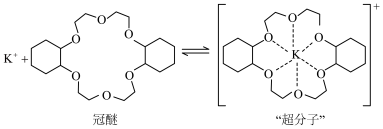
(2)“超分子”中各元素(除H外)电负性由大到小的顺序为
(3)副族元素
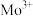 、
、 等元素比
等元素比 更易形成配合物,其原因是
更易形成配合物,其原因是 与配体
与配体 形成共价键,提供孤电子对的原子是
形成共价键,提供孤电子对的原子是 结合1个O和1个
结合1个O和1个 得到一种常见微粒,其空间构型为
得到一种常见微粒,其空间构型为(4)冠醚能够提升高锰酸钾氧化己烯的速率的原因是
(5)氮化钼晶胞结构如图所示,N原子填充Mo围成的八面体空隙中,填充率为100%。

②
 的熔点
的熔点 ;
;③若该八面体边长为
 ,则晶胞的密度为
,则晶胞的密度为
 (
( 表示啊伏伽德罗常数)。
表示啊伏伽德罗常数)。
您最近一年使用:0次
名校
解题方法
6 . 锂离子电池作为重要储能设备在手机、汽车等行业得到了大规模应用。一种基于微波辅助低共熔溶剂的回收方法可实现对废旧锂离子电池中 的回收利用,其主要工艺流程如下:
的回收利用,其主要工艺流程如下: 在溶液中常以
在溶液中常以 (蓝色)和
(蓝色)和 (粉红色)形式存在;
(粉红色)形式存在;
②25℃时,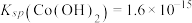 。
。
回答下列问题:
(1) 中Co的化合价为
中Co的化合价为___________ 。
(2)微波具有选择性加热和穿透性强的特点,采用微波共熔技术的优点除了可以减少杂质溶解还有___________ 。
(3)低共熔溶剂中含有一定量的草酸,其作用为___________ ;已知在水浸过程中溶液由蓝色变为粉红色,写出该变化的离子反应方程式___________ 。
(4)25℃时,沉钴反应完成后,溶液的pH=10,此时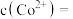
___________ mg/L。
(5)滤饼1在空气中煅烧得 ,写出该反应的化学反应方程式
,写出该反应的化学反应方程式___________ 。
(6)高温烧结过程中需通入空气,该反应中氧化剂与还原剂物质的量之比为___________ ,若通入空气过多过快,造成的不利影响是___________ 。
 的回收利用,其主要工艺流程如下:
的回收利用,其主要工艺流程如下: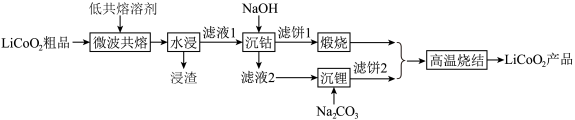
 在溶液中常以
在溶液中常以 (蓝色)和
(蓝色)和 (粉红色)形式存在;
(粉红色)形式存在;②25℃时,
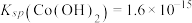 。
。回答下列问题:
(1)
 中Co的化合价为
中Co的化合价为(2)微波具有选择性加热和穿透性强的特点,采用微波共熔技术的优点除了可以减少杂质溶解还有
(3)低共熔溶剂中含有一定量的草酸,其作用为
(4)25℃时,沉钴反应完成后,溶液的pH=10,此时
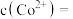
(5)滤饼1在空气中煅烧得
 ,写出该反应的化学反应方程式
,写出该反应的化学反应方程式(6)高温烧结过程中需通入空气,该反应中氧化剂与还原剂物质的量之比为
您最近一年使用:0次
名校
7 . 我国科学家设计一种以ZnI2水溶液作为锌离子电池介质的Zn-BiOI电池,通过Bi/Bi3+与I-/I 转化反应之间的协同作用实现优异的电化学性能,原理如图所示。碘离子作为氧化还原媒介体,可以加快动力学转化过程,促进更快的电荷转移。下列说法错误的是
转化反应之间的协同作用实现优异的电化学性能,原理如图所示。碘离子作为氧化还原媒介体,可以加快动力学转化过程,促进更快的电荷转移。下列说法错误的是
 转化反应之间的协同作用实现优异的电化学性能,原理如图所示。碘离子作为氧化还原媒介体,可以加快动力学转化过程,促进更快的电荷转移。下列说法错误的是
转化反应之间的协同作用实现优异的电化学性能,原理如图所示。碘离子作为氧化还原媒介体,可以加快动力学转化过程,促进更快的电荷转移。下列说法错误的是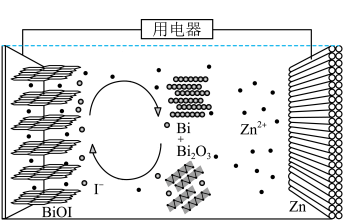
| A.充电时,主要发生的电池反应为2Bi+2Bi2O3+3ZnI2=6BiOI+3Zn |
B.放电时,部分I-在Zn电极转化为I |
| C.充电时,每生成1molBiOI,转移电子数为3mol |
D.电池工作时,I-与I 之间转化反应能够提供额外的电化学容量 之间转化反应能够提供额外的电化学容量 |
您最近一年使用:0次
2024-05-16更新
|
198次组卷
|
4卷引用:T12-电化学原理
(已下线)T12-电化学原理(已下线)选择题6-102024届宁夏回族自治区银川一中高三下学期第二次模拟考试理科综合试卷-高中化学河南省焦作市博爱县第一中学2023-2024学年高三下学期5月月考化学试题
名校
8 . 烟道气中的 本身对于
本身对于 是一种很好的还原剂,二者反应可得到硫磺,实现变废为宝。
是一种很好的还原剂,二者反应可得到硫磺,实现变废为宝。 还原
还原 的反应有:
的反应有:
ⅰ.
ⅱ.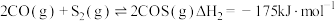
ⅲ.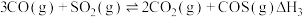
(1)已知:在标准压强、 时,由最稳定的单质合成
时,由最稳定的单质合成 物质
物质 的反应焓变,叫做物质B的标准摩尔生成焓。部分物质的标准摩尔生成焓如下图所示,计算:
的反应焓变,叫做物质B的标准摩尔生成焓。部分物质的标准摩尔生成焓如下图所示,计算:
______ 。 与
与 按物质的量之比为
按物质的量之比为 进行反应,相同时间内,在不同过渡金属氧化物催化剂作用下,
进行反应,相同时间内,在不同过渡金属氧化物催化剂作用下, 的转化率及生成硫的选择性[硫的选择性
的转化率及生成硫的选择性[硫的选择性 ]随反应温度变化的结果如下表所示:
]随反应温度变化的结果如下表所示:
①当以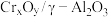 作催化剂时,试分析400℃时反应是否达到平衡状态
作催化剂时,试分析400℃时反应是否达到平衡状态______ (填“平衡”或“未平衡”),理由______ ;请解释 转化率随温度变化的可能原因是
转化率随温度变化的可能原因是______ 。
②根据以上数据判断, 与
与 反应得到硫磺的最合适条件是
反应得到硫磺的最合适条件是______ 。
(3)在一定温度和某催化剂的条件下,将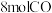 和
和 混合气体置于
混合气体置于 刚性密闭容器中进行上述反应,
刚性密闭容器中进行上述反应, 时反应达到平衡状态,测得
时反应达到平衡状态,测得 的转化率为
的转化率为 ,得到
,得到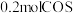 ,计算
,计算 内用
内用 表示的平均反应速率为
表示的平均反应速率为______ ;硫的选择性
______ ;反应ⅰ的平衡常数
______ (列出计算式,不用化简)。
 本身对于
本身对于 是一种很好的还原剂,二者反应可得到硫磺,实现变废为宝。
是一种很好的还原剂,二者反应可得到硫磺,实现变废为宝。 还原
还原 的反应有:
的反应有:ⅰ.

ⅱ.
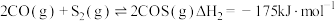
ⅲ.
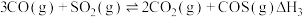
(1)已知:在标准压强、
 时,由最稳定的单质合成
时,由最稳定的单质合成 物质
物质 的反应焓变,叫做物质B的标准摩尔生成焓。部分物质的标准摩尔生成焓如下图所示,计算:
的反应焓变,叫做物质B的标准摩尔生成焓。部分物质的标准摩尔生成焓如下图所示,计算:
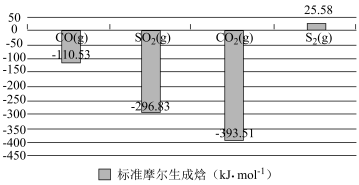
 与
与 按物质的量之比为
按物质的量之比为 进行反应,相同时间内,在不同过渡金属氧化物催化剂作用下,
进行反应,相同时间内,在不同过渡金属氧化物催化剂作用下, 的转化率及生成硫的选择性[硫的选择性
的转化率及生成硫的选择性[硫的选择性 ]随反应温度变化的结果如下表所示:
]随反应温度变化的结果如下表所示:| 温度(℃) | 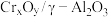 | 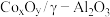 | 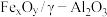 | 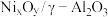 | ||||
| 转化率 | 选择性 | 转化率 | 选择性 | 转化率 | 选择性 | 转化率 | 选择性 | |
| 300 | 0.30 | 0.33 | 0.05 | 0.84 | 0.24 | 0.48 | 0.11 | 0.48 |
| 350 | 0.32 | 0.55 | 0.11 | 0.90 | 0.34 | 0.70 | 0.12 | 0.48 |
| 400 | 0.30 | 0.68 | 0.25 | 0.95 | 0.45 | 0.87 | 0.14 | 0.50 |
| 450 | 0.29 | 0.72 | 0.40 | 0.95 | 0.49 | 0.98 | 0.15 | 0.50 |
| 500 | 0.28 | 0.85 | 0.48 | 0.95 | 0.50 | 1.00 | 0.17 | 0.51 |
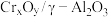 作催化剂时,试分析400℃时反应是否达到平衡状态
作催化剂时,试分析400℃时反应是否达到平衡状态 转化率随温度变化的可能原因是
转化率随温度变化的可能原因是②根据以上数据判断,
 与
与 反应得到硫磺的最合适条件是
反应得到硫磺的最合适条件是(3)在一定温度和某催化剂的条件下,将
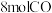 和
和 混合气体置于
混合气体置于 刚性密闭容器中进行上述反应,
刚性密闭容器中进行上述反应, 时反应达到平衡状态,测得
时反应达到平衡状态,测得 的转化率为
的转化率为 ,得到
,得到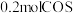 ,计算
,计算 内用
内用 表示的平均反应速率为
表示的平均反应速率为

您最近一年使用:0次
解题方法
9 . 南宁伊岭岩溶洞水体中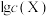 (X为
(X为 、
、 、
、 或
或 )与pH的关系如图所示,
)与pH的关系如图所示,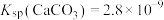 。下列说法错误的是
。下列说法错误的是
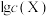 (X为
(X为 、
、 、
、 或
或 )与pH的关系如图所示,
)与pH的关系如图所示,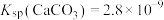 。下列说法错误的是
。下列说法错误的是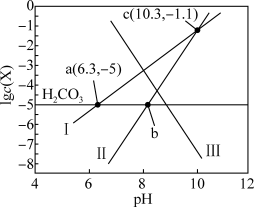
A.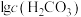 不变的原因是水体中的 不变的原因是水体中的 与空气中的 与空气中的 保持平衡 保持平衡 |
B.该温度下 与 与 为线性关系 为线性关系 |
C. 时, 时,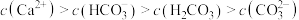 |
D.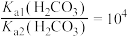 |
您最近一年使用:0次
10 . 环戊二烯 分子可与金属Na反应形成盐
分子可与金属Na反应形成盐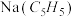 ,该盐与
,该盐与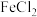 反应生成最著名的夹心化合物——二茂铁
反应生成最著名的夹心化合物——二茂铁 。回答下列问题:
。回答下列问题:
(2)第一电离能
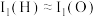 ,从原子结构角度解释
,从原子结构角度解释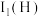
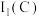 (填“>”或“<”)。
(填“>”或“<”)。(3)已知阴离子
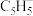 中所有原子共平面,则其中C原子的杂化轨道类型是
中所有原子共平面,则其中C原子的杂化轨道类型是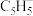 离子配体与1个
离子配体与1个 离子形成的配合物,已知中心离子价电子数与配体提供电子总数之和为18,则每个配体提供
离子形成的配合物,已知中心离子价电子数与配体提供电子总数之和为18,则每个配体提供(4)相比于吡咯(
 ),环戊二烯在水中溶解度远小于吡咯,可能原因是
),环戊二烯在水中溶解度远小于吡咯,可能原因是(5)二茂铁熔点173℃,100℃以上升华,沸点249℃,由此判断二茂铁的晶体类型为
(6)二茂铁隔绝空气受热分解为一种化学式为
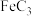 的铁碳合金,其立方晶胞结构如图所示。分析C原子旁最近的Fe原子有
的铁碳合金,其立方晶胞结构如图所示。分析C原子旁最近的Fe原子有
 (列出计算式,设阿伏加德罗常数的值为
(列出计算式,设阿伏加德罗常数的值为 )。
)。
您最近一年使用:0次



