1 . 下列制取SO2、验证其漂白性、收集并进行尾气处理的装置和原理能达到实验目的的是
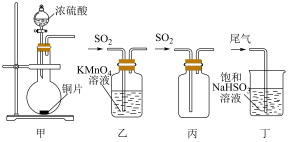
| A.用装置甲制取SO2 | B.用装置乙验证SO2的漂白性 |
| C.用装置丙收集SO2 | D.用装置丁处理实验中的尾气 |
您最近一年使用:0次
2024-03-25更新
|
1025次组卷
|
108卷引用:江苏省徐州市沛县2021-2022学年高三上学期第一次学情调研化学试题
江苏省徐州市沛县2021-2022学年高三上学期第一次学情调研化学试题2017年全国普通高等学校招生统一考试化学(江苏卷精编版)江苏省海安高级中学2018届高三1月月考化学试题(已下线)【中等生百日捷进提升系列-基础练测】专题2.15 物质的制备及实验方案设计与评价(已下线)解密16 化学实验基础(教师版)——备战2018年高考化学之高频考点解密百所名校联考-非金属及其化合物2019年秋高三化学复习强化练习—— 硫及其化合物2020届高三化学一轮复习 化学基础实验(选择题和大题训练)(已下线)专题3.4 硫及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》(已下线)专题4.3 硫及其化合物(练)——2020年高考化学一轮复习讲练测(已下线)专题4.3 硫及其化合物(讲)——2020年高考化学一轮复习讲练测(已下线)第6单元 常见的非金属元素(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷(已下线)专题讲座(四) 常见气体的实验室制备、净化和收集(精练)-2021年高考化学一轮复习讲练测(已下线)考向12 硫及其化合物-备战2022年高考化学一轮复习考点微专题(已下线)考向34 物质的检验、分离和提纯-备战2022年高考化学一轮复习考点微专题(已下线)卷13 化学基础实验(检验、鉴别、分离、提纯)-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)【教材实验热点】06 二氧化硫的漂白性(已下线)考点10 硫及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)江苏省南京市中华中学2021-2022学年高三上学期期中考试化学试题(已下线)专题突破卷13 化学实验基础(二)-2024年高考化学一轮复习考点通关卷(新教材新高考)(已下线)考点巩固卷04 非金属及其化合物(4大考点60题)?-2024年高考化学一轮复习考点通关卷(新高考通用)北京市丰台区2018届高三上学期期末考试化学试题北京市密云区2017-2018学年高三第二学期阶段性练习理综化学试题山东省淄博市淄川中学2019届高三上学期开学考试化学试题福建省莆田市莆田第二十五中学2020届高三上学期期中考试化学试题安徽省合肥二中2019-2020学年度高三上学期第一次段考化学试题安徽省芜湖市严桥中学2019-2020学年高三第一学期第三次月考化学试题宁夏回族自治区吴忠市青铜峡市高级中学2020届高三上学期第二次月考化学试题上海市同济大学第一附属中学2019—2020学年高三上学期期中考试化学试题上海市普陀区2020届高三上学期一模化学试题江苏省苏州市2018-2019学年高一上学期期末考试化学试题(已下线)广东省深圳中学2020届高三3月份教学质量监测卷理综化学试题四川省成都市第七中学2020年高中毕业班教学质量监测卷理科综合化学试题北京市丰台区首师大附属云岗中学2019届高三上学期10月月考化学试题(已下线)考点15 常见非金属元素单质及其重要化合物3——硫-2020年【衔接教材·暑假作业】新高三一轮复习化学湖南省长沙市雅礼中学2021届高三上学期第二次月考化学试题福建省漳州市平和县第一中学2021届高三上学期期中考试化学试题江苏省苏州市苏州大学附属中学2020-2021学年高一上学期月考化学试卷2江苏省苏州市园区苏州大学附属中学2020-2021学年高一上学期12月月考化学试题(已下线)【苏州新东方】04 吴县中学吉林省松原市前郭尔罗斯蒙古族自治县第五中学2021届高三下学期5月月考化学试题江苏省启东市吕四中学2020-2021学年高一下学期第二次月考化学试题江苏省昆山市周市高级中学2020-2021学年高一上学期第二次模块测试化学试题广东省深圳市第七高级中学2022届高三第一次月考化学试卷江苏省盐城市伍佑中学2021-2022学年高二上学期第一次阶段考试化学(必修)试题陕西省西安市高新第一中学2020届高三教学质量监测理综化学试题江苏省徐州市2021-2022学年高一上学期12月月考化学试题江苏省盐城市滨海县五汛中学2021-2022学年高二上学期期中考试化学试题江苏省苏州市常熟中学2022-2023学年高一上学期末测试卷一化学试题山东省鄄城县第一中学2023-2024学年高三上学期9月月考化学试题(已下线)押题卷01-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(江苏专用)(已下线)北京市西城区2024届高三下学期第三次模拟测试化学试题广东省东莞市东华高级中学 东华松山湖高级中学 2024届高三下学期第三次模拟考试 化学试题 河南省洛阳市第一高级中学2016-2017学年高一6月月考化学试题安徽省宣城市2016-2017学年高一下学期期末调研测试化学试题重庆市第一中学2017-2018学年高一下学期第一次月考化学试题【全国百强校】四川省雅安中学2018-2019学年高一上学期开学考试化学试题【校级联考】湖北省宜昌县域高中协同发展共合体2018-2019学年高一上学期期末考试化学试题【全国百强校】吉林省延边市第二中学2018-2019学年高一下学期开学考试化学试题步步为赢 高二化学暑假作业:作业十二 化学实验基础知识重庆市璧山大路中学校2018-2019学年高一下学期4月月考化学试题重庆市第三十中学2018-2019学年高一下学期期中考试化学试题第2章 第3节 化学反应的利用福建省福州市第一中学2020年高一在线自测自评质检化学试题福建省泉州第十六中学2019-2020学年高一下学期5月月考化学试题河北省衡水市桃城区第十四中学2019-2020学年高一下学期第二次调研考试化学试题广东省珠海市2019-2020学年高一下学期期末学业质量监测化学试题苏教版(2020)高一必修第一册专题4 总结检测鲁科版(2019)高一必修第一册第3章 物质的性质与转化 总结检测鲁科版(2019)高一必修第一册第三章C 高考挑战区 过高考 3年真题强化闯关北京师范大学珠海分校附属外国语学校2019-2020学年高一下学期期末考试化学试题高一必修第一册(鲁科2019)第3章 第2节 硫的转化 高考帮高一必修第二册(人教2019版)第五章 素养检测高一必修第一册(苏教2019版)专题4 C 高考挑战区高一必修第一册(苏教2019)专题4 第一单元 含硫化合物的性质3安徽省灵璧县第一中学2020-2021学年高一上学期12月月考试题山东省胶州市实验中学2020-2021学年高一上学期12月月考化学试题(已下线)练习9 硫和二氧化硫-2020-2021学年【补习教材·寒假作业】高一化学(人教版2019)专题4 第一单元综合拔高练-高中化学苏教2019版必修第一册(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第一节 硫及其化合物宁夏银川一中2020-2021学年高一上学期期末考试(GAC)化学试题(已下线)5.1.3 不同价态含硫物质的转化(基础过关)-2020-2021学年高一化学新教材新理念新设计同步课堂(人教2019必修第二册)湖南省长沙市第一中学2020-2021学年高一下学期第一次月考化学试题黑龙江省哈尔滨市阿城区龙涤中学2020-2021学年高一4月月考化学试题黑龙江省哈尔滨市第一六二中学校2020-2021学年高一下学期4月月考化学试题甘肃省金昌市第一中学2020-2021学年高一下学期期中考试化学(理)试题云南省楚雄天人中学2020-2021学年高一下学期3月月考化学(B)试题云南省楚雄天人中学2020-2021学年高一下学期3月月考化学(A)试题吉林省白城一中、大安一中、通榆一中、洮南一中、镇赉一中2020-2021学年高一下学期期末考试化学试题浙江省温州市瑞安市上海新纪元高级中学2021-2022学年高一9月份月考(5-6班)化学试题(已下线)上海市华东师范大学第二附属中学2021-2022学年高一上学期12月质量检测化学试题(已下线)第10练 硫及其化合物-2022年【寒假分层作业】高一化学(苏教版2019必修第一册)甘肃省张掖市第二中学 2021-2022学年高一下学期3月月考化学试题宁夏青铜峡市高级中学2021-2022学年高一上学期期末考试化学试题上海市七宝中学 2021-2022学年高一下学期期中考试化学试题(已下线)【期末复习】必刷题(1)-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)广东省广州市育才中学2021-2022学年高一下学期期中考试化学试题天津市第二十一中学2021-2022学年高一下学期期中学情调研化学试题新疆维吾尔自治区阿克苏地区第二中学2021-2022学年高一年级下学期第二次月考化学试题江西省上饶市2019-2020学年高一下学期期末教学质量测试化学试题四川省资阳市乐至中学2022-2023学年高一下学期3月月考化学试题四川省自贡市荣县2022-2023学年高一下学期4月期中考试化学试题广东省广州市协和中学2022-2023学年高一下学期期中考试化学试题广东省广州科学城中学2022-2023学年高一下学期期中考试化学试题福建省漳州市第一中学2023-2024学年高一上学期化学12月月考(第二单元)江西省丰城市东煌学校2022-2023学年高一下学期6月期末考试化学试题广东实验中学越秀学校2023-2024学年高一3月段考化学试题黑龙江省双鸭山市第一中学2023-2024学年高一下学期4月月考化学试题
2 . 已知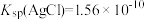 ,
,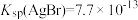 ,
, 。某溶液中含有
。某溶液中含有 、
、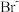 和
和 ,浓度均为0.010
,浓度均为0.010 ,向该溶液中逐滴加入0.010
,向该溶液中逐滴加入0.010 的
的 溶液时,三种阴离子产生沉淀的先后顺序为
溶液时,三种阴离子产生沉淀的先后顺序为
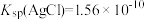 ,
,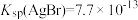 ,
, 。某溶液中含有
。某溶液中含有 、
、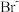 和
和 ,浓度均为0.010
,浓度均为0.010 ,向该溶液中逐滴加入0.010
,向该溶液中逐滴加入0.010 的
的 溶液时,三种阴离子产生沉淀的先后顺序为
溶液时,三种阴离子产生沉淀的先后顺序为A. | B. |
C. | D.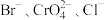 |
您最近一年使用:0次
2023-12-31更新
|
268次组卷
|
100卷引用:2018版化学(苏教版)高考总复习专题八对接高考精练--难溶电解质的沉淀溶解平衡
2018版化学(苏教版)高考总复习专题八对接高考精练--难溶电解质的沉淀溶解平衡夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——溶度积常数及相关计算(强化练习)(已下线)易错17 难溶电解质的溶解平衡及应用-备战2021年高考化学一轮复习易错题(已下线)第28讲 难溶电解质的溶解平衡 (精练)-2021年高考化学一轮复习讲练测(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第24讲 沉淀溶解平衡(练) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)第5讲 沉淀溶解平衡-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)(已下线)考点29 沉淀溶解平衡-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点巩固卷09 水溶液中的离子反应与平衡(4大考点62题)-2024年高考化学一轮复习考点通关卷(新高考通用)2013年全国普通高等学校招生统一考试理科综合能力测试化学(新课标Ⅰ卷)2016届山东省寿光现代中学高三下学期开学检测化学试卷2016届山东省青岛市高三上学期期末考试化学试卷(已下线)2018年11月15日 《每日一题》人教选修4-溶度积的应用(已下线)2019年11月14日 《每日一题》人教版(选修4)——溶度积的应用内蒙古通辽市开鲁县第一中学2021届高三上学期第一次月考化学试题江苏省盐城市阜宁中学2020-2021学年高二下学期期中考试化学试题云南省陆良县2019届高三毕业班第二次教学质量摸底考化学试题四川省成都市第七中学2023届高三上学期零诊模拟考试化学试题河南省郑州市宇华实验学校2023-2024学年高三上学期开学(摸底)考试化学试题(已下线)2013-2014学年湖南省常德市一中高二上学期第二次检测理科化学试卷(已下线)2013-2014重庆市重庆八中下学期高二期中考试化学试卷(已下线)2013-2014福建省安溪八中高二下学期期末考试化学试卷2014-2015河南省濮阳市一中高二上学期第三次质量检测化学试卷2014-2015河南省濮阳市一中高二上学期第三次月考化学试卷2014-2015湖北省武汉华中师大附高二上学期期末化学试卷2014-2015广西桂林市第十八中学高二下学期期中考试化学试卷2015-2016学年山西省太原五中高二上12月月考化学试卷12015-2016学年山西省太原五中高二上12月月考化学试卷22015-2016学年黑龙江省哈尔滨三中高二上期末化学试卷2015-2016学年贵州省凯里一中高二上学期期末化学试卷2015-2016学年宁夏育才中学高二上期末考试化学试卷2015-2016学年湖南省株洲十八中高二上学期期末理化学试卷2015-2016学年福建省龙海市程溪中学高二下学期期中化学试卷2015-2016学年广西桂林十八学高二下期中化学试卷2016-2017学年河北省邯郸一中高二上期中化学卷2016-2017学年宁夏育才中学高二上月考二化学卷22016-2017学年西藏拉萨中学高二上期末化学试卷2016-2017学年河北省张家口市高二上学期期末考试化学试卷2016-2017学年河北省邯郸市高二上学期期末考试化学试卷广西桂林市桂林中学2016-2017学年高二下学期期中考试化学试题四川省成都市双流中学2016-2017学年高二5月月考化学试题内蒙古北京八中乌兰察布分校2016-2017学年高二下学期期末考试化学试题福建省福州市第八中学2016-2017学年高二下学期期末考试(理)化学试题河北省定州中学2017-2018学年高二上学期开学考试化学试题贵州省遵义航天高级中学2017-2018学年高二上学期第三次月考理综(理)化学试题天津市静海县第一中学2017-2018学年高二12月学生学业能力调研考试化学试题山西省大同市第一中学2017-2018学年高二上学期期末考试化学试题【全国百强校】甘肃省天水市一中2018-2019学年高二(理)上学期第二学段考试化学试题安徽省滁州市定远县民族中学2018-2019学年高二上学期12月月考化学试题内蒙古集宁一中西校区2017-2018学年高二上学期期中考试化学试题云南省保山市第一中学2018-2019学年高二下学期期末化学试题安徽省太和第一中学2019-2020学年高二上学期第一次月考(飞越班)化学试题重庆市凤鸣山中学2018-2019学年高二上学期期中考试化学试题湖北省黄冈市黄梅国际育才高级中学2019-2020学年高二上学期10月月考化学试题鲁科版(2019)选择性必修1第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡 课时1 沉淀溶解平衡及其应用鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡高中必刷题高二选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 课时1 溶解平衡及其应用(已下线)第03章 物质在水溶液中的行为 (B卷能力提升卷) -2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 方法帮黑龙江省鹤岗市第一中学2020-2021学年高二10月月考化学试题黑龙江绥化市第一中学2020-2021学年高二上学期第一次月考化学试题 (已下线)第03章 水溶液中的离子反应与平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)重庆市万州第三中学2020-2021学年高二上学期期中考试化学试题(已下线)3.4 难溶电解质的溶解平衡(基础练)-2020-2021学年高二化学上学期十分钟同步课堂专练(人教版选修4)吉林省长春市第二十九中学2020-2021学年高二上学期期末考试化学试题(已下线)练习14 难溶电解质的沉淀溶解平衡-2020-2021学年【补习教材·寒假作业】高二化学(苏教版)吉林省长春市清蒲中学2020-2021学年度高二上学期期末化学试题甘肃省民勤县第一中学2020-2021学年高二下学期(理)开学考试化学试题山西省潞城第一中学2020-2021学年高二下学期3月月考化学试卷题云南省玉溪市华宁二中2020-2021学年高二下学期期中考试化学试题四川省绵阳市2020-2021学年高二下学期期末考试化学试题江西省靖安中学2020-2021学年高二上学期第二次月考化学试题四川省绵阳市盐亭中学2021-2022学年高二下学期4月月考化学试题四川省遂宁市第二中学校2021-2022学年高二下学期半期考试化学试题山东省德州市2020-2021学年高二上学期反应原理月考(B)化学试题第四节 沉淀溶解平衡 第2课时 沉淀溶解平衡的应用(已下线)3.4.1 沉淀溶解平衡-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)湖南省长沙市明德中学2022-2023学年高二上学期期中考试化学试题广东省江门市第一中学2022-2023学年高二上学期第二次月考化学试题(已下线)3.4 沉淀溶解平衡-同步学习必备知识山东省淄博市桓台第二中学2021-2022学年高一9月月考化学试题河北省邯郸市永年区第二中学2022-2023学年高二上学期12月月考化学试题黑龙江省伊春市伊美区第二中学2022-2023学年高二上学期期中化学试题黑龙江省双鸭山市第一中学2022-2023学年高二下学期开学考试化学试题吉林省洮南市第一中学2022-2023学年高二上学期期末考试化学试题四川省内江市第六中学2022-2023学年高二下学期第一次月考(创新班)化学试题广东番禺中学2022-2023学年高二上学期期末测试化学试题第2课时 沉淀的溶解与生成、转化及应用第1课时 沉淀溶解平衡与溶度积第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 第2课时 沉淀溶解平衡的应用新疆奎屯市第一高级中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假作业07 沉淀溶解平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)四川省泸州市合江县马街中学校2023-2024学年高二上学期11月期中化学试题(已下线)专题06 沉淀溶解平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)陕西省咸阳市武功县普集高级中学2023-2024学年高二上学期12月月考化学试题陕西省汉中市西乡县第一中学2023-2024学年高二上学期12月月考化学试题宁夏石嘴山市第三中学2023-2024学年高二上学期第二次月考化学试题四川省眉山市仁寿县2023-2024学年高二上学期12月联考化学试题河北省衡水市安平中学2023-2024学年高二下学期开学考试化学试题
11-12高二上·吉林·期末
名校
3 . 已知维生素C的结构简式为图1,丁香油酚的结构简式为图2。

下列关于两者的说法正确的是

下列关于两者的说法正确的是
| A.均含酯基 | B.均含碳碳双键 |
| C.均含醇羟基和酚羟基 | D.均为芳香族化合物 |
您最近一年使用:0次
2023-10-28更新
|
169次组卷
|
25卷引用:2018版化学(苏教版)高考总复习专题十二课时跟踪训练--认识有机化合物
2018版化学(苏教版)高考总复习专题十二课时跟踪训练--认识有机化合物(已下线)第1讲 有机化合物的结构特点与研究方法(已下线)狂刷01 有机化合物的分类—《小题狂刷》2017-2018学年高二化学人教选修5(已下线)2010—2011学年吉林省实验中学高二上学期期末质量检测化学试卷(已下线)2011-2012学年辽宁省开原高中高二第三次月考化学试卷(已下线)2012-2013学年内蒙古巴市一中高二上学期期末考试化学试卷(已下线)2012年人教版高中化学选修5 1.1有机化合物的分类练习卷(已下线)2013-2014广东清远市市高二下学期期末考试化学试卷(已下线)同步君 选修五 第一章 第一节 有机化合物的分类高中化学人教版 选修五 第一章 第一节 有机化合物的分类2018-2019学年苏教版高二化学选修5《 专题2 有机物的结构与分类 》同步检测题人教化学选修5第一章第一节云南省曲靖市宣威市第九中学2019-2020高二上学期期中考试化学试题北京市第十四中学2019-2020学年高二下学期期中考试化学试题安徽省合肥市庐江三中2019-2020学年度高二下学期月考化学试题吉林省白城市通榆县第一中学2019-2020学年高二下学期第三次月考(5月)化学试题云南省玉龙纳西族自治县田家炳民族中学2020-2021学年高二上学期期中考试化学试题山东省济宁市曲阜一中2020-2021学年高二下学期4月月考化学试题山东省滨州市惠民县第二中学致远高中部2020-2021学年高二上学期期中考试化学试题(鲁科版2019)选3第1章 第1节 认识有机化学 课时2广东省广州市北大附中为明广州实验学校2020-2021学年高二下学期3月月考化学试题课后-1.1.1 有机化合物的分类-人教2019选择性必修3黑龙江省鸡西市第四中学2021-2022学年高二下学期期中考试化学试题第一节 有机化合物的结构特点 第1课时 有机化合物的分类方法宁夏石嘴山市平罗中学2023-2024学年高二上学期期中考试化学试题
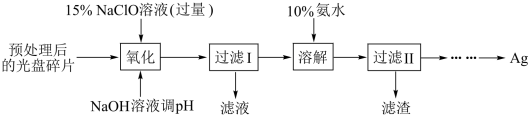
4 . 某科研小组采用如下方案回收一种光盘金属层中的少量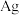 (金属层中其他金属含量过低,对实验的影响可忽略)。
(金属层中其他金属含量过低,对实验的影响可忽略)。
已知:① 溶液在受热或酸性条件下易分解,如:
溶液在受热或酸性条件下易分解,如: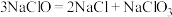
② 可溶于氨水生成
可溶于氨水生成
③常温时 (水合肼)在碱性条件下能还原
(水合肼)在碱性条件下能还原 :
: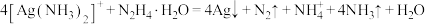 。
。
(1)“氧化”阶段需在 条件下进行,适宜的加热方式为
条件下进行,适宜的加热方式为___________ 。
(2) 溶液与
溶液与 反应的产物为
反应的产物为 、
、 和
和 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。 也能氧化
也能氧化 ,从反应产物的角度分析,以
,从反应产物的角度分析,以 代替
代替 的缺点是
的缺点是___________ 。
(3)为提高 的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并
的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并___________ 。
(4)若省略“过滤Ⅰ”,直接向冷却后的反应容器中滴加 氨水,则需要增加氨水的用量,除因过量
氨水,则需要增加氨水的用量,除因过量 与
与 反应外(该条件下
反应外(该条件下 与
与 不反应),还因为
不反应),还因为___________ 。
(5)“溶解”阶段发生反应的离子方程式为___________ 。
(6)请设计从“过滤Ⅱ”后的滤液中获取单质 的实验方案:
的实验方案:___________ (实验中须使用的试剂有: 水合肼溶液,
水合肼溶液,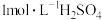 )。
)。
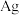 (金属层中其他金属含量过低,对实验的影响可忽略)。
(金属层中其他金属含量过低,对实验的影响可忽略)。
已知:①
 溶液在受热或酸性条件下易分解,如:
溶液在受热或酸性条件下易分解,如: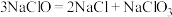
②
 可溶于氨水生成
可溶于氨水生成
③常温时
 (水合肼)在碱性条件下能还原
(水合肼)在碱性条件下能还原 :
: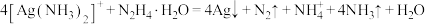 。
。(1)“氧化”阶段需在
 条件下进行,适宜的加热方式为
条件下进行,适宜的加热方式为(2)
 溶液与
溶液与 反应的产物为
反应的产物为 、
、 和
和 ,该反应的化学方程式为
,该反应的化学方程式为 也能氧化
也能氧化 ,从反应产物的角度分析,以
,从反应产物的角度分析,以 代替
代替 的缺点是
的缺点是(3)为提高
 的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并
的回收率,需对“过滤Ⅱ”的滤渣进行洗涤,并(4)若省略“过滤Ⅰ”,直接向冷却后的反应容器中滴加
 氨水,则需要增加氨水的用量,除因过量
氨水,则需要增加氨水的用量,除因过量 与
与 反应外(该条件下
反应外(该条件下 与
与 不反应),还因为
不反应),还因为(5)“溶解”阶段发生反应的离子方程式为
(6)请设计从“过滤Ⅱ”后的滤液中获取单质
 的实验方案:
的实验方案: 水合肼溶液,
水合肼溶液,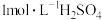 )。
)。
您最近一年使用:0次
2023高三上·江苏·专题练习
5 . 二氧化碳的排放受到环境和能源领域的关注,其综合利用是研究的重要课题。
Ⅰ.第19届亚洲运动会使用废碳再生的绿色零碳甲醇作为主火炬塔燃料,利用焦炉气中的 与从工业尾气中捕集的
与从工业尾气中捕集的 合成,实现循环内零碳排放。
合成,实现循环内零碳排放。
(1)已知:反应I: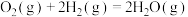
 kJ/mol
kJ/mol
反应Ⅱ:
 kJ/mol
kJ/mol
合成甲醇的反应:

_______ kJ/mol。
(2) 催化加氢制甲醇可能的反应历程如下图。
催化加氢制甲醇可能的反应历程如下图。 首先在Zn-Ga-O表面解离成2个
首先在Zn-Ga-O表面解离成2个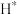 ,随后参与到
,随后参与到 的还原过程。
的还原过程。
理论上,反应历程中消耗的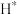 与生成的甲醇的物质的量之比为
与生成的甲醇的物质的量之比为_______ 。
(3)该催化条件下,主要的副反应为: 。实际工业生产中,需要在260℃、压强恒为4.0 MPa的反应釜中进行上述反应。为确保反应的连续性,需向反应釜中以进气流量0.04 mol/min、
。实际工业生产中,需要在260℃、压强恒为4.0 MPa的反应釜中进行上述反应。为确保反应的连续性,需向反应釜中以进气流量0.04 mol/min、 持续通入原料,同时控制出气流量。
持续通入原料,同时控制出气流量。
①需控制出气流量小于进气流量的原因为_______ 。
②已知出气流量为0.03 mol/min,单位时间 的转化率为60%,则流出气体中
的转化率为60%,则流出气体中 的百分含量为
的百分含量为_______ 。
Ⅱ.高炉气中捕集 制储氢物质HCOOH的综合利用示意图如下图所示:
制储氢物质HCOOH的综合利用示意图如下图所示: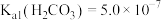 ,
,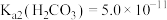
(4)T温度下,当吸收池中溶液的 时,此时该溶液中
时,此时该溶液中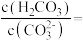
_______ 。
(5)电解池中 电催化还原为HCOOH。
电催化还原为HCOOH。
①铂电极反应方程式为_______ 。
②铂电极上的副反应除析氢外,没有其它放电过程。若生成HCOOH的电解效率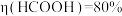 。当电路中转移3 mol
。当电路中转移3 mol  时,阴极室溶液的质量增加
时,阴极室溶液的质量增加_______ g。定义:
Ⅰ.第19届亚洲运动会使用废碳再生的绿色零碳甲醇作为主火炬塔燃料,利用焦炉气中的
 与从工业尾气中捕集的
与从工业尾气中捕集的 合成,实现循环内零碳排放。
合成,实现循环内零碳排放。(1)已知:反应I:
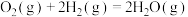
 kJ/mol
kJ/mol反应Ⅱ:

 kJ/mol
kJ/mol合成甲醇的反应:


(2)
 催化加氢制甲醇可能的反应历程如下图。
催化加氢制甲醇可能的反应历程如下图。 首先在Zn-Ga-O表面解离成2个
首先在Zn-Ga-O表面解离成2个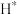 ,随后参与到
,随后参与到 的还原过程。
的还原过程。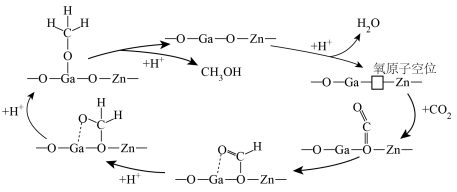
理论上,反应历程中消耗的
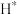 与生成的甲醇的物质的量之比为
与生成的甲醇的物质的量之比为(3)该催化条件下,主要的副反应为:
 。实际工业生产中,需要在260℃、压强恒为4.0 MPa的反应釜中进行上述反应。为确保反应的连续性,需向反应釜中以进气流量0.04 mol/min、
。实际工业生产中,需要在260℃、压强恒为4.0 MPa的反应釜中进行上述反应。为确保反应的连续性,需向反应釜中以进气流量0.04 mol/min、 持续通入原料,同时控制出气流量。
持续通入原料,同时控制出气流量。①需控制出气流量小于进气流量的原因为
②已知出气流量为0.03 mol/min,单位时间
 的转化率为60%,则流出气体中
的转化率为60%,则流出气体中 的百分含量为
的百分含量为Ⅱ.高炉气中捕集
 制储氢物质HCOOH的综合利用示意图如下图所示:
制储氢物质HCOOH的综合利用示意图如下图所示:
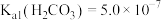 ,
,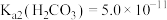
(4)T温度下,当吸收池中溶液的
 时,此时该溶液中
时,此时该溶液中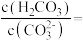
(5)电解池中
 电催化还原为HCOOH。
电催化还原为HCOOH。①铂电极反应方程式为
②铂电极上的副反应除析氢外,没有其它放电过程。若生成HCOOH的电解效率
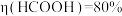 。当电路中转移3 mol
。当电路中转移3 mol  时,阴极室溶液的质量增加
时,阴极室溶液的质量增加
您最近一年使用:0次
2023高三上·江苏·专题练习
解题方法
6 . 以银锰精矿(主要含 、MnS、
、MnS、 )和氧化锰矿(主要含
)和氧化锰矿(主要含 )为原料联合提取银和锰的一种流程示意图如下。
)为原料联合提取银和锰的一种流程示意图如下。
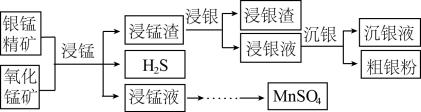
已知:酸性条件下, 的氧化性强于
的氧化性强于 。
。
(1)“浸锰”过程是在 溶液中使矿石中的锰元素浸出,同时去除
溶液中使矿石中的锰元素浸出,同时去除 ,有利于后续银的浸出:矿石中的银以
,有利于后续银的浸出:矿石中的银以 的形式残留于浸锰渣中。“浸锰”过程中,银锰精矿中的
的形式残留于浸锰渣中。“浸锰”过程中,银锰精矿中的 和氧化锰矿中的
和氧化锰矿中的 发生反应,则浸锰液中主要的金属阳离子有
发生反应,则浸锰液中主要的金属阳离子有_______ 。
(2)“浸银”时,使用过量 、HCl和
、HCl和 的混合液作为浸出剂,将
的混合液作为浸出剂,将 中的银以
中的银以 形式浸出并生成S。写出“浸银”反应的离子方程式:
形式浸出并生成S。写出“浸银”反应的离子方程式:_______ 。结合平衡移动原理,解释浸出剂中 、
、 的作用:
的作用:_______ 。
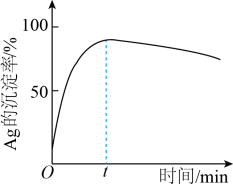
(3)“沉银”过程中需要过量的铁粉作为还原剂。
①写出“沉银”的离子方程式_______ 。
②一定温度下,Ag的沉淀率随反应时间的变化如图所示。解释t分钟后Ag的沉淀率逐渐减小的原因:_______ 。
(4)结合“浸锰”过程,从两种矿石中各物质利用的角度,分析联合提取银和锰的优点:可将两种矿石中的锰元素同时提取到浸锰液中得到 ;将银元素和锰元素分离;
;将银元素和锰元素分离;_______ 。
 、MnS、
、MnS、 )和氧化锰矿(主要含
)和氧化锰矿(主要含 )为原料联合提取银和锰的一种流程示意图如下。
)为原料联合提取银和锰的一种流程示意图如下。
已知:酸性条件下,
 的氧化性强于
的氧化性强于 。
。(1)“浸锰”过程是在
 溶液中使矿石中的锰元素浸出,同时去除
溶液中使矿石中的锰元素浸出,同时去除 ,有利于后续银的浸出:矿石中的银以
,有利于后续银的浸出:矿石中的银以 的形式残留于浸锰渣中。“浸锰”过程中,银锰精矿中的
的形式残留于浸锰渣中。“浸锰”过程中,银锰精矿中的 和氧化锰矿中的
和氧化锰矿中的 发生反应,则浸锰液中主要的金属阳离子有
发生反应,则浸锰液中主要的金属阳离子有(2)“浸银”时,使用过量
 、HCl和
、HCl和 的混合液作为浸出剂,将
的混合液作为浸出剂,将 中的银以
中的银以 形式浸出并生成S。写出“浸银”反应的离子方程式:
形式浸出并生成S。写出“浸银”反应的离子方程式: 、
、 的作用:
的作用:(3)“沉银”过程中需要过量的铁粉作为还原剂。
①写出“沉银”的离子方程式
②一定温度下,Ag的沉淀率随反应时间的变化如图所示。解释t分钟后Ag的沉淀率逐渐减小的原因:

(4)结合“浸锰”过程,从两种矿石中各物质利用的角度,分析联合提取银和锰的优点:可将两种矿石中的锰元素同时提取到浸锰液中得到
 ;将银元素和锰元素分离;
;将银元素和锰元素分离;
您最近一年使用:0次
名校
7 . 有关反应Si(s)+3HCl(g) SiHCl3(g)+H2(g) ΔH=-141.8kJ•mol-1的说法正确的是
SiHCl3(g)+H2(g) ΔH=-141.8kJ•mol-1的说法正确的是
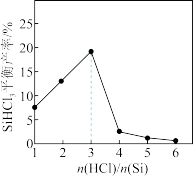
 SiHCl3(g)+H2(g) ΔH=-141.8kJ•mol-1的说法正确的是
SiHCl3(g)+H2(g) ΔH=-141.8kJ•mol-1的说法正确的是
| A.该反应在低温条件下不能自发 |
| B.其他条件不变,增大压强SiHCl3平衡产率减小 |
| C.实际工业生产选择高温,原因是高温时Si的平衡转化率比低温时大 |
D.如图所示,当 >3,SiHCl3平衡产率减小可能发生了副反应 >3,SiHCl3平衡产率减小可能发生了副反应 |
您最近一年使用:0次
2023-10-19更新
|
213次组卷
|
3卷引用:选择题11-13
名校
解题方法
8 . 黏土钒矿中,钒以+3价、+4价、+5价的化合物存在,还包括SiO2、Fe2O3和铝硅酸盐(Al2O3•SiO2)等。采用以下流程可由黏土钒矿制备V2O5、Fe2O3和硫酸铝铵。
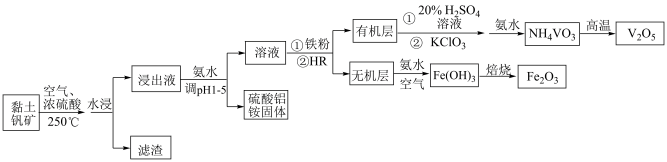
已知:i.有机酸性萃取剂HR的萃取原理为:Mn+(aq)+nHR(org) MRn(org)+Nh+(aq)(org表示有机溶液)
MRn(org)+Nh+(aq)(org表示有机溶液)
ii.酸性溶液中,HR对VO2+、Fe3+萃取能力强,而对 的萃取能力较弱
的萃取能力较弱
(1)从黏土钒矿到浸出液的流程中,加快浸出速率的措施还有_______ 。(任写一条)
(2)滤渣的主要成分是_______ 。
(3)浸出液中钒以+4价、+5价的形式存在,简述加入铁粉的原因_______ 。
(4)KClO3和VO2+反应生成 和Cl-的离子方程式
和Cl-的离子方程式_______ 。
(5)硫酸工业中,V2O5是反应2SO2+O2 2SO3的催化剂,催化过程经两步完成,可能的催化过程为:
2SO3的催化剂,催化过程经两步完成,可能的催化过程为:_______ 、_______ 。(用化学方程式表示,中间产物为VO2)。
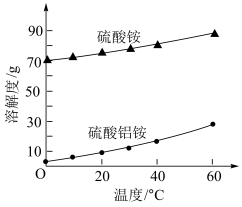
(6)从无机层获得Fe(OH)3的离子方程式是_______ 。
(7)硫酸铝铵固体中含有少量硫酸铵杂质,根据如图的溶解度曲线,进一步提纯硫酸铝铵的操作名称是_______ 。

已知:i.有机酸性萃取剂HR的萃取原理为:Mn+(aq)+nHR(org)
 MRn(org)+Nh+(aq)(org表示有机溶液)
MRn(org)+Nh+(aq)(org表示有机溶液)ii.酸性溶液中,HR对VO2+、Fe3+萃取能力强,而对
 的萃取能力较弱
的萃取能力较弱(1)从黏土钒矿到浸出液的流程中,加快浸出速率的措施还有
(2)滤渣的主要成分是
(3)浸出液中钒以+4价、+5价的形式存在,简述加入铁粉的原因
(4)KClO3和VO2+反应生成
 和Cl-的离子方程式
和Cl-的离子方程式(5)硫酸工业中,V2O5是反应2SO2+O2
 2SO3的催化剂,催化过程经两步完成,可能的催化过程为:
2SO3的催化剂,催化过程经两步完成,可能的催化过程为:(6)从无机层获得Fe(OH)3的离子方程式是
(7)硫酸铝铵固体中含有少量硫酸铵杂质,根据如图的溶解度曲线,进一步提纯硫酸铝铵的操作名称是

您最近一年使用:0次
名校
解题方法
9 . 铬和铝广泛用于冶金、国防、化工等领域。从铝热法冶炼金属得到的铬废渣(主要含Al2O3、Cr2O3,还含有少量SiO2、KCl)中提取铬和铝的主要工艺流程如下:
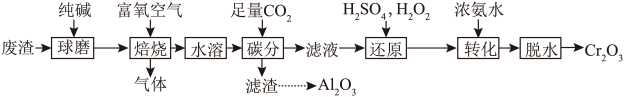
已知:SiO2、Al2O3 在高温下能与纯碱反应生成Na2SiO3和NaAlO2。
回答下列问题:
(1)“球磨”工序的目的是_______ 。
(2)“焙烧”时生成Na2CrO4的化学方程式为_______ 。
(3)“水溶”时,温度为80℃,其他条件相同,铬的溶出率与液固比的变化关系如图1所示;Na2CrO4的溶解度曲线如图2所示。
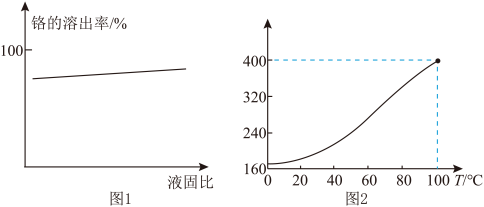
80℃时, 随液固比的增大,铬的溶出率变化不大的原因是_______ 。
(4)“碳分“工序所得滤渣中除含有H2SiO3 外,还含有_______ (填化学式)。滤液中含碳物种经回收并煅烧后所得产物可分别循环到_______ 工序中再利用。
(5)还原”时,Na2CrO4被还原的离子方程式为_______ ;若用盐酸代替H2SO4和H2O2的混合液,主要缺点为_______ ;
(6)“转化“时,控制温度不能过高或过低的原因是_______ 。

已知:SiO2、Al2O3 在高温下能与纯碱反应生成Na2SiO3和NaAlO2。
回答下列问题:
(1)“球磨”工序的目的是
(2)“焙烧”时生成Na2CrO4的化学方程式为
(3)“水溶”时,温度为80℃,其他条件相同,铬的溶出率与液固比的变化关系如图1所示;Na2CrO4的溶解度曲线如图2所示。

80℃时, 随液固比的增大,铬的溶出率变化不大的原因是
(4)“碳分“工序所得滤渣中除含有H2SiO3 外,还含有
(5)还原”时,Na2CrO4被还原的离子方程式为
(6)“转化“时,控制温度不能过高或过低的原因是
您最近一年使用:0次
2023-10-17更新
|
245次组卷
|
3卷引用:工业流程题
名校
10 . 化合物J是一种昆虫生长调节剂,其人工合成路线如下:

(1)F用系统命名法命名为_______ ;G中含有的官能团的名称为_______ 。
(2)C的分子式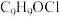 ,其结构简式为
,其结构简式为_______ 。
(3) 反应需控制在130℃左右,温度过高会有一种分子式为
反应需控制在130℃左右,温度过高会有一种分子式为 的副产物生成,该副产物的结构筒式为
的副产物生成,该副产物的结构筒式为_______ 。
(4)H的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:_______ 。
①能发生银镜反应,能与 溶液发生显色,碱性条件水解
溶液发生显色,碱性条件水解
②分子中含有4种不同化学环境的氢原子;
(5)合成时不采用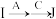 的方法,原因是
的方法,原因是_______ 。
(6)已知: 。写出以甲苯、
。写出以甲苯、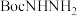 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图_______ (无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)

(1)F用系统命名法命名为
(2)C的分子式
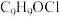 ,其结构简式为
,其结构简式为(3)
 反应需控制在130℃左右,温度过高会有一种分子式为
反应需控制在130℃左右,温度过高会有一种分子式为 的副产物生成,该副产物的结构筒式为
的副产物生成,该副产物的结构筒式为(4)H的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:
①能发生银镜反应,能与
 溶液发生显色,碱性条件水解
溶液发生显色,碱性条件水解②分子中含有4种不同化学环境的氢原子;
(5)合成时不采用
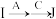 的方法,原因是
的方法,原因是(6)已知:
 。写出以甲苯、
。写出以甲苯、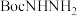 为原料制备
为原料制备 的合成路线流程图
的合成路线流程图
您最近一年使用:0次



