名校
1 . 化学家们对化学学科的发展做出巨大的贡献。下列有关说法错误的是
| A.俄国化学家盖斯提出盖斯定律,为化学动力学发展奠定了基础 |
| B.德国化学家维勒合成了尿素,开创了人工合成有机化合物的新时代 |
| C.中国化学家侯德榜发明了联合制碱法,打破外国对我国的技术封锁 |
| D.法国化学家拉瓦锡提出燃烧的氧化学说,使近代化学取得革命性的进展 |
您最近一年使用:0次
2024-04-04更新
|
847次组卷
|
4卷引用:选择题6-10
解题方法
2 . Ⅰ. 又称臭碱、硫化碱,实验室拟用以下方案研究
又称臭碱、硫化碱,实验室拟用以下方案研究 的性质。
的性质。
(1)用离子方程式说明 溶液呈碱性的原因
溶液呈碱性的原因________ 。
(2)向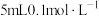 的酸性
的酸性 溶液(pH=0)中滴加10滴同浓度的
溶液(pH=0)中滴加10滴同浓度的 溶液,观察到溶液紫色变浅(pH>1),生成棕褐色沉淀(
溶液,观察到溶液紫色变浅(pH>1),生成棕褐色沉淀( ),说明
),说明 具有还原性。有同学预测该反应中
具有还原性。有同学预测该反应中 转化为
转化为 ,该预测
,该预测________ (填“正确”或“不正确”),原因是________ 。
Ⅱ.探究向 溶液中滴加
溶液中滴加 溶液的反应本质。
溶液的反应本质。
反应原理预测:发生氧化还原反应或发生完全双水解反应

已知:单质硫在酒精中的溶解度随乙醇质量分数的增大而增大
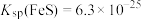
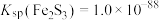
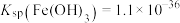
(3)根据试管a中的“局部产生红褐色沉淀”现象,推测 与
与 局部发生强烈双水解反应,生成
局部发生强烈双水解反应,生成 和
和________ (填化学式)。
(4)推测c中的沉淀为 ,根据b到c的实验现象,推测红褐色消失发生的离子方程式为
,根据b到c的实验现象,推测红褐色消失发生的离子方程式为________ 。
(5)取c中黑色固体,洗净后分别置于两支试管i、ii中进行如下实验:
试管i中涉及的化学反应方程式为________ ,试管ii中加入的试剂为________ ,结合试管i、ii现象,推测黑色固体中________ (填“含有”或“不含有”)FeS,原因是________ 。
 又称臭碱、硫化碱,实验室拟用以下方案研究
又称臭碱、硫化碱,实验室拟用以下方案研究 的性质。
的性质。(1)用离子方程式说明
 溶液呈碱性的原因
溶液呈碱性的原因(2)向
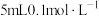 的酸性
的酸性 溶液(pH=0)中滴加10滴同浓度的
溶液(pH=0)中滴加10滴同浓度的 溶液,观察到溶液紫色变浅(pH>1),生成棕褐色沉淀(
溶液,观察到溶液紫色变浅(pH>1),生成棕褐色沉淀( ),说明
),说明 具有还原性。有同学预测该反应中
具有还原性。有同学预测该反应中 转化为
转化为 ,该预测
,该预测Ⅱ.探究向
 溶液中滴加
溶液中滴加 溶液的反应本质。
溶液的反应本质。反应原理预测:发生氧化还原反应或发生完全双水解反应

已知:单质硫在酒精中的溶解度随乙醇质量分数的增大而增大
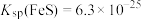
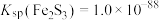
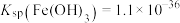
(3)根据试管a中的“局部产生红褐色沉淀”现象,推测
 与
与 局部发生强烈双水解反应,生成
局部发生强烈双水解反应,生成 和
和(4)推测c中的沉淀为
 ,根据b到c的实验现象,推测红褐色消失发生的离子方程式为
,根据b到c的实验现象,推测红褐色消失发生的离子方程式为(5)取c中黑色固体,洗净后分别置于两支试管i、ii中进行如下实验:
| 序号 | 实验步骤 | 现象 |
| i | 加入过量稀盐酸,充分振荡 | 黑色沉淀完全溶解,溶液出现淡黄色浑浊,放出少量臭鸡蛋味道气体 |
| ii | 向试管中加入________,振荡、静置,取上层清液少许加入蒸馏水中 | 未见淡黄色浑浊出现 |
您最近一年使用:0次
3 . 某研究小组按下列路线合成第三代喹诺酮类抗菌药物环丙沙星(Ⅰ)。
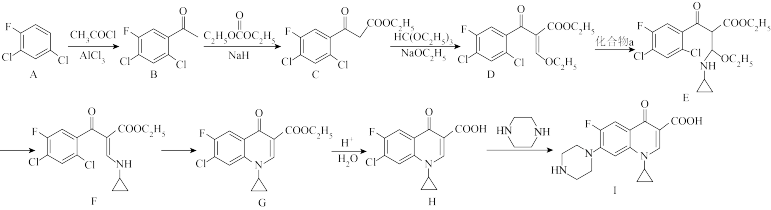
回答下列问题:
(1)C中含氧官能团名称是________ 。
(2)化合物D到化合物E的反应是原子利用率100%的反应,且1molD与1mol化合物a反应生成1molE,则化合物a的结构简式为________ 。
(3)F→G的反应类型为________ 。
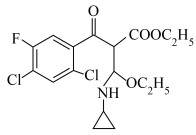
(4)试用*在下图标出化合物E中的手性碳原子。
(5)化合物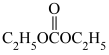 的同分异构体中,同时满足如下条件的有
的同分异构体中,同时满足如下条件的有________ 种,
a)能与碳酸氢钠反应;b)最多能与2倍物质的量的Na反应。
其中核磁共振氢谱有4组峰,且峰面积之比为6:2:1:1的结构简式为________ 。(写出一种即可)
(6)某研究小组设计以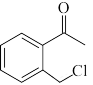 和
和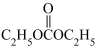 为原料合成
为原料合成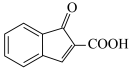 的路线如下。
的路线如下。
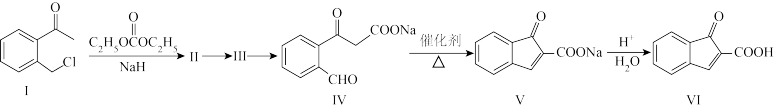
(a)化合物Ⅱ的结构简式为________ 。
(b)写出Ⅱ→Ⅲ反应所需的试剂和条件________ 。
(c)写出反应Ⅳ→Ⅴ的化学反应方程式________ 。

回答下列问题:
(1)C中含氧官能团名称是
(2)化合物D到化合物E的反应是原子利用率100%的反应,且1molD与1mol化合物a反应生成1molE,则化合物a的结构简式为
(3)F→G的反应类型为
(4)试用*在下图标出化合物E中的手性碳原子。

(5)化合物
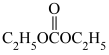 的同分异构体中,同时满足如下条件的有
的同分异构体中,同时满足如下条件的有a)能与碳酸氢钠反应;b)最多能与2倍物质的量的Na反应。
其中核磁共振氢谱有4组峰,且峰面积之比为6:2:1:1的结构简式为
(6)某研究小组设计以
 和
和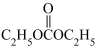 为原料合成
为原料合成 的路线如下。
的路线如下。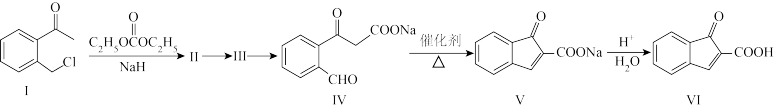
(a)化合物Ⅱ的结构简式为
(b)写出Ⅱ→Ⅲ反应所需的试剂和条件
(c)写出反应Ⅳ→Ⅴ的化学反应方程式
您最近一年使用:0次
解题方法
4 . 18世纪70年代,瑞典化学家舍勒发现一种黄绿色、有刺激性气味的气体,某兴趣小组利用下列装置进行如下实验,操作正确且能达到目的的是
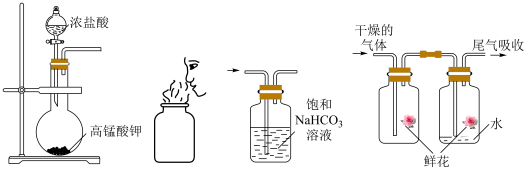

| A.制备气体 | B.闻气体气味 |
| C.除去气体中的杂质HCl | D.验证气体的漂白性 |
您最近一年使用:0次
5 . “民以食为天”,化学丰富了我们的饮食文化。下列有关说法正确的是
| A.食品添加剂都是人工合成的化学品,都有副作用 |
| B.为了让腌肉颜色更鲜艳,可添加大量亚硝酸钠 |
| C.天然的食品添加剂比人工化学食品添加剂合成的安全 |
| D.长期饮用含防腐剂、人工色素的饮品会影响人类的健康 |
您最近一年使用:0次
2024-03-15更新
|
653次组卷
|
4卷引用:选择题6-10
23-24高一下·全国·课后作业
名校
解题方法
6 . 生活处处有化学。下列有关说法错误的是
| A.傍晚看到万丈霞光穿云而过是因为丁达尔效应带来的美景 |
| B.食品包装袋内的铁粉起干燥、抗氧化的作用 |
C.豆科植物的根瘤菌能将空气中的 转化成氨,实现氮的固定 转化成氨,实现氮的固定 |
| D.氧化铁是质地疏松的红色固体,用做颜料为生活带来一抹红 |
您最近一年使用:0次
2024-03-15更新
|
1026次组卷
|
5卷引用:选择题1-5
(已下线)选择题1-52024届广东省汕头市高三下学期一模化学试题广东省汕头市2024届高三一化学试题(已下线)5.2.1氮气和氮的氧化物课后作业基础篇河南省驻马店市新蔡县第一高级中学2023-2024学年高一下学期3月月考化学试题
名校
7 . 化合物ⅸ是一种烯丙胺类抗真菌药物,可用于皮肤浅部真菌感染的治疗,它的一种合成路线如下:
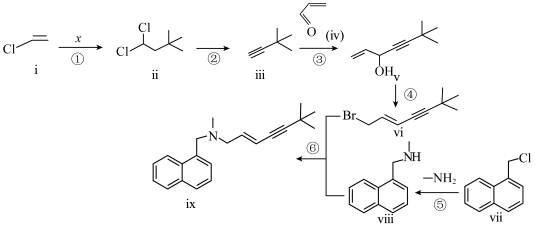
(1)根据化合物ⅰ的结构特征,分析预测其可能的化学性质,完成下表:
(2)反应①中,化合物ⅰ与有机物x反应,生成化合物ⅱ,原子利用率为100%,x为___________ (写结构简式)。
(3)化合物ⅳ中含氧官能团的名称是___________ ,反应③的类型是___________ 。
(4)关于反应⑤的说法中,不正确的有___________。
(5)化合物ⅲ有多种同分异构体,其中含 结构的有
结构的有___________ 种(不考虑立体异构),核磁共振氢谱图上只有两组峰的结构简式为___________ 。
(6)以苯乙烯和乙醛为含碳原料,利用反应③的原理,通过四步反应合成结构简式如下的化合物y,基于你设计的合成路线,回答下列问题:

(a)从苯乙烯出发,第一步反应的化学方程式为___________ 。
(b)合成路线中涉及两步消去反应,最后一步通过消去反应得到产物的化学方程式为___________ (注明反应条件)。

(1)根据化合物ⅰ的结构特征,分析预测其可能的化学性质,完成下表:
| 序号 | 反应试剂、条件 | 反应形成的新结构 | 反应类型 |
| a | 消去反应 | ||
| b | 取代反应 |
(2)反应①中,化合物ⅰ与有机物x反应,生成化合物ⅱ,原子利用率为100%,x为
(3)化合物ⅳ中含氧官能团的名称是
(4)关于反应⑤的说法中,不正确的有___________。
A.反应过程中,有 键和 键和 键断裂 键断裂 | B.反应过程中,有 键和 键和 键的形成 键的形成 |
| C.反应物ⅶ中,所有原子可能处于同一平面上 | D.生成物ⅷ具有碱性,能与稀盐酸发生反应 |
(5)化合物ⅲ有多种同分异构体,其中含
 结构的有
结构的有(6)以苯乙烯和乙醛为含碳原料,利用反应③的原理,通过四步反应合成结构简式如下的化合物y,基于你设计的合成路线,回答下列问题:

(a)从苯乙烯出发,第一步反应的化学方程式为
(b)合成路线中涉及两步消去反应,最后一步通过消去反应得到产物的化学方程式为
您最近一年使用:0次
名校
解题方法
8 . 化学与生活密切相关,下列说法正确的是
| A.日常生活中所用的花生油、牛油、石蜡油分子中均含有酯基 |
| B.用激光笔照射淀粉溶液、鸡蛋白溶液均能观察到丁达尔效应 |
| C.泡沫灭火器中所用硫酸铝、碳酸氢钠溶于水后,溶液均显酸性 |
| D.计算机芯片、硅太阳能电池、光导纤维的主要材料均为高纯硅 |
您最近一年使用:0次
名校
解题方法
9 . 化学处处呈现美。下列说法不正确的是
A.五颜六色的水晶饰品的主要成分是 |
B.莫高窟壁画历经千年仍精美绚丽,颜料中用的铁红主要成分为 |
| C.蔗糖在稀硫酸中水解后加入银氨溶液,水浴加热,试管内壁会出现光亮的银镜 |
| D.陶瓷之美惊艳世界,陶瓷是以黏土为主要原料经高温烧结而成,其主要成分属于无机非金属材料 |
您最近一年使用:0次
10 . 铁及其化合物在催化、生产实验中具有重要作用
(1)铁钴催化剂中基态Co原子的电子排布式:________ 。
(2)已知:

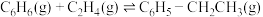

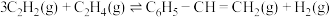

① 催化乙苯脱氢制得苯乙烯反应Ⅰ:
催化乙苯脱氢制得苯乙烯反应Ⅰ: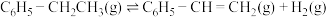

________ (用 、
、 、
、 表示)。
表示)。
②下列关于反应Ⅰ说法正确的是________ 。
A.X射线衍射技术可测得 晶体结构
晶体结构
B. 可改变乙苯平衡转化率
可改变乙苯平衡转化率
C.升高温度,正、逆反应速率均加快
D.仅从平衡移动角度分析,生产苯乙烯选择恒容条件优于恒压条件
③某温度下,向2.0L恒容密闭容器中充入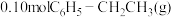 ,在催化剂作用下发生反应Ⅰ,测得乙苯脱氢反应时间(t)与容器内气体总压强(p)的数据见下表:
,在催化剂作用下发生反应Ⅰ,测得乙苯脱氢反应时间(t)与容器内气体总压强(p)的数据见下表:
用单位时间内气体分压的变化来表示反应速率,即 ,则前4h内平均反应速率
,则前4h内平均反应速率
________ 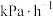 。
。
(3)常温下构建Fe(Ⅲ)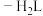 溶液体系,已知
溶液体系,已知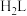 为某邻苯二酚类配体,其电离平衡常数
为某邻苯二酚类配体,其电离平衡常数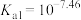 ,
,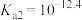 ,其中
,其中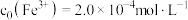 ,
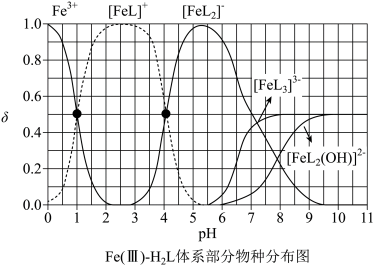
,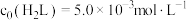 。体系中含Fe物种的组分分布系数δ与pH的关系如图所示(分布系数
。体系中含Fe物种的组分分布系数δ与pH的关系如图所示(分布系数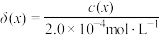 ):
):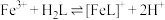 ,此时该反应的K≈
,此时该反应的K≈________ 。
②当pH=4时,参与配位的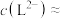
________ mol/L。
③pH在9.5~10.5之间,含L的物种主要为________ (填“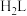 ”、“
”、“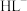 ”、“
”、“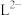 ”),列出相关计算式进行说明:
”),列出相关计算式进行说明:________ 。
(1)铁钴催化剂中基态Co原子的电子排布式:
(2)已知:


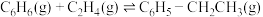

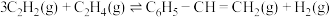

①
 催化乙苯脱氢制得苯乙烯反应Ⅰ:
催化乙苯脱氢制得苯乙烯反应Ⅰ: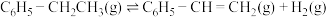

 、
、 、
、 表示)。
表示)。②下列关于反应Ⅰ说法正确的是
A.X射线衍射技术可测得
 晶体结构
晶体结构B.
 可改变乙苯平衡转化率
可改变乙苯平衡转化率C.升高温度,正、逆反应速率均加快
D.仅从平衡移动角度分析,生产苯乙烯选择恒容条件优于恒压条件
③某温度下,向2.0L恒容密闭容器中充入
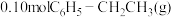 ,在催化剂作用下发生反应Ⅰ,测得乙苯脱氢反应时间(t)与容器内气体总压强(p)的数据见下表:
,在催化剂作用下发生反应Ⅰ,测得乙苯脱氢反应时间(t)与容器内气体总压强(p)的数据见下表:时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
总压强p/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
 ,则前4h内平均反应速率
,则前4h内平均反应速率
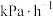 。
。(3)常温下构建Fe(Ⅲ)
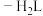 溶液体系,已知
溶液体系,已知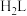 为某邻苯二酚类配体,其电离平衡常数
为某邻苯二酚类配体,其电离平衡常数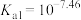 ,
,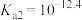 ,其中
,其中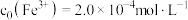 ,
,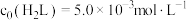 。体系中含Fe物种的组分分布系数δ与pH的关系如图所示(分布系数
。体系中含Fe物种的组分分布系数δ与pH的关系如图所示(分布系数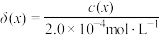 ):
):
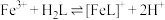 ,此时该反应的K≈
,此时该反应的K≈②当pH=4时,参与配位的
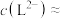
③pH在9.5~10.5之间,含L的物种主要为
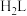 ”、“
”、“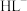 ”、“
”、“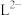 ”),列出相关计算式进行说明:
”),列出相关计算式进行说明:
您最近一年使用:0次
2024-03-06更新
|
1052次组卷
|
4卷引用:T19-原理综合题



