解题方法
1 .  是高中化学中常见铵盐,试运用所学相关的化学知识解答下列问题。
是高中化学中常见铵盐,试运用所学相关的化学知识解答下列问题。
已知:i.25℃时, 的
的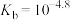 。
。
ii.氯化铵的抗碱容量是指用 溶液滴定
溶液滴定 溶液至
溶液至 时,单位质量的
时,单位质量的 所消耗
所消耗 的物质的量,即
的物质的量,即 。
。
(1) 的电子式
的电子式___________ 。
(2) 溶液呈
溶液呈___________ 性(填“酸”或“碱”),现有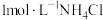 溶液,则该溶液在25℃时的pH为
溶液,则该溶液在25℃时的pH为___________ 。
(3)某化学小组测定 固体抗碱容量
固体抗碱容量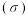 ,实验步骤如下:
,实验步骤如下:
a.配置 溶液。
溶液。
b.称取 固体,溶于
固体,溶于 水中,用上述
水中,用上述 溶液滴定至
溶液滴定至 。
。
①步骤a需要称量 固体为
固体为___________ g。
②步骤b需要用到下图所示仪器中的___________ (填名称)。 的体积为y mL,则
的体积为y mL,则
___________ 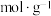 。
。
(4)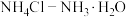 混合溶液具有抗碱能力。向该溶液中加入少量
混合溶液具有抗碱能力。向该溶液中加入少量 ,溶液的pH变化不大。现有
,溶液的pH变化不大。现有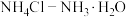 混合溶液(物质的量之比为
混合溶液(物质的量之比为 ),对于该混合溶液的下列叙述中正确的是___________。
),对于该混合溶液的下列叙述中正确的是___________。
 是高中化学中常见铵盐,试运用所学相关的化学知识解答下列问题。
是高中化学中常见铵盐,试运用所学相关的化学知识解答下列问题。已知:i.25℃时,
 的
的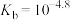 。
。ii.氯化铵的抗碱容量是指用
 溶液滴定
溶液滴定 溶液至
溶液至 时,单位质量的
时,单位质量的 所消耗
所消耗 的物质的量,即
的物质的量,即 。
。(1)
 的电子式
的电子式(2)
 溶液呈
溶液呈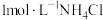 溶液,则该溶液在25℃时的pH为
溶液,则该溶液在25℃时的pH为(3)某化学小组测定
 固体抗碱容量
固体抗碱容量 ,实验步骤如下:
,实验步骤如下:a.配置
 溶液。
溶液。b.称取
 固体,溶于
固体,溶于 水中,用上述
水中,用上述 溶液滴定至
溶液滴定至 。
。①步骤a需要称量
 固体为
固体为②步骤b需要用到下图所示仪器中的
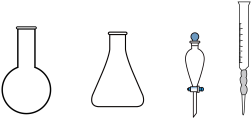
 的体积为y mL,则
的体积为y mL,则
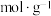 。
。(4)
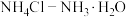 混合溶液具有抗碱能力。向该溶液中加入少量
混合溶液具有抗碱能力。向该溶液中加入少量 ,溶液的pH变化不大。现有
,溶液的pH变化不大。现有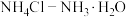 混合溶液(物质的量之比为
混合溶液(物质的量之比为 ),对于该混合溶液的下列叙述中正确的是___________。
),对于该混合溶液的下列叙述中正确的是___________。| A.常温下,该混合溶液呈酸性 |
B.溶液中离子浓度大小关系为: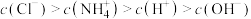 |
C.溶液中离子浓度存在恒等式: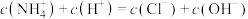 |
D.溶液中微粒间满足: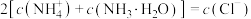 |
您最近一年使用:0次
解题方法
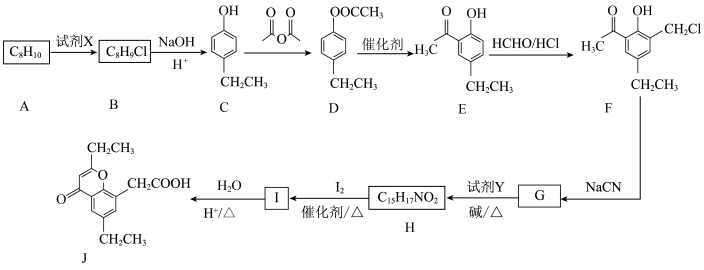
2 . 具有抗菌、消炎作用的药物有机物J的合成路线如下:
②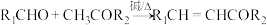
(1)有机物A的名称为___________ 。
(2)C到D的反应类型为___________ ,I的结构简式为___________ 。
(3)请写出G和试剂Y反应生成H的化学方程式:___________ 。
(4)根据有机物D的结构特征,分析预测其可能的化学性质,完成下表。
(5)同时满足下列条件的D的同分异构体共___________ 种。(不考虑立体异构)
①能发生银镜反应;
②能发生水解反应;
③属于芳香族化合物;
④苯环上含2个取代基。
(6)结合图中信息,写出以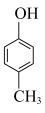 、
、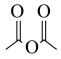 和
和 为原料设计路线合成
为原料设计路线合成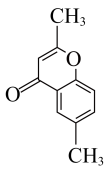 (模仿已知②③)的简单流程
(模仿已知②③)的简单流程__________ 。

②
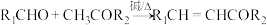
③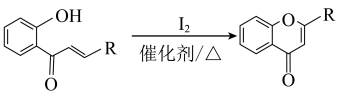
(1)有机物A的名称为
(2)C到D的反应类型为
(3)请写出G和试剂Y反应生成H的化学方程式:
(4)根据有机物D的结构特征,分析预测其可能的化学性质,完成下表。
| 序号 | 反应试剂及条件 | 反应形成的新结构 | 反应类型 |
| ① | 加成反应 | ||
| ② | 水解反应 |
(5)同时满足下列条件的D的同分异构体共
①能发生银镜反应;
②能发生水解反应;
③属于芳香族化合物;
④苯环上含2个取代基。
(6)结合图中信息,写出以
 、
、 和
和 为原料设计路线合成
为原料设计路线合成 (模仿已知②③)的简单流程
(模仿已知②③)的简单流程
您最近一年使用:0次
3 . Ⅰ.配制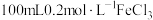 溶液。
溶液。
(1)该实验需要用到的玻璃仪器有烧杯、量筒、玻璃棒、___________ 、___________ 。
(2)为了抑制 水解,在配制过程中可以加入少量
水解,在配制过程中可以加入少量___________ 。
Ⅱ.探究盐酸酸化的 溶液显黄色,硝酸酸化的
溶液显黄色,硝酸酸化的 溶液显无色的原因。
溶液显无色的原因。
资料信息:
① 以水合离子
以水合离子 形式存在,
形式存在, 为无色,
为无色,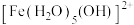 为橙黄色,
为橙黄色, 为黄色;
为黄色;
② 存在水解平衡:
存在水解平衡: 。
。
某实验小组用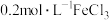 溶液、
溶液、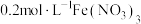 溶液、
溶液、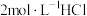 溶液、
溶液、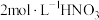 溶液、蒸馏水设计如下实验,并记录实验现象。
溶液、蒸馏水设计如下实验,并记录实验现象。
(3)根据表中信息,补充数据:a=___________ ,b=___________ 。
(4)结合实验1、2和资料信息,写出盐酸酸化的 溶液显黄色发生反应的离子方程式:
溶液显黄色发生反应的离子方程式:___________ ,通过以上实验说明 与
与 的配位能力强于
的配位能力强于 。
。
(5)结合实验3、4和资料信息,解释硝酸酸化的 溶液显无色的原因:
溶液显无色的原因:___________ 。
Ⅲ.探究不同配体与 的配位能力。
的配位能力。
开展实验并观察现象:___________ 。
(7)由上述实验可知,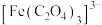 在水溶液中显
在水溶液中显___________ 色。
(8)由上述实验可知,存在配体___________ (填微粒化学式)的溶液体系中不能用 检验
检验 。
。
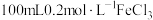 溶液。
溶液。(1)该实验需要用到的玻璃仪器有烧杯、量筒、玻璃棒、
(2)为了抑制
 水解,在配制过程中可以加入少量
水解,在配制过程中可以加入少量Ⅱ.探究盐酸酸化的
 溶液显黄色,硝酸酸化的
溶液显黄色,硝酸酸化的 溶液显无色的原因。
溶液显无色的原因。资料信息:
①
 以水合离子
以水合离子 形式存在,
形式存在, 为无色,
为无色,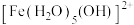 为橙黄色,
为橙黄色, 为黄色;
为黄色;②
 存在水解平衡:
存在水解平衡: 。
。某实验小组用
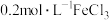 溶液、
溶液、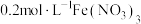 溶液、
溶液、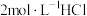 溶液、
溶液、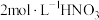 溶液、蒸馏水设计如下实验,并记录实验现象。
溶液、蒸馏水设计如下实验,并记录实验现象。| 实验序号 | V(FeCl3溶液)/mL | V[Fe(NO3)3溶液]/mL | V(HCl溶液)/mL | V(HNO3溶液)/mL | V(H2O)/mL | 现象 |
| 1 | 2 | 0 | 0 | 0 | 1 | 橙黄色 |
| 2 | 2 | 0 | 1 | 0 | 0 | 黄色 |
| 3 | 0 | 2 | 0 | 0 | 1 | 橙黄色 |
| 4 | 0 | a | 0 | b | 0 | 无色 |
(4)结合实验1、2和资料信息,写出盐酸酸化的
 溶液显黄色发生反应的离子方程式:
溶液显黄色发生反应的离子方程式: 与
与 的配位能力强于
的配位能力强于 。
。(5)结合实验3、4和资料信息,解释硝酸酸化的
 溶液显无色的原因:
溶液显无色的原因:Ⅲ.探究不同配体与
 的配位能力。
的配位能力。开展实验并观察现象:
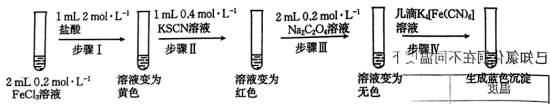
(7)由上述实验可知,
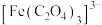 在水溶液中显
在水溶液中显(8)由上述实验可知,存在配体
 检验
检验 。
。
您最近一年使用:0次
4 . 乙烯是重要的基础化工原料,工业上利用乙烷制乙烯涉及的相关反应如下:
反应Ⅰ: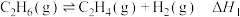
反应Ⅱ: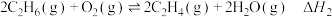
(1)在特定温度下,由稳定态单质生成1mol化合物的焓变叫该物质在此温度下的标准摩尔生成焓,下表为几种物质在298K下的标准摩尔生成焓,则反应Ⅱ的
___________  。
。
(2)过渡金属氧化物中,金属离子的最外层电子有着较强的得失电子能力,使得金属离子具有多种可变价态,因而成为应用于乙烷一氧气氧化脱氢反应最广泛的一类催化剂,含钒(V)催化剂催化乙烷制乙烯每步反应的机理如图所示,下列说法不正确的是___________(填标号)。
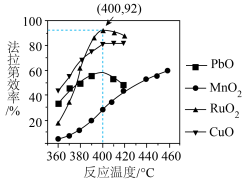
(3)一定电压下,不同催化剂电催化乙烷脱氢制乙烯的法拉第效率随温度的变化如图所示(已知法拉第效率是指实际生成物和理论生成物的百分比)。为了保证生成乙烯的法拉第效率,最合适的温度为___________ ℃,最佳催化剂是___________ 。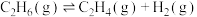 的速率方程为
的速率方程为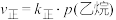 ,
,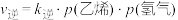 ,其中
,其中 、
、 分别为正、逆反应速率常数,
分别为正、逆反应速率常数, 为各组分分压。
为各组分分压。
①在实际生产中,t℃时,向恒容密闭容器中通入乙烷和 (作稀释剂,提高乙烷转化率),测得容器总压(
(作稀释剂,提高乙烷转化率),测得容器总压( )和乙烷转化率
)和乙烷转化率 随时间变化的结果如图所示。平衡时,平衡常数
随时间变化的结果如图所示。平衡时,平衡常数
___________ kPa(用平衡分压代替平衡浓度计算);a处的
___________ 。 的反应速率的是
的反应速率的是___________ (填标号)。
a.升高温度 b.增大压强 c.加入催化剂 d.适当增大 浓度
浓度
(5)有机反应中容易产生积碳,使催化剂失活,相同反应条件下,反应Ⅱ相比反应Ⅰ不容易产生积碳而使催化剂失活的原因是___________ 。
反应Ⅰ:
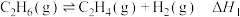
反应Ⅱ:
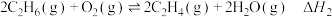
(1)在特定温度下,由稳定态单质生成1mol化合物的焓变叫该物质在此温度下的标准摩尔生成焓,下表为几种物质在298K下的标准摩尔生成焓,则反应Ⅱ的

 。
。| 物质 |  |  | 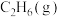 |  |  |
标准摩尔生成焓 | 0 | 0 | -86 | 53 | -241 |
(2)过渡金属氧化物中,金属离子的最外层电子有着较强的得失电子能力,使得金属离子具有多种可变价态,因而成为应用于乙烷一氧气氧化脱氢反应最广泛的一类催化剂,含钒(V)催化剂催化乙烷制乙烯每步反应的机理如图所示,下列说法不正确的是___________(填标号)。
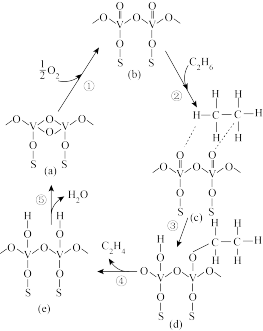
| A.物质a可以降低总反应的焓变 |
| B.总反应包括5个基元反应 |
| C.物质c含有共价键和氢键 |
| D.反应历程中钒(V)的化合价发生了变化 |
(3)一定电压下,不同催化剂电催化乙烷脱氢制乙烯的法拉第效率随温度的变化如图所示(已知法拉第效率是指实际生成物和理论生成物的百分比)。为了保证生成乙烯的法拉第效率,最合适的温度为
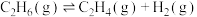 的速率方程为
的速率方程为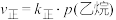 ,
,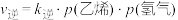 ,其中
,其中 、
、 分别为正、逆反应速率常数,
分别为正、逆反应速率常数, 为各组分分压。
为各组分分压。①在实际生产中,t℃时,向恒容密闭容器中通入乙烷和
 (作稀释剂,提高乙烷转化率),测得容器总压(
(作稀释剂,提高乙烷转化率),测得容器总压( )和乙烷转化率
)和乙烷转化率 随时间变化的结果如图所示。平衡时,平衡常数
随时间变化的结果如图所示。平衡时,平衡常数

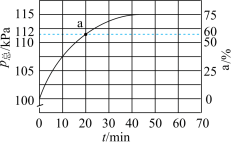
 的反应速率的是
的反应速率的是a.升高温度 b.增大压强 c.加入催化剂 d.适当增大
 浓度
浓度(5)有机反应中容易产生积碳,使催化剂失活,相同反应条件下,反应Ⅱ相比反应Ⅰ不容易产生积碳而使催化剂失活的原因是
您最近一年使用:0次
5 . 298K时,向 溶液中滴加
溶液中滴加 溶液,滴定曲线如图所示。下列说法不正确的是
溶液,滴定曲线如图所示。下列说法不正确的是
 溶液中滴加
溶液中滴加 溶液,滴定曲线如图所示。下列说法不正确的是
溶液,滴定曲线如图所示。下列说法不正确的是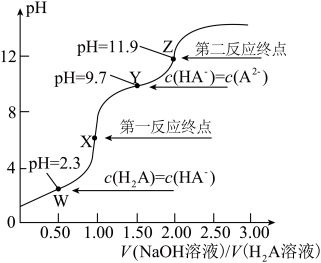
| A.该滴定过程应该选择酚酞溶液作指示剂 |
B.W点到X点发生的主要反应的离子方程式为 |
C.Y点对应的溶液中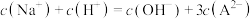 |
D.反应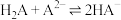 的平衡常数 的平衡常数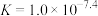 |
您最近一年使用:0次
解题方法
6 . 相比传统工艺在ZnSO4-H2SO4体系中电解精炼锌,络合物电解法实现粗锌(主要杂质有Fe、Cu、Pb)的提纯,可以避免析氢和锌复溶等副反应的发生,原理如图所示。下列说法不正确的是
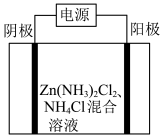
| A.阴极材料为粗锌 |
| B.获得高纯锌的电极反应式为[Zn(NH3)2]2++2e-+2H2O=Zn+2NH3⋅H2O |
| C.电解产生的阳极泥主要成分为Fe、Cu、Pb |
| D.传统工艺中析氢和锌复溶的离子反应为Zn+2H+=Zn2++H2↑ |
您最近一年使用:0次
解题方法
7 . 2023年化学诺贝尔奖授予“量子点”研究领域的科学家,有机半导体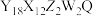 ,由于其良好的热稳定性和高荧光量子效应,常被用于有机发光二极管等电子器件中。其中短周期主族元素Y、Z、W为同周期相邻元素且原子序数依次增大,X原子核外电子只有一种自旋取向,W基态原子核外s能级上的电子总数与p能级上的电子总数相等,Q的基态价电子为
,由于其良好的热稳定性和高荧光量子效应,常被用于有机发光二极管等电子器件中。其中短周期主族元素Y、Z、W为同周期相邻元素且原子序数依次增大,X原子核外电子只有一种自旋取向,W基态原子核外s能级上的电子总数与p能级上的电子总数相等,Q的基态价电子为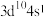 ,且形成的配离子
,且形成的配离子 为蓝色。下列说法正确的是
为蓝色。下列说法正确的是
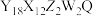 ,由于其良好的热稳定性和高荧光量子效应,常被用于有机发光二极管等电子器件中。其中短周期主族元素Y、Z、W为同周期相邻元素且原子序数依次增大,X原子核外电子只有一种自旋取向,W基态原子核外s能级上的电子总数与p能级上的电子总数相等,Q的基态价电子为
,由于其良好的热稳定性和高荧光量子效应,常被用于有机发光二极管等电子器件中。其中短周期主族元素Y、Z、W为同周期相邻元素且原子序数依次增大,X原子核外电子只有一种自旋取向,W基态原子核外s能级上的电子总数与p能级上的电子总数相等,Q的基态价电子为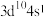 ,且形成的配离子
,且形成的配离子 为蓝色。下列说法正确的是
为蓝色。下列说法正确的是A.氢化物的沸点: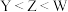 |
B.碱性条件下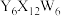 与Q的最高价氧化物对应的水化物能发生氧化还原反应 与Q的最高价氧化物对应的水化物能发生氧化还原反应 |
| C.X、Z、W三种元素组成的化合物一定为共价化合物 |
D.该配离子 水溶液中滴加过量氨水会产生蓝色沉淀 水溶液中滴加过量氨水会产生蓝色沉淀 |
您最近一年使用:0次
8 . 分类观和价态观是研究物质性质的两个重要维度,氮元素的价类二维图如图所示,下列说法不正确的是
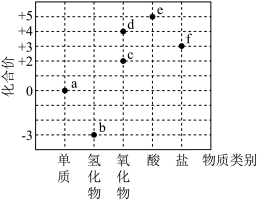
| A.在一定催化剂作用下,b与c可以发生归中反应生成a |
| B.“雷雨发庄稼”涉及的转化过程包含a→c→d→e |
| C.b与e生成f属于固氮反应 |
| D.f的含钠化合物可以作食品防腐剂 |
您最近一年使用:0次
9 .  为绿色菱形晶体,常用作有机合成的催化剂,其实验室制法如图所示,下列说法不正确的是
为绿色菱形晶体,常用作有机合成的催化剂,其实验室制法如图所示,下列说法不正确的是
 为绿色菱形晶体,常用作有机合成的催化剂,其实验室制法如图所示,下列说法不正确的是
为绿色菱形晶体,常用作有机合成的催化剂,其实验室制法如图所示,下列说法不正确的是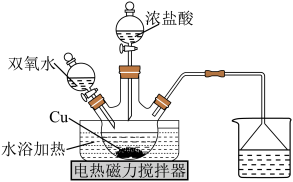
| 温度 | 低于288K | 288~298.7K | 299~315K | 高于315K |
| 结晶水合物 | 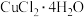 |  |  | 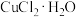 |
A. 晶体有X射线特征衍射峰 晶体有X射线特征衍射峰 |
B.制备 的离子方程式为 的离子方程式为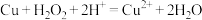 |
C.烧杯中溶液可以是 溶液 溶液 |
D.反应完全后,为得到 晶体,将滤液加热蒸发浓缩,降温至26~42℃结晶,过滤,洗涤,干燥 晶体,将滤液加热蒸发浓缩,降温至26~42℃结晶,过滤,洗涤,干燥 |
您最近一年使用:0次
10 . 中华文明源远流长,下列说法不正确的是
| A.制造宣纸所使用的青檀树皮及稻草的主要成分为纤维素 |
| B.岭南非遗服饰粤绣所用的孔雀毛和马尾的主要成分都是蛋白质 |
C.活字印刷术中所使用的胶泥含有的氧化物 、 、 都属于碱性氧化物 都属于碱性氧化物 |
| D.糯米酿造糯米酒的过程中涉及氧化还原反应 |
您最近一年使用:0次



