名校
1 . 已知R2-核内共有N个中子,R的质量数为A,则mgR2-中含有电子的物质的量为
A. | B.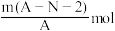 |
C. | D. |
您最近一年使用:0次
2024-01-06更新
|
187次组卷
|
23卷引用:新疆塔城地区第一高级中学2022-2023学年高一下学期开学考试化学试题
新疆塔城地区第一高级中学2022-2023学年高一下学期开学考试化学试题浙江省宁波市北仑中学2022-2023学年高一下学期期初返校考试(选考)化学试题云南省腾冲市第八中学2023-2024学年高一下学期开学化学试题【全国百强校】宁夏回族自治区银川一中2018-2019学年高一下学期期中考试化学试题云南省麒麟高中2018-2019学年高一6月份考试化学试题山西省应县第一中学校2018-2019学年高一下学期期中考试化学试题河北省邯郸市第一中学2019—2020学年高一4月月考化学试题四川省三台中学2019-2020学年高一4月空中课堂质量检测化学试题吉林省辽源市辽县第一高级中学2019-2020高一下学期期中考试化学试题四川省棠湖中学2019-2020学年高一下学期期中考试化学试题四川省南充高级中学2020-2021学年高一下学期第一次月考化学试题四川乐山市峨眉二中2020-2021学年高一下学期4月月考化学试题云南省玉溪第二中学2020-2021学年高一下学期第一次月考化学(理)试题甘肃省嘉峪关市第一中学2020-2021学年高一下学期期中考试化学试题四川省内江市资中县球溪中学2021-2022学年高一下学期3月月考化学试题四川省泸县第一中学2021-2022学年高一下学期期中考试化学试题福建省连城县第一中学2021-2022学年高一下学期第一次月考化学试题四川省南充市蓬安中学2021-2022学年高一下学期第一次月考化学试题江苏省洪泽中学六校联考2022-2023学年高一上学期期中考试化学试题陕西省榆林中学2022-2023学年高一上学期期末考试化学试题吉林省长春市实验中学2022-2023学年高一上学期期末考试化学试题(已下线)第15讲 人类对原子结构的认识-【暑假自学课】2023年新高一暑假精品课(苏教版2019)吉林省白山市2023-2024学年高一上学期1月期末考试化学试题
名校
解题方法
2 . 高铁酸钾( ,其中
,其中 元素为
元素为 价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。已知:在碱性溶液中的溶解度:
价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。已知:在碱性溶液中的溶解度: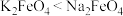

(1)过程Ⅰ的目的是制备 ,反应的离子方程式为
,反应的离子方程式为_______ 。
(2)过程Ⅱ为碱性条件下制备高铁酸钠 。
。
①补全过程Ⅱ中发生反应的离子方程式;

_______ 。若反应过程中转移了 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为_______ 
②除 外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为
外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为_______
(3) 可将氨氮废水中的
可将氨氮废水中的 转化为
转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是_______ 。
(4)高铁酸钾 是水处理过程中常用的新型净水剂,原因是
是水处理过程中常用的新型净水剂,原因是 被还原为
被还原为 ,形成
,形成 胶体,使水中悬浮物沉聚,
胶体,使水中悬浮物沉聚, 胶体微粒直径的范围是
胶体微粒直径的范围是_______  ,高铁酸钾在水溶液中的电离方程式是
,高铁酸钾在水溶液中的电离方程式是_______ 。
 ,其中
,其中 元素为
元素为 价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。已知:在碱性溶液中的溶解度:
价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。已知:在碱性溶液中的溶解度: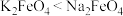

(1)过程Ⅰ的目的是制备
 ,反应的离子方程式为
,反应的离子方程式为(2)过程Ⅱ为碱性条件下制备高铁酸钠
 。
。①补全过程Ⅱ中发生反应的离子方程式;

 电子,则还原产物的物质的量为
电子,则还原产物的物质的量为
②除
 外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为
外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为(3)
 可将氨氮废水中的
可将氨氮废水中的 转化为
转化为 除去。从价态角度分析,
除去。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是(4)高铁酸钾
 是水处理过程中常用的新型净水剂,原因是
是水处理过程中常用的新型净水剂,原因是 被还原为
被还原为 ,形成
,形成 胶体,使水中悬浮物沉聚,
胶体,使水中悬浮物沉聚, 胶体微粒直径的范围是
胶体微粒直径的范围是 ,高铁酸钾在水溶液中的电离方程式是
,高铁酸钾在水溶液中的电离方程式是
您最近一年使用:0次
名校
解题方法
3 . 已知A为金属单质,下列物质相互转化如图所示:

(1)写出B的化学式_______ ,D的化学式_______ 。
(2)写出由E转变成F的化学方程式_______ 。
(3)检验G溶液中阳离子的试剂为_______ ;写出F转化为G的离子方程式_______ 。
(4)写出G转变成B的离子方程式_______ 。

(1)写出B的化学式
(2)写出由E转变成F的化学方程式
(3)检验G溶液中阳离子的试剂为
(4)写出G转变成B的离子方程式
您最近一年使用:0次
名校
4 . 元素周期表对化学的发展有很大影响,在材料、能源、环境和生命科学研究上发挥着越来越重要的作用。如表是元素周期表的一部分,请按题目要求回答下列问题:

根据表中所列元素回答下列问题:
(1)e元素在周期表中的位置是_______
(2)元素d、g、n的原子半径从大到小的顺序:_______ (填写元素符号)。
(3)c的离子结构示意图为_______ 。
(4)写出:f、g的最高价氧化物对应的水化物相互反应的离子方程式_______ ,写出f、e的最高价氧化物对应的水化物相互反应的化学方程式_______ 。
(5)非金属性强弱比较g_______ n(填写“大于”或“小于”),下列表述中能证明这一事实的是_______ (填字母)。
①g的氢化物比n的氢化物稳定
②g最高价氧化物对应的水化物的酸性强于最高价氧化物对应的水化物的酸性
③g的单质能将n从其钠盐溶液中置换出来

根据表中所列元素回答下列问题:
(1)e元素在周期表中的位置是
(2)元素d、g、n的原子半径从大到小的顺序:
(3)c的离子结构示意图为
(4)写出:f、g的最高价氧化物对应的水化物相互反应的离子方程式
(5)非金属性强弱比较g
①g的氢化物比n的氢化物稳定
②g最高价氧化物对应的水化物的酸性强于最高价氧化物对应的水化物的酸性
③g的单质能将n从其钠盐溶液中置换出来
您最近一年使用:0次
名校
解题方法
5 . 砹 属于卤族元素之一,试推测砹
属于卤族元素之一,试推测砹 单质及其化合物不可能具有的性质
单质及其化合物不可能具有的性质
 属于卤族元素之一,试推测砹
属于卤族元素之一,试推测砹 单质及其化合物不可能具有的性质
单质及其化合物不可能具有的性质| A.单质砹易溶于某些有机溶剂 | B. 是不溶于水的有色固体 是不溶于水的有色固体 |
C.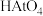 酸性比 酸性比 弱 弱 | D.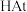 受热很难分解 受热很难分解 |
您最近一年使用:0次
名校
6 . 下列说法中,正确的是
A.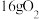 和 和 混合气体中含有的原子数约为 混合气体中含有的原子数约为 |
B.标况下, 的体积为 的体积为 |
C. 的摩尔质量是 的摩尔质量是 |
D.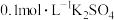 溶液中含有 溶液中含有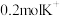 |
您最近一年使用:0次
7 . 数学计算令人头大,物理公式也难拿下,化学计算数字不大,得个高分不在话下。请认真完成以下计算,让化学成绩为你舔砖加瓦。
(1)常温下,0.05mol/L硫酸溶液中,C(H+)=___________ mol/L
(2)某温度,纯水中C(H+)=3×10-7mol/L,则:纯水中C(OH-)=___________ mol/L,此时温度___________ (填“高于”“低于”或“等于”)25℃。若温度不变,滴入盐酸后C(H+)=5×10-4mol/L,则溶液中C(OH-)=___________ mol/L,由水电离的C(H+)=___________ mol/L。
(3)室温下,pH=3的盐酸与pH=5的H2SO4溶液等体积混合(忽略体积变化),混合溶液的pH=___________ 。
(4)常温向水中加入少量碳酸钠固体,得到pH为11的溶液,溶液中c(OH-)=_____ mol·L-1。
(1)常温下,0.05mol/L硫酸溶液中,C(H+)=
(2)某温度,纯水中C(H+)=3×10-7mol/L,则:纯水中C(OH-)=
(3)室温下,pH=3的盐酸与pH=5的H2SO4溶液等体积混合(忽略体积变化),混合溶液的pH=
(4)常温向水中加入少量碳酸钠固体,得到pH为11的溶液,溶液中c(OH-)=
您最近一年使用:0次
8 . 某学生用0.1000 mol/LKOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
(A)移取20.00 mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准溶液润洗滴定管2-3次
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm
(E)调节液面至0或0刻度以下,记下读数
(F)把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写):B_______ C、E_________ F
(2)上述(A)操作之前,如先用待测液润洗锥形瓶,则对测定结果的影响是(填偏大、偏小、不变,下同)___________ 。
(3)实验滴定过程中用左手控制滴定管___________ 部位(填活塞或者橡胶),眼睛注视___________ ,直至滴定终点。判断到达终点的现象是___________ 。
(4)下列是操作过程中用到的仪器:

滴定管的使用:如图1是滴定管中的液面,其读数为___________ mL。
(5)盛装0.2000 mol·L-1盐酸标准液应该用图2的___________ (甲或乙)滴定管。
(A)移取20.00 mL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准溶液润洗滴定管2-3次
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm
(E)调节液面至0或0刻度以下,记下读数
(F)把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空:
(1)正确操作的顺序是(用序号字母填写):B
(2)上述(A)操作之前,如先用待测液润洗锥形瓶,则对测定结果的影响是(填偏大、偏小、不变,下同)
(3)实验滴定过程中用左手控制滴定管
(4)下列是操作过程中用到的仪器:

滴定管的使用:如图1是滴定管中的液面,其读数为
(5)盛装0.2000 mol·L-1盐酸标准液应该用图2的
您最近一年使用:0次
名校
9 . 锌—空气燃料电池可用作电动车动力电源,电池的电解质溶液为KOH溶液,反应为2Zn+O2+4OH-+2H2O=2Zn(OH) 下列说法正确的是
下列说法正确的是
 下列说法正确的是
下列说法正确的是A.放电时,负极反应为:Zn+4OH--2e-=Zn(OH) |
| B.放电时,电路中通过2 mol电子,消耗氧气22.4 L(标准状况) |
| C.充电时,电解质溶液中K+向阳极移动 |
| D.充电时,电解质溶液中c(OH-)逐渐减小 |
您最近一年使用:0次
2023-07-30更新
|
91次组卷
|
3卷引用:新疆维吾尔自治区塔城地区2022-2023学年高二下学期开学考试化学试题
10 . 为检验某溶液中是否含有 ,可以选择的试剂是
,可以选择的试剂是
 ,可以选择的试剂是
,可以选择的试剂是| A.KSCN溶液 | B. 溶液 溶液 | C.酸性 溶液 溶液 | D. 溶液 溶液 |
您最近一年使用:0次
2023-05-27更新
|
518次组卷
|
16卷引用:新疆乌苏市第一中学2021-2022学年高一下学期开学考试化学(B)试题
新疆乌苏市第一中学2021-2022学年高一下学期开学考试化学(B)试题湖南省茶陵县第三中学2018-2019学年高二下学期第一次月考化学试题湖南省株洲市茶陵县第三中学2019-2020学年高二上学期12月月考化学试题(学考)河北省武邑中学2019-2020学年高二12月月考化学试题湖南省邵阳市双清区十一中2019-2020学年高一12月月考化学试题山东省临沂市2018-2019学年学业水平考试预测试题(一)北京市新学道临川学校2021届高三上学期第一次月考化学试题湖南省张家界市2020-2021学年高一上学期期末考试化学试题广东省汕尾市2021-2022学年高一上学期末教学质量监测化学试题湖南省娄底市新化县2021-2022学年高一上学期期末考试化学试题(已下线)3.1.2 铁盐和亚铁盐-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)新疆叶城县第八中学2021-2022学年高一上学期期末考试化学试题2023年湖南省娄底市高一学业水平考试模拟化学试题(已下线)专题六 物质的电离与离子反应(已下线)专题二 物质的检验、除杂和鉴别湖南省株洲市南方中学2023-2024学年高一下学期期中考试化学试题



