名校
1 . 下列有关含碳微粒的说法,按要求填空:
(1)常温下,0.1mol·L-1的Na2CO3溶液的碱性___________ 0.1mol·L-1的 NaHCO3 溶液的碱性(填“大于”、“小于”、“等于”),请设计一个较简便的实验证明___________ 。
(2)相同温度下,将浓度均为0.1mol·L-1的Na2CO3和 NaHCO3 溶液按体积比1:1混合,则该混合溶液中物料守恒等式为___________ ;该混合溶液中离子浓度由大到小的顺序是___________ 。
(3)在25 ℃时,在10 mL 0.1 mol/L Na2CO3溶液中逐滴加入0.1 mol/L HCl溶液20 mL,溶液中含碳微粒的物质的量随溶液pH的变化如图所示。
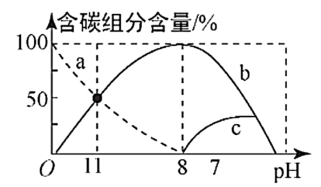
①HCl溶液滴加到一半时,溶液呈___________ (填“酸性”、“碱性”或“中性”),理由是___________ (用主要的离子方程式表示)。
②关于图象下列说法不正确的是___________ 。
A、b曲线代表CO
B、0.1 mol/L Na2CO3溶液中: c(OH-) = 2c(H2CO3) + c(HCO )+c(H+)
)+c(H+)
C、pH=11时,c(HCO ) > c(Cl-)
) > c(Cl-)
D、pH=11 时,c(Na+) + c(H+) = 3c(CO ) + c(OH-)
) + c(OH-)
E、在同一溶液中,H2CO3、HCO 、CO
、CO 不能大量共存
不能大量共存
(1)常温下,0.1mol·L-1的Na2CO3溶液的碱性
(2)相同温度下,将浓度均为0.1mol·L-1的Na2CO3和 NaHCO3 溶液按体积比1:1混合,则该混合溶液中物料守恒等式为
(3)在25 ℃时,在10 mL 0.1 mol/L Na2CO3溶液中逐滴加入0.1 mol/L HCl溶液20 mL,溶液中含碳微粒的物质的量随溶液pH的变化如图所示。

①HCl溶液滴加到一半时,溶液呈
②关于图象下列说法不正确的是
A、b曲线代表CO

B、0.1 mol/L Na2CO3溶液中: c(OH-) = 2c(H2CO3) + c(HCO
 )+c(H+)
)+c(H+)C、pH=11时,c(HCO
 ) > c(Cl-)
) > c(Cl-)D、pH=11 时,c(Na+) + c(H+) = 3c(CO
 ) + c(OH-)
) + c(OH-)E、在同一溶液中,H2CO3、HCO
 、CO
、CO 不能大量共存
不能大量共存
您最近一年使用:0次
名校
2 . 食品安全关系国计民生,影响食品安全的因素很多.下面是以食品为主题的相关问题,请根据要求回答.
(1)聚偏二氯乙烯(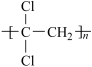 )具有超强阻隔性能,可作为保鲜食品的包装材料.它是由
)具有超强阻隔性能,可作为保鲜食品的包装材料.它是由___________ (写结构简式) 单体发生加聚反应生成的.若以乙炔为原料,通过加成反应生成1,1,2三氯乙烷,再和氢氧化钠醇溶液反应可合成这种单体,则在加成反应中宜选择的试剂是_________ .(选填编号字母)
a.HCl b.Cl2 c.HClO d.NaCl
(2)人们从食用植物油中摄取的亚油酸[ ]对人体健康是十分有益的,然而市场上经常会出现价格低廉的植物油,其中的亚油酸含量很低.下列关于亚油酸的说法中不正确的是
]对人体健康是十分有益的,然而市场上经常会出现价格低廉的植物油,其中的亚油酸含量很低.下列关于亚油酸的说法中不正确的是___________ (选填编号字母).
a.分子式为C18H34O2
b.在食用油中亚油酸通常是以甘油酯的形式存在
c.亚油酸属于一种不饱和低级脂肪酸,所以能和NaOH溶液反应
d.亚油酸含量高的植物油在空气中易氧化变质
(3)食用酱油中的“氯丙醇”是多种氯代丙醇的总称,它们是在酱油配制过程中植物蛋白水解发生一系列化学变化而产生的,氯丙醇中部分异构体对人体有不同程度的致癌效应.则氯丙醇中三氯丙醇异构体共有_________ 种(已知卤原子和羟基一般不会连在同一碳原子上).
(4)在淀粉中加入吊白块制得的粉丝有毒.淀粉最终的水解产物是葡萄糖,请设计实验证明淀粉已经全部水解,写出操作方法、现象和结论______________ .
(5)木糖醇[CH2OH(CHOH)3CH2OH]作为一种甜味剂,食用后不会引起血糖升高,比较适合于糖尿病人食用.预测木糖醇能和新制备的Cu(OH)2浊液发生化学反应的依据是___________ .
(6)酒精在人体肝脏内可转化为多种有害物质,有机物A是其中的一种,对A的结构进行如下分析:
①通过样品的质谱分析测得A的相对分子质量为60.
②对A的水溶液进行测定发现该溶液pH<7.
③核磁共振氢原子光谱能对有机物分子中同性氢原子给出相同的峰值,根据峰值可以确定分子中氢原子的种类和数目.例如乙醇有三种氢原子(图1).经测定有机物A的核磁共振氢谱示意图如图2
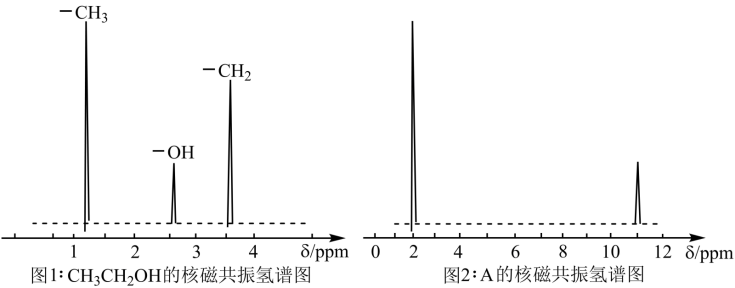
根据以上分析,写出A的结构简式__________ .
(1)聚偏二氯乙烯(
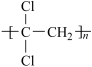 )具有超强阻隔性能,可作为保鲜食品的包装材料.它是由
)具有超强阻隔性能,可作为保鲜食品的包装材料.它是由a.HCl b.Cl2 c.HClO d.NaCl
(2)人们从食用植物油中摄取的亚油酸[
 ]对人体健康是十分有益的,然而市场上经常会出现价格低廉的植物油,其中的亚油酸含量很低.下列关于亚油酸的说法中不正确的是
]对人体健康是十分有益的,然而市场上经常会出现价格低廉的植物油,其中的亚油酸含量很低.下列关于亚油酸的说法中不正确的是a.分子式为C18H34O2
b.在食用油中亚油酸通常是以甘油酯的形式存在
c.亚油酸属于一种不饱和低级脂肪酸,所以能和NaOH溶液反应
d.亚油酸含量高的植物油在空气中易氧化变质
(3)食用酱油中的“氯丙醇”是多种氯代丙醇的总称,它们是在酱油配制过程中植物蛋白水解发生一系列化学变化而产生的,氯丙醇中部分异构体对人体有不同程度的致癌效应.则氯丙醇中三氯丙醇异构体共有
(4)在淀粉中加入吊白块制得的粉丝有毒.淀粉最终的水解产物是葡萄糖,请设计实验证明淀粉已经全部水解,写出操作方法、现象和结论
(5)木糖醇[CH2OH(CHOH)3CH2OH]作为一种甜味剂,食用后不会引起血糖升高,比较适合于糖尿病人食用.预测木糖醇能和新制备的Cu(OH)2浊液发生化学反应的依据是
(6)酒精在人体肝脏内可转化为多种有害物质,有机物A是其中的一种,对A的结构进行如下分析:
①通过样品的质谱分析测得A的相对分子质量为60.
②对A的水溶液进行测定发现该溶液pH<7.
③核磁共振氢原子光谱能对有机物分子中同性氢原子给出相同的峰值,根据峰值可以确定分子中氢原子的种类和数目.例如乙醇有三种氢原子(图1).经测定有机物A的核磁共振氢谱示意图如图2

根据以上分析,写出A的结构简式
您最近一年使用:0次
3 . 苯是一种重要的化工原料。
(1)下图是某些有机物的分子模型,其中表示苯的是_______________ 。

(2)若苯泄漏会造成严重的危险,下列说法有科学性错误的是___________ (填字母)。
A.若大量苯溶入水中、渗入土壤,会对周边农田、水源造成严重的污染
B.由于苯是一种易挥发、易燃的物质,周围地区如果有火星就可能引起爆炸
C.可以采取抽吸水渠中上层液体的办法,达到部分清除泄漏物的目的
D.由于苯有毒,所有工作人员在处理事故时,都要做相关防护措施
(3)小彭同学利用下图所示的实验来探究苯的性质。
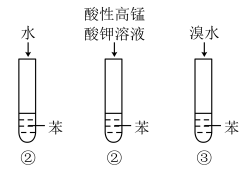
图中所示实验①②③中,分别加入所给试剂并不断振荡、静置,均出现分层现象,其中下层颜色比上层浅的是__________________ (填序号);实验②_________________ (填“能”或“不能”)证明苯分子中不存在单、双键交替的结构。
(4)在 催化作用下,苯与液溴发生反应的化学方程式为
催化作用下,苯与液溴发生反应的化学方程式为________________________ 。
(5)苯在一定条件下可与氢气发生________ (填反应类型)反应,反应产物的名称是_________ 。
(1)下图是某些有机物的分子模型,其中表示苯的是

(2)若苯泄漏会造成严重的危险,下列说法有科学性错误的是
A.若大量苯溶入水中、渗入土壤,会对周边农田、水源造成严重的污染
B.由于苯是一种易挥发、易燃的物质,周围地区如果有火星就可能引起爆炸
C.可以采取抽吸水渠中上层液体的办法,达到部分清除泄漏物的目的
D.由于苯有毒,所有工作人员在处理事故时,都要做相关防护措施
(3)小彭同学利用下图所示的实验来探究苯的性质。

图中所示实验①②③中,分别加入所给试剂并不断振荡、静置,均出现分层现象,其中下层颜色比上层浅的是
(4)在
 催化作用下,苯与液溴发生反应的化学方程式为
催化作用下,苯与液溴发生反应的化学方程式为(5)苯在一定条件下可与氢气发生
您最近一年使用:0次
名校
解题方法
4 . 胶体是一种常见的分散系。用Fe(OH)3胶体进行下列实验。
(1)向其中滴入过量稀硫酸,现象是_________ ,其原因是_________ 。
(2)下列关于胶体的说法正确的是_________
①将直径等于2.5微米的颗粒物分散于水中即成为胶体
②胶体与溶液的本质区别是胶体具有丁达尔效应
③雾具有丁达尔效应
④同种胶体带同种电荷,相互排斥,是胶体稳定的主要原因
⑤处理废水时可加入明矾作为混凝剂,是利用了胶体的性质
⑥含1molFeCl3的饱和溶液完全与水反应生成1molFe(OH)3胶体粒子
⑦“血液透析”原理和胶体的渗析原理类似
A.③④⑤B.①④⑥C.③⑤⑦D.②③⑥
(3)提纯Fe(OH)3胶体的装置是如图中_________ ,该操作属于_________ (均填序号)
A.蒸馏B.萃取C.盐析D.渗析

现有10mLFe(OH)3胶体与5mLNa2SO4溶液混合装装入半透膜内,将此半透膜浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜:
能够透过半透膜:_________
(1)向其中滴入过量稀硫酸,现象是
(2)下列关于胶体的说法正确的是
①将直径等于2.5微米的颗粒物分散于水中即成为胶体
②胶体与溶液的本质区别是胶体具有丁达尔效应
③雾具有丁达尔效应
④同种胶体带同种电荷,相互排斥,是胶体稳定的主要原因
⑤处理废水时可加入明矾作为混凝剂,是利用了胶体的性质
⑥含1molFeCl3的饱和溶液完全与水反应生成1molFe(OH)3胶体粒子
⑦“血液透析”原理和胶体的渗析原理类似
A.③④⑤B.①④⑥C.③⑤⑦D.②③⑥
(3)提纯Fe(OH)3胶体的装置是如图中
A.蒸馏B.萃取C.盐析D.渗析

现有10mLFe(OH)3胶体与5mLNa2SO4溶液混合装装入半透膜内,将此半透膜浸入盛蒸馏水的烧杯中,设计实验证明
 能够透过半透膜:
能够透过半透膜:
您最近一年使用:0次
5 . (1)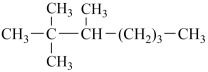 用系统命名法命名为
用系统命名法命名为__
(2)请同学们根据官能团的不同对下列有机物进行分类:
①CH3CH2OH ②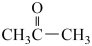 ③
③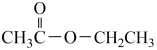 ④CH3CH2Br ⑤
④CH3CH2Br ⑤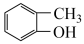 ⑥
⑥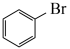 ⑦
⑦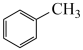 ⑧
⑧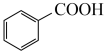 ⑨
⑨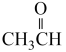 ⑩
⑩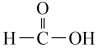
A.属于芳香烃的是_____ ;(填序号,下同) B.属于卤代烃的是_____ ;
C.属于醇的是______ ; D.属于羧酸的是____ 。
(3)实验室常用浓硫酸和乙醇混合加热制取乙烯。
①实验室制乙烯的化学方程式为____ 。
②关于该实验的说法中正确的是_____ 。
a.浓硫酸只有催化剂的作用
b.可用向下排空气法收集乙烯
c.在反应容器中放入几片碎瓷片防止混合液暴沸
③实验后期制得的乙烯气体中常含有杂质气体SO2和CO2,将此混合气体直接通入溴水中,若观察到溴水褪色,能否证明乙烯发生了加成反应?____ (填“能”或“否”),原因是___ (用化学方程式说明)。
(4)为了测定芳香烃A的结构,做如下实验:
①将9.2g该芳香烃A完全燃烧,生成标况下15.68L CO2和7.2gH2O;
②用质谱仪测定其相对分子质量,得如图所示的质谱图,由图可知该分子的相对分子质量是___ ,有机物A的分子式为___ 。
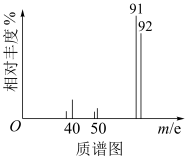
③用核磁共振仪处理该有机物得到四个峰,且四个峰的面积之比是1∶2∶2∶3,则该有机物A的结构简式为____ 。
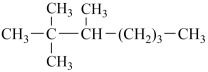 用系统命名法命名为
用系统命名法命名为(2)请同学们根据官能团的不同对下列有机物进行分类:
①CH3CH2OH ②
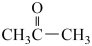 ③
③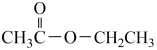 ④CH3CH2Br ⑤
④CH3CH2Br ⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨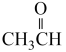 ⑩
⑩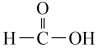
A.属于芳香烃的是
C.属于醇的是
(3)实验室常用浓硫酸和乙醇混合加热制取乙烯。
①实验室制乙烯的化学方程式为
②关于该实验的说法中正确的是
a.浓硫酸只有催化剂的作用
b.可用向下排空气法收集乙烯
c.在反应容器中放入几片碎瓷片防止混合液暴沸
③实验后期制得的乙烯气体中常含有杂质气体SO2和CO2,将此混合气体直接通入溴水中,若观察到溴水褪色,能否证明乙烯发生了加成反应?
(4)为了测定芳香烃A的结构,做如下实验:
①将9.2g该芳香烃A完全燃烧,生成标况下15.68L CO2和7.2gH2O;
②用质谱仪测定其相对分子质量,得如图所示的质谱图,由图可知该分子的相对分子质量是

③用核磁共振仪处理该有机物得到四个峰,且四个峰的面积之比是1∶2∶2∶3,则该有机物A的结构简式为
您最近一年使用:0次
解题方法
6 . 电能是现代社会应用最广泛的能源之一。
(1)如图所示装置中,Zn是_____ 极(填“正”或“负”)。
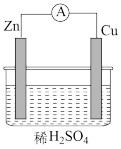
(2)如图所示装置可将______ (写化学方程式)反应释放的能量直接转变为电能;能证明产生电能的实验现象是_____ 。
(3)氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图所示。下列有关氢氧燃料电池的说法,正确的是______ 。

①电极b是正极
②外电路中电子由电极b通过导线流向电极a
③该电池的总反应:2H2+O2=2H2O
(1)如图所示装置中,Zn是

(2)如图所示装置可将
(3)氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图所示。下列有关氢氧燃料电池的说法,正确的是

①电极b是正极
②外电路中电子由电极b通过导线流向电极a
③该电池的总反应:2H2+O2=2H2O
您最近一年使用:0次
7 . Ⅰ.(1)有人设想合成具有以下结构的烃分子
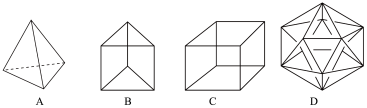
结构______________ 显然是不可能合成的,B的一种同分异构体是最简单的芳香烃(含苯环),能证明该芳香烃中的化学键不是单双键交替排列的事实是______________ 。
a.它的对位二元取代物只有一种 b.它的邻位二元取代物只有一种
c.分子中所有碳碳键的键长均相等 d.能发生取代反应和加成反应
(2)CO2 的有效利用可以缓解温室效应和能源短缺问题。CO2的电子式是_____ 。中科院的科研 人员在 Na-Fe3O4 和HMCM-22 的表面将 CO2转化为烷烃,其过程如图。
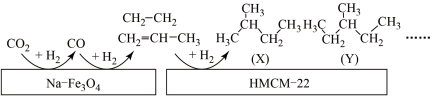
①Na-Fe3O4和HMCM-22 在反应中的作用为_________________
②(X)的系统命名的名称为_____________________
(3)如图是乙酸乙酯的绿色合成路线之一:
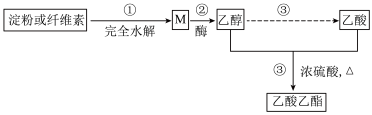
①M 的分子式为_____ 。
②下列说法不正确的是_____ (填字母序号)。
A.淀粉和纤维素都属于天然高分子化合物
B.M 可与新制的氢氧化铜悬浊液在加热条件下生成砖红色沉淀
C.所有的糖类都有甜味,都可以发生水解反应
D.用饱和碳酸钠溶液可以鉴别乙醇、乙酸和乙酸乙酯
(4)乙醇分子结构中的化学键如图所示:
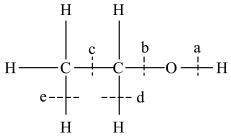
①乙醇在铜作催化剂时与氧气反应,断裂的化学键是_____ (填字母 序号)。
②乙醇和乙酸在一定条件下制备乙酸乙酯。生成乙酸乙酯的反应是可逆反应,下列能说明该反应已达到化学平衡状态的是_____ (填序号)。
A.单位时间里,生成 1mol 乙酸乙酯,同时生成 1mol 水
B.单位时间里,生成 1mol 乙酸乙酯,同时生成 1mol 乙酸
C.单位时间里,消耗 1mol 乙醇,同时消耗 1mol 乙酸
D.正反应的速率与逆反应的速率相等
E.混合物中各物质的物质的量相等
Ⅱ.苧烯有新鲜橙子香气,结构简式为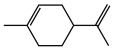 。回答下列问题:
。回答下列问题:
(1)下列有关苧烯的说法正确的是_____
a.苧烯属于芳香烃 b.苧烯与 1,3-丁二烯互为同系物
c.苧烯分子中键角均为 120° d.苧烯不能发生 1,4-加成反应
(2)有机物A 是苧烯的同分异构体,分子中含有两个六元环,能使溴水褪色,一氯代物只有两种,则A的结构简式为_____ 。
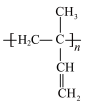
(3)苧烯在较高温度下分解为异戊二烯,异戊二烯发生加聚反应得到 4 种聚异戊二烯,其结构简式为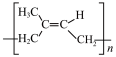 、
、 、
、__________ 、_________ 。

结构
a.它的对位二元取代物只有一种 b.它的邻位二元取代物只有一种
c.分子中所有碳碳键的键长均相等 d.能发生取代反应和加成反应
(2)CO2 的有效利用可以缓解温室效应和能源短缺问题。CO2的电子式是

①Na-Fe3O4和HMCM-22 在反应中的作用为
②(X)的系统命名的名称为
(3)如图是乙酸乙酯的绿色合成路线之一:

①M 的分子式为
②下列说法不正确的是
A.淀粉和纤维素都属于天然高分子化合物
B.M 可与新制的氢氧化铜悬浊液在加热条件下生成砖红色沉淀
C.所有的糖类都有甜味,都可以发生水解反应
D.用饱和碳酸钠溶液可以鉴别乙醇、乙酸和乙酸乙酯
(4)乙醇分子结构中的化学键如图所示:

①乙醇在铜作催化剂时与氧气反应,断裂的化学键是
②乙醇和乙酸在一定条件下制备乙酸乙酯。生成乙酸乙酯的反应是可逆反应,下列能说明该反应已达到化学平衡状态的是
A.单位时间里,生成 1mol 乙酸乙酯,同时生成 1mol 水
B.单位时间里,生成 1mol 乙酸乙酯,同时生成 1mol 乙酸
C.单位时间里,消耗 1mol 乙醇,同时消耗 1mol 乙酸
D.正反应的速率与逆反应的速率相等
E.混合物中各物质的物质的量相等
Ⅱ.苧烯有新鲜橙子香气,结构简式为
 。回答下列问题:
。回答下列问题: (1)下列有关苧烯的说法正确的是
a.苧烯属于芳香烃 b.苧烯与 1,3-丁二烯互为同系物
c.苧烯分子中键角均为 120° d.苧烯不能发生 1,4-加成反应
(2)有机物A 是苧烯的同分异构体,分子中含有两个六元环,能使溴水褪色,一氯代物只有两种,则A的结构简式为
(3)苧烯在较高温度下分解为异戊二烯,异戊二烯发生加聚反应得到 4 种聚异戊二烯,其结构简式为
 、
、 、
、
您最近一年使用:0次
8 . 回答下列问题:
(1)下列说法正确的是_______
A.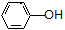 和
和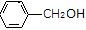 都属于酚类
都属于酚类
B.某烯烃的名称是2-甲基-4-乙基-2-戊烯
C.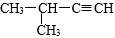 的名称为2-甲基-3-丁炔
的名称为2-甲基-3-丁炔
D.苯乙烯(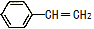 )分子的所有原子可能在同一平面上
)分子的所有原子可能在同一平面上
(2)分子式为C5H10O2,且能与饱和 NaHCO3溶液反应放出气体的有机物(不含立体异构)有_______
A.3种 B.4种 C.5种 D.6种
(3)下列实验事实不能用基团间相互作用来解释的是_______
A.与Na反应时,乙醇的反应速率比水慢
B.苯酚能与NaOH溶液反应而乙醇不能
C.乙醇能使重铬酸钾溶液变色而乙酸不能
D.甲苯能使KMnO4酸性溶液褪色而乙烷不能
(4)下列说法中,正确的是_______
A.将电石与水反应产生的气体通入酸性KMnO4溶液中,溶液褪色说明有乙炔生成
B.实验室制备乙烯时,温度计水银球应该插入浓硫酸和无水乙醇的混合液液面以下
C.溴乙烷和NaOH醇溶液共热,产生的气体通入KMnO4酸性溶液,发现溶液褪色,证明溴乙烷发生了消去反应
D.检验乙醛时,将4~6滴2%的NaOH溶液滴入2mL 2%的CuSO4溶液中,边滴边振荡,制备新制Cu(OH)2悬浊液
(5)六苯乙烷为白色固体,其结构如图。下列有关说法中正确的是_______
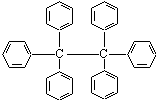
A.它的一氯代物只有三种
B.它的分子式为C38H30,只含有非极性键
C.它是一种苯的同系物,易溶于有机溶剂中
D.它的分子中所有原子共平面
(6)图是一些常见有机物的转化关系,①—⑦中没有发生的反应类型是_______
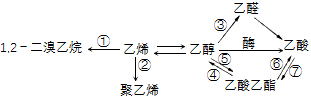
A.加成反应 B.消去反应 C.加聚反应 D.取代反应
(7)莽草酸是合成达菲的主要原料,其结构简式如图,下列说法正确的是_______
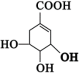
A.分子式为C7H8O5 B.分子中含有2种官能团
C.只能发生加成反应和取代反应 D.能使溴的四氯化碳溶液褪色
(1)下列说法正确的是
A.
 和
和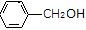 都属于酚类
都属于酚类B.某烯烃的名称是2-甲基-4-乙基-2-戊烯
C.
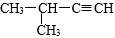 的名称为2-甲基-3-丁炔
的名称为2-甲基-3-丁炔D.苯乙烯(
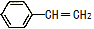 )分子的所有原子可能在同一平面上
)分子的所有原子可能在同一平面上(2)分子式为C5H10O2,且能与饱和 NaHCO3溶液反应放出气体的有机物(不含立体异构)有
A.3种 B.4种 C.5种 D.6种
(3)下列实验事实不能用基团间相互作用来解释的是
A.与Na反应时,乙醇的反应速率比水慢
B.苯酚能与NaOH溶液反应而乙醇不能
C.乙醇能使重铬酸钾溶液变色而乙酸不能
D.甲苯能使KMnO4酸性溶液褪色而乙烷不能
(4)下列说法中,正确的是
A.将电石与水反应产生的气体通入酸性KMnO4溶液中,溶液褪色说明有乙炔生成
B.实验室制备乙烯时,温度计水银球应该插入浓硫酸和无水乙醇的混合液液面以下
C.溴乙烷和NaOH醇溶液共热,产生的气体通入KMnO4酸性溶液,发现溶液褪色,证明溴乙烷发生了消去反应
D.检验乙醛时,将4~6滴2%的NaOH溶液滴入2mL 2%的CuSO4溶液中,边滴边振荡,制备新制Cu(OH)2悬浊液
(5)六苯乙烷为白色固体,其结构如图。下列有关说法中正确的是

A.它的一氯代物只有三种
B.它的分子式为C38H30,只含有非极性键
C.它是一种苯的同系物,易溶于有机溶剂中
D.它的分子中所有原子共平面
(6)图是一些常见有机物的转化关系,①—⑦中没有发生的反应类型是

A.加成反应 B.消去反应 C.加聚反应 D.取代反应
(7)莽草酸是合成达菲的主要原料,其结构简式如图,下列说法正确的是

A.分子式为C7H8O5 B.分子中含有2种官能团
C.只能发生加成反应和取代反应 D.能使溴的四氯化碳溶液褪色
您最近一年使用:0次
名校
解题方法
9 . 如图所示,U形管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混合气体,假定氯气在水中不溶解。将封闭有甲烷和氯气的混合气体的装置放置在有光亮的地方,让混合气体缓慢的反应一段时间。

(1)下列关于甲烷结构的说法中正确的是________ 。
A.甲烷的分子式是CH4,5个原子共面
B.甲烷分子的空间构型属于正四面体结构
C.甲烷中的任意三个原子都不共面
(2)假设甲烷与氯气反应充分,且只产生一种有机物,请写出化学方程式________ 。
(3)下列事实能证明甲烷分子是正四面体结构的是_____ 。
a.CH3Cl只代表一种物质b.CH2Cl2只代表一种物质
c.CHCl3只代表一种物质d.CCl4只代表一种物质
(4)烃分子中的碳原子与氢原子结合的方式是_____ 。
a.形成4对共用电子对b.通过1个共价键
c.通过2个共价键d.通过离子键和共价键
(5)若CH4、C2H6、C3H8、C4H10四种烃各为1g,在足量O2中燃烧,消耗O2最多的是_____ 。

(1)下列关于甲烷结构的说法中正确的是
A.甲烷的分子式是CH4,5个原子共面
B.甲烷分子的空间构型属于正四面体结构
C.甲烷中的任意三个原子都不共面
(2)假设甲烷与氯气反应充分,且只产生一种有机物,请写出化学方程式
(3)下列事实能证明甲烷分子是正四面体结构的是
a.CH3Cl只代表一种物质b.CH2Cl2只代表一种物质
c.CHCl3只代表一种物质d.CCl4只代表一种物质
(4)烃分子中的碳原子与氢原子结合的方式是
a.形成4对共用电子对b.通过1个共价键
c.通过2个共价键d.通过离子键和共价键
(5)若CH4、C2H6、C3H8、C4H10四种烃各为1g,在足量O2中燃烧,消耗O2最多的是
您最近一年使用:0次
解题方法
10 . Ⅰ.已知:反应aA(g)+bB(g) cC(g),某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
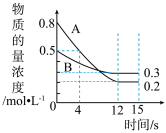
(1)经测4s时间,v(C)=0.05mol·L-1·s-1,则4s时物质C的物质的量为___________________ ,该反应的化学方程式为______________________ 。
(2)经12s时间,v(A)=___________ ,v(C)=___________ ,该反应12s时___________ 达到化学平衡(“是”或“否”)。
Ⅱ.(3)下列说法可以证明H2(g)+I2(g) 2HI(g)已达平衡状态的是
2HI(g)已达平衡状态的是________ (填序号)。
A.单位时间内生成nmolH2的同时,生成nmolHI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)= v(HI)
v(HI)
 cC(g),某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
cC(g),某温度下,在2L的密闭容器中投入一定量的A、B,两种气体的物质的量浓度随时间变化的曲线如图所示。
(1)经测4s时间,v(C)=0.05mol·L-1·s-1,则4s时物质C的物质的量为
(2)经12s时间,v(A)=
Ⅱ.(3)下列说法可以证明H2(g)+I2(g)
 2HI(g)已达平衡状态的是
2HI(g)已达平衡状态的是A.单位时间内生成nmolH2的同时,生成nmolHI
B.一个H—H键断裂的同时有两个H—I键断裂
C.温度和体积一定时,混合气体颜色不再变化
D.反应速率v(H2)=v(I2)=
 v(HI)
v(HI)
您最近一年使用:0次



