名校
解题方法
1 . 赤泥是氧化铝生产排放的固体废弃物。由赤泥(主要成分为 、
、 、
、 、
、 、
、 、
、 等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:
等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:
(1)基态铝原子的核外电子排布式为_______ , 的空间构型是
的空间构型是_______ 。
(2)“焙烧”时,需将赤泥粉碎的目的是_______ 。
(3)“氧化”时发生反应的离子方程式为_______ ,向“氧化”后的溶液中滴加 溶液至
溶液至 ,生成沉淀。
,生成沉淀。
(4)为了测试所制得的聚合硫酸铝铁的性能,取某水样在不同 条件下加入PAFS
条件下加入PAFS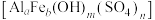 并测定其去浊率,结果如图所示(已知去浊率越高,净水效果越好)。由图可知在偏酸性和偏碱性的
并测定其去浊率,结果如图所示(已知去浊率越高,净水效果越好)。由图可知在偏酸性和偏碱性的 条件下,水样的去浊率均不高。试分析
条件下,水样的去浊率均不高。试分析 时,去浊率较低的可能原因为
时,去浊率较低的可能原因为_______ 。
 、
、 、
、 、
、 、
、 、
、 等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:
等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:
(1)基态铝原子的核外电子排布式为
 的空间构型是
的空间构型是(2)“焙烧”时,需将赤泥粉碎的目的是
(3)“氧化”时发生反应的离子方程式为
 溶液至
溶液至 ,生成沉淀。
,生成沉淀。(4)为了测试所制得的聚合硫酸铝铁的性能,取某水样在不同
 条件下加入PAFS
条件下加入PAFS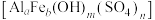 并测定其去浊率,结果如图所示(已知去浊率越高,净水效果越好)。由图可知在偏酸性和偏碱性的
并测定其去浊率,结果如图所示(已知去浊率越高,净水效果越好)。由图可知在偏酸性和偏碱性的 条件下,水样的去浊率均不高。试分析
条件下,水样的去浊率均不高。试分析 时,去浊率较低的可能原因为
时,去浊率较低的可能原因为
您最近一年使用:0次
名校
2 . 钴及其化合物广泛应用于航天、电池、磁性合金等高科技领域,我国钴资源贫乏,再生钴资源的回收利用是解决钴资源供给的重要途径.一种利用含钴废料(主要成分为 ,含少量
,含少量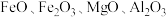 、有机物)制取
、有机物)制取 的工艺流程如下:
的工艺流程如下: ,回答下列问题:
,回答下列问题:
(1)“焙烧”的主要目的是____________ 。
(2)“浸取”过程中 发生反应的离子方程式为
发生反应的离子方程式为________ 。
(3)“沉淀"时先加入 溶液,
溶液, 的作用主要是
的作用主要是_____________ 。再加入 溶液调节
溶液调节 为6.0,此时滤液中的
为6.0,此时滤液中的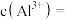
________  ,滤渣的主要成分为:
,滤渣的主要成分为:________ 。
(4)“萃取”用到的玻璃仪器主要有________ 烧杯。为得到纯净的 ,“沉钴”后要进行洗涤,如何判断沉淀是否洗涤干净?
,“沉钴”后要进行洗涤,如何判断沉淀是否洗涤干净?____________ 。
(5)萃取原理可表述为: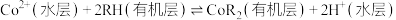 ,“反萃取”需加入A的水溶液,试剂A为
,“反萃取”需加入A的水溶液,试剂A为________ 。
 ,含少量
,含少量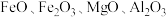 、有机物)制取
、有机物)制取 的工艺流程如下:
的工艺流程如下:
 ,回答下列问题:
,回答下列问题:金属离子 |
|
|
|
|
|
开始沉淀 | 7.5 | 1.8 | 3.4 | 9.1 | 6.5 |
沉淀完全 | 9.5 | 3.2 | 4.7 | 11.1 | 8.5 |
(1)“焙烧”的主要目的是
(2)“浸取”过程中
 发生反应的离子方程式为
发生反应的离子方程式为(3)“沉淀"时先加入
 溶液,
溶液, 的作用主要是
的作用主要是 溶液调节
溶液调节 为6.0,此时滤液中的
为6.0,此时滤液中的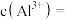
 ,滤渣的主要成分为:
,滤渣的主要成分为:(4)“萃取”用到的玻璃仪器主要有
 ,“沉钴”后要进行洗涤,如何判断沉淀是否洗涤干净?
,“沉钴”后要进行洗涤,如何判断沉淀是否洗涤干净?(5)萃取原理可表述为:
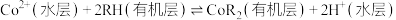 ,“反萃取”需加入A的水溶液,试剂A为
,“反萃取”需加入A的水溶液,试剂A为
您最近一年使用:0次
3 .  是生产多晶硅的副产物。利用
是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下:
(1)Co位于元素周期表第___________ 周期第___________ 族,Co位于元素周期表___________ 区。
(2)烧渣是LiCl、 和
和 的混合物,“500℃焙烧”后剩余的
的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因
应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因___________ 。
(3)鉴别洗净的“滤饼3”和固体 常用方法的名称是
常用方法的名称是___________ 。
(4)已知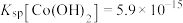 ,若“沉钴过滤”的pH控制为10.0,则溶液中
,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
浓度为___________  。“850℃煅烧”时的化学方程式为
。“850℃煅烧”时的化学方程式为___________ 。
(5)导致 比
比 易水解的因素有
易水解的因素有___________ (填标号)。
a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
 是生产多晶硅的副产物。利用
是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下:
(1)Co位于元素周期表第
(2)烧渣是LiCl、
 和
和 的混合物,“500℃焙烧”后剩余的
的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因
应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因(3)鉴别洗净的“滤饼3”和固体
 常用方法的名称是
常用方法的名称是(4)已知
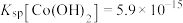 ,若“沉钴过滤”的pH控制为10.0,则溶液中
,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
浓度为 。“850℃煅烧”时的化学方程式为
。“850℃煅烧”时的化学方程式为(5)导致
 比
比 易水解的因素有
易水解的因素有a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
您最近一年使用:0次
名校
解题方法
4 . 硼镁泥是硼镁矿生产硼砂晶体(Na2B4O7·10H2O)时的废渣,其主要成分是MgO,还含有Na2B4O7、CaO、Fe2O3、FeO、MnO、SiO2等杂质。以硼镁泥为原料制取七水硫酸镁的工艺流程如下, 回答下列问题:_______ 。
(2)Na2B4O7易溶于水,也易发生水解: (硼酸在常温下溶解度较小)。写出加入硫酸时Na2B4O7发生反应的化学方程式:
(硼酸在常温下溶解度较小)。写出加入硫酸时Na2B4O7发生反应的化学方程式:_______ 。
(3)滤渣B中含有不溶于稀盐酸但能溶于热浓盐酸的黑色固体,写出生成黑色固体的离子方程式_______ 。加入MgO的目的是_______ 。
(4)已知MgSO4、CaSO4的溶解度(g/100g)如下表:
“操作A”是除去MgSO4和CaSO4混合溶液中的CaSO4,根据上表数据,简要说明“操作A”步骤为_______ 。
(5)NaBH4被称为有机化学中的“万能还原剂”,工业上可由硼砂制取,其晶胞结构及晶胞参数如图所示:_______ 。
②若选定A为坐标原点,则B的分数坐标为_______ 。
③NA代表阿伏加德罗常数的值,则NaBH4晶体的密度为_______ g•cm-3(用含a、NA的式子表示)。

(2)Na2B4O7易溶于水,也易发生水解:
 (硼酸在常温下溶解度较小)。写出加入硫酸时Na2B4O7发生反应的化学方程式:
(硼酸在常温下溶解度较小)。写出加入硫酸时Na2B4O7发生反应的化学方程式:(3)滤渣B中含有不溶于稀盐酸但能溶于热浓盐酸的黑色固体,写出生成黑色固体的离子方程式
(4)已知MgSO4、CaSO4的溶解度(g/100g)如下表:
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
(5)NaBH4被称为有机化学中的“万能还原剂”,工业上可由硼砂制取,其晶胞结构及晶胞参数如图所示:

②若选定A为坐标原点,则B的分数坐标为
③NA代表阿伏加德罗常数的值,则NaBH4晶体的密度为
您最近一年使用:0次
名校
5 . 高纯MgO具有优良的电绝缘性、高导热性等,常被用作绝缘材料填料、高温耐热材料。由白云石[主要成分为 ,含少量
,含少量 、
、 、
、 等杂质]制备高纯MgO和副产品
等杂质]制备高纯MgO和副产品 的一种流程如下:
的一种流程如下:
(1)请写出基态Ca原子的价电子排布式___________ 。
(2)步骤“煅烧1”中, 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
(3)“铵浸”时,含钙化合物被浸取,含镁化合物部分水化生成 (
(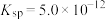 )。若铵浸液中
)。若铵浸液中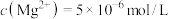 ,则其pH=
,则其pH=___________ ;滤饼“水化反应”后,将体系冷却到与铵浸液相同温度,得到主要含有 的悬浊液,其中
的悬浊液,其中
___________ 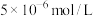 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
(4)“沉钙”时主要发生反应的离子方程式为___________ 。
(5)“碳化反应”时,镁化合物转化为可溶于水的___________ (填化学式,下同),滤渣的主要成分为___________ 。
(6)“热解”时生成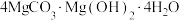 (碱式碳酸铁)沉淀,煅烧碱式碳酸镁比煅烧氢氧化镁所得MgO活性更强,平均粒径更小,比表面积更大,可能的原因是
(碱式碳酸铁)沉淀,煅烧碱式碳酸镁比煅烧氢氧化镁所得MgO活性更强,平均粒径更小,比表面积更大,可能的原因是___________ 。
 ,含少量
,含少量 、
、 、
、 等杂质]制备高纯MgO和副产品
等杂质]制备高纯MgO和副产品 的一种流程如下:
的一种流程如下: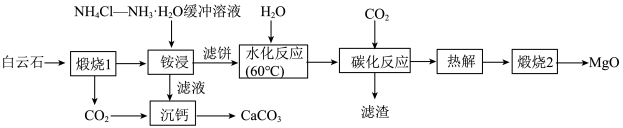
(1)请写出基态Ca原子的价电子排布式
(2)步骤“煅烧1”中,
 发生反应的化学方程式为
发生反应的化学方程式为(3)“铵浸”时,含钙化合物被浸取,含镁化合物部分水化生成
 (
(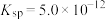 )。若铵浸液中
)。若铵浸液中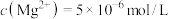 ,则其pH=
,则其pH= 的悬浊液,其中
的悬浊液,其中
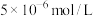 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。(4)“沉钙”时主要发生反应的离子方程式为
(5)“碳化反应”时,镁化合物转化为可溶于水的
(6)“热解”时生成
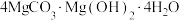 (碱式碳酸铁)沉淀,煅烧碱式碳酸镁比煅烧氢氧化镁所得MgO活性更强,平均粒径更小,比表面积更大,可能的原因是
(碱式碳酸铁)沉淀,煅烧碱式碳酸镁比煅烧氢氧化镁所得MgO活性更强,平均粒径更小,比表面积更大,可能的原因是
您最近一年使用:0次
名校
解题方法
6 . 利用含锌废料(主要成分是氧化锌,含有少量铁、铝、铜、锰等金属氧化物或盐)制备氯化锌的一种工艺流程如下:_______ 。(写出任意两点)
(2)为优化工艺流程,盐酸浸取后直接进行高锰酸钾氧化除杂。结合下列图表选择浸取工艺最佳pH范围为_______ ,理由是_______ 。
A.1.5~2.0 B.2.0~3.0 C.3.0~4.0 D.4.5~5.0
(3)滤渣的主要成分有Fe(OH)3、_______ 和MnO2,该工艺中去除锰的离子方程式为_______ 。
(4)最适宜使用的还原剂是_______ 。
(5)氯化锌溶液在蒸发浓缩过程中如操作不当将有碱式盐Zn(OH)Cl生成,该反应方程式为_______ 。
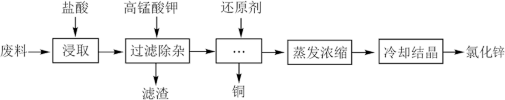
(2)为优化工艺流程,盐酸浸取后直接进行高锰酸钾氧化除杂。结合下列图表选择浸取工艺最佳pH范围为
A.1.5~2.0 B.2.0~3.0 C.3.0~4.0 D.4.5~5.0
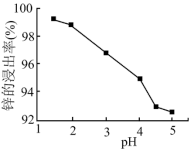
| 金属离子 | Fe2+ | Al3+ | Fe3+ | Cu2+ | Mn2+ | Zn2+ |
| 开始沉淀的pH c=0.01mol·L-1 | 6.8 | 3.7 | 1.8 | 5.2 | 8.6 | 6.7 |
| 沉淀完全的pH c=1.0×10-5mol·L-1 | 8.3 | 4.7 | 2.8 | 6.7 | 10.1 | 8.2 |
(4)最适宜使用的还原剂是
(5)氯化锌溶液在蒸发浓缩过程中如操作不当将有碱式盐Zn(OH)Cl生成,该反应方程式为
您最近一年使用:0次
7 . 硫酸铝是一种具有广泛用途的重要化工产品,以高岭土(含 、
、 、少量
、少量 等)为原料制备硫酸铝晶体[
等)为原料制备硫酸铝晶体[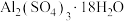 ]的实验流程如图所示。
]的实验流程如图所示。
(1)为加快酸溶速率,可采取的措施_______ (写出一条,合理即可)。
(2)滤渣1经过处理可作为制备水玻璃( 水溶液)的原料,写出滤渣1与烧碱溶液反应的离子方程式
水溶液)的原料,写出滤渣1与烧碱溶液反应的离子方程式_______ 。
(3)加入试剂除铁前,滤液1中的阳离子除了 、
、 外还有的阳离子是
外还有的阳离子是_______ (填离子符号)。滤渣2主要成分为 ,由于条件控制不当,常使
,由于条件控制不当,常使 中混有
中混有 影响其回收利用,用离子方程式表示除去
影响其回收利用,用离子方程式表示除去 的原理
的原理_______ 。
(4)向滤液1中加入的试剂可以是 ,试结合平衡移动原理说明其原因
,试结合平衡移动原理说明其原因_______ 。
(5)已知常温时:Ksp[Fe(OH)3] =1×10-37.4、Kw=1×10-14;当溶液中Fe3+浓度低于10-5mol/L时即认为Fe3+沉淀完全,实验中为确保Fe3+完全沉淀需控制PH不低于_______ (保留小数点一位)。
(6)某兴趣小组为了测定晶体中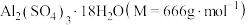 的质量分数,进行如下实验:
的质量分数,进行如下实验:
①准确称取1.00g晶体样品,溶于一定量水中;
②滴入 EDTA溶液,与
EDTA溶液,与 反应所消耗EDTA溶液的体积25.00mL。(已知:EDTA与
反应所消耗EDTA溶液的体积25.00mL。(已知:EDTA与 以物质的量之比1:1反应,假设杂质不与EDTA反应)。
以物质的量之比1:1反应,假设杂质不与EDTA反应)。
则晶体中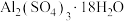 的质量分数是
的质量分数是_______ 。
 、
、 、少量
、少量 等)为原料制备硫酸铝晶体[
等)为原料制备硫酸铝晶体[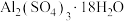 ]的实验流程如图所示。
]的实验流程如图所示。
(1)为加快酸溶速率,可采取的措施
(2)滤渣1经过处理可作为制备水玻璃(
 水溶液)的原料,写出滤渣1与烧碱溶液反应的离子方程式
水溶液)的原料,写出滤渣1与烧碱溶液反应的离子方程式(3)加入试剂除铁前,滤液1中的阳离子除了
 、
、 外还有的阳离子是
外还有的阳离子是 ,由于条件控制不当,常使
,由于条件控制不当,常使 中混有
中混有 影响其回收利用,用离子方程式表示除去
影响其回收利用,用离子方程式表示除去 的原理
的原理(4)向滤液1中加入的试剂可以是
 ,试结合平衡移动原理说明其原因
,试结合平衡移动原理说明其原因(5)已知常温时:Ksp[Fe(OH)3] =1×10-37.4、Kw=1×10-14;当溶液中Fe3+浓度低于10-5mol/L时即认为Fe3+沉淀完全,实验中为确保Fe3+完全沉淀需控制PH不低于
(6)某兴趣小组为了测定晶体中
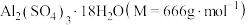 的质量分数,进行如下实验:
的质量分数,进行如下实验:①准确称取1.00g晶体样品,溶于一定量水中;
②滴入
 EDTA溶液,与
EDTA溶液,与 反应所消耗EDTA溶液的体积25.00mL。(已知:EDTA与
反应所消耗EDTA溶液的体积25.00mL。(已知:EDTA与 以物质的量之比1:1反应,假设杂质不与EDTA反应)。
以物质的量之比1:1反应,假设杂质不与EDTA反应)。则晶体中
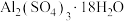 的质量分数是
的质量分数是
您最近一年使用:0次
8 . 某厂利用废旧铅蓄电池中的铅膏(主要成分为 、
、 、
、 和
和 ,还有少量铁、铝的氧化物)回收
,还有少量铁、铝的氧化物)回收 ,工艺流程如下:
,工艺流程如下: ,
, ,
,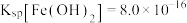 ,
, ,
, ,
, 。
。
(1)PbO中O元素的价电子的轨道表示式为___________ 。
(2)“脱硫”过程中涉及含 沉淀转化的离子方程式为
沉淀转化的离子方程式为___________ ,反应的平衡常数K的表达式___________ 。
(3)“酸浸”时, 能使
能使 转化为
转化为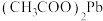 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 此外, 还能氧化溶液中的
还能氧化溶液中的___________ (填化学式或离子符号)。
(4)常温下,溶液中部分含铅物质的质量分数 与溶液
与溶液 变化的关系如图所示:
变化的关系如图所示: 由10增大到了11,发生反应的离子方程式为
由10增大到了11,发生反应的离子方程式为___________ 。
②“除杂”时,为了使 、
、 沉淀完全(离子浓度低于
沉淀完全(离子浓度低于 ),结合图与已知的信息,需调节溶液
),结合图与已知的信息,需调节溶液 的理论范围为
的理论范围为___________ 。
(5)PbO的溶解度曲线如图所示,结合图像分析,为得到高纯PbO固体,需将粗品PbO溶解在___________ (填“ ”或“
”或“ ”)浓度的
”)浓度的 溶液中,加热至
溶液中,加热至 ,充分溶解后趁热过滤,将滤液冷却结晶,过滤、洗涤并干燥得到高纯产品。
,充分溶解后趁热过滤,将滤液冷却结晶,过滤、洗涤并干燥得到高纯产品。
 、
、 、
、 和
和 ,还有少量铁、铝的氧化物)回收
,还有少量铁、铝的氧化物)回收 ,工艺流程如下:
,工艺流程如下: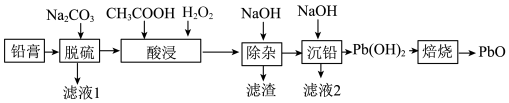
 ,
, ,
,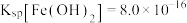 ,
, ,
, ,
, 。
。(1)PbO中O元素的价电子的轨道表示式为
(2)“脱硫”过程中涉及含
 沉淀转化的离子方程式为
沉淀转化的离子方程式为(3)“酸浸”时,
 能使
能使 转化为
转化为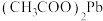 ,写出该反应的化学方程式
,写出该反应的化学方程式 还能氧化溶液中的
还能氧化溶液中的(4)常温下,溶液中部分含铅物质的质量分数
 与溶液
与溶液 变化的关系如图所示:
变化的关系如图所示:
 由10增大到了11,发生反应的离子方程式为
由10增大到了11,发生反应的离子方程式为②“除杂”时,为了使
 、
、 沉淀完全(离子浓度低于
沉淀完全(离子浓度低于 ),结合图与已知的信息,需调节溶液
),结合图与已知的信息,需调节溶液 的理论范围为
的理论范围为(5)PbO的溶解度曲线如图所示,结合图像分析,为得到高纯PbO固体,需将粗品PbO溶解在
 ”或“
”或“ ”)浓度的
”)浓度的 溶液中,加热至
溶液中,加热至 ,充分溶解后趁热过滤,将滤液冷却结晶,过滤、洗涤并干燥得到高纯产品。
,充分溶解后趁热过滤,将滤液冷却结晶,过滤、洗涤并干燥得到高纯产品。
您最近一年使用:0次
名校
解题方法
9 . 镍、铬、铜及其化合物在工业上有广泛的应用,从电镀污泥[含有 、
、 、
、 、
、 和
和 等]中回收制备
等]中回收制备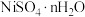 和其它金属及其化合物的工艺流程如图所示。
和其它金属及其化合物的工艺流程如图所示。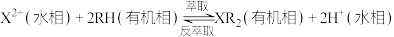 。
。
回答下列问题:
(1)与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有___________ (填元素符号)。
(2)已知NiO与MgO的晶体结构相同,其中 和
和 的离子半径分别为66pm和69pm。则熔点:NiO
的离子半径分别为66pm和69pm。则熔点:NiO___________ MgO(填“>”“<”或“=”),理由是___________ 。
(3)滤渣1的主要成分为___________ (填化学式)。
(4)电解之后加入碳酸钠调节pH的目的是___________ 。
(5)反萃取剂A为___________ 。
(6)“反萃取”得到的 溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为
溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为___________ 。
(7)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
由 溶液获得
溶液获得 晶体的操作依次是蒸发浓缩、
晶体的操作依次是蒸发浓缩、___________ 、过滤、洗涤、干燥。
(8)铁能形成多种氧化物,其中一种氧化物的晶胞结构如图所示:___________ ,该氧化物的化学式为___________ 。
②设 表示阿伏加德罗常数的值,若该晶胞的参数为anm,则该晶体的密度为
表示阿伏加德罗常数的值,若该晶胞的参数为anm,则该晶体的密度为___________  (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
 、
、 、
、 、
、 和
和 等]中回收制备
等]中回收制备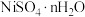 和其它金属及其化合物的工艺流程如图所示。
和其它金属及其化合物的工艺流程如图所示。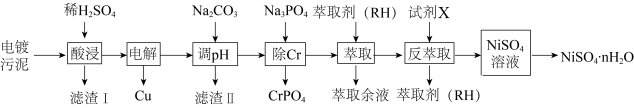
 。
。回答下列问题:
(1)与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有
(2)已知NiO与MgO的晶体结构相同,其中
 和
和 的离子半径分别为66pm和69pm。则熔点:NiO
的离子半径分别为66pm和69pm。则熔点:NiO(3)滤渣1的主要成分为
(4)电解之后加入碳酸钠调节pH的目的是
(5)反萃取剂A为
(6)“反萃取”得到的
 溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为
溶液,在碱性条件下可被NaClO氧化生成NiOOH沉淀,该反应的离子方程式为(7)资料显示,硫酸镍结晶水合物的形态与温度有如表关系:
| 温度 | 低于30.8℃ | 30.8℃~53.8℃ | 53.8℃~280℃ | 高于280℃ |
| 晶体形态 |  |  | 多种结晶水合物 |  |
 溶液获得
溶液获得 晶体的操作依次是蒸发浓缩、
晶体的操作依次是蒸发浓缩、(8)铁能形成多种氧化物,其中一种氧化物的晶胞结构如图所示:

②设
 表示阿伏加德罗常数的值,若该晶胞的参数为anm,则该晶体的密度为
表示阿伏加德罗常数的值,若该晶胞的参数为anm,则该晶体的密度为 (用含a、
(用含a、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
名校
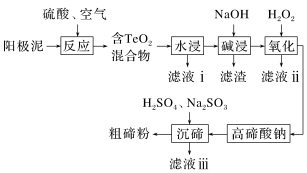
10 . 碲(Te)广泛应用于冶金、航空航天、电子等领域。从精炼钢的阳极泥(主要成分为Cu2Te,还含有金、银、铂等)中回收碲的工艺流程如图:
(1)为提高“反应”效率,可采取的措施为_______ (任答一条)。
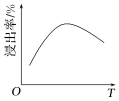
(2)滤液i的主要成分是_______ (写化学式)。滤液i中溶质的浸出率与温度的关系如图所示,解释浸出率随温度变化的可能原因_______ 。_______ 。滤液ii可循环使用,应将其导入到_______ (写操作单元名称)操作中。
(4)“沉碲”过程中发生反应的化学方程式为_______ 。
(5)粗碲粉中碲质量分数的测定步骤如下:取mg粗碲粉,加入酸使其转化为亚碲酸(H2TeO3),配制成100mL溶液,取25.00mL于锥形瓶中。向锥形瓶中加入V1mLc1mol•L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为碲酸(H6TeO6)。用c2mol•L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]标准溶液滴定剩余的酸性K2Cr2O7溶液,消耗V2mL硫酸亚铁铵标准溶液。该粗碲粉中碲的质量分数为_______ 。
(1)为提高“反应”效率,可采取的措施为
(2)滤液i的主要成分是
(4)“沉碲”过程中发生反应的化学方程式为
(5)粗碲粉中碲质量分数的测定步骤如下:取mg粗碲粉,加入酸使其转化为亚碲酸(H2TeO3),配制成100mL溶液,取25.00mL于锥形瓶中。向锥形瓶中加入V1mLc1mol•L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为碲酸(H6TeO6)。用c2mol•L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]标准溶液滴定剩余的酸性K2Cr2O7溶液,消耗V2mL硫酸亚铁铵标准溶液。该粗碲粉中碲的质量分数为
您最近一年使用:0次


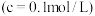 的
的 的
的

