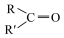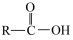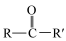名校
1 . Ⅰ.部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如图所示。
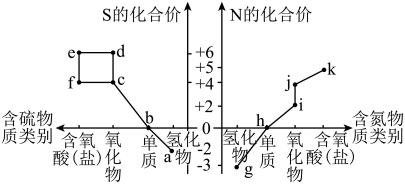
回答下列问题:
(1)j的化学名称是___________ 。
(2)下列有关a和g的叙述中,能说明N的非金属性比S强的是___________ (填字母)。
A.物质a的水溶液为酸性,而物质g的水溶液为碱性
B.物质a在300℃左右分解生成b,而物质g分解生成h的温度高于300℃
C.物质a液化的温度为-60℃,而物质g液化的温度为-34℃
(3)将pH=1的物质k的稀溶液倒入物质f的溶液中,会生成物质e,该反应的离子方程式是___________ 。
Ⅱ.S4N4(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质g通入S2Cl2的CCl4溶液中,可制得该物质:6S2Cl2+16g=S4N4+S8+12NH4Cl(已知S8是硫单质中最稳定的)。
(4)上述制备反应中,物质g体现的性质有___________ ,其中被氧化的元素是___________ (填元素符号)。
(5)S4N4在常温下较稳定,但撞击或加热时会引起爆炸,生成非常稳定的单质产物,该爆炸反应的化学方程式是___________ 。
Ⅲ.二氯化二硫(S2Cl2)可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。S2Cl2可通过硫与少量氯气在110~140℃反应制得,氯气过量则会生成SCl2,S2Cl2遇水剧烈水解,生成SO2、HCl和一种常见的固体。
(6)该固体是___________ (填名称)。
(7)甲同学为了验证两种气体产物,将水解生成的气体依次通过硝酸银与稀硝酸的混合溶液、品红溶液、NaOH溶液,该方案___________ (填“可行”或“不可行”),原因是___________ 。
(8)乙同学按如下实验方案检验S2Cl2是否含有杂质:
①取1.25g产品,在密闭容器中依次加入足量水、双氧水、Ba(NO3)2溶液,过滤;
②往①的滤液中加入足量AgNO3溶液,过滤、洗涤、干燥,称得固体质量为2.87g。
则产品中氯元素的质量分数为___________ ,由此可知产品中___________ (填“含有”或“不含有”)SCl2杂质。

回答下列问题:
(1)j的化学名称是
(2)下列有关a和g的叙述中,能说明N的非金属性比S强的是
A.物质a的水溶液为酸性,而物质g的水溶液为碱性
B.物质a在300℃左右分解生成b,而物质g分解生成h的温度高于300℃
C.物质a液化的温度为-60℃,而物质g液化的温度为-34℃
(3)将pH=1的物质k的稀溶液倒入物质f的溶液中,会生成物质e,该反应的离子方程式是
Ⅱ.S4N4(S是+2价)具有很好的导电性,在光学、电学等行业有着重要的用途。将干燥的物质g通入S2Cl2的CCl4溶液中,可制得该物质:6S2Cl2+16g=S4N4+S8+12NH4Cl(已知S8是硫单质中最稳定的)。
(4)上述制备反应中,物质g体现的性质有
(5)S4N4在常温下较稳定,但撞击或加热时会引起爆炸,生成非常稳定的单质产物,该爆炸反应的化学方程式是
Ⅲ.二氯化二硫(S2Cl2)可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。S2Cl2可通过硫与少量氯气在110~140℃反应制得,氯气过量则会生成SCl2,S2Cl2遇水剧烈水解,生成SO2、HCl和一种常见的固体。
(6)该固体是
(7)甲同学为了验证两种气体产物,将水解生成的气体依次通过硝酸银与稀硝酸的混合溶液、品红溶液、NaOH溶液,该方案
(8)乙同学按如下实验方案检验S2Cl2是否含有杂质:
①取1.25g产品,在密闭容器中依次加入足量水、双氧水、Ba(NO3)2溶液,过滤;
②往①的滤液中加入足量AgNO3溶液,过滤、洗涤、干燥,称得固体质量为2.87g。
则产品中氯元素的质量分数为
您最近一年使用:0次
2 . 钒、钨、锌在工业上用途广泛。
(1)基态钒(V)元素在周期表中的位置为_______ ,其最高化合价为_______ ,与其同周期且未成对电子数相同的元素符号为_______ ;
(2)钒能形成多种配合物。钒的两种配合物X、Y化学式均为V(NH3)3ClSO4,取X、Y的溶液进行如下实验(已知配体难电离出来),所用试剂及所得现象如表所示:
则X的配离子为_______ ,Y的配体为_______ 。
(3)NaxWO3是一类色彩丰富的非整比化合物,其晶体结构如图2所示,若Na+无空缺,化学式为NaWO3,完全空缺则为WO3,每填入1个Na+,相应有1个W6+还原为W5+。NaxWO3的颜色与x值的对应关系如图1所示,已知NaxWO3晶体中n(W6+):n(W5+)=2:3,则其颜色为_______ 色。

(4)如图3是金属钨晶体中的一个晶胞的结构模型(原子间实际是相互接触的)。其中心的原子位于立方体的体心。实验测得金属钨的半径为rcm,假定金属钨为等直径的刚性球,请回答以下各题:

①每一个晶胞中分摊到_______ 个钨原子。
②计算晶胞的空间利用率_______ (写出表达式,不计算具体数值)。
(1)基态钒(V)元素在周期表中的位置为
(2)钒能形成多种配合物。钒的两种配合物X、Y化学式均为V(NH3)3ClSO4,取X、Y的溶液进行如下实验(已知配体难电离出来),所用试剂及所得现象如表所示:
| 原溶液 | X溶液 | X溶液 | Y溶液 | Y溶液 |
| 所加试剂 | BaCl2溶液 | AgNO3溶液 | BaCl2溶液 | AgNO3溶液 |
| 现象 | 白色沉淀 | 无明显变化 | 无明显变化 | 白色沉淀 |
则X的配离子为
(3)NaxWO3是一类色彩丰富的非整比化合物,其晶体结构如图2所示,若Na+无空缺,化学式为NaWO3,完全空缺则为WO3,每填入1个Na+,相应有1个W6+还原为W5+。NaxWO3的颜色与x值的对应关系如图1所示,已知NaxWO3晶体中n(W6+):n(W5+)=2:3,则其颜色为

(4)如图3是金属钨晶体中的一个晶胞的结构模型(原子间实际是相互接触的)。其中心的原子位于立方体的体心。实验测得金属钨的半径为rcm,假定金属钨为等直径的刚性球,请回答以下各题:

①每一个晶胞中分摊到
②计算晶胞的空间利用率
您最近一年使用:0次
名校
3 . 合成氨是人工固氮比较成熟的技术,在工业上有重要的用途。
(1)已知化学键的键能如下表,
_______ 。
(2)恒温条件下,在体积固定的容器中发生合成氨的反应,下列叙述表明反应已达平衡状态的是_______ 。
①体系压强保持不变
②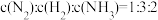
③每消耗 ,有
,有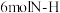 键发生断裂
键发生断裂
④混合气体的密度保持不变
⑤混合气体的平均摩尔质量保持不变
⑥v正(NH3)=0
(3)合成氨反应的平衡常数与温度的对应关系如下表:
试解释平衡常数随温度的升高而减小的原因_______ 。工业上合成氨一般以α-铁触媒为催化剂,400~500℃条件下反应,选取该反应温度而非室温或更高温度的原因是_______ 。
(4)在恒温条件下实验室模拟合成氨反应,甲、乙两容器充入相同量的N2与H2后体积相同,甲容器保持体积不变,乙容器保持压强不变,则反应到达平衡状态时,转化率甲_______ 乙(填“>”、“<”或“=”)。
(1)已知化学键的键能如下表,

| 化学键 | H-H | N≡N | N-H | N-N |
| 键能(kJ·mol-1) | 435.9 | 946.5 | 391.1 | 192.8 |
(2)恒温条件下,在体积固定的容器中发生合成氨的反应,下列叙述表明反应已达平衡状态的是
①体系压强保持不变
②
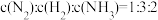
③每消耗
 ,有
,有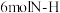 键发生断裂
键发生断裂④混合气体的密度保持不变
⑤混合气体的平均摩尔质量保持不变
⑥v正(NH3)=0
(3)合成氨反应的平衡常数与温度的对应关系如下表:
| 温度(℃) | 25 | 400 | 450 |
| 平衡常数 | 5×108 | 0.507 | 0.152 |
试解释平衡常数随温度的升高而减小的原因
(4)在恒温条件下实验室模拟合成氨反应,甲、乙两容器充入相同量的N2与H2后体积相同,甲容器保持体积不变,乙容器保持压强不变,则反应到达平衡状态时,转化率甲
您最近一年使用:0次
4 . (一)强还原剂液态肼(N2H4)和强氧化剂液态过氧化氢可构成火箭推进剂。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量热。已知:0.4mol液态肼与足量的液态过氧化氢反应生成N2和水蒸气时放出256.0kJ的热量。
(1)该反应的热化学方程式为_______ 。
(2)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是_______
(二)火箭发射时可以用肼( ,液态)作燃料,
,液态)作燃料, 作氧化剂,已知
作氧化剂,已知
①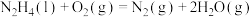
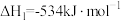
②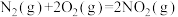
 ,
,
(3)写出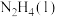 和
和 反应只生成氮气和水蒸气的热化学方程式为
反应只生成氮气和水蒸气的热化学方程式为_______ 。
(三)二氧化碳催化加氢生成甲醇和水,也有利于减少温室效应。其总反应分为以下两步:
第一步: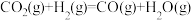
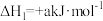
第二步: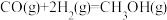
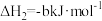
(4)已知 ,第一步反应为决定速率的反应。请在图中补全上述总反应过程的“能量变化-反应历程”示意图
,第一步反应为决定速率的反应。请在图中补全上述总反应过程的“能量变化-反应历程”示意图_______ 。_______ “a或者b”代表有催化剂参与,请利用有效碰撞理论解释催化剂加快反应速率的机理_______
(6)该反应是_______ 反应(填“放热”或者“吸热”)反应热为_______
(1)该反应的热化学方程式为
(2)此反应用于火箭推进,除释放大量热和快速产生大量气体外,还有一个很大的优点是
(二)火箭发射时可以用肼(
 ,液态)作燃料,
,液态)作燃料, 作氧化剂,已知
作氧化剂,已知①
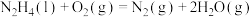
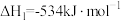
②
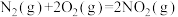
 ,
,(3)写出
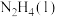 和
和 反应只生成氮气和水蒸气的热化学方程式为
反应只生成氮气和水蒸气的热化学方程式为(三)二氧化碳催化加氢生成甲醇和水,也有利于减少温室效应。其总反应分为以下两步:
第一步:
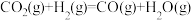
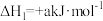
第二步:
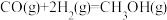
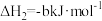
(4)已知
 ,第一步反应为决定速率的反应。请在图中补全上述总反应过程的“能量变化-反应历程”示意图
,第一步反应为决定速率的反应。请在图中补全上述总反应过程的“能量变化-反应历程”示意图

(6)该反应是
您最近一年使用:0次
解题方法
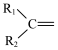
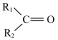
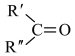
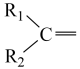
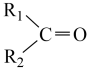
5 . 异戊二烯[CH2=C(CH3)CH=CH2]是一种重要的化工原料,能发生以下反应:
(1)反应①中异戊二烯与溴水中的Br2按物质的量之比为1∶1发生加成反应所得有机产物有___________ 种。
(2)Y的结构简式为___________ ,所含官能团的名称是___________ 。
(3)反应②的反应类型为___________ 。
(4)B为含有六元环的有机物,其结构简式为___________ 。
(5)异戊二烯的同分异构体有很多,写出符合下列条件的同分异构体的结构简式:___________ 、___________ 。
a.链状;b.含碳碳三键;c.核磁共振氢谱图显示有三组吸收峰。

| 烯烃被氧化的部位 | CH2= | RCH= |
|
| 氧化产物 | CO2 | RCOOH |
|
② 。
。
(1)反应①中异戊二烯与溴水中的Br2按物质的量之比为1∶1发生加成反应所得有机产物有
(2)Y的结构简式为
(3)反应②的反应类型为
(4)B为含有六元环的有机物,其结构简式为
(5)异戊二烯的同分异构体有很多,写出符合下列条件的同分异构体的结构简式:
a.链状;b.含碳碳三键;c.核磁共振氢谱图显示有三组吸收峰。
您最近一年使用:0次
6 . 异戊二烯(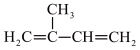 )是一种重要的化工原料,能发生以下反应:
)是一种重要的化工原料,能发生以下反应:

| 烯烃被氧化的部分 | CH2= | RCH= |
|
| 氧化产物 | CO2、H2O |
|
|
②狄尔斯-阿尔德反应(也称双烯合成反应)如图所示: (也可表示为
(也可表示为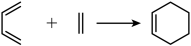 )。
)。
(2)异戊二烯中碳原子的杂化方式为
(3)反应①中异戊二烯和等物质的量的溴发生加成反应,其加成产物中二溴代物有
(4)写出Y的结构简式
(5)狄尔斯-阿尔德反应属于
您最近一年使用:0次
名校
7 . I.异戊二烯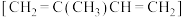 是一种重要的化工原料,能发生以下反应:
是一种重要的化工原料,能发生以下反应:

已知:④烯烃与酸性KMnO4溶液反应的氧化产物对应关系:
共轭双烯体系能与烯或炔键发生环加成反应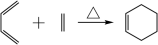
请回答下列问题:
(1)异戊二烯的一氯代物有________ 种(不包含顺反异构),若包含顺反异构,将会有________ 种一氯代物;写出一种反应①发生1,2—加成所得有机产物的结构简式为________ 。
(2)X存在顺反异构,写出它的反式异构体的结构简式:________ ,X可能发生的反应有________ (填字母)。
A.加成反应 B.氧化反应 C.酯化反应
(3)Y的结构简式为________ ;B为含有六元环的有机物,其结构简式为________ 。
Ⅱ.如图所示是以石油为原料制备某些化工产品的部分流程。请回答:
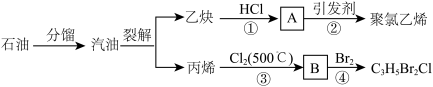
(4)写出反应②的化学方程式________ 。
(5)B分子中无甲基,则B的结构简式为________ 。
(6)反应①和③的类型依次是________ 、________ 。
(7)反应④化学方程式为________ 。
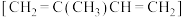 是一种重要的化工原料,能发生以下反应:
是一种重要的化工原料,能发生以下反应:
已知:④烯烃与酸性KMnO4溶液反应的氧化产物对应关系:
烯烃被氧化的部位 | CH2= | RCH= |
|
氧化产物 | CO2 | RCOOH |
|
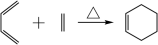
请回答下列问题:
(1)异戊二烯的一氯代物有
(2)X存在顺反异构,写出它的反式异构体的结构简式:
A.加成反应 B.氧化反应 C.酯化反应
(3)Y的结构简式为
Ⅱ.如图所示是以石油为原料制备某些化工产品的部分流程。请回答:

(4)写出反应②的化学方程式
(5)B分子中无甲基,则B的结构简式为
(6)反应①和③的类型依次是
(7)反应④化学方程式为
您最近一年使用:0次
名校
解题方法
8 . 氮、硫的氧化物都会引起环境问题,越来越引起人们的重视。如图是氮、硫元素的各种价态与物质类别的对应关系:

(1)硫酸是一种重要的化工产品。在实验室中,向蔗糖中加入浓硫酸会产生“黑面包”现象并有难闻气味,其中产生难闻气味体现了浓硫酸的___________ (填“强氧化性”“吸水性”或“脱水性”)。
(2)由上图,可知A为___________ (写分子式),从氮元素的化合价能否发生变化的角度判断,图中既有氧化性又有还原性的含氮化合物有___________ ;在催化剂作用下CO跟NO反应生成两种无毒气体的化学方程式为___________ 。
(3)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层,发生反应的化学方程式为___________ 。
(4)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学方程式:___________ 。
(5)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。常用的方法是先用热空气吹出Br2,再用SO2水溶液吸收Br2,取吸收后的溶液,向其中加入氯化钡溶液有白色沉淀析出。写出SO2水溶液吸收Br2反应的离子方程式:___________ 。

(1)硫酸是一种重要的化工产品。在实验室中,向蔗糖中加入浓硫酸会产生“黑面包”现象并有难闻气味,其中产生难闻气味体现了浓硫酸的
(2)由上图,可知A为
(3)浓、稀硝酸的性质既相似又有差别,若要除去铁制品表面的铜镀层,发生反应的化学方程式为
(4)工厂里常采用NaOH溶液吸收NO、NO2的混合气体,使其转化为化工产品NaNO2,试写出其化学方程式:
(5)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。常用的方法是先用热空气吹出Br2,再用SO2水溶液吸收Br2,取吸收后的溶液,向其中加入氯化钡溶液有白色沉淀析出。写出SO2水溶液吸收Br2反应的离子方程式:
您最近一年使用:0次
名校
解题方法
9 . 异戊二烯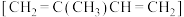 是一种重要的化工原料,能发生以下反应。
是一种重要的化工原料,能发生以下反应。 溶液反应的氧化产物对应关系如表。
溶液反应的氧化产物对应关系如表。
(1)异戊二烯的核磁共振H谱有___________ 组特征峰。
(2)异戊二烯的一氯代物有___________ 种(含顺反异构);写出一种反应①发生1,2加成所得有机产物的结构简式:___________ 。
(3)写出反应②的化学方程式:___________ 。
(4)X可能发生的反应有___________ (填序号)。
A.加成反应 B.消去反应 C.酯化反应
(5)Y的结构简式为___________ 。
(6)B为分子中含有六元环的有机化合物,其结构为___________ 。
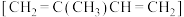 是一种重要的化工原料,能发生以下反应。
是一种重要的化工原料,能发生以下反应。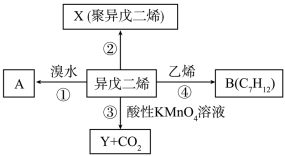
 溶液反应的氧化产物对应关系如表。
溶液反应的氧化产物对应关系如表。| 烯烃被氧化的部分 | 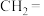 | 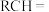 |
|
| 氧化物 |  |
|
|
②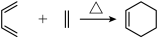
(1)异戊二烯的核磁共振H谱有
(2)异戊二烯的一氯代物有
(3)写出反应②的化学方程式:
(4)X可能发生的反应有
A.加成反应 B.消去反应 C.酯化反应
(5)Y的结构简式为
(6)B为分子中含有六元环的有机化合物,其结构为
您最近一年使用:0次
名校
解题方法
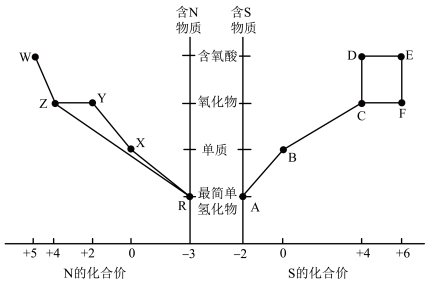
10 . Ⅰ.元素的“价-类”二维图体现了化学变化之美。部分含硫、氮物质的类别与硫元素和氮元素化合价的对应关系如图所示。回答下列问题:
(1)写出检验某溶液中含有铵根离子的实验方法_____ 。
(2)物质R→Y是工业制硝酸的重要反应,其化学方程式是_____ 。
(3)写出在加热条件下物质E的浓溶液与碳单质反应的化学方程式:_____ 。
(4)下列有关图中所示含N、S物质的叙述,正确的是_____(填标号)。
(5)将 铜与
铜与 一定浓度的物质W充分反应,铜完全溶解,产生标准状况下的物质Y和二氧化氮混合气体共
一定浓度的物质W充分反应,铜完全溶解,产生标准状况下的物质Y和二氧化氮混合气体共 。则混合气体中物质Y的体积为
。则混合气体中物质Y的体积为_____ L(标准状况下)。
(6)在 混合液中,W和E的浓度分别是
混合液中,W和E的浓度分别是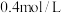 和
和 ,向该混合液中加入
,向该混合液中加入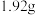 铜粉,加热充分反应后,假设所得溶液体积不变,溶液
铜粉,加热充分反应后,假设所得溶液体积不变,溶液 的物质的量浓度是
的物质的量浓度是_____ 。
Ⅱ.某同学欲选用如图的部分装置和药品探究 的性质。
的性质。
(7) 通入D装置中溶液褪色,体现
通入D装置中溶液褪色,体现 具有
具有_____ 性。
(8)为验证 具有还原性,设计装置的连接顺序为
具有还原性,设计装置的连接顺序为_____ (用字母表示);写出体现该性质的离子反应方程式_____ 。

(1)写出检验某溶液中含有铵根离子的实验方法
(2)物质R→Y是工业制硝酸的重要反应,其化学方程式是
(3)写出在加热条件下物质E的浓溶液与碳单质反应的化学方程式:
(4)下列有关图中所示含N、S物质的叙述,正确的是_____(填标号)。
| A.在催化剂的作用下,R可将Y、Z还原为X |
| B.图中所示的物质中,C与A反应出现淡黄色沉淀,体现C的还原性 |
| C.用玻璃棒分别蘸取浓的R溶液和浓的W溶液,玻璃棒靠近时有白烟产生 |
D.Z、C、F均能与 溶液反应,都是酸性氧化物 溶液反应,都是酸性氧化物 |
(5)将
 铜与
铜与 一定浓度的物质W充分反应,铜完全溶解,产生标准状况下的物质Y和二氧化氮混合气体共
一定浓度的物质W充分反应,铜完全溶解,产生标准状况下的物质Y和二氧化氮混合气体共 。则混合气体中物质Y的体积为
。则混合气体中物质Y的体积为(6)在
 混合液中,W和E的浓度分别是
混合液中,W和E的浓度分别是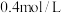 和
和 ,向该混合液中加入
,向该混合液中加入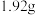 铜粉,加热充分反应后,假设所得溶液体积不变,溶液
铜粉,加热充分反应后,假设所得溶液体积不变,溶液 的物质的量浓度是
的物质的量浓度是Ⅱ.某同学欲选用如图的部分装置和药品探究
 的性质。
的性质。 |  |  |  |  |
| A | B | C | D | E |
(7)
 通入D装置中溶液褪色,体现
通入D装置中溶液褪色,体现 具有
具有(8)为验证
 具有还原性,设计装置的连接顺序为
具有还原性,设计装置的连接顺序为
您最近一年使用:0次