名校
1 . 黄色固体X,可能含有漂白粉、FeSO4、Fe2(SO4)3、CuCl2、KI之中的几种或全部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是
| A.X中必有CuCl2,可能含有KI、FeSO4 |
| B.X中必有漂白粉和CuCl2而Fe2(SO4)3和FeSO4至少有一种 |
| C.Y中必有Cu(OH)2和Fe(OH)3,可能有I2 |
| D.用H2SO4酸化溶液Z,若有黄绿色气体放出,说明X中含有CuCl2 |
您最近一年使用:0次
名校
2 . 已知22℃下水的蒸气压为2.7kPa,在该温度和100.0kPa下,用排水集气法收集到H2(g)0.05mol,则干燥后H2(g)的体积应为
| A.1.26L | B.2.45L | C.12.6L | D.24.5L |
您最近一年使用:0次
3 . 一块铜板被等分成两块,Cu(a)和Cu(b);锤打Cu(a),Cu(b)不动。再由Cu(a)、Cu(b)及CuSO4溶液组成电池:Cu(a)|CuSO4(cmol·L-1)|Cu(b),测得电动势E>0,因为Cu(a)的
| A.△S>0,△H=0 | B.△S>0,△H<0 |
| C.△S<0,△H=0 | D.△S<0,△H<0 |
您最近一年使用:0次
名校
4 . 已知H3PO4的pKa1=2.1,pKa2=7.2,pKa3=12.7,则0.10mol·L-1Na2HPO4水溶液的pH值约为
| A.4.65 | B.9.95 | C.7.40 | D.7.33 |
您最近一年使用:0次
名校
5 . 室温下,某溶液初始时仅溶有M和N且浓度相等,同时发生以下两个反应:①M+N=X+Y;②M+N=X+Z,反应①的速率可表示为v1=k1c2(M),反应②的速率可表示为v2=k2c2(M)(k1、k2为速率常数)。反应体系中组分M、Z的浓度(mol。L-1)随时间(分)变化情况如图,下列说法正确的是
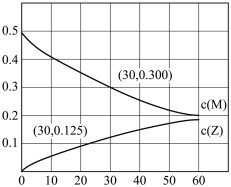
| A.0~30min时间段内,Y的平均反应速率为6.67×10-3mol·L-1·min-1 |
B.反应过程中体系Y和Z的浓度之比保持不变,30min时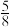 的M转化为Z 的M转化为Z |
| C.反应②的活化能比反应①的活化能大 |
| D.若该平行反应为可逆反应,正反应都为放热,升高温度,可提高Y的产率 |
您最近一年使用:0次
名校
6 . 钾氩定年法可用于分析火星矿物形成的年代。已40K衰变时,10.5%为β+衰变生成40Ar,89.5%为β衰变生成40Ca,40K的半衰期为12.5亿年。则40K发生β+衰变和β衰变的速率常数k1和k2分别为
| A.k1=5.82×10-1ly-1,k2=4.96×10-10y-1 | B.k1=7612×10-12y-1,k2=9.64×10-11y-1 |
| C.k1=5.56亿年-1,k2=6.68亿年-1 | D.k1=4.80亿年-1,k2=7.68亿年-1 |
您最近一年使用:0次
名校
解题方法
7 . 据文献报道:Fe(CO)5催化某反应的一种反应机理如图。下列叙述错误的是
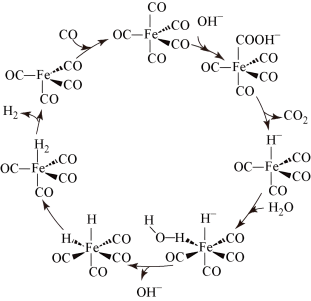
| A.该催化循环中OH-参与了反应 |
| B.该反应可消耗温室气体CO2产生清洁燃料H2 |
| C.Fe(CO)5铁的氧化数为0 |
| D.该催化循环中Fe的成键数目和类型都发生变化 |
您最近一年使用:0次
名校
解题方法
8 . 最近我国科学家设计了一种CO2+H2S协同转化装置,实现对天然气中CO和H2S的高效去除。示意图如图所示,其中电极分别为ZnO@石墨烯(石墨烯包裹的ZnO)和石墨烯,石墨烯电极区发生反应为:
①EDTA-Fe2+-e-=EDTA-Fe3+
②2EDTA-Fe3++H2S=2H++S+2EDTA-Fe2+
该装置工作时,下列叙述错误的是
①EDTA-Fe2+-e-=EDTA-Fe3+
②2EDTA-Fe3++H2S=2H++S+2EDTA-Fe2+
该装置工作时,下列叙述错误的是
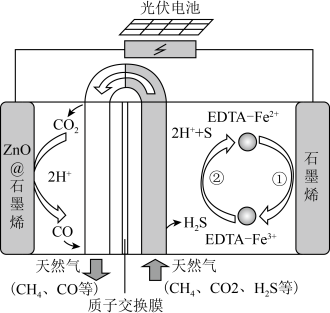
| A.阴极的电极反应:CO2+2H++2e-=CO+H2O |
| B.若生成3.2gS,理论上通过两极电量都为0.4F(C)(F为法拉第常数) |
| C.石墨烯上的电势比ZnO@石墨烯上的高 |
| D.若采用Fe3+/Fe2+取代EDTA-Fe3+/EDTA-Fe2+,溶液需为酸性 |
您最近一年使用:0次
9 . 一定温度下的难溶电解质AmBn在水溶液中达到沉淀溶解平衡时,其平衡常数数据:
对含等物质的量的CuSO4、FeSO4、Fe(SO4)3的混合溶液的下列说法,正确的是
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp/25℃ | 8.0×10-16 | 2.2×10-20 | 4.0×10-36 |
| 完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | ≥3 |
| A.向该混合溶液中逐滴加入NaOH溶液,当Cu开始沉淀时,溶液中c(Fe3+)=4.0×10-13.2 |
B.该溶液中C( ):c(Cu2+)=5:1 ):c(Cu2+)=5:1 |
| C.向该溶液中加入适量氯水,调节pH到4~5后过滤,可获得纯净的CuSO4溶液 |
| D.常温下向该溶液中加入0.10mol/L氨水过量(K=1.8×10-5)三种离子都完全沉淀 |
您最近一年使用:0次
名校
解题方法
10 . 用0.1000mol/LNaOH溶液滴定同浓度CH3COOH,若两者的浓度均增大10倍,下列对化学计量点(sp)前后滴定突跃范围大小描述正确的是
| A.sp前后0.1%的pH均增大 |
| B.sp前0.1%的pH不变,sp后0.1%的pH增大 |
| C.sp前后0.1%的pH均减小 |
| D.sp前0.1%的pH增大,sp后0.1%的pH不变 |
您最近一年使用:0次



