解题方法
1 . 下列有关离子方程式的书写正确的是
A.Na2S2O3溶液与稀硫酸的反应: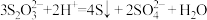 |
B.用纯铜电板电解CuCl2溶液:Cu2++2Cl- Cu+Cl2↑ Cu+Cl2↑ |
C.NH4Al(SO4)2溶液与足量的Ba(OH)2溶液反应: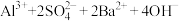 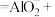 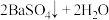 |
D.用Na2CO3溶液吸收少量Cl2: |
您最近一年使用:0次
2 . 下列表示正确的是
| A.乙醇的分子式:CH3CH2OH |
B.BaSO4的电离方程式:BaSO4 Ba2++SO Ba2++SO |
C.质量数为127的碘原子: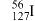 |
D.过氧化钠的电子式: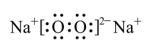 |
您最近一年使用:0次
解题方法
3 . 已知某种二次锂离子电池工作时反应为LixCn+Li1-xCoO2=LiCoO2+nC。电池如图所示。下列说法正确的是
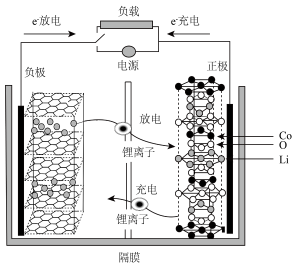

| A.放电时,碳材料极得到电子发生还原反应,电子经外电路,Li+经内电路同时移向正极 |
| B.放电时正极反应为Li1-xCoO2+xLi+-xe-=LiCoO2 |
| C.充电时, Li+从负极脱出,又嵌入正极 |
| D.锂离子二次电池正、负极之间充、放电时发生传输 Li+的反应,少有副反应 |
您最近一年使用:0次
4 . 砷及其化合物有着广泛的用途。砷有两种常见的弱酸,砷酸(H3AsO4)和亚砷酸(H3AsO3)。已知砷酸(H3AsO4)的pKa1、pKa2、pKa3依次为2.25、6.77、11.40(pKa=-lgKa)。亚砷酸(H3AsO3)水溶液中存在多种微粒形态,各种微粒分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与溶液的pH关系如图所示。下列说法正确的是


A.砷酸(H3AsO4)的电离方程式为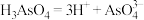 |
B.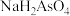 溶液呈碱性 溶液呈碱性 |
C.以酚酞为指示剂(变色范围pH8.2~10.0)将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加。该过程中主要反应的离子方程式为 |
D.在H3AsO4溶液中有: |
您最近一年使用:0次
5 . 一氧化碳甲烷化反应为:CO(g)+3H2(g)=CH4(g)+H2O(g)。如图是使用某种催化剂时转化过程中的能量变化(部分物质省略)。下列说法正确的是
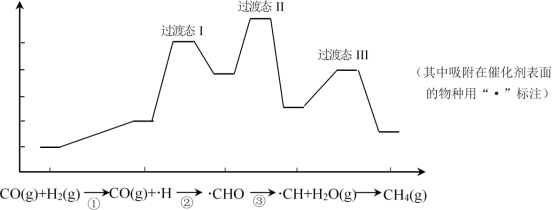

| A.步骤①是放热过程 |
B.步骤① ②只有极性键的断裂 ②只有极性键的断裂 |
| C.过渡态I能量最高,因此其对应的步骤①反应速率最慢,对整个反应的速率起决定作用 |
| D.该方法可以清除剧毒气体CO,从而保护环境 |
您最近一年使用:0次
6 . 在复杂的体系中,确认化学反应先后顺序有利于解决问题,下列化学反应先后顺序判断正确的是
A.在含有 、Ag+、 、Ag+、 、 、 等离子且浓度相等的溶液中加入锌粉: 等离子且浓度相等的溶液中加入锌粉: 、Ag+、 、Ag+、 、 、 |
B.在含 、 、 、 、 的溶液中逐滴加入KOH溶液: 的溶液中逐滴加入KOH溶液: 、 、 、 、 、 、 |
C.在含 、 、 、 、 的溶液中逐滴加入盐酸: 的溶液中逐滴加入盐酸: 、 、 、 、 、 、 |
D.在含 、KOH的混合溶液中缓慢通入CO2:KOH、 、KOH的混合溶液中缓慢通入CO2:KOH、 、 、 、 、 |
您最近一年使用:0次
7 . 对羟基肉桂酸甲酯M具有高光敏性和强效导电性等优良特性,是一种优良的触摸屏和高端光纤材料,结构简式如图所示。下列有关说法正确的是
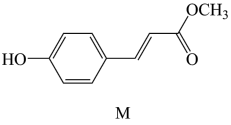

A.M的分子式为 |
| B.分子M能发生水解、加成、氧化等反应 |
| C.分子M中所含所有碳原子不可能处于同一平面内 |
D.1 mol M一定条件下能被5mol 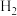 还原 还原 |
您最近一年使用:0次
8 . 原子序数小于36的X、Y、Z、W四种元素,其中X是原子半径最小的元素,Y原子基态时最外层电子数是其内层电子数的3倍,Z原子基态时2p原子轨道上有3个未成对电子,W的原子序数为29,下列说法正确的是
| A.X2Y分子中Y原子轨道的杂化类型为sp2 |
B.1molX2Y2含 键的数目为2 键的数目为2 |
| C.化合物ZX3的沸点比X2Y低 |
| D.原子半径大小顺序为Y>Z>X |
您最近一年使用:0次
9 . 下列实验操作能达到实验目的的是
| A.用向上排空气法收集NO |
| B.用烧杯配制100 mL 0.100 mol·L-1的硫酸 |
| C.用蒸发CuCl2溶液可得到CuCl2固体 |
| D.向含少量水的乙醇中加入生石灰后蒸馏可得到无水乙醇 |
您最近一年使用:0次
10 . Ni和Cu均为重要的合金元素,其单质和化合物在社会发展和国防科技等领域应用广泛。其中Cu(NH3)4SO4是一种广谱杀菌剂,下列说法正确的是
| A.基态Ni原子价层电子的核外电子排布式为3d84s2 |
| B.基态Cu原子核外未成对电子的数目为2 |
| C.基态N、S、O原子的第一电离能由大到小的顺序为N>S>O |
| D.Cu(NH3)4SO4配位数是5 |
您最近一年使用:0次



