1 . 设NA表示阿伏加德罗常数,下列叙述中正确的是
A.标准状况下,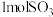 的分子数为 的分子数为 |
B. 和 和 充分反应,生成 充分反应,生成 |
C.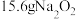 与过量 与过量 反应时,转移的电子数为 反应时,转移的电子数为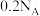 |
D.标准状况下,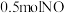 和 和 组成的混合气体,体积约为 组成的混合气体,体积约为 |
您最近一年使用:0次
名校
解题方法
2 . 对于反应2SO2(g)+O2(g)⇌2SO3(g) ΔH=akJ·mol-1,能量变化如图所示:(已知:焓变ΔH<0为放热反应)。下列说法中不正确的是
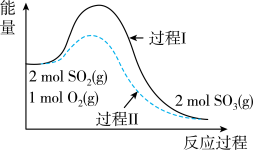

| A.反应过程中反应物断键吸收能量之和小于生成物成键释放能量之和 |
| B.2SO2(g)+O2(g)⇌2SO3(l) ΔH>akJ·mol-1 |
| C.过程Ⅱ使用了催化剂,使反应更快,放热更多 |
| D.将2molSO2(g)和1molO2(g)置于密闭容器中发生上述反应,充分反应后放出的热量小于|a|kJ |
您最近一年使用:0次
2023高三·全国·专题练习
名校
解题方法
3 . 已知短周期元素的四种离子A2+、B+、C3-、D-具有相同的电子层结构,则下列叙述中正确的是
| A.原子序数:D>C>B>A | B.原子半径:B>A>C>D |
| C.离子半径:C3->D->A2+>B+ | D.氧化性:A2+>B+,还原性:C3->D- |
您最近一年使用:0次
名校
4 . 如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是
| X | |||
| W | Y | R | |
| Z |
| A.W、R元素单质分子内的化学键都是非极性键 |
| B.X、Z元素都能够形成双原子分子 |
| C.键能:W-H>Y-H,键的极性:Y-H>W-H |
| D.键长:X-H<W-H,键能:X-H>W-H |
您最近一年使用:0次
名校
解题方法
5 . 下列有关电子排布式或排布图的结论错误的是
| 选项 | 电子排布式 | 结论 |
| A |  | 违背洪特规则 |
| B | 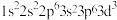 | 书写正确 |
| C | N的电子排布图: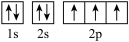 | 违背泡利原理 |
| D |  | 书写正确 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-02-17更新
|
359次组卷
|
3卷引用:四川省内江市第六中学2022-2023学年高二下学期入学考试化学试题
名校
解题方法
6 . 下列除去杂质的实验方法正确的是(括号里为少量杂质)
| A.Na2CO3( NaHCO3):加热 |
| B.CO2( CO):用酒精灯点燃 |
| C.FeCl2( FeCl3):加入足量铜粉,过滤 |
| D.Fe2O3(Al2O3):氢氧化钠溶液,过滤、洗涤 |
您最近一年使用:0次
解题方法
7 . 在容积不变的绝热密闭容器中通入 ,发生反应:
,发生反应: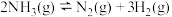
 ,下列不能说明该反应达到化学平衡状态的是
,下列不能说明该反应达到化学平衡状态的是
 ,发生反应:
,发生反应: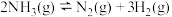
 ,下列不能说明该反应达到化学平衡状态的是
,下列不能说明该反应达到化学平衡状态的是| A.混合气体平均相对分子质量不再改变 | B.平衡常数K值不变 |
C. 和 和 的浓度的比值不变 的浓度的比值不变 | D.混合气体的总物质的量不再改变 |
您最近一年使用:0次
8 . 某兴趣小组利用数字化实验测定光照过程中氯水的pH、氯水中氯离子的浓度、广口瓶中氧气的体积分数三者的变化,实验结果如图所示。下列说法正确的是
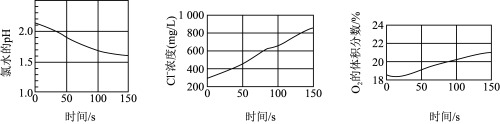

| A.氯水中存在能自由移动的离子、能导电,故Cl2属于电解质 |
| B.氯水中不存在H+,光照过程中才有H+生成 |
| C.O2体积分数逐渐增加,说明发生了氧化还原反应 |
D.由图可知,50s时Cl-浓度约为0.45g/L,计算可知氯水中c(Cl-)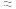 0.013 mol·L-1 0.013 mol·L-1 |
您最近一年使用:0次
2022-11-04更新
|
0次组卷
|
3卷引用:四川省南充市嘉陵区嘉陵第一中学2022-2023学年高一上学期(12月)月考化学试题
名校
解题方法
9 . 若反应: ΔH<0在绝热恒容的密闭体系中进行,下列示意图正确且能说明该反应在进行到t1时刻达到平衡状态的是
ΔH<0在绝热恒容的密闭体系中进行,下列示意图正确且能说明该反应在进行到t1时刻达到平衡状态的是
 ΔH<0在绝热恒容的密闭体系中进行,下列示意图正确且能说明该反应在进行到t1时刻达到平衡状态的是
ΔH<0在绝热恒容的密闭体系中进行,下列示意图正确且能说明该反应在进行到t1时刻达到平衡状态的是A.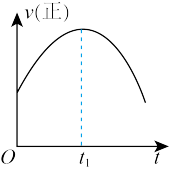 | B.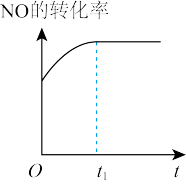 |
C.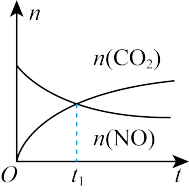 | D.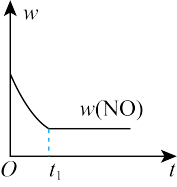 |
您最近一年使用:0次
2022-11-03更新
|
209次组卷
|
6卷引用:四川省遂宁二中2018-2019学年高二上学期半期考试化学试题
解题方法
10 . 已知元素X、Y同周期,且电负性:X>Y。下列说法错误的是
| A.X原子序数一定大于Y |
| B.Y的第一电离能一定大于X |
| C.X和Y形成化合物时,X显正价、Y显负价 |
| D.气体氢化物的稳定性:HmX>HnY |
您最近一年使用:0次
2022-09-15更新
|
87次组卷
|
2卷引用:四川省安岳县兴隆中学高2021-2022学年 高二上学期10月月考化学试题



