1 . 如图所示是s能级和p能级的电子云轮廓图。试回答下列问题。___________ 个原子轨道,其能量___________ (填“相同”或“不相同”)。
(2)元素X的原子最外层的电子排布式为nsnnpn+1,则元素X的氢化物的电子式是___________ 。
(3)若元素Y的原子最外层的电子排布式为 ,则Y的元素符号应为
,则Y的元素符号应为___________ ,其基态原子的核外电子排布图为___________ 。
(4)基态Al原子核外共有___________ 种不同能级的电子,有___________ 种不同运动状态的电子。
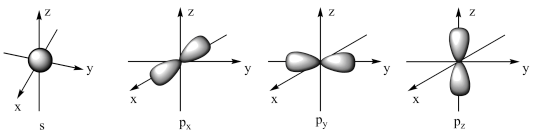
(2)元素X的原子最外层的电子排布式为nsnnpn+1,则元素X的氢化物的电子式是
(3)若元素Y的原子最外层的电子排布式为
 ,则Y的元素符号应为
,则Y的元素符号应为(4)基态Al原子核外共有
您最近一年使用:0次
2 . 在氮的单质和常见的含氮化合物中:
(1)常用作保护气(如填充灯泡、焊接保护等)的物质是___________ (填名称),原因是___________ 。
(2)常用作制冷剂的物质是___________ (填名称),原因是 ___________ 。
(3)能与酸反应生成盐,在常温下为气态的物质是___________ (填名称);它与盐酸反应的离子方程式是___________ 。
(1)常用作保护气(如填充灯泡、焊接保护等)的物质是
(2)常用作制冷剂的物质是
(3)能与酸反应生成盐,在常温下为气态的物质是
您最近一年使用:0次
解题方法
3 . 电解质的水溶液中存在电离平衡。
(1)NH3·H2O是常见的弱碱。
①NH3·H2O在水溶液中的电离方程式为_______ 。
②下列方法中,可以使氨水中NH3·H2O电离程度减小的是(填字母序号)________ 。
a.微热溶液 b.滴加浓盐酸 c.加水稀释 d.加入氯化铵晶体
(2)常温条件下,用0.1000mol/L NaOH溶液分别滴定体积均为 、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。_______ 。
②滴定醋酸的曲线是_______ (填“I”或“Ⅱ”),则V1______ V2(填“>”、 “<”“或“=”)。
(3)如图为盛放盐酸的滴定管中液面的位置。盐酸的体积读数:滴定后读数为_____ mL。 未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
①该滴定过程应选择______ (填“甲基橙”或“酚酞”)为指示剂,根据上述数据,可计算出该醋酸的浓度约为_____  。
。
②在上述实验中,下列操作会造成测定结果偏大的有______ 。(填字母序号)。
A.滴定前仰视读数,滴定后俯视读数
B.碱式滴定管使用前,水洗后未用标准氢氧化钠溶液润洗
C.滴定过程中,溶液刚出现变色,立即停止滴定
D.锥形瓶水洗后未干燥
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(1)NH3·H2O是常见的弱碱。
①NH3·H2O在水溶液中的电离方程式为
②下列方法中,可以使氨水中NH3·H2O电离程度减小的是(填字母序号)
a.微热溶液 b.滴加浓盐酸 c.加水稀释 d.加入氯化铵晶体
(2)常温条件下,用0.1000mol/L NaOH溶液分别滴定体积均为
 、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。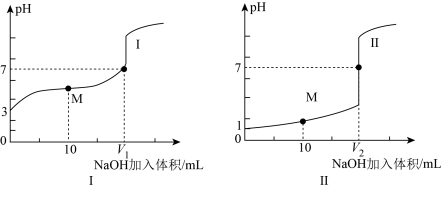
②滴定醋酸的曲线是
(3)如图为盛放盐酸的滴定管中液面的位置。盐酸的体积读数:滴定后读数为

 未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。| 实验编号 | NaOH溶液的浓度(mol·L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测醋酸的体积(mL) |
| 1 | 0.1000 | 22.48 | 20.00 |
| 2 | 0.1000 | 25.72 | 20.00 |
| 3 | 0.1000 | 22.52 | 20.00 |
 。
。②在上述实验中,下列操作会造成测定结果偏大的有
A.滴定前仰视读数,滴定后俯视读数
B.碱式滴定管使用前,水洗后未用标准氢氧化钠溶液润洗
C.滴定过程中,溶液刚出现变色,立即停止滴定
D.锥形瓶水洗后未干燥
E.碱式滴定管尖嘴部分有气泡,滴定后消失
您最近一年使用:0次
名校
解题方法
4 . 某研究性学习小组为确定一种从煤中提取的液态烃X的结构,对其进行探究。
步骤二:通过仪器分析得知X的相对分子质量为106。
步骤三:用核磁共振仪测出X的1H核磁共振谱有2个峰,其面积之比为2∶3.如图Ⅰ。
步骤四:利用红外光谱仪测得X分子的红外光谱如图Ⅱ。
(1)X的分子式为_______ ;X的名称为_______ 。
(2)步骤二中的仪器分析方法称为_______ 。
(3)写出X符合下列条件的同分异构体可能的结构简式_______ 。
①芳香烃 ②苯环上一氯代物有三种
(4)X以醋酸为溶剂在催化剂作用下用氧气氧化得到另一种重要的化工原料PTA,查阅资料得知PTA的溶解度:25℃时0.25g、50℃时0.97g、95℃时7.17g。得到的粗产品中有部分不溶性杂质,请分析实验室中提纯PTA的实验方法为:_______ 。
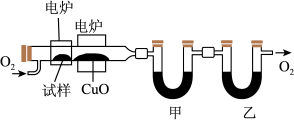
步骤二:通过仪器分析得知X的相对分子质量为106。
步骤三:用核磁共振仪测出X的1H核磁共振谱有2个峰,其面积之比为2∶3.如图Ⅰ。
步骤四:利用红外光谱仪测得X分子的红外光谱如图Ⅱ。

(1)X的分子式为
(2)步骤二中的仪器分析方法称为
(3)写出X符合下列条件的同分异构体可能的结构简式
①芳香烃 ②苯环上一氯代物有三种
(4)X以醋酸为溶剂在催化剂作用下用氧气氧化得到另一种重要的化工原料PTA,查阅资料得知PTA的溶解度:25℃时0.25g、50℃时0.97g、95℃时7.17g。得到的粗产品中有部分不溶性杂质,请分析实验室中提纯PTA的实验方法为:
您最近一年使用:0次
名校
解题方法
5 . 依据图中氮元素及其化合物的转化关系,回答问题:___________ ,从化合价上看,X具有___________ (填“氧化”或“还原”)性。依据X的物质类别推断,X转化为 的化学反应方程式为
的化学反应方程式为___________
(2)实验室常用 与
与 制取氨气,该反应的化学方程式为
制取氨气,该反应的化学方程式为___________ ,下列试剂能用于干燥产物的是___________ (填序号)。
A.浓硫酸 B.碱石灰 C.无水氯化钙 D.五氧化二磷固体
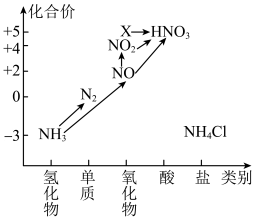
 的化学反应方程式为
的化学反应方程式为(2)实验室常用
 与
与 制取氨气,该反应的化学方程式为
制取氨气,该反应的化学方程式为A.浓硫酸 B.碱石灰 C.无水氯化钙 D.五氧化二磷固体
您最近一年使用:0次
6 . 一定温度下,现有a.盐酸,b.硫酸,c.醋酸三种酸
(1)当三种酸体积相同,物质的量浓度相同时,使其恰好完全中和所需NaOH的物质的量由大到小的顺序是___________ (用a、b、c表示)。
(2)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是___________ (用a、b、c表示)。
(3)当c(H+)相同、体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为___________ (用a、b、c表示)。
(1)当三种酸体积相同,物质的量浓度相同时,使其恰好完全中和所需NaOH的物质的量由大到小的顺序是
(2)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是
(3)当c(H+)相同、体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为
您最近一年使用:0次
名校
解题方法
7 . 碳是地球上组成生命的最基本元素之一、不仅能形成丰富多彩的有机化合物,还能形成多种无机化合物,碳及其化合物的用途广泛。根据要求回答下列问题:
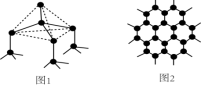
(1)下图中分别代表了碳单质的两种常见晶体,图1晶体中C原子的杂化方式为___________ ,图2晶体中,每个六元环占有___________ 个 C原子。 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的碳原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的碳原子,其价电子自旋磁量子数的代数和为___________ 。
(3)丙炔( )分子中π键、σ键数目之比为
)分子中π键、σ键数目之比为___________ 。
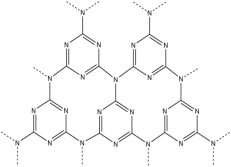
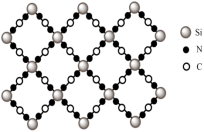
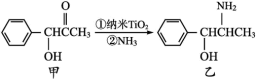
(4)g-C3N4具有和石墨相似的层状结构,其中一种二维平面结构如下图(左)所示,用硅原子替换氮化碳的部分碳原子可形成具有相似性质的化合物如下图(右)所示,该化合物的化学式为___________ ,该化合物中所有元素的电负性由大到小的顺序为 ___________ 。___________ 个手性碳原子。
(1)下图中分别代表了碳单质的两种常见晶体,图1晶体中C原子的杂化方式为
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态的碳原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。对于基态的碳原子,其价电子自旋磁量子数的代数和为(3)丙炔(
 )分子中π键、σ键数目之比为
)分子中π键、σ键数目之比为(4)g-C3N4具有和石墨相似的层状结构,其中一种二维平面结构如下图(左)所示,用硅原子替换氮化碳的部分碳原子可形成具有相似性质的化合物如下图(右)所示,该化合物的化学式为
您最近一年使用:0次
8 . 按要求填空。
Ⅰ.已知铜在常温下能被稀HNO3溶解,反应为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(1)用单线桥法标出该反应的电子转移情况:___________ 。
(2)该反应转移3mol电子时,生成的NO的体积为___________ (标况下),若反应后溶液体积为500mL,则溶液中Cu2+的浓度为___________
Ⅱ.乙酸是实验室常用的一种化学试剂,某乙酸试剂瓶上标签的部分内容如图所示。利用标签提供的信息,回答下列问题:___________ 。
(4)若该乙酸溶液的密度为1.2g/mL,此乙酸溶液的物质的量浓度为___________ 。
(5)某实验中要配制3.6mol/L的乙酸溶液80mL,则需量取上述乙酸溶液___________ mL进行稀释,此过程中所需的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和___________ 。
(6)在配制乙酸浓度时,浓度偏大的是___________ (填字母序号)。
a.定容时俯视刻度线 b.用量筒量取乙酸时,俯视读数 c.转移液体时,有少量液体流出
Ⅰ.已知铜在常温下能被稀HNO3溶解,反应为3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
(1)用单线桥法标出该反应的电子转移情况:
(2)该反应转移3mol电子时,生成的NO的体积为
Ⅱ.乙酸是实验室常用的一种化学试剂,某乙酸试剂瓶上标签的部分内容如图所示。利用标签提供的信息,回答下列问题:

(4)若该乙酸溶液的密度为1.2g/mL,此乙酸溶液的物质的量浓度为
(5)某实验中要配制3.6mol/L的乙酸溶液80mL,则需量取上述乙酸溶液
(6)在配制乙酸浓度时,浓度偏大的是
a.定容时俯视刻度线 b.用量筒量取乙酸时,俯视读数 c.转移液体时,有少量液体流出
您最近一年使用:0次
解题方法
9 . 已知25℃时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
(1)物质的量浓度均为0.1mol/L的下列四种溶液:pH由小到大排列的顺序是___________ 。
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是________ (填序号)。
A. B.
B.  C.
C.  D.
D.  E.
E. 
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:_____________ 。
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数Ka=_________ (用含a、b的代数式表示)。
(5)标准状况下将1.12LCO2通入100mL1mol/LNaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+___________ 。
(6)将碳酸钠溶液与次氯酸溶液混合,________ (填“是”或“否”)发生反应,若反应请写出反应的离子方程式:_______________ 。(不反应此问不答)
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | Ka=1×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | Ka=3.0×10-8 |
a.CH3COONa b.Na2CO3 c.NaClO d.NaHCO3
(2)常温下,0.1mol/LCH3COOH溶液加水稀释过程中,下列表达式的数据变大的是
A.
 B.
B.  C.
C.  D.
D.  E.
E. 
(3)写出向次氯酸钠溶液中通入少量二氧化碳的离子方程式:
(4)25℃时,将amol/L的醋酸溶液与bmol/L氢氧化钠溶液等体积混合,反应后溶液恰好显中性,表示醋酸的电离平衡常数Ka=
(5)标准状况下将1.12LCO2通入100mL1mol/LNaOH溶液中,用溶液中微粒的浓度符号完成下列等式:c(OH-)=2c(H2CO3)+
(6)将碳酸钠溶液与次氯酸溶液混合,
您最近一年使用:0次
10 . 磷酸亚铁锂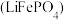 和锰酸锂
和锰酸锂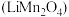 均可用作锂离子电池正极材料。回答下列问题:
均可用作锂离子电池正极材料。回答下列问题:
(1)基态O原子的价电子轨道表示式为___________ ;Mn的原子结构示意图为___________ 。
(2) 的熔、沸点
的熔、沸点___________ (填“高于”或“低于”) 。
。
(3) 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性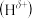 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性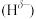 ,H、B、N电负性由小到大的顺序是
,H、B、N电负性由小到大的顺序是___________ 。
(4)已知: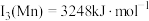 ,
,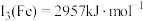 。Mn的第三电离能大于Fe的第三电离能,其主要原因是
。Mn的第三电离能大于Fe的第三电离能,其主要原因是___________ 。
(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种 配合物的结构如图所示,2mol该配合物中通过
配合物的结构如图所示,2mol该配合物中通过螯合作用 形成的配位键有___________ mol。
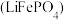 和锰酸锂
和锰酸锂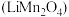 均可用作锂离子电池正极材料。回答下列问题:
均可用作锂离子电池正极材料。回答下列问题:(1)基态O原子的价电子轨道表示式为
(2)
 的熔、沸点
的熔、沸点 。
。(3)
 分子中,与N原子相连的H呈正电性
分子中,与N原子相连的H呈正电性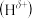 ,与B原子相连的H呈负电性
,与B原子相连的H呈负电性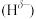 ,H、B、N电负性由小到大的顺序是
,H、B、N电负性由小到大的顺序是(4)已知:
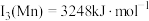 ,
,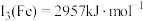 。Mn的第三电离能大于Fe的第三电离能,其主要原因是
。Mn的第三电离能大于Fe的第三电离能,其主要原因是(5)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。一种
 配合物的结构如图所示,2mol该配合物中通过
配合物的结构如图所示,2mol该配合物中通过
您最近一年使用:0次



