1 . 烃类物质是整个有机化学的基础,烃及其衍生物共同构成了庞大的有机物世界。
(1)实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。___________ 。___________ (填化学式)。
③甲烷与氯气反应生成的产物最多的是___________ (填化学式)。
④若将1molCH4与一定量的 反应,得到等物质的量的4种有机产物,则消耗
反应,得到等物质的量的4种有机产物,则消耗 的物质的量为
的物质的量为___________ mol。
(2)我国已对酒驾实行了“醉驾入刑”,酒的主要成分是乙醇。乙醇的官能团名称是___________ 。使用酸性 溶液可以检测酒驾,利用了乙醇的
溶液可以检测酒驾,利用了乙醇的___________ (填“氧化性”或“还原性”),其原理是:司机口中呼出的乙醇可以使检测仪中的橙色重铬酸钾(K2Cr2O)转变为绿色的硫酸铬[Cr2(SO4)3],上述反应涉及的乙醇性质有___________ 。
A.无色液体 B.密度比水的小 C.易挥发 D.具有还原性
(1)实验室中用如图所示的装置进行甲烷与氯气在光照下反应的实验。

A.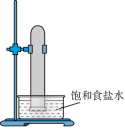 B.
B. C.
C.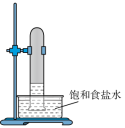 D.
D.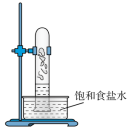
③甲烷与氯气反应生成的产物最多的是
④若将1molCH4与一定量的
 反应,得到等物质的量的4种有机产物,则消耗
反应,得到等物质的量的4种有机产物,则消耗 的物质的量为
的物质的量为(2)我国已对酒驾实行了“醉驾入刑”,酒的主要成分是乙醇。乙醇的官能团名称是
 溶液可以检测酒驾,利用了乙醇的
溶液可以检测酒驾,利用了乙醇的A.无色液体 B.密度比水的小 C.易挥发 D.具有还原性
您最近一年使用:0次
2 . 乙烯(CH2=CH2)是非常重要的化工基础原料,由乙烯可以制备很多有机物。
在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol氢气,发生CH2=CH2(g)+H2(g)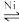 C2H6(g),容器内气体的压强与反应时间的关系如下图:
C2H6(g),容器内气体的压强与反应时间的关系如下图:
(1)有机物C2H6的名称是___________ 。该有机物属于___________ (填序号)。
A.烯烃 B.芳香烃 C.环状饱和烃 D.链状饱和烃(烷烃)
(2)该反应的类型属于___________(填序号)。
(3)达到化学平衡状态时,下列数值与开始时相同的是___________(填序号)
(4)反应进行到10min时,乙烯(CH2=CH2)的转化率a%=___________ 。
在恒温1L的刚性密闭容器中,加入1mol乙烯和1mol氢气,发生CH2=CH2(g)+H2(g)
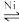 C2H6(g),容器内气体的压强与反应时间的关系如下图:
C2H6(g),容器内气体的压强与反应时间的关系如下图:| 时间(min) | 0 | 2 | 4 | 6 | 8 | 10 |
| 乙烯的物质的量(mol) | 1.00 | 0.80 | 0.70 | 0.64 | 0.60 | 0.60 |
A.烯烃 B.芳香烃 C.环状饱和烃 D.链状饱和烃(烷烃)
(2)该反应的类型属于___________(填序号)。
| A.取代反应 | B.加成反应 | C.加成聚合反应 | D.聚合反应 |
| A.容器内气体的压强 | B.容器内n(H2) | C.容器内c(CH2=CH2) | D.容器内气体的总质量 |
您最近一年使用:0次
名校
3 . 2019年是元素周期表诞生150周年,元素周期表在学习、研究和生产实践中有很重要的作用。①~⑦七种元素在元素周期表中的位置如表:
请回答下列问题:
(1)⑦的元素符号是______ ,其在元素周期表中的位置是______ 。
(2)元素①④⑤原子半径由大到小的顺序是______ ,由这三种元素组成的化合物是一种强碱,其化学式是______ ,电子式是______ ,该化合物中含有的化学键______ 。
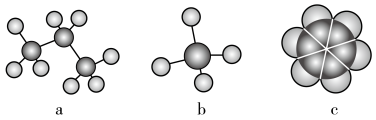
(3)由①②形成的最简单化合物的分子模型是______ (填序号)。______ 。
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
1 | ① | ||||||
2 | ② | ③ | ④ | ||||
3 | ⑤ | ⑥ | ⑦ |
(1)⑦的元素符号是
(2)元素①④⑤原子半径由大到小的顺序是
(3)由①②形成的最简单化合物的分子模型是
您最近一年使用:0次
名校
解题方法
4 . 某化学兴趣小组为了探究铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
根据表中记录的实验现象,回答下列问题。
(1)实验1、2中Al电极的作用是否相同______ (填“相同”或“不相同”)。
(2)实验3中Al为______ 极,电极反应式为______ ;
石墨为______ 极,电极反应式为______ ;
电池总反应为(离子方程式)______ 。
| 编号 | 电极材料 | 电解质溶液 | 电流表指针偏转方向 |
| 1 | Mg、Al | 稀盐酸 | 偏向Al |
| 2 | Al、Cu | 稀盐酸 | 偏向Cu |
| 3 | Al、石墨 | 稀盐酸 | 偏向石墨 |
(1)实验1、2中Al电极的作用是否相同
(2)实验3中Al为
石墨为
电池总反应为(离子方程式)
您最近一年使用:0次
5 . 回答下列问题。
(1)已知在K2Cr2O7的溶液中存在如下平衡:Cr2O (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+,向5mL0.1mol/L K7Cr2O7溶液中滴加5-10滴6mol/LNaOH溶液,
(黄色)+2H+,向5mL0.1mol/L K7Cr2O7溶液中滴加5-10滴6mol/LNaOH溶液,___________ 色加深,在此基础上再滴加3~10滴浓H2SO4溶液,___________ 色加深。
(2)草酸与高猛酸钾在酸性条件下能够发生如下反应:2MnO +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
①如果研究催化剂对化学反应速率的影响,使用实验___________ 和___________ (用 ~
~ 表示,下同);如果研究温度对化学反应速率的影响,使用实验
表示,下同);如果研究温度对化学反应速率的影响,使用实验___________ 和___________ 。
②对比实验 和
和 ,可以研究
,可以研究___________ 对化学反应速率的影响。
(1)已知在K2Cr2O7的溶液中存在如下平衡:Cr2O
 (橙色)+H2O
(橙色)+H2O 2CrO
2CrO (黄色)+2H+,向5mL0.1mol/L K7Cr2O7溶液中滴加5-10滴6mol/LNaOH溶液,
(黄色)+2H+,向5mL0.1mol/L K7Cr2O7溶液中滴加5-10滴6mol/LNaOH溶液,(2)草酸与高猛酸钾在酸性条件下能够发生如下反应:2MnO
 +5H2C2O4+6H+=2Mn2++10CO2↑+8H2O用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:| 组别 | 10%硫酸体积/mL | 温度/℃ | 其他物质 |
 | 2mL | 20 | |
 | 2mL | 20 | 少量MnSO4粉末 |
 | 2mL | 30 | |
 | 1mL | 20 | 1mL蒸馏水 |
 ~
~ 表示,下同);如果研究温度对化学反应速率的影响,使用实验
表示,下同);如果研究温度对化学反应速率的影响,使用实验②对比实验
 和
和 ,可以研究
,可以研究
您最近一年使用:0次
6 . 3H2(g) + 3CO(g) CH3OCH3(g) + CO2(g) ΔH>0一定条件下的密闭容器中,该反应达到平衡后,若要提高CO的转化率,可以采取的措施是
CH3OCH3(g) + CO2(g) ΔH>0一定条件下的密闭容器中,该反应达到平衡后,若要提高CO的转化率,可以采取的措施是___________ (填字母代号)。
a.高温高压 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度 e.分离出二甲醚
 CH3OCH3(g) + CO2(g) ΔH>0一定条件下的密闭容器中,该反应达到平衡后,若要提高CO的转化率,可以采取的措施是
CH3OCH3(g) + CO2(g) ΔH>0一定条件下的密闭容器中,该反应达到平衡后,若要提高CO的转化率,可以采取的措施是a.高温高压 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度 e.分离出二甲醚
您最近一年使用:0次
7 . 在25℃、101 kPa下,1g液态甲醇完全燃烧放热22.68 kJ,写出甲醇燃烧热的热化学方程式:___________ 。
您最近一年使用:0次
8 . 在一定温度下,10L密闭容器中加入5molSO2,2.5molO2,经10min后反应达平衡时有3molSO2发生了反应。试计算:
(1)O2的转化率为___________ 。
(2)平衡时体系中SO3的百分含量(体积分数,保留一位小数)为___________ 。
(1)O2的转化率为
(2)平衡时体系中SO3的百分含量(体积分数,保留一位小数)为
您最近一年使用:0次
9 . 合成氨反应N2 (g)+3H2(g) 2NH3(g)
2NH3(g)  H。若在恒温、恒压条件下向平衡体系中通入氩气,则平衡向
H。若在恒温、恒压条件下向平衡体系中通入氩气,则平衡向___________ 移动(填“正向”、“逆向”或“不”);若使用催化剂,上述反应的 H
H___________ (填“增大”、“减小” 或“不变”)。
 2NH3(g)
2NH3(g)  H。若在恒温、恒压条件下向平衡体系中通入氩气,则平衡向
H。若在恒温、恒压条件下向平衡体系中通入氩气,则平衡向 H
H
您最近一年使用:0次
解题方法
10 . 某温度时,在容积为2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示,根据图中数据,试回答:___________ 。
(2)写出该反应的化学方程式___________ 。
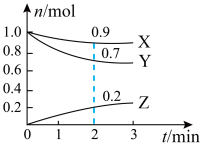
(2)写出该反应的化学方程式
您最近一年使用:0次



