1 . 短周期元素A、B、C、D的原子序数依次增大,A元素原子的核外电子只有一种运动状态:基态B原子s能级的电子总数比p能级的多1;基态C原子中成对电子数是未成对电子数的3倍;D形成简单离子的半径在同周期元素形成的简单离子中最小。回答下列问题
(1)B原子的轨道表示式___________ 。
(2)A和C原子个数比为1∶1的化合物的电子式___________ 。
(3)元素A、B、C中,第一电离能最大的是___________ (填元素名称)。
(4)在B、C、D三种元素的简单离子中,其离子的半径最小的是___________ 。(填离子符号)
(5)C的简单氢化物的键角小于B的简单氢化物,其原因是___________ 。
(6)BC₃的空间结构为___________ 。
(7)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB晶体的密度为a g⋅cm ,则晶体中两个最近D原子之间的距离为
,则晶体中两个最近D原子之间的距离为___________ pm(用 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。
(1)B原子的轨道表示式
(2)A和C原子个数比为1∶1的化合物的电子式
(3)元素A、B、C中,第一电离能最大的是
(4)在B、C、D三种元素的简单离子中,其离子的半径最小的是
(5)C的简单氢化物的键角小于B的简单氢化物,其原因是
(6)BC₃的空间结构为
(7)化合物DB是人工合成的半导体材料,它的晶胞结构与金刚石(晶胞结构如图所示)相似。若DB晶体的密度为a g⋅cm
 ,则晶体中两个最近D原子之间的距离为
,则晶体中两个最近D原子之间的距离为 表示阿伏加德罗常数)。
表示阿伏加德罗常数)。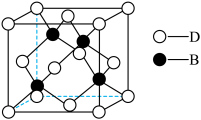
您最近一年使用:0次
2 . 完成下列问题
(1)下列四个合成反应路线的设计哪些是错误的?(请写出错误路线的编号) 和
和 从大到小排序:
从大到小排序:_________


_________ _________ _________ _________ _________
(1)下列四个合成反应路线的设计哪些是错误的?(请写出错误路线的编号)
①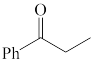

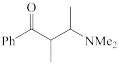
②


③

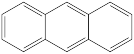
④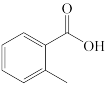


 和
和 从大到小排序:
从大到小排序:



(a)  (b)
(b) 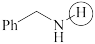 (c)
(c) 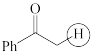 (d)
(d) 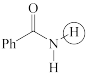 (e)
(e) 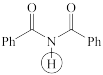
A. B.
B. C.
C.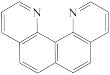 D.
D.
A.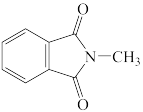 B.
B. C.
C. D.
D.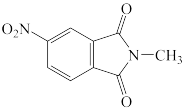
A. 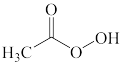 B.
B. 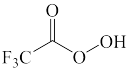 C.
C. 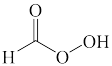 D.
D.  E.
E.  F.
F. 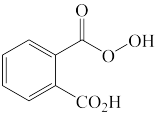
①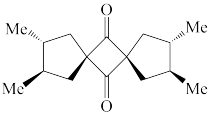 ②
② ③
③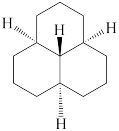 ④
④ ⑤
⑤
⑥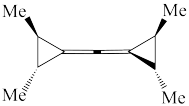 ⑦
⑦ ⑧
⑧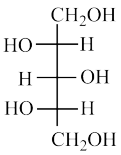 ⑨
⑨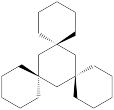 ⑩
⑩
您最近一年使用:0次
名校
3 . 碱性锌锰电池的工作原理:Zn+2MnO2+2H2O=2MnO(OH)+Zn(OH)2,其中的电解质溶液是KOH溶液。某课题组用废旧铁壳无汞碱性锌锰电池为原料,制备一种新型材料——MnxZn(1−x)Fe2O4,其工艺流程如图所示:
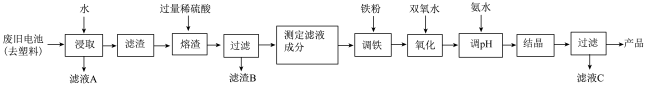
(1)已知MnxZn(1−x)Fe2O4中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中的锰相同,则铁元素的化合价为___________ 。
(2)滤液A中溶质的电子式为___________ 。
(3)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn2+,写出该反应的离子方程式:___________________________________ 。
(4)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式MnxZn(1−x)Fe2O4相符合。
①写出“调铁”工序中发生反应的离子方程式:__________________ 、_______________ 。
②若测得滤液的成分为c(Mn2+)+c(Zn2+)=a mol·L−1,c(Fe2+)+c(Fe3+)=b mol·L−1,滤液体积为1m3,“调铁”工序中,需加入的铁粉质量为___________ kg(忽略溶液体积变化,用含a、b的代数式表示)。
(5)在“氧化”工序中,加入双氧水的目的是_________________ ,生产过程中发现实际消耗双氧水的量大于理论值,其可能原因除温度外,主要是______________________ 。
(6)用氨水“调pH”后,经“结晶”、“过滤”可得到产品和滤液C(C为正盐),从滤液C中还可分离出一种氮肥,该氮肥的溶液中离子浓度由大到小的排序为_____________ 。

(1)已知MnxZn(1−x)Fe2O4中锰元素的化合价与实验室用二氧化锰制取氯气时还原产物中的锰相同,则铁元素的化合价为
(2)滤液A中溶质的电子式为
(3)“溶渣”工序中稀硫酸与铁反应生成的硫酸亚铁可将+3价锰的化合物全部还原成Mn2+,写出该反应的离子方程式:
(4)“调铁”工序的目的是调整滤液中铁离子的总浓度,使其中金属元素的物质的量之比与产品的化学式MnxZn(1−x)Fe2O4相符合。
①写出“调铁”工序中发生反应的离子方程式:
②若测得滤液的成分为c(Mn2+)+c(Zn2+)=a mol·L−1,c(Fe2+)+c(Fe3+)=b mol·L−1,滤液体积为1m3,“调铁”工序中,需加入的铁粉质量为
(5)在“氧化”工序中,加入双氧水的目的是
(6)用氨水“调pH”后,经“结晶”、“过滤”可得到产品和滤液C(C为正盐),从滤液C中还可分离出一种氮肥,该氮肥的溶液中离子浓度由大到小的排序为
您最近一年使用:0次
2019-07-04更新
|
255次组卷
|
2卷引用:四川省成都市蒲江县蒲江中学2021-2022学年高二下学期5月月考化学试题
4 . 过渡金属催化的新型碳﹣碳偶联反应是近年来有机合成的研究热点之一,如:
反应①
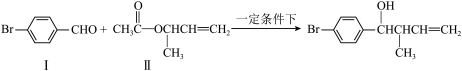
化合物Ⅱ可由化合物Ⅲ合成:

(1)化合物Ⅰ的分子式______
(2)化合物Ⅱ与Br2加成的产物的结构简式为_____________
(3)化合物Ⅲ的结构简式为_______________
(4)在浓硫酸存在和加热条件下,化合物Ⅳ易发生消去反应生成不含甲基的产物,该反应的方程式为___________ (注明反应条件),因此,在碱性条件下,由Ⅳ与CH3CO﹣Cl反应生成Ⅱ,其反应类型为__________ 。
(5)Ⅳ的一种同分异构体Ⅴ能发生银镜反应,Ⅴ与Ⅱ也可以发生类似反应①的反应,生成化合物Ⅵ,Ⅵ的结构简式为____________________ (写出其中一种)。
反应①

化合物Ⅱ可由化合物Ⅲ合成:

(1)化合物Ⅰ的分子式
(2)化合物Ⅱ与Br2加成的产物的结构简式为
(3)化合物Ⅲ的结构简式为
(4)在浓硫酸存在和加热条件下,化合物Ⅳ易发生消去反应生成不含甲基的产物,该反应的方程式为
(5)Ⅳ的一种同分异构体Ⅴ能发生银镜反应,Ⅴ与Ⅱ也可以发生类似反应①的反应,生成化合物Ⅵ,Ⅵ的结构简式为
您最近一年使用:0次
2019-01-30更新
|
1644次组卷
|
11卷引用:2015届四川省新津中学高三入学考试化学试卷
(已下线)2015届四川省新津中学高三入学考试化学试卷(已下线)2011-2012学年安徽省铜陵一中高二6月月考化学试卷(已下线)2014年高中化学二轮创新训练上 专题15有机化学基础选考练习卷2012年普通高等学校招生全国统一考试化学(广东卷)2015-2016学年山东省东平一中高二下期6月月考化学试卷云南省马关县第二中学2019-2020学年高二上学期期末考试化学试题云南省开远市第二中学校2019-2020学年高二上学期期末考试化学试题贵州省黔南布依族苗族自治州瓮安第二中学2019-2020学年高二上学期期末考试化学试题贵州省榕江县第三高级中学2019-2020学年高二上学期期末考试化学试题云南省曲靖市师宗县第二中学2019-2020学年高二上学期期末考试化学试题广西壮族自治区崇左市大新县大新中学2019-2020学年高二上学期期末考试化学试题
真题
名校
5 . 元素X 位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。元素Y基态原子的3p 轨道上有4个电子。元素Z 的原子最外层电子数是其内层的3倍。
(1)X与Y所形成化合物晶体的晶胞如图所示。

①在1个晶胞中,X离子的数目为_____ 。
②该化合物的化学式为_________ 。
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是_______ 。
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是______________ 。
(4)Y 与Z 可形成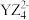
①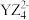 的空间构型为
的空间构型为__________ (用文字描述)。
②写出一种与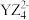 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:_________ 。
(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为___ 。
(1)X与Y所形成化合物晶体的晶胞如图所示。

①在1个晶胞中,X离子的数目为
②该化合物的化学式为
(2)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是
(3)Z的氢化物(H2Z)在乙醇中的溶解度大于H2Y,其原因是
(4)Y 与Z 可形成
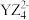
①
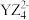 的空间构型为
的空间构型为②写出一种与
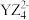 互为等电子体的分子的化学式:
互为等电子体的分子的化学式:(5)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为
您最近一年使用:0次
2019-01-30更新
|
2185次组卷
|
12卷引用:四川省雅安市2017-2018学年高二上学期期末考试化学试题
四川省雅安市2017-2018学年高二上学期期末考试化学试题2013年全国普通高等学校招生统一考试化学(江苏卷)(已下线)2012-2013学年福建省师大附中高二下学期期末考试化学试卷(已下线)2014届高考化学二轮专题冲刺第16讲 物质结构与性质练习卷2016届安徽省六安一中高三上第四次月考化学试卷2015-2016学年福建省师大附中高二上期末理化学试卷2016届福建省福州八中高三上学期第六次质检化学试卷2017届甘肃省定西市通渭县高三上学期期末化学试卷2016-2017学年山东省滨州市高二下学期第一次阶段性测试化学试卷宁夏回族自治区吴忠市吴忠中学2019-2020学年高二下学期期末考试化学试题(已下线)模块同步卷08 分子晶体与原子晶体-《灯塔金卷系列》2020-2021学年高二化学模块同步卷(人教版选修3)(已下线)2020年海南卷化学高考真题变式题15-19
6 . 某蓄电池反应为NiO2+Fe+2H2O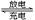 Fe(OH)2+Ni(OH)2
Fe(OH)2+Ni(OH)2
(1)该蓄电池充电时,发生还原反应的物质是_______ (填下列字母),放电时生成Fe(OH)2的质量18 g,则外电路中转移的电子数是_____________ 。
(2)为防止远洋轮船的钢铁船体在海水中发生电化学腐蚀,通常把船体与浸在海水里的Zn块相连,或与该蓄电池这样的直流电源的______ 极(填“正”或“负”)相连。
(3)以该蓄电池做电源,用下图所示装置,在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示__________________________________ 。

(4)精炼铜时,粗铜应与直流电源的________ 极(填“正”或“负”)相连,精炼过程中,电解质溶液中c(Fe2+)、c(Zn2+)会逐渐增大而影响进一步电解,甲同学设计如下除杂方案:

已知各离子沉淀时的情况如下表:
则加入H2O2的目的是__________________________________________________ ,
发生反应的离子方程式为_________ 。乙同学认为应将方案中的pH调节到8,你认为此观点______ (填“正确”或“不正确”),理由是______________________________ 。
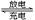 Fe(OH)2+Ni(OH)2
Fe(OH)2+Ni(OH)2(1)该蓄电池充电时,发生还原反应的物质是
| A.NiO2 | B.Fe | C.Fe(OH)2 | D.Ni(OH)2 |
(3)以该蓄电池做电源,用下图所示装置,在实验室模拟铝制品表面“钝化”处理的过程中,发现溶液逐渐变浑浊,原因是(用相关的电极反应式和离子方程式表示

(4)精炼铜时,粗铜应与直流电源的

已知各离子沉淀时的情况如下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Zn(OH)2 |
| 开始沉淀时的pH | 2.3 | 7.5 | 5.6 | 6.2 |
| 完全沉淀时的pH | 3.9 | 9.7 | 6.4 | 8.0 |
发生反应的离子方程式为
您最近一年使用:0次
7 . A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A、B、C、D、E为短周期元素,F、G为第四周期元素。已知:A是原子半径最小的元素,B、C、D是紧邻的三个族的元素,C的三价阴离子和E的二价阳离子具有相同的电子层结构,F元素的基态原子具有六个单电子,G的核电荷数比F多5。请回答下列问题(用相应的元素符号、化学式和化学术语填空)
(1)G在周期表中的位置是____ ,F元素的原子基态价层电子排布式__________ 。
(2)BD2分子的电子式为__________ ,CA3分子的空间立体构型为__________ 。
(3)A元素分别与B、D元素形成的两种微粒H、I都具有N2H4相似的结构,属于等电子数微粒,它们的化学式分别是H:__________ 、I:__________ 。
(4)向G的硫酸盐溶液中逐滴加入足量的氨水至得到的沉淀完全溶解,再向该溶液中加入一定量乙醇,析出一种深蓝色晶体。在该晶体中存在的化学键的种类有__________ 。
(5)0.3g H在足量氧气中燃烧,生成气态CO2和液态H2O,放出Q kJ热量,则表示H的燃烧热的热化学方程式为____________________ 。
(6)G的一种氧化物的晶胞结构如图所示(黑球代表G原子),该氧化物的化学式为____________________ 。

(1)G在周期表中的位置是
(2)BD2分子的电子式为
(3)A元素分别与B、D元素形成的两种微粒H、I都具有N2H4相似的结构,属于等电子数微粒,它们的化学式分别是H:
(4)向G的硫酸盐溶液中逐滴加入足量的氨水至得到的沉淀完全溶解,再向该溶液中加入一定量乙醇,析出一种深蓝色晶体。在该晶体中存在的化学键的种类有
(5)0.3g H在足量氧气中燃烧,生成气态CO2和液态H2O,放出Q kJ热量,则表示H的燃烧热的热化学方程式为
(6)G的一种氧化物的晶胞结构如图所示(黑球代表G原子),该氧化物的化学式为

您最近一年使用:0次
8 . A、B、X、Y和Z是原子序数依次递增的短周期元素,其中A与Y同主族,X与Z同主族,A与B和A与X均可形成10个电子化合物;B的最高价含氧酸可与其气态氢化物反应生成盐,常见化合物Y2X2与水反应生成X的单质,其溶液可使酚酞试液变红。用元素符号或化学式回答下列问题。
(1)X在周期表中的位置是_________ ;五种元素的原子半径从大到小的顺序是____________ ;化合物Y2X2的电子式为________________ 。
(2)X、Z的简单氢化物中沸点较高的是_______ ;原因是_____________________ 。
(3)A与X和A与Z均能形成18个电子的化合物,这两种化合物发生反应可生成Z,其反应的化学方程式为:_________________________ ;
(4)A的单质与X的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则负极电极反应式为:_____________ 。
(5)写出化合物Y2X2与水反应的离子方程式:_________________________ 。
(1)X在周期表中的位置是
(2)X、Z的简单氢化物中沸点较高的是
(3)A与X和A与Z均能形成18个电子的化合物,这两种化合物发生反应可生成Z,其反应的化学方程式为:
(4)A的单质与X的单质可制成新型的化学电源(KOH溶液作电解质溶液),两个电极均由多孔性碳制成,通入的气体由孔隙中逸出,并在电极表面放电,则负极电极反应式为:
(5)写出化合物Y2X2与水反应的离子方程式:
您最近一年使用:0次
9 . 现有A、B、C、D、E五种原子序数依次增大的前四周期元素,A元素原子序数与周期序数相同;B、C同周期左右紧邻且二者能形成多种常见有害于大气的气态化合物;D是所在周期的原子序数最大的金属元素; E处于第四周期且其基态原子价层电子排布式为md2mnsn-2。请回答下列问题(用元素符号或化学式作答):

(1)BA3分子的空间构型为___ ,B、C元素的第一电离能大小关系为___ 。
(2)与D元素同族的短周期元素M与B元素形成的某种化合物是具有特殊功能的陶瓷,其晶胞结构如图,则每个晶胞中含M原子的个数为___ ,该功能陶瓷的化学式为___ 。
(3)A、C两元素形成原子个数比1∶1的化合物在酸性条件下能将E2+氧化,写出其离子方程式___ 。
(4)写出以金属D、E为两电极、NaOH溶液为电解质溶液组成原电池的负极反应式___ 。
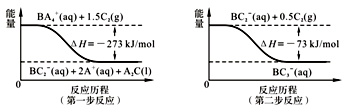
(5)已知在微生物作用的条件下,BA4+经过两步反应被氧化成BC3-。两步反应的能量变化如右图。试写出1 mol BA4+(aq)全部氧化成BC3-(aq)的热化学方程式___ 。

(1)BA3分子的空间构型为
(2)与D元素同族的短周期元素M与B元素形成的某种化合物是具有特殊功能的陶瓷,其晶胞结构如图,则每个晶胞中含M原子的个数为
(3)A、C两元素形成原子个数比1∶1的化合物在酸性条件下能将E2+氧化,写出其离子方程式
(4)写出以金属D、E为两电极、NaOH溶液为电解质溶液组成原电池的负极反应式
(5)已知在微生物作用的条件下,BA4+经过两步反应被氧化成BC3-。两步反应的能量变化如右图。试写出1 mol BA4+(aq)全部氧化成BC3-(aq)的热化学方程式

您最近一年使用:0次
10 . 现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。A元素的核外电子数和电子层数相等,B元素原子的核外p电子数比s电子数少1, C原子的第一至第四电离能:I1=738 kJ·mol-1、I2=1451 kJ·mol-1、I3=7733 kJ·mol-1、I4=10540 kJ·mol-1,D原子价电子层的p轨道半满,E元素的主族序数与周期数的差为4, F是前四周期中电负性最小的元素,G在周期表的第七列。
(1)BA3的电子式为________ ,晶体类型为_______________ 。
(2)B元素基态原子中能量最高的电子,其电子云在空间有________ 个取向,原子轨道呈________ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了__________________ 。
(4)比较B和D的电负性较大的是________ (填元素符号),BE3中心原子的杂化类型_________ ,其分子构型为___________ 。
(5)G位于周期表的________ 区,该元素的核外电子排布式为______________ 。
(6)检验F元素的方法是____________ 。
(1)BA3的电子式为
(2)B元素基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为
 ,该同学所画的电子排布图违背了
,该同学所画的电子排布图违背了(4)比较B和D的电负性较大的是
(5)G位于周期表的
(6)检验F元素的方法是
您最近一年使用:0次



