2024高三下·全国·专题练习
解题方法
1 . 探究pH对 溶液的配制和保存的影响。
溶液的配制和保存的影响。
I. 溶液的配制
溶液的配制
将 分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:
分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:
II. 溶液的保存
溶液的保存
将实验I中配制的三份溶液分别在空气中放置24小时后,记录如下。
(1)①中的浑浊主要是FeOOH,用离子方程式表示其生成过程_______ 。
(2)该实验的初步结论:保存 溶液的最佳pH是
溶液的最佳pH是_______ 。
(3)进一步探究pH对 变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后:
变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后: 接近2mol/L,电流没有明显变化;
接近2mol/L,电流没有明显变化;
ii.向右池滴加等量浓硫酸,电流明显增大。
已知:电流增大表明化学反应速率加快,在该实验条件下与物质的氧化性(还原性)增强有关。
a.结合电极反应式分析ii中电流增大的原因_______ 。
b.依据实验i和ii推断:③比②中 更易变质的原因是
更易变质的原因是_______ 。
c.按上述原理进行实验,证实①中 更易变质的主要原因是
更易变质的主要原因是 的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,
的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,_______ 。
 溶液的配制和保存的影响。
溶液的配制和保存的影响。I.
 溶液的配制
溶液的配制将
 分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:
分别溶于10mL蒸馏水或10mL稀硫酸,现象如下:| 编号 | 溶剂 | 溶液性状 | |
| ① | 蒸馏水 | 浅黄色澄清溶液 |  ;滴加1mol/LKSCN溶液无明显变化 ;滴加1mol/LKSCN溶液无明显变化 |
| ② |  | 无色澄清溶液 |  ;滴加1mol/LKSCN溶液微微变红 ;滴加1mol/LKSCN溶液微微变红 |
| ③ |  | 无色澄清溶液 | 滴加1mol/LKSCN溶液微微变红 |
 溶液的保存
溶液的保存将实验I中配制的三份溶液分别在空气中放置24小时后,记录如下。
| 编号 | 溶液性状 | |
| ① | 橙色浑浊 | 用 酸化后,浊液变澄清,再滴加1mol/LKSCN溶液后变深红 酸化后,浊液变澄清,再滴加1mol/LKSCN溶液后变深红 |
| ② | 无色溶液 | 滴加1mol/L的KSCN溶液后显浅红色 |
| ③ | 无色溶液 | 滴加1mol/L的KSCN溶液后显红色,颜色比②略深 |
(2)该实验的初步结论:保存
 溶液的最佳pH是
溶液的最佳pH是(3)进一步探究pH对
 变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后:
变质影响的原因。用下图所示装置完成实验(滴加试剂时溶液体积和导电性变化可忽略)。向右池持续稳定通入氧气,待电流计示数稳定后: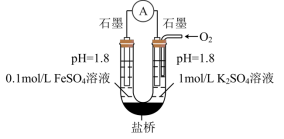
 接近2mol/L,电流没有明显变化;
接近2mol/L,电流没有明显变化;ii.向右池滴加等量浓硫酸,电流明显增大。
已知:电流增大表明化学反应速率加快,在该实验条件下与物质的氧化性(还原性)增强有关。
a.结合电极反应式分析ii中电流增大的原因
b.依据实验i和ii推断:③比②中
 更易变质的原因是
更易变质的原因是c.按上述原理进行实验,证实①中
 更易变质的主要原因是
更易变质的主要原因是 的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,
的还原性增强,氧化速率加快,而与氧气性质变化关系不大。实验方案及预期现象是:向右池持续稳定通入氧气,待电流计示数稳定后,
您最近一年使用:0次
2024高三下·全国·专题练习
2 . 硫及其化合物在日常生活、工业生产中都非常普遍。
(1)在水中,硫酸是一种强酸,但实际上只有第一步电离是完全的,第二步电离并不完全,电离方程式可表示为:H2SO4=H++ ,
,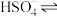 H++
H++ 。
。
①25℃时,Na2SO4溶液的pH___________ (填“>”“<”或“=”)7。
②0.100 mol∙L−1的稀硫酸中,c(H+)=0.109 mol∙L−1,求硫酸第二步电离的电离常数___________ (写出计算过程,结果保留三位有效数字)。
(2)液态水中,水存在自偶电离:H2O+H2O H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。
H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。
①液态的醋酸(用HAc表示)中,同样存在HAc的自偶电离,其方程式可表示为___________ 。
②用醋酸作溶剂时,硫酸是一种二元弱酸。将少量H2SO4溶于冰醋酸中,第一步电离的完整写法是___________ 。若保持温度不变,关于该所得溶液,下列说法正确的是___________ 。
A.加入少量冰醋酸,c( )与c(
)与c( )均减小
)均减小
B.加入少量H2SO4,H2SO4的电离程度增大
C.加入少量NaAc固体。c( )与c(
)与c( )的比值减小
)的比值减小
D.加入少量Na2SO4固体,c(Ac-)减小
(1)在水中,硫酸是一种强酸,但实际上只有第一步电离是完全的,第二步电离并不完全,电离方程式可表示为:H2SO4=H++
 ,
,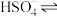 H++
H++ 。
。①25℃时,Na2SO4溶液的pH
②0.100 mol∙L−1的稀硫酸中,c(H+)=0.109 mol∙L−1,求硫酸第二步电离的电离常数
(2)液态水中,水存在自偶电离:H2O+H2O
 H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。
H3O++OH-。平常书写的H+,实际上是纯水或水溶液中H3O+的缩写。如HCl在水中电离,完整写法是HCl+H2O=H3O++Cl-。①液态的醋酸(用HAc表示)中,同样存在HAc的自偶电离,其方程式可表示为
②用醋酸作溶剂时,硫酸是一种二元弱酸。将少量H2SO4溶于冰醋酸中,第一步电离的完整写法是
A.加入少量冰醋酸,c(
 )与c(
)与c( )均减小
)均减小B.加入少量H2SO4,H2SO4的电离程度增大
C.加入少量NaAc固体。c(
 )与c(
)与c( )的比值减小
)的比值减小D.加入少量Na2SO4固体,c(Ac-)减小
您最近一年使用:0次
2024高三下·全国·专题练习
3 . 尽管NOx、SO2、CO都是有毒气体,但是它们在生产、医学领域中都有重要应用。合理利用或转化CO、NOx等污染性气体是人们共同关注的课题。回答下列问题:
(1)已知:①CO(g)+ H2O(g)=CO2(g)+H2(g) H=-41.0kJ·mol-1
H=-41.0kJ·mol-1
②N2(g)+ O2(g)=2NO(g) H=+ 180.0kJ· mol-1
H=+ 180.0kJ· mol-1
③H2(g)+ O2 (g)=H2O(g)
O2 (g)=H2O(g)  H=- 241.8kJ·mol-l
H=- 241.8kJ·mol-l
CO和NO按一定比例混合,在适当催化剂作用下可生成无毒气体实现安全排放,该反应的热化学方程式为___________ 。
(2)利用NaClO2/H2O2酸性复合吸收剂可同时对NO、SO2进行氧化得到硝酸和硫酸而除去。在温度一定时,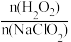 、 溶液pH对脱硫脱硝的影响如图所示:
、 溶液pH对脱硫脱硝的影响如图所示:___________ 。
②根据图示SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释NO去除率减小的可能原因是___________ 。
(1)已知:①CO(g)+ H2O(g)=CO2(g)+H2(g)
 H=-41.0kJ·mol-1
H=-41.0kJ·mol-1②N2(g)+ O2(g)=2NO(g)
 H=+ 180.0kJ· mol-1
H=+ 180.0kJ· mol-1③H2(g)+
 O2 (g)=H2O(g)
O2 (g)=H2O(g)  H=- 241.8kJ·mol-l
H=- 241.8kJ·mol-lCO和NO按一定比例混合,在适当催化剂作用下可生成无毒气体实现安全排放,该反应的热化学方程式为
(2)利用NaClO2/H2O2酸性复合吸收剂可同时对NO、SO2进行氧化得到硝酸和硫酸而除去。在温度一定时,
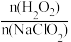 、 溶液pH对脱硫脱硝的影响如图所示:
、 溶液pH对脱硫脱硝的影响如图所示:
②根据图示SO2的去除率随pH的增大而增大,而NO的去除率在pH>5.5时反而减小,请解释NO去除率减小的可能原因是
您最近一年使用:0次
2024高三下·全国·专题练习
4 . 近年来,我国大力加强温室气体 氢化合成甲醇技术的工业化量产研究,实现可持续发展。在合适的催化剂作用下,二氧化碳可催化加氢制甲醇。
氢化合成甲醇技术的工业化量产研究,实现可持续发展。在合适的催化剂作用下,二氧化碳可催化加氢制甲醇。
(1)已知:①


②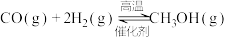


则反应③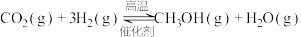

___________  。
。
(2)在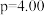 MPa、原料气
MPa、原料气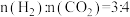 、合适催化剂的条件下发生反应,温度对
、合适催化剂的条件下发生反应,温度对 转化率、
转化率、 产率、
产率、 选择性的影响如图所示。已知:
选择性的影响如图所示。已知: 选择性
选择性 。
。 转化率随温度升高而增大的原因可能是
转化率随温度升高而增大的原因可能是___________ ;
b. 选择性随温度升高而减小的原因可能是
选择性随温度升高而减小的原因可能是___________ ;
c.写出240℃时反应①的平衡常数的表达式:___________ 。
(3)除调控合适的温度外,使 选择性增大的方法有
选择性增大的方法有___________ 。
 氢化合成甲醇技术的工业化量产研究,实现可持续发展。在合适的催化剂作用下,二氧化碳可催化加氢制甲醇。
氢化合成甲醇技术的工业化量产研究,实现可持续发展。在合适的催化剂作用下,二氧化碳可催化加氢制甲醇。(1)已知:①



②
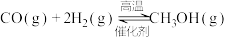


则反应③
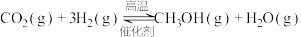

 。
。(2)在
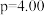 MPa、原料气
MPa、原料气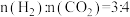 、合适催化剂的条件下发生反应,温度对
、合适催化剂的条件下发生反应,温度对 转化率、
转化率、 产率、
产率、 选择性的影响如图所示。已知:
选择性的影响如图所示。已知: 选择性
选择性 。
。
 转化率随温度升高而增大的原因可能是
转化率随温度升高而增大的原因可能是b.
 选择性随温度升高而减小的原因可能是
选择性随温度升高而减小的原因可能是c.写出240℃时反应①的平衡常数的表达式:
(3)除调控合适的温度外,使
 选择性增大的方法有
选择性增大的方法有
您最近一年使用:0次
2024高三下·全国·专题练习
5 . 甲醇是重要的化工原料,可以使用多种方法制备甲醇。
(1)利用CO2和H2合成甲醇,在催化剂Cu/ZnO作用下可发生如下两个平行反应。
反应I:CO2(g)+3H2(g)→CH3OH(g)+H2O(g)
反应II:CO2(g)+H2(g)→CO(g)+H2O(g);
温度对CO2转化率及甲醇和CO产率的影响如图乙所示。___________ 。
②由图可知,温度升高CH3OH产率先升高后降低,降低的可能原因是___________ 。
③下列措施有利于提高CO2转化为CH3OH的平衡转化率的有___________ 。
A.增大体系压强
B.提高CO2和H2的投料比
C.体积和投料比不变,提高反应物浓度
(2)利用CH4与O2在催化剂的作用下合成甲醇。主反应:CH4(g)+
 O2(g)→CH3OH(g),副反应:CH4(g)+2O2(g)→CO2(g)+2H2O(g)。在温度为T℃、压强为PKPa条件下,向容器中充入2molCH4、1molO2和6molH2O,充分反应达平衡时CH4的转化率为50%,产物的选择性(如甲醇的选择性=
O2(g)→CH3OH(g),副反应:CH4(g)+2O2(g)→CO2(g)+2H2O(g)。在温度为T℃、压强为PKPa条件下,向容器中充入2molCH4、1molO2和6molH2O,充分反应达平衡时CH4的转化率为50%,产物的选择性(如甲醇的选择性= )如图丙所示:
)如图丙所示:___________
②主反应的相对压力平衡常数 =
=___________ 。(用含P和p0的计算式表示。 表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压除以p0)
表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压除以p0)
(1)利用CO2和H2合成甲醇,在催化剂Cu/ZnO作用下可发生如下两个平行反应。
反应I:CO2(g)+3H2(g)→CH3OH(g)+H2O(g)
反应II:CO2(g)+H2(g)→CO(g)+H2O(g);
温度对CO2转化率及甲醇和CO产率的影响如图乙所示。
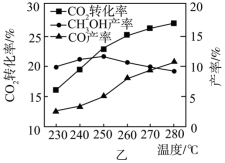
②由图可知,温度升高CH3OH产率先升高后降低,降低的可能原因是
③下列措施有利于提高CO2转化为CH3OH的平衡转化率的有
A.增大体系压强
B.提高CO2和H2的投料比
C.体积和投料比不变,提高反应物浓度
(2)利用CH4与O2在催化剂的作用下合成甲醇。主反应:CH4(g)+

 O2(g)→CH3OH(g),副反应:CH4(g)+2O2(g)→CO2(g)+2H2O(g)。在温度为T℃、压强为PKPa条件下,向容器中充入2molCH4、1molO2和6molH2O,充分反应达平衡时CH4的转化率为50%,产物的选择性(如甲醇的选择性=
O2(g)→CH3OH(g),副反应:CH4(g)+2O2(g)→CO2(g)+2H2O(g)。在温度为T℃、压强为PKPa条件下,向容器中充入2molCH4、1molO2和6molH2O,充分反应达平衡时CH4的转化率为50%,产物的选择性(如甲醇的选择性= )如图丙所示:
)如图丙所示:
②主反应的相对压力平衡常数
 =
= 表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压除以p0)
表达式写法:在浓度平衡常数表达式中,用相对分压代替浓度。气体的相对分压等于其分压除以p0)
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
6 . I、 的资源化可以推动经济高质量发展和生态环境质量的持续改善,回答下列问题:
的资源化可以推动经济高质量发展和生态环境质量的持续改善,回答下列问题:
(1) 和
和 都是主要的温室气体。发生催化重整反应
都是主要的温室气体。发生催化重整反应

已知 时,相关物质的燃烧热数据如下表:
时,相关物质的燃烧热数据如下表:
反应的
___________ 
(2)在恒温恒容装置中通入等体积 和
和 ,发生上述反应,起始压强为p,
,发生上述反应,起始压强为p, 的平衡转化率为
的平衡转化率为 。达平衡时,容器内总压为
。达平衡时,容器内总压为___________ 。该反应的平衡常数
___________ (用平衡分压代替平衡浓度计算,分压 总压×物质的量分数,用
总压×物质的量分数,用 、
、 表达,并化为最简式)。
表达,并化为最简式)。
 的资源化可以推动经济高质量发展和生态环境质量的持续改善,回答下列问题:
的资源化可以推动经济高质量发展和生态环境质量的持续改善,回答下列问题:(1)
 和
和 都是主要的温室气体。发生催化重整反应
都是主要的温室气体。发生催化重整反应

已知
 时,相关物质的燃烧热数据如下表:
时,相关物质的燃烧热数据如下表:| 物质 |  |  |  |
燃烧热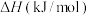 |  |  |  |


(2)在恒温恒容装置中通入等体积
 和
和 ,发生上述反应,起始压强为p,
,发生上述反应,起始压强为p, 的平衡转化率为
的平衡转化率为 。达平衡时,容器内总压为
。达平衡时,容器内总压为
 总压×物质的量分数,用
总压×物质的量分数,用 、
、 表达,并化为最简式)。
表达,并化为最简式)。
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
7 . 氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列问题:
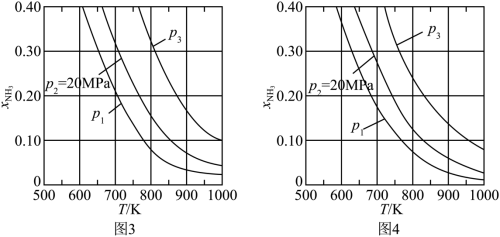
(1)在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果如下图所示。其中一种进料组成为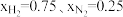 ,另一种为
,另一种为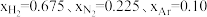 。(物质i的摩尔分数:
。(物质i的摩尔分数: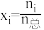 )
)___________ ,判断的依据是___________ 。
②进料组成中含有惰性气体 的图是
的图是___________ 。
③图3中,当 、
、 时,氮气的转化率
时,氮气的转化率
___________ 。该温度时,反应 的平衡常数
的平衡常数
___________  (化为最简式)。
(化为最简式)。
(1)在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果如下图所示。其中一种进料组成为
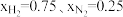 ,另一种为
,另一种为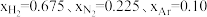 。(物质i的摩尔分数:
。(物质i的摩尔分数: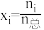 )
)
②进料组成中含有惰性气体
 的图是
的图是③图3中,当
 、
、 时,氮气的转化率
时,氮气的转化率
 的平衡常数
的平衡常数
 (化为最简式)。
(化为最简式)。
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
8 . 合成氨厂和硝酸厂的烟气中含有大量的氮氧化物,脱硝是指将烟气中的氮氧化物转化为无毒无害物质的化学过程。回答下列问题:
(1)在一定条件下,向某反应容器中投入5molN2、15molH2在不同温度(T)下发生反应: ,平衡体系中
,平衡体系中 的质量分数随平衡时气体总压强变化的曲线如图所示。
的质量分数随平衡时气体总压强变化的曲线如图所示。___________ 。
②M点时, 的转化率为
的转化率为___________ 。
③下列情况能说明反应达到平衡状态的是___________ (填标号)。
A.2v(NH3)=3v(H2)
B.混合气体的相对分子质量不再变化
C.N2体积分数不再变化
D.恒容容器中混合气体的密度保持不变
(1)在一定条件下,向某反应容器中投入5molN2、15molH2在不同温度(T)下发生反应:
 ,平衡体系中
,平衡体系中 的质量分数随平衡时气体总压强变化的曲线如图所示。
的质量分数随平衡时气体总压强变化的曲线如图所示。
②M点时,
 的转化率为
的转化率为③下列情况能说明反应达到平衡状态的是
A.2v(NH3)=3v(H2)
B.混合气体的相对分子质量不再变化
C.N2体积分数不再变化
D.恒容容器中混合气体的密度保持不变
您最近一年使用:0次
9 . 实验室用氧化锌作催化剂、以乙二醇和碳酸氢钠为复合解聚剂常压下快速、彻底解聚聚对苯二甲酸乙二醇酯(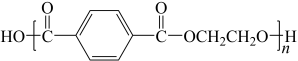 ),同时回收对苯二甲酸和乙二醇。其实验流程与有关数据如图1所示,实验部分装置如图2所示。
),同时回收对苯二甲酸和乙二醇。其实验流程与有关数据如图1所示,实验部分装置如图2所示。
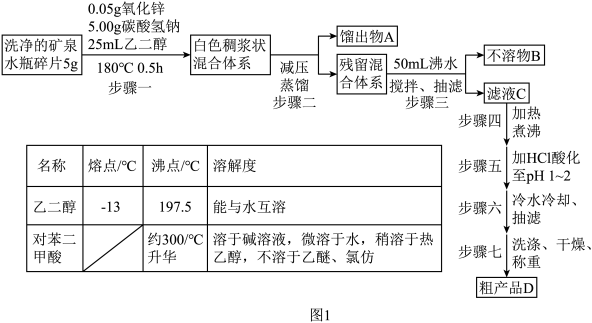
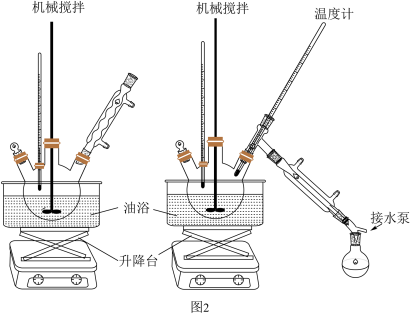
(1)步骤一反应的化学方程式为
(2)仪器X的名称为
(3)将矿泉水瓶剪成碎片的目的是
(4)步骤六中冰水冷却的目的是
A.先拔下抽气泵与吸滤瓶问的橡皮管,再关闭抽气泵
B.先关闭抽气泵,再拔下抽气泵与吸滤瓶问的橡皮管
(5)粗产品可用N,N-二甲基甲酰胺
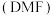 -水混合溶剂重结晶,称取
-水混合溶剂重结晶,称取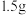 粗产品,先用
粗产品,先用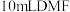 使粗产品在回流下溶解
使粗产品在回流下溶解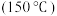 ,若没有溶完,则如何操作?
,若没有溶完,则如何操作?
您最近一年使用:0次
10 . 水合肼 常用于生产火箭燃料,其沸点是
常用于生产火箭燃料,其沸点是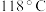 ,受热易分解。尿素法合成水合肼的基本流程如图所示。
,受热易分解。尿素法合成水合肼的基本流程如图所示。

回答下列问题:
(1) 是二元弱碱,在水中的电离方式与氨相似,写出
是二元弱碱,在水中的电离方式与氨相似,写出 第二步电离的方程式:
第二步电离的方程式:___________ 。
(2)已知次氯酸钠与盐酸混合能够生成 ,说明氧化性
,说明氧化性
___________  (填“>”或“<”)。实验发现,
(填“>”或“<”)。实验发现, 与烧碱溶液反应可以生成
与烧碱溶液反应可以生成 ,说明
,说明 与
与 的氧化性强弱关系与
的氧化性强弱关系与___________ 有关。
(3) 强碱性溶液与尿素
强碱性溶液与尿素 水溶液加热制备水合肼的离子方程式为
水溶液加热制备水合肼的离子方程式为___________ 。
(4)常通过减压蒸馏从反应后的混合溶液中获得水合肼,采用该操作的原因是___________ 。
(5)水合肼与硫酸反应生成的盐是农业上重要的杀虫剂、灭菌剂,写出水合肼与硫酸反应生成的碱式盐的化学式:___________ 。
(6)电化学方法制备 的装置如图所示。其中双极膜是阴、阳复合膜,层间的
的装置如图所示。其中双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。

①双极膜中产生的___________ (填“ ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。
②若电路中转移2mol电子,理论上负极区溶液增重___________ g。
 常用于生产火箭燃料,其沸点是
常用于生产火箭燃料,其沸点是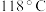 ,受热易分解。尿素法合成水合肼的基本流程如图所示。
,受热易分解。尿素法合成水合肼的基本流程如图所示。
回答下列问题:
(1)
 是二元弱碱,在水中的电离方式与氨相似,写出
是二元弱碱,在水中的电离方式与氨相似,写出 第二步电离的方程式:
第二步电离的方程式:(2)已知次氯酸钠与盐酸混合能够生成
 ,说明氧化性
,说明氧化性
 (填“>”或“<”)。实验发现,
(填“>”或“<”)。实验发现, 与烧碱溶液反应可以生成
与烧碱溶液反应可以生成 ,说明
,说明 与
与 的氧化性强弱关系与
的氧化性强弱关系与(3)
 强碱性溶液与尿素
强碱性溶液与尿素 水溶液加热制备水合肼的离子方程式为
水溶液加热制备水合肼的离子方程式为(4)常通过减压蒸馏从反应后的混合溶液中获得水合肼,采用该操作的原因是
(5)水合肼与硫酸反应生成的盐是农业上重要的杀虫剂、灭菌剂,写出水合肼与硫酸反应生成的碱式盐的化学式:
(6)电化学方法制备
 的装置如图所示。其中双极膜是阴、阳复合膜,层间的
的装置如图所示。其中双极膜是阴、阳复合膜,层间的 解离成
解离成 和
和 并可分别通过阴、阳膜定向移动。
并可分别通过阴、阳膜定向移动。
①双极膜中产生的
 ”或“
”或“ ”)移向多孔铂电极。
”)移向多孔铂电极。②若电路中转移2mol电子,理论上负极区溶液增重
您最近一年使用:0次



