1 . 工业上利用锌焙砂(主要成分为  ,含有少量
,含有少量 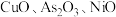 等)生产高纯
等)生产高纯  的流程示意图如下。
的流程示意图如下。
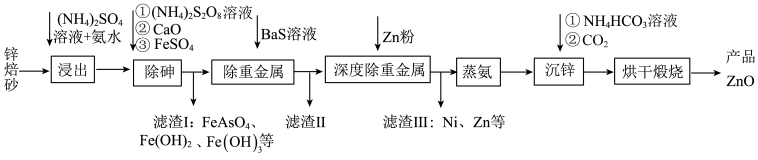
(1)用足量 溶液和氨水 “浸出” 锌焙砂。
溶液和氨水 “浸出” 锌焙砂。
①“浸出”前,锌焙砂预先粉碎的目的是___________ 。
②通过“浸出”步骤,锌焙砂中的 转化为
转化为  ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(2)“浸出”时 转化为
转化为  。“除砷”步骤①中用
。“除砷”步骤①中用  作氧化剂,步骤①反应中的氧化剂与还原剂物质 的量之比为
作氧化剂,步骤①反应中的氧化剂与还原剂物质 的量之比为___________
(3)“除重金属”时,加入 溶液。滤渣II中含有的主要物质是
溶液。滤渣II中含有的主要物质是___________ 和  。
。
(4)“蒸氨”时会出现白色固体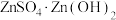 ,运用平衡移动原理解释原因:
,运用平衡移动原理解释原因:___________ 。
(5)“沉锌”步骤①中加入足量 溶液将白色固体转化为
溶液将白色固体转化为  的离子方程式为
的离子方程式为___________ 。
(6)煅烧”步骤中,在一定温度下,煅烧 一定时间后固体失重质量分数为
一定时间后固体失重质量分数为  ,则
,则  的分解率 为
的分解率 为___________  (保留到小数点后一位)。已知: 固体失重质量分数
(保留到小数点后一位)。已知: 固体失重质量分数  。
。
(7)该流程中可循环利用的物质有___________ (答出任意 2 种即可)
 ,含有少量
,含有少量 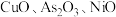 等)生产高纯
等)生产高纯  的流程示意图如下。
的流程示意图如下。
(1)用足量
 溶液和氨水 “浸出” 锌焙砂。
溶液和氨水 “浸出” 锌焙砂。①“浸出”前,锌焙砂预先粉碎的目的是
②通过“浸出”步骤,锌焙砂中的
 转化为
转化为  ,该反应的离子方程式为
,该反应的离子方程式为(2)“浸出”时
 转化为
转化为  。“除砷”步骤①中用
。“除砷”步骤①中用  作氧化剂,步骤①反应中的氧化剂与还原剂物质 的量之比为
作氧化剂,步骤①反应中的氧化剂与还原剂物质 的量之比为(3)“除重金属”时,加入
 溶液。滤渣II中含有的主要物质是
溶液。滤渣II中含有的主要物质是 。
。(4)“蒸氨”时会出现白色固体
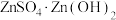 ,运用平衡移动原理解释原因:
,运用平衡移动原理解释原因:(5)“沉锌”步骤①中加入足量
 溶液将白色固体转化为
溶液将白色固体转化为  的离子方程式为
的离子方程式为(6)煅烧”步骤中,在一定温度下,煅烧
 一定时间后固体失重质量分数为
一定时间后固体失重质量分数为  ,则
,则  的分解率 为
的分解率 为 (保留到小数点后一位)。已知: 固体失重质量分数
(保留到小数点后一位)。已知: 固体失重质量分数  。
。(7)该流程中可循环利用的物质有
您最近一年使用:0次
名校
解题方法
2 . 氧钒(Ⅳ)碱式碳酸铵晶体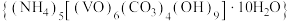 是制备多种含钒产品的前驱体。已知:氧钒(Ⅳ)碱式碳酸铵晶体呈紫红色,难溶于水和乙醇。实验室制备该晶体的流程如图所示。
是制备多种含钒产品的前驱体。已知:氧钒(Ⅳ)碱式碳酸铵晶体呈紫红色,难溶于水和乙醇。实验室制备该晶体的流程如图所示。
 溶液
溶液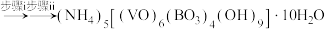
步骤i:用 排除装置中的氧气,将
排除装置中的氧气,将 溶液缓慢加入足量
溶液缓慢加入足量 溶液中,有气泡产生,析出紫红色晶体。
溶液中,有气泡产生,析出紫红色晶体。
步骤ii:待反应结束后,在 保护气的环境中,将混合液静置一段时间,抽滤,所得晶体用饱和
保护气的环境中,将混合液静置一段时间,抽滤,所得晶体用饱和 溶液洗涤3次,再用无水乙醇洗涤2次,得到粗产品。
溶液洗涤3次,再用无水乙醇洗涤2次,得到粗产品。
(1)仪器E的名称为________ ;上述装置连接的顺序为________ 。
(2)装置B中发生反应的化学方程式是________ 。
(3)①预测 保护气排除氧气的目的是
保护气排除氧气的目的是________ ;判断装置中的 基本上排尽的方法是
基本上排尽的方法是________ (填实验现象)。
②晶体用无水乙醇代替水洗涤的目的是________ 。
(4)称bg粗品,用 溶液氧化,再除去多余的
溶液氧化,再除去多余的 (方法略),滴入2滴
(方法略),滴入2滴 溶液,最后用
溶液,最后用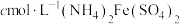 标准溶液滴定,滴定终点消耗标准溶液的体积如下图(已知钒的相对原子质量为M,滴定反应为
标准溶液滴定,滴定终点消耗标准溶液的体积如下图(已知钒的相对原子质量为M,滴定反应为 )。
)。
I.配制 标准溶液:称量→溶解→冷却→操作①→洗涤→注入→混匀→定容→操作②→装瓶贴标签,下列图示中,操作①②分别为
标准溶液:称量→溶解→冷却→操作①→洗涤→注入→混匀→定容→操作②→装瓶贴标签,下列图示中,操作①②分别为________ (填序号)。 溶液的体积为
溶液的体积为________ ;产品中钒的质量分数为________ %(用含b、c、M的代数式表示)。
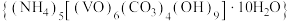 是制备多种含钒产品的前驱体。已知:氧钒(Ⅳ)碱式碳酸铵晶体呈紫红色,难溶于水和乙醇。实验室制备该晶体的流程如图所示。
是制备多种含钒产品的前驱体。已知:氧钒(Ⅳ)碱式碳酸铵晶体呈紫红色,难溶于水和乙醇。实验室制备该晶体的流程如图所示。 溶液
溶液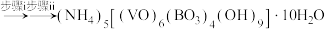
步骤i:用
 排除装置中的氧气,将
排除装置中的氧气,将 溶液缓慢加入足量
溶液缓慢加入足量 溶液中,有气泡产生,析出紫红色晶体。
溶液中,有气泡产生,析出紫红色晶体。步骤ii:待反应结束后,在
 保护气的环境中,将混合液静置一段时间,抽滤,所得晶体用饱和
保护气的环境中,将混合液静置一段时间,抽滤,所得晶体用饱和 溶液洗涤3次,再用无水乙醇洗涤2次,得到粗产品。
溶液洗涤3次,再用无水乙醇洗涤2次,得到粗产品。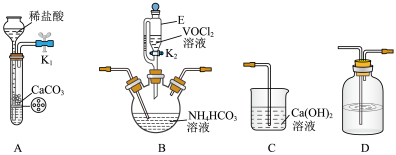
(1)仪器E的名称为
(2)装置B中发生反应的化学方程式是
(3)①预测
 保护气排除氧气的目的是
保护气排除氧气的目的是 基本上排尽的方法是
基本上排尽的方法是②晶体用无水乙醇代替水洗涤的目的是
(4)称bg粗品,用
 溶液氧化,再除去多余的
溶液氧化,再除去多余的 (方法略),滴入2滴
(方法略),滴入2滴 溶液,最后用
溶液,最后用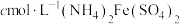 标准溶液滴定,滴定终点消耗标准溶液的体积如下图(已知钒的相对原子质量为M,滴定反应为
标准溶液滴定,滴定终点消耗标准溶液的体积如下图(已知钒的相对原子质量为M,滴定反应为 )。
)。I.配制
 标准溶液:称量→溶解→冷却→操作①→洗涤→注入→混匀→定容→操作②→装瓶贴标签,下列图示中,操作①②分别为
标准溶液:称量→溶解→冷却→操作①→洗涤→注入→混匀→定容→操作②→装瓶贴标签,下列图示中,操作①②分别为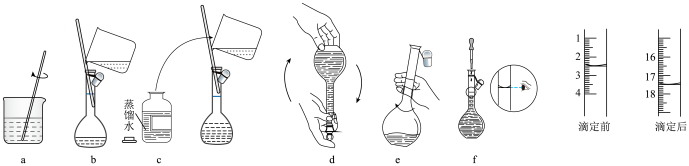
 溶液的体积为
溶液的体积为
您最近一年使用:0次
2024-06-04更新
|
177次组卷
|
2卷引用:2024届四川省成都石室中学高三下学期5月高考适应性考试(一)理科综合试卷-高中化学
名校
3 . 配合物在许多尖端领域如激光材料、超导材料、抗癌药物的研究、催化剂的研制、自组装超分子等方面有广泛的应用。回答下列问题:
(1)《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的 、
、 生成的红色配合物X是最早的媒染染料。
生成的红色配合物X是最早的媒染染料。 的核外电子的运动状态有
的核外电子的运动状态有________ 种,配合物X中 的配体有
的配体有________ ,茜素的水溶性较好的主要原因是________ 。
(2)Ni与CO形成的配合物 为无色液体,易溶于
为无色液体,易溶于 、
、 等有机溶剂。
等有机溶剂。 为
为________ (填“极性”或“非极性”)分子,分子中 键与
键与 键的个数之比为
键的个数之比为________ 。
(3)向 溶液中滴加铁氰化钾溶液后,经提纯、结晶可得到一种蓝色晶体
溶液中滴加铁氰化钾溶液后,经提纯、结晶可得到一种蓝色晶体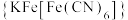 。实验表明,
。实验表明, 、
、 、
、 通过配位键构成了晶体的骨架,其局部结构如图1,记为Ⅰ型立方结构。将Ⅰ型立方结构平移、旋转、并置,可得到晶体的复晶胞(如图2,记为Ⅱ型立方结构,下层左后的小立方体g未标出)。
通过配位键构成了晶体的骨架,其局部结构如图1,记为Ⅰ型立方结构。将Ⅰ型立方结构平移、旋转、并置,可得到晶体的复晶胞(如图2,记为Ⅱ型立方结构,下层左后的小立方体g未标出)。________ 实验,可确定该晶体结构。
② 的配位数为
的配位数为________ 。
③若 位于Ⅱ型立方结构的棱心和体心,则
位于Ⅱ型立方结构的棱心和体心,则 位于Ⅱ型立方结构的
位于Ⅱ型立方结构的________ ;一个Ⅱ型立方结构中含________ 个 ;若该蓝色晶体的密度为
;若该蓝色晶体的密度为 ,Ⅱ型立方结构的边长为anm,则阿伏加德罗常数的值可表示为
,Ⅱ型立方结构的边长为anm,则阿伏加德罗常数的值可表示为________ 。
(1)《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的
 、
、 生成的红色配合物X是最早的媒染染料。
生成的红色配合物X是最早的媒染染料。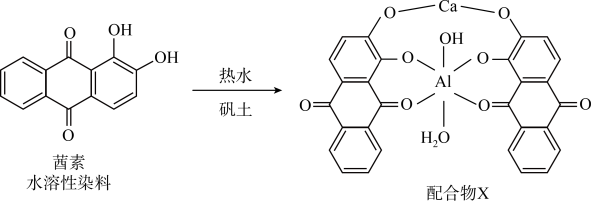
 的核外电子的运动状态有
的核外电子的运动状态有 的配体有
的配体有(2)Ni与CO形成的配合物
 为无色液体,易溶于
为无色液体,易溶于 、
、 等有机溶剂。
等有机溶剂。 为
为 键与
键与 键的个数之比为
键的个数之比为(3)向
 溶液中滴加铁氰化钾溶液后,经提纯、结晶可得到一种蓝色晶体
溶液中滴加铁氰化钾溶液后,经提纯、结晶可得到一种蓝色晶体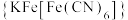 。实验表明,
。实验表明, 、
、 、
、 通过配位键构成了晶体的骨架,其局部结构如图1,记为Ⅰ型立方结构。将Ⅰ型立方结构平移、旋转、并置,可得到晶体的复晶胞(如图2,记为Ⅱ型立方结构,下层左后的小立方体g未标出)。
通过配位键构成了晶体的骨架,其局部结构如图1,记为Ⅰ型立方结构。将Ⅰ型立方结构平移、旋转、并置,可得到晶体的复晶胞(如图2,记为Ⅱ型立方结构,下层左后的小立方体g未标出)。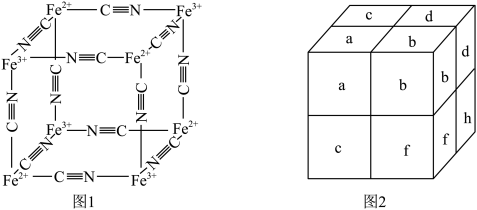
②
 的配位数为
的配位数为③若
 位于Ⅱ型立方结构的棱心和体心,则
位于Ⅱ型立方结构的棱心和体心,则 位于Ⅱ型立方结构的
位于Ⅱ型立方结构的 ;若该蓝色晶体的密度为
;若该蓝色晶体的密度为 ,Ⅱ型立方结构的边长为anm,则阿伏加德罗常数的值可表示为
,Ⅱ型立方结构的边长为anm,则阿伏加德罗常数的值可表示为
您最近一年使用:0次
名校
4 . 铁元素在地壳中含量丰富,应用广泛。回答下列问题:
(1)原子核外运动的电子有两种相反的自旋状态,若有一种自旋状态用 ,则与之相反的用
,则与之相反的用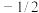 ,称为电子的自旋磁量子数,基态Fe原子核外电子自旋磁量子数的代数和为
,称为电子的自旋磁量子数,基态Fe原子核外电子自旋磁量子数的代数和为______ 。
(2) 水溶液中
水溶液中 可水解生成双核阳离子
可水解生成双核阳离子 ,结构如图所示。该双核阳离子中
,结构如图所示。该双核阳离子中 键角
键角______ (填“大于”、“小于”或“等于”) 中的
中的 键角;若对
键角;若对 水溶液进行加热,该双核阳离子内部首先断开的是
水溶液进行加热,该双核阳离子内部首先断开的是____________ 键(填“a”或“b”)。 】是一种重要的配合物,用作有机铁肥,简称铁氮肥。该配合物中所含非金属元素的第一电离能从大到小的顺序为
】是一种重要的配合物,用作有机铁肥,简称铁氮肥。该配合物中所含非金属元素的第一电离能从大到小的顺序为______ , 的空间构型是
的空间构型是______ ;已知尿素分子所有原子在同一平面且含有与苯类似的“大 键”,其“大
键”,其“大 键”可表示为
键”可表示为______ (用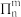 表示,其中
表示,其中 表示参与形成大
表示参与形成大 键的原子数,
键的原子数, 表示形成大
表示形成大 键的电子数);尿素晶体的熔点为132.7℃,比相同摩尔质量的乙酸熔点(16.7℃)高116℃,主要原因是
键的电子数);尿素晶体的熔点为132.7℃,比相同摩尔质量的乙酸熔点(16.7℃)高116℃,主要原因是______ 。
(4) 有良好的磁性和光学性能,广泛应用于电子工业和材料工业。
有良好的磁性和光学性能,广泛应用于电子工业和材料工业。 晶体中,
晶体中, 围成正四面体空隙(如:1、3、6、7围成)和正八面体空隙(如:3、6、7、8、9、12围成),
围成正四面体空隙(如:1、3、6、7围成)和正八面体空隙(如:3、6、7、8、9、12围成), 中有一半的
中有一半的 填充在正四面体空隙中,
填充在正四面体空隙中, 和另一半
和另一半 填充在正八面体空隙中(如图所示)。则正四面体空隙填充率与正八面体空隙填充率之比为
填充在正八面体空隙中(如图所示)。则正四面体空隙填充率与正八面体空隙填充率之比为______ , 晶胞中有8个图示结构单元,该晶胞参数为apm,则晶体密度为
晶胞中有8个图示结构单元,该晶胞参数为apm,则晶体密度为______  (写出含
(写出含 和
和 的计算表达式)。
的计算表达式)。
(1)原子核外运动的电子有两种相反的自旋状态,若有一种自旋状态用
 ,则与之相反的用
,则与之相反的用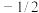 ,称为电子的自旋磁量子数,基态Fe原子核外电子自旋磁量子数的代数和为
,称为电子的自旋磁量子数,基态Fe原子核外电子自旋磁量子数的代数和为(2)
 水溶液中
水溶液中 可水解生成双核阳离子
可水解生成双核阳离子 ,结构如图所示。该双核阳离子中
,结构如图所示。该双核阳离子中 键角
键角 中的
中的 键角;若对
键角;若对 水溶液进行加热,该双核阳离子内部首先断开的是
水溶液进行加热,该双核阳离子内部首先断开的是
 】是一种重要的配合物,用作有机铁肥,简称铁氮肥。该配合物中所含非金属元素的第一电离能从大到小的顺序为
】是一种重要的配合物,用作有机铁肥,简称铁氮肥。该配合物中所含非金属元素的第一电离能从大到小的顺序为 的空间构型是
的空间构型是 键”,其“大
键”,其“大 键”可表示为
键”可表示为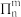 表示,其中
表示,其中 表示参与形成大
表示参与形成大 键的原子数,
键的原子数, 表示形成大
表示形成大 键的电子数);尿素晶体的熔点为132.7℃,比相同摩尔质量的乙酸熔点(16.7℃)高116℃,主要原因是
键的电子数);尿素晶体的熔点为132.7℃,比相同摩尔质量的乙酸熔点(16.7℃)高116℃,主要原因是(4)
 有良好的磁性和光学性能,广泛应用于电子工业和材料工业。
有良好的磁性和光学性能,广泛应用于电子工业和材料工业。 晶体中,
晶体中, 围成正四面体空隙(如:1、3、6、7围成)和正八面体空隙(如:3、6、7、8、9、12围成),
围成正四面体空隙(如:1、3、6、7围成)和正八面体空隙(如:3、6、7、8、9、12围成), 中有一半的
中有一半的 填充在正四面体空隙中,
填充在正四面体空隙中, 和另一半
和另一半 填充在正八面体空隙中(如图所示)。则正四面体空隙填充率与正八面体空隙填充率之比为
填充在正八面体空隙中(如图所示)。则正四面体空隙填充率与正八面体空隙填充率之比为 晶胞中有8个图示结构单元,该晶胞参数为apm,则晶体密度为
晶胞中有8个图示结构单元,该晶胞参数为apm,则晶体密度为 (写出含
(写出含 和
和 的计算表达式)。
的计算表达式)。
您最近一年使用:0次
5 . Si、S、Se在自然界中形成多种多样的物质结构。回答下列问题:
(1)Se与O同族,电负性较大的是_____ ;基态Se原子的价电子运动状态有_____ 种。
(2)已知液态的二氧化硫可以发生类似水的自电离: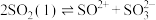 。
。 中各原子满足8电子结构,则其
中各原子满足8电子结构,则其 键和
键和 键数目之比为
键数目之比为__ , 的空间结构为
的空间结构为_______ 。
(3)有一种观点认为:由于硅的价层有可以利用的空d轨道,而碳没有,因此两者化合物结构和性质存在较大差异。化合物 和
和 的结构如图所示,
的结构如图所示, 为平面形,二者中N的杂化方式分别为
为平面形,二者中N的杂化方式分别为_______ ,二者中更易与 形成配位键的是
形成配位键的是_______ 。 熔点(>1700℃)明显高于
熔点(>1700℃)明显高于 (315℃),原因是
(315℃),原因是_______ 。
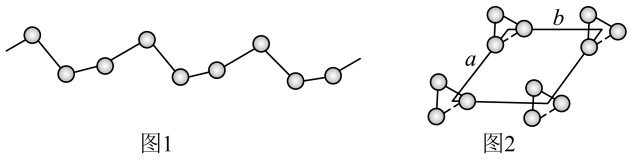
(5) -硒为六方晶胞结构,原子排列为相互平行的螺旋长链(如图1),沿着螺旋链方向的晶胞投影图如图2。
-硒为六方晶胞结构,原子排列为相互平行的螺旋长链(如图1),沿着螺旋链方向的晶胞投影图如图2。 -硒六方晶胞参数为
-硒六方晶胞参数为 、
、 、
、 (其中
(其中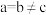 ),a轴与b轴间夹角为120°,c轴垂直于a轴与b轴,阿伏加德罗常数的值为
),a轴与b轴间夹角为120°,c轴垂直于a轴与b轴,阿伏加德罗常数的值为 。
。_______ 。晶胞中含有Se原子的数目为_______ ;则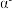 -硒晶胞的摩尔体积为
-硒晶胞的摩尔体积为______  (列出算式)。
(列出算式)。
(1)Se与O同族,电负性较大的是
(2)已知液态的二氧化硫可以发生类似水的自电离:
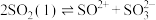 。
。 中各原子满足8电子结构,则其
中各原子满足8电子结构,则其 键和
键和 键数目之比为
键数目之比为 的空间结构为
的空间结构为(3)有一种观点认为:由于硅的价层有可以利用的空d轨道,而碳没有,因此两者化合物结构和性质存在较大差异。化合物
 和
和 的结构如图所示,
的结构如图所示, 为平面形,二者中N的杂化方式分别为
为平面形,二者中N的杂化方式分别为 形成配位键的是
形成配位键的是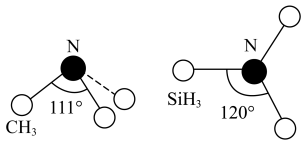
 熔点(>1700℃)明显高于
熔点(>1700℃)明显高于 (315℃),原因是
(315℃),原因是(5)
 -硒为六方晶胞结构,原子排列为相互平行的螺旋长链(如图1),沿着螺旋链方向的晶胞投影图如图2。
-硒为六方晶胞结构,原子排列为相互平行的螺旋长链(如图1),沿着螺旋链方向的晶胞投影图如图2。 -硒六方晶胞参数为
-硒六方晶胞参数为 、
、 、
、 (其中
(其中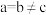 ),a轴与b轴间夹角为120°,c轴垂直于a轴与b轴,阿伏加德罗常数的值为
),a轴与b轴间夹角为120°,c轴垂直于a轴与b轴,阿伏加德罗常数的值为 。
。
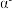 -硒晶胞的摩尔体积为
-硒晶胞的摩尔体积为 (列出算式)。
(列出算式)。
您最近一年使用:0次
6 . 研究二氧化碳的转化与减排具有重要的社会意义。用 还原
还原 的反应过程如下:
的反应过程如下:
①
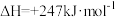
②

回答下列问题:
(1)

_______ 。
(2)同时提高 与
与 的平衡转化率和速率的措施是
的平衡转化率和速率的措施是_______ 。
(3)在密闭容器中分别充入0.1mol 与0.3mol
与0.3mol 。
。
①保持密闭容器体积为10L,只发生①②反应,经10min反应达到平衡,测定出 和
和 均为0.05mol。10min内
均为0.05mol。10min内 的平均反应速率为
的平均反应速率为____ ;该条件下,反应②的平衡常数为_____ 。
②在150℃时,改变密闭容器的体积,测得 和
和 平衡转化率随压强变化如图所示。
平衡转化率随压强变化如图所示。 平衡转化率随压强增大而减小的主要原因是
平衡转化率随压强增大而减小的主要原因是____ ; 后
后 平衡转化率随压强增大而减小缓慢甚至增大,可能的原因是
平衡转化率随压强增大而减小缓慢甚至增大,可能的原因是_______ 。 和
和 ,加入催化剂,仅发生反应①②。经实验测出两步反应过程的能量变化示意图如下:
,加入催化剂,仅发生反应①②。经实验测出两步反应过程的能量变化示意图如下: 体积分数很低,主要原因是活化能
体积分数很低,主要原因是活化能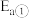
_______ 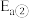 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②随温度升高, 的体积分数变化趋势为先增后减小,其可能原因是
的体积分数变化趋势为先增后减小,其可能原因是_______ 。
 还原
还原 的反应过程如下:
的反应过程如下:①

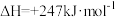
②


回答下列问题:
(1)


(2)同时提高
 与
与 的平衡转化率和速率的措施是
的平衡转化率和速率的措施是(3)在密闭容器中分别充入0.1mol
 与0.3mol
与0.3mol 。
。①保持密闭容器体积为10L,只发生①②反应,经10min反应达到平衡,测定出
 和
和 均为0.05mol。10min内
均为0.05mol。10min内 的平均反应速率为
的平均反应速率为②在150℃时,改变密闭容器的体积,测得
 和
和 平衡转化率随压强变化如图所示。
平衡转化率随压强变化如图所示。 平衡转化率随压强增大而减小的主要原因是
平衡转化率随压强增大而减小的主要原因是 后
后 平衡转化率随压强增大而减小缓慢甚至增大,可能的原因是
平衡转化率随压强增大而减小缓慢甚至增大,可能的原因是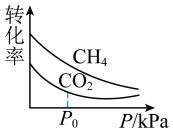
 和
和 ,加入催化剂,仅发生反应①②。经实验测出两步反应过程的能量变化示意图如下:
,加入催化剂,仅发生反应①②。经实验测出两步反应过程的能量变化示意图如下: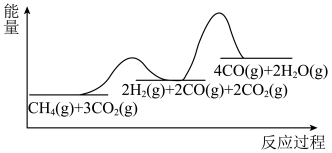
 体积分数很低,主要原因是活化能
体积分数很低,主要原因是活化能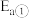
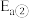 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②随温度升高,
 的体积分数变化趋势为先增后减小,其可能原因是
的体积分数变化趋势为先增后减小,其可能原因是
您最近一年使用:0次
7 . 实验室用废铁屑制取无水氯化铁并测其纯度。实验方案如下:
Ⅰ. 制备
制备
①将废铁屑加入30%NaOH溶液中,煮沸30分钟,过滤,洗涤2~3次。
②将洗涤后废铁屑加入20%盐酸,控制温度在40~50℃之间,至反应完毕,过滤。
③向滤液中逐滴加入10%双氧水,同时加入25%盐酸,充分搅拌至溶液呈棕黄色。
④将溶液转移至蒸发皿中,加热浓缩,缓慢冷却至大量晶体析出,抽滤,洗涤。
回答下列问题:
(1)用NaOH溶液洗涤废铁屑的目的是_______ 。
(2)控制温度在40~50℃的原因是_______ 。
(3)滴加10%双氧水时,滴加速率过快会产生气泡。该气体为_______ 。
Ⅱ.无水 制备
制备
已知 熔点―156℃,沸点77℃,易水解生成
熔点―156℃,沸点77℃,易水解生成 和HCl。
和HCl。
(4)按图装置进行实验。锥形瓶中生成无水 的总化学方程式为
的总化学方程式为_______ ;仪器A的作用是_______ 。
(5)称取3.250g产品试样,配制成100.00mL溶液,取20.00mL于锥形瓶中,加入足量KI溶液,经充分反应后,滴入淀粉溶液3~5滴,然后用 溶液滴定(
溶液滴定(
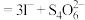 ),经三次平行实验,平均消耗
),经三次平行实验,平均消耗 溶液19.00ml。
溶液19.00ml。
①所制产品的纯度为_______ (以无水 质量分数表示,保留三位有效数字);
质量分数表示,保留三位有效数字);
②所制产品中可能含有 杂质,检验
杂质,检验 的试剂为
的试剂为_______ (填化学式)溶液;产生 的原因可能是
的原因可能是_______ 。
Ⅰ.
 制备
制备①将废铁屑加入30%NaOH溶液中,煮沸30分钟,过滤,洗涤2~3次。
②将洗涤后废铁屑加入20%盐酸,控制温度在40~50℃之间,至反应完毕,过滤。
③向滤液中逐滴加入10%双氧水,同时加入25%盐酸,充分搅拌至溶液呈棕黄色。
④将溶液转移至蒸发皿中,加热浓缩,缓慢冷却至大量晶体析出,抽滤,洗涤。
回答下列问题:
(1)用NaOH溶液洗涤废铁屑的目的是
(2)控制温度在40~50℃的原因是
(3)滴加10%双氧水时,滴加速率过快会产生气泡。该气体为
Ⅱ.无水
 制备
制备已知
 熔点―156℃,沸点77℃,易水解生成
熔点―156℃,沸点77℃,易水解生成 和HCl。
和HCl。(4)按图装置进行实验。锥形瓶中生成无水
 的总化学方程式为
的总化学方程式为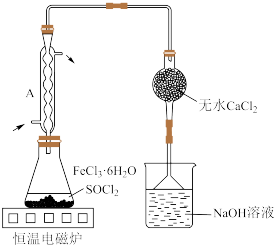
(5)称取3.250g产品试样,配制成100.00mL溶液,取20.00mL于锥形瓶中,加入足量KI溶液,经充分反应后,滴入淀粉溶液3~5滴,然后用
 溶液滴定(
溶液滴定(
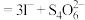 ),经三次平行实验,平均消耗
),经三次平行实验,平均消耗 溶液19.00ml。
溶液19.00ml。①所制产品的纯度为
 质量分数表示,保留三位有效数字);
质量分数表示,保留三位有效数字);②所制产品中可能含有
 杂质,检验
杂质,检验 的试剂为
的试剂为 的原因可能是
的原因可能是
您最近一年使用:0次
名校
解题方法
8 . 二氧化钒(VO2)是一种新型热敏材料,实验室以V2O5为原料合成用于制备VO2的氧钒(Ⅳ)碱式碳酸铵晶体{化学式为(NH4)5[(VO)6(CO3)4(OH)9]•10H2O},过程如图:

已知:+4价钒在弱酸性条件下具有还原性,VO2+能被O2氧化。回答下列问题:
(1)步骤ⅰ中生成VOCl2同时生成N2的化学方程式为_____ 。
(2)常温下,只用浓盐酸与V2O5反应也能制备VOCl2溶液,但该方法未被推广,从环保角度分析该方法未被推广的主要原因是_____ (用化学方程式说明)。
(3)步骤ii可用如图仪器组装完成。
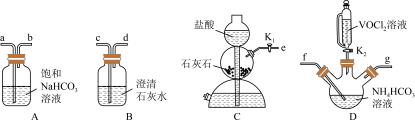
①装置D中盛放NH4HCO3溶液的仪器名称是_____ ;
②反应前通数分钟CO2的目的是_____ 。上述装置从左到右的连接顺序为_____ (用各接口字母表示)。
③反应结束后,将三颈烧瓶置于CO2保护下的干燥器中,静置后可得到紫红色晶体,然后抽滤,先用饱和NH4HCO3溶液洗涤3次,再用无水乙醇洗涤2次,最后用乙醚洗涤2次。检验晶体已经洗涤干净的操作是_____ 。
(4)测定氧钒(Ⅳ)碱式碳酸铵晶体粗产品中钒的含量。
称量wg样品于锥形瓶中,用30mL稀硫酸溶解后,加入稍过量的0.01mol/LKMnO4溶液,充分反应后,再加入稍过量的2%NaNO2溶液,再加入适量尿素除去过量的NaNO2,最后用1mol/L(NH4)2Fe(SO4)2标准溶液滴定至终点,重复实验两次。消耗滴定液的体积如表:
已知:滴定反应为VO +Fe2++2H+=VO2++Fe3++H2O
+Fe2++2H+=VO2++Fe3++H2O
①滴定时,向锥形瓶中加入几滴_____ (填化学式)溶液作指示剂。
②粗产品中钒的质量分数为_____ %。
③下列情况会导致所测钒元素的质量分数可能偏小的是_____ (填序号)。
A.称量样品时,样品与砝码的位置放颠倒了
B.(NH4)2Fe(SO4)2标准溶液中部分Fe2+被氧化
C.滴定过程中,往锥形瓶内加入少量蒸馏水
D.滴定达终点时发现滴定管尖嘴内有气泡

已知:+4价钒在弱酸性条件下具有还原性,VO2+能被O2氧化。回答下列问题:
(1)步骤ⅰ中生成VOCl2同时生成N2的化学方程式为
(2)常温下,只用浓盐酸与V2O5反应也能制备VOCl2溶液,但该方法未被推广,从环保角度分析该方法未被推广的主要原因是
(3)步骤ii可用如图仪器组装完成。

①装置D中盛放NH4HCO3溶液的仪器名称是
②反应前通数分钟CO2的目的是
③反应结束后,将三颈烧瓶置于CO2保护下的干燥器中,静置后可得到紫红色晶体,然后抽滤,先用饱和NH4HCO3溶液洗涤3次,再用无水乙醇洗涤2次,最后用乙醚洗涤2次。检验晶体已经洗涤干净的操作是
(4)测定氧钒(Ⅳ)碱式碳酸铵晶体粗产品中钒的含量。
称量wg样品于锥形瓶中,用30mL稀硫酸溶解后,加入稍过量的0.01mol/LKMnO4溶液,充分反应后,再加入稍过量的2%NaNO2溶液,再加入适量尿素除去过量的NaNO2,最后用1mol/L(NH4)2Fe(SO4)2标准溶液滴定至终点,重复实验两次。消耗滴定液的体积如表:
| 实验次数 | 滴定前读数/mL | 滴定后读数/mL |
| 1 | 0.00 | 19.99 |
| 2 | 1.10 | 21.10 |
| 3 | 1.56 | 21.57 |
 +Fe2++2H+=VO2++Fe3++H2O
+Fe2++2H+=VO2++Fe3++H2O①滴定时,向锥形瓶中加入几滴
②粗产品中钒的质量分数为
③下列情况会导致所测钒元素的质量分数可能偏小的是
A.称量样品时,样品与砝码的位置放颠倒了
B.(NH4)2Fe(SO4)2标准溶液中部分Fe2+被氧化
C.滴定过程中,往锥形瓶内加入少量蒸馏水
D.滴定达终点时发现滴定管尖嘴内有气泡
您最近一年使用:0次
名校
解题方法
9 . 化学平衡是中学化学的重点研究对象
I.氮及其化合物是重要的化工原料。回答下列问题:
(1)汽车尾气的储存还原技术法(NSR)可有效消除机动车尾气中NOx和CO的排放。
已知:

则2NO(g)+2CO(g)⇌2CO2(g)+N2(g) △H3=___________ kJ∙mol-1。
(2)在不同压强下,向恒容密闭容器中通入初始浓度为3.0molmol∙L-1NO、1.0mol∙L-1 ,使其发生反应:
,使其发生反应: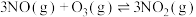
 kJ•mol-1。测得平衡时
kJ•mol-1。测得平衡时 的体积百分含量随着温度、压强变化情况如图所示:
的体积百分含量随着温度、压强变化情况如图所示:

① 、
、 、
、 由大到小的顺序为
由大到小的顺序为___________ 。
②下列数据能表明反应处于平衡状态的是___________ (填字母)。
A.混合气体的密度不变 B.混合气体的平均摩尔质量不变
C. D.混合气体的颜色深浅不变
D.混合气体的颜色深浅不变
③温度为 时,反应的平衡常数
时,反应的平衡常数
___________ (填具体数字)。
(3)对于可逆反应 ,若起始投料
,若起始投料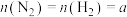 mol,达到平衡后,增大压强,
mol,达到平衡后,增大压强, 的体积分数
的体积分数___________ (填“增大”“减小”或“不变”)。
Ⅱ.
(4)水是极弱的电解质,常温下某电解质溶解在水中后,溶液中的 mol∙L-1,则该电解质可能是___________(填字母)。
mol∙L-1,则该电解质可能是___________(填字母)。
(5)已知次氯酸是比碳酸还弱的酸,要使新制稀氯水中的 增大,可以采取的措施为___________(填字母)。
增大,可以采取的措施为___________(填字母)。
(6)常温下,为证明 是弱电解质,某同学取出10mL0·10mol•L-1氨水,用pH试纸测其pH为a;用蒸馏水稀释至1000mL,再用pH试纸测其pH为b;只要a、b满足关系
是弱电解质,某同学取出10mL0·10mol•L-1氨水,用pH试纸测其pH为a;用蒸馏水稀释至1000mL,再用pH试纸测其pH为b;只要a、b满足关系___________ (用等式或不等式表示),就可确认 是弱电解质。
是弱电解质。
(7)已知:25℃时,两种常见弱酸的电离平衡常数:
①25℃时,10mL0.10mol⋅L
 溶液与10mL0.10mol•L-1
溶液与10mL0.10mol•L-1 溶液中,离子总数大小关系:
溶液中,离子总数大小关系: 溶液
溶液___________  溶液(填“>”、“<”或“=”)。
溶液(填“>”、“<”或“=”)。
②向 溶液中通入过量
溶液中通入过量 反应的离子方程式为
反应的离子方程式为___________ 。
(8)已知:常温下, ,(在溶液中某离子完全沉淀时,认为该离子浓度小于
,(在溶液中某离子完全沉淀时,认为该离子浓度小于 )
)
① 的溶度积常数表达式
的溶度积常数表达式
___________ 。
② 完全沉淀的
完全沉淀的 为
为___________ 。
I.氮及其化合物是重要的化工原料。回答下列问题:
(1)汽车尾气的储存还原技术法(NSR)可有效消除机动车尾气中NOx和CO的排放。
已知:


则2NO(g)+2CO(g)⇌2CO2(g)+N2(g) △H3=
(2)在不同压强下,向恒容密闭容器中通入初始浓度为3.0molmol∙L-1NO、1.0mol∙L-1
 ,使其发生反应:
,使其发生反应: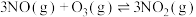
 kJ•mol-1。测得平衡时
kJ•mol-1。测得平衡时 的体积百分含量随着温度、压强变化情况如图所示:
的体积百分含量随着温度、压强变化情况如图所示:
①
 、
、 、
、 由大到小的顺序为
由大到小的顺序为②下列数据能表明反应处于平衡状态的是
A.混合气体的密度不变 B.混合气体的平均摩尔质量不变
C.
 D.混合气体的颜色深浅不变
D.混合气体的颜色深浅不变③温度为
 时,反应的平衡常数
时,反应的平衡常数
(3)对于可逆反应
 ,若起始投料
,若起始投料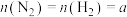 mol,达到平衡后,增大压强,
mol,达到平衡后,增大压强, 的体积分数
的体积分数Ⅱ.
(4)水是极弱的电解质,常温下某电解质溶解在水中后,溶液中的
 mol∙L-1,则该电解质可能是___________(填字母)。
mol∙L-1,则该电解质可能是___________(填字母)。A. | B.HCl | C. | D.NaOH |
(5)已知次氯酸是比碳酸还弱的酸,要使新制稀氯水中的
 增大,可以采取的措施为___________(填字母)。
增大,可以采取的措施为___________(填字母)。A.再通入 | B.加碳酸钙粉末 | C.加氯化钠溶液 | D.加足量NaOH |
(6)常温下,为证明
 是弱电解质,某同学取出10mL0·10mol•L-1氨水,用pH试纸测其pH为a;用蒸馏水稀释至1000mL,再用pH试纸测其pH为b;只要a、b满足关系
是弱电解质,某同学取出10mL0·10mol•L-1氨水,用pH试纸测其pH为a;用蒸馏水稀释至1000mL,再用pH试纸测其pH为b;只要a、b满足关系 是弱电解质。
是弱电解质。(7)已知:25℃时,两种常见弱酸的电离平衡常数:
| 酸 | 电离平衡常数 |
 |   |
 | 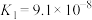 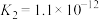 |

 溶液与10mL0.10mol•L-1
溶液与10mL0.10mol•L-1 溶液中,离子总数大小关系:
溶液中,离子总数大小关系: 溶液
溶液 溶液(填“>”、“<”或“=”)。
溶液(填“>”、“<”或“=”)。②向
 溶液中通入过量
溶液中通入过量 反应的离子方程式为
反应的离子方程式为(8)已知:常温下,
 ,(在溶液中某离子完全沉淀时,认为该离子浓度小于
,(在溶液中某离子完全沉淀时,认为该离子浓度小于 )
)①
 的溶度积常数表达式
的溶度积常数表达式
②
 完全沉淀的
完全沉淀的 为
为
您最近一年使用:0次
名校
10 . 已知一定条件下,1-苯基丙炔( )可与HCl发生加成反应,反应如下:
)可与HCl发生加成反应,反应如下:
回答下列问题:
(1)在473K、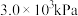 的高压HCl氛围下,以
的高压HCl氛围下,以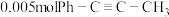 为原料进行上述反应。当产物Ⅰ和产物Ⅱ的产率均为10%时,体系放热akJ;当产物Ⅰ产率为15%和产物Ⅱ的产率为25%时,体系放热bkJ。若2a<b,则反应Ⅲ的焓变
为原料进行上述反应。当产物Ⅰ和产物Ⅱ的产率均为10%时,体系放热akJ;当产物Ⅰ产率为15%和产物Ⅱ的产率为25%时,体系放热bkJ。若2a<b,则反应Ⅲ的焓变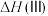
___________ 0(填“>”“=”或“<”),反应Ⅱ在该条件下的焓变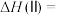
___________ (用含a、b的代数式表示)。
(2)下列能说明反应已经达到平衡的是___________(填标号)。
(3)在473K、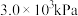 的高压HCl氛围下,以
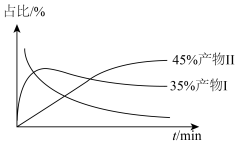
的高压HCl氛围下,以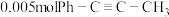 为原料进行上述反应,反应过程中除HCl外该炔烃及反应产物的占比[如:
为原料进行上述反应,反应过程中除HCl外该炔烃及反应产物的占比[如: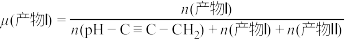 ]随时间的变化如图,则反应的活化能反应Ⅰ
]随时间的变化如图,则反应的活化能反应Ⅰ___________ 反应Ⅱ(填“大于”“小于”或“等于”), 的平衡转化率为
的平衡转化率为___________ ,反应Ⅱ的
___________ ,为获得产物Ⅰ可采取的措施为___________ 。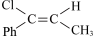 ,假定只发生反应Ⅲ,甲中
,假定只发生反应Ⅲ,甲中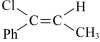 的相关量随时间变化如图所示:
的相关量随时间变化如图所示:
___________ (填“大于”“小于”或“等于”,下同)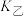 ,
,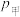
___________ 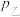 。
。
 )可与HCl发生加成反应,反应如下:
)可与HCl发生加成反应,反应如下: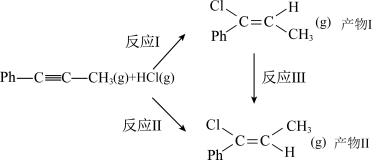
回答下列问题:
(1)在473K、
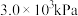 的高压HCl氛围下,以
的高压HCl氛围下,以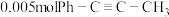 为原料进行上述反应。当产物Ⅰ和产物Ⅱ的产率均为10%时,体系放热akJ;当产物Ⅰ产率为15%和产物Ⅱ的产率为25%时,体系放热bkJ。若2a<b,则反应Ⅲ的焓变
为原料进行上述反应。当产物Ⅰ和产物Ⅱ的产率均为10%时,体系放热akJ;当产物Ⅰ产率为15%和产物Ⅱ的产率为25%时,体系放热bkJ。若2a<b,则反应Ⅲ的焓变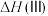
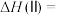
(2)下列能说明反应已经达到平衡的是___________(填标号)。
| A.反应体系内总质量不再变化 |
| B.恒容条件下,反应压强不再改变 |
| C.气体的平均相对分子质量不再变化 |
D.v(Ph-C≡C-CH3)=v( ) ) |
(3)在473K、
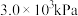 的高压HCl氛围下,以
的高压HCl氛围下,以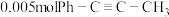 为原料进行上述反应,反应过程中除HCl外该炔烃及反应产物的占比[如:
为原料进行上述反应,反应过程中除HCl外该炔烃及反应产物的占比[如: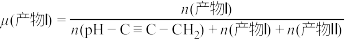 ]随时间的变化如图,则反应的活化能反应Ⅰ
]随时间的变化如图,则反应的活化能反应Ⅰ 的平衡转化率为
的平衡转化率为
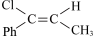 ,假定只发生反应Ⅲ,甲中
,假定只发生反应Ⅲ,甲中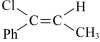 的相关量随时间变化如图所示:
的相关量随时间变化如图所示: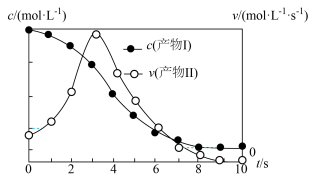
①0~3s内,甲容器中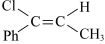 的反应速率增大的原因是
的反应速率增大的原因是

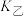 ,
,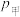
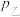 。
。
您最近一年使用:0次
2024-01-22更新
|
418次组卷
|
2卷引用:四川省成都市石室中学2023-2024学年高二下学期4月月考化学试卷



