解题方法
1 . 化学与生产、生活密切相关。下列说法不正确的是
A.《美国陶瓷学会会刊》发表我国故宫研究院的考古成果:乾隆时期紫金釉中发现特殊晶体-亚稳相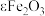 晶体,该样品溶于盐酸,滴加KSCN溶液,可验证 晶体,该样品溶于盐酸,滴加KSCN溶液,可验证 |
| B.利用酸性重铬酸钾检测酒驾利用了酸性重铬酸钾的强氧化性和酒精的还原性、挥发性 |
| C.石油的分馏,煤的气化、液化均属于物理变化 |
| D.采取“汽车尾气催化净化”“静电除尘”“燃煤固硫”等方法,可提高空气质量 |
您最近一年使用:0次
2 . 历史上诺贝尔化学奖曾经3次颁给研究合成氨的化学家。合成氨的原理为N2(g)+3H2(g)⇌2NH3(g)。回答下列问题。
(1)t℃时,向填充有催化剂、体积为2L的刚性容器中充入一定量的H2和N2合成氨,实验中测得c(NH3)随时间的变化如表所示:
①5~15min内N2的平均反应速率v(N2)=___________ mol•L-1•min-1。
②根据表中数据,在___________ min以后反应处于平衡状态。能加快反应达到平衡的措施有___________ (写出两条)。
③下列情况能说明反应达到平衡状态的是___________ (填标号)。
A.2v(NH3)=3v(H2) B.混合气体的相对分子质量不再变化
C.N2体积分数不再变化 D.混合气体的密度保持不变
(2)如表列出了在不同温度和压强下,反应达到平衡时NH3的百分含量w(NH3)。
①从表中数据得出,最优的条件是___________ 。
②工业上通常选择在400~500℃和10~30MPa条件下合成氨,原因是___________ 。
(1)t℃时,向填充有催化剂、体积为2L的刚性容器中充入一定量的H2和N2合成氨,实验中测得c(NH3)随时间的变化如表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol•L﹣1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
②根据表中数据,在
③下列情况能说明反应达到平衡状态的是
A.2v(NH3)=3v(H2) B.混合气体的相对分子质量不再变化
C.N2体积分数不再变化 D.混合气体的密度保持不变
(2)如表列出了在不同温度和压强下,反应达到平衡时NH3的百分含量w(NH3)。
| 压强/MPa v(NH3)/% 温度/℃ | 0.1 | 10 | 20 | 30 | 60 | 100 |
| 200 | 15.3 | 81.5 | 86.4 | 89.9 | 95.4 | 98.8 |
| 300 | 2.2 | 52.0 | 64.2 | 71.0 | 84.2 | 92.6 |
| 400 | 0.4 | 25.1 | 38.2 | 47.0 | 65.5 | 79.8 |
| 500 | 0.1 | 10.6 | 19.1 | 26.4 | 42.2 | 57.5 |
| 600 | 0.05 | 4.5 | 9.1 | 13.8 | 23.1 | 31.4 |
②工业上通常选择在400~500℃和10~30MPa条件下合成氨,原因是
您最近一年使用:0次
3 . 目前工业上常用的一种海水提溴技术“吹出法”,工艺流程图如图:
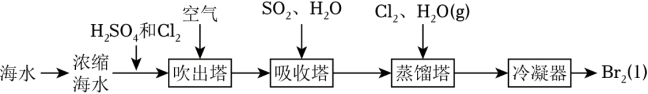
回答下列问题:
(1)溴在元素周期表中的位置___________ 。
(2)下列试剂可用于代替Cl2的是(填标号)___________。
(3)吸收塔内发生的主要反应化学方程式为___________ ;蒸馏塔内发生的主要反应离子方程式为___________ 。
(4)工业生产中,不是将H2SO4酸化和Cl2氧化后的海水直接蒸馏,而是经过“空气吹出”、“SO2吸收”、“Cl2氯化”后再蒸馏得到液溴,目的是___________ 。
(5)工业生产中,测得浓缩海水中溴的含量为800g•m-3,通过吹出塔、吸收塔时共损失了25%的溴,蒸馏和冷凝时共损失了10%的溴。处理10m3该浓缩海水,实际可得到液溴___________ mol。

回答下列问题:
(1)溴在元素周期表中的位置
(2)下列试剂可用于代替Cl2的是(填标号)___________。
| A.I2 | B.H2O2 | C.FeCl3 | D.NaBrO3 |
(4)工业生产中,不是将H2SO4酸化和Cl2氧化后的海水直接蒸馏,而是经过“空气吹出”、“SO2吸收”、“Cl2氯化”后再蒸馏得到液溴,目的是
(5)工业生产中,测得浓缩海水中溴的含量为800g•m-3,通过吹出塔、吸收塔时共损失了25%的溴,蒸馏和冷凝时共损失了10%的溴。处理10m3该浓缩海水,实际可得到液溴
您最近一年使用:0次
4 . 三氧化硫(SO3)是生产硫酸重要的中间产物,熔点16.8℃,沸点44.8℃,与水反应的化学方程式为SO3+H2O=H2SO4。某小组设计了如图实验装置制备并吸收SO3(夹持仪器略)。回答下列问题:
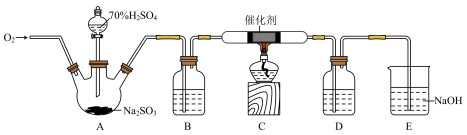
(1)盛放70%H2SO4的仪器名称是________ ,A中制备SO2的化学方程式为_________ 。
(2)装置B、D中盛放的试剂相同,该试剂是___________ 。
(3)O2除作反应物外,另一个作用是________ ,C中发生反应的化学方程式为________ 。
(4)对装置E中吸收液的成分进行探究,完成下表实验过程(限选试剂:稀盐酸、稀硫酸、稀硝酸、MgCl2溶液、BaCl2溶液、酸性KMnO4溶液、品红溶液、石蕊溶液)

(1)盛放70%H2SO4的仪器名称是
(2)装置B、D中盛放的试剂相同,该试剂是
(3)O2除作反应物外,另一个作用是
(4)对装置E中吸收液的成分进行探究,完成下表实验过程(限选试剂:稀盐酸、稀硫酸、稀硝酸、MgCl2溶液、BaCl2溶液、酸性KMnO4溶液、品红溶液、石蕊溶液)
| 操作步骤 | 实验现象 | 结论 |
| 取少量吸收液于试管中,滴加几滴MgCl2溶液 | 有白色沉淀生成 | 吸收液中含有NaOH |
| 取少量吸收液于试管中,滴加几滴酸性KMnO4溶液 | ① | 吸收液中含有② |
| 取少量吸收液于试管中,③ | ④ | 吸收液中含有Na2SO4 |
您最近一年使用:0次
5 . 常温下氯气能溶解于水,得到的氯水中既含有Cl2、H2O、HClO分子,也含有H+、Cl-、ClO-等离子。这说明
| A.氯气能与H2O反应生成盐酸和次氯酸 |
| B.盐酸不能与次氯酸反应生成氯气和H2O |
| C.盐酸不能完全电离成H+和Cl- |
| D.次氯酸能完全电离成H+和ClO- |
您最近一年使用:0次
6 . 下列说法错误的是
| A.食盐中常添加碘酸钾(KlO3)作为营养强化剂 |
| B.抗坏血酸(维生素C)常用于水果罐头的抗氧化剂 |
| C.“OTC”是非处方药的标识,消费者可从药店自行购买和使用 |
| D.现代农业中,只需施用有机肥和天然农药,不需施用化肥和有机合成农药 |
您最近一年使用:0次
7 . 2021年6月5日世界地球日主题为“生态系统恢复”。下列说法错误的是
| A.CO2、NO2和SO2都会导致酸雨的形成 |
| B.煤经过液化可转化为甲醇等清洁能源 |
| C.废旧电池回收处理可保护环境和变废为宝 |
| D.新能源汽车的推广与使用有助于减少光化学烟雾 |
您最近一年使用:0次
名校
解题方法
8 . 甲酸(HCOOH)在Pd/C催化剂表面催化释氢的机理如图所示。已知第一步与第三步是快反应,第二步是慢反应。下列说法正确的是


| A.第一步与第二步断裂的化学键相同 |
| B.HCOOH→CO2+H2的反应速率由第一步和第三步决定 |
| C.使用更高效的催化剂,该总反应的ΔH将变大 |
| D.用氘化甲酸(HCOOD或DCOOH)代替HCOOH,得到的是HD和CO2 |
您最近一年使用:0次
2023-08-10更新
|
442次组卷
|
5卷引用:云南省保山市腾冲市第八中学2020-2021学年高一下学期期末考试化学试题
9 . 下列做法不会产生大气污染物的是
| A.使用太阳能发电 | B.汽车单双号限行 |
| C.循环利用工业尾气 | D.燃烧硫黄以漂白纸张 |
您最近一年使用:0次
10 . 某校化学兴趣小组同学,利用下列装置探究 试纸上的微型电解。
试纸上的微型电解。
(1)如图,取一条广泛 试纸,浸润了饱和
试纸,浸润了饱和 溶液后放置于玻璃片上,取两只回形针(铁制)夹住试纸两端,另取导线、鳄鱼夹、6V电池连接好电路。
溶液后放置于玻璃片上,取两只回形针(铁制)夹住试纸两端,另取导线、鳄鱼夹、6V电池连接好电路。

当两根鳄鱼夹夹住回形针后,试纸上立刻出现以下现象:阳极回形针处很快出现大片红棕色;阴极附近迅速呈现大片蓝紫色,对照比色卡发现其 约为13。
约为13。
①如图,右端回形针为___________ 极(填“阴”或“阳”);阴极试纸上出现大片蓝紫色的原因是(用电极反应式表示):___________ 。
②推测阳极回形针处出现的红棕色物质可能是___________ (写化学式)。
(2)小组同学另取两根铅笔芯作为电极,对 试纸上的
试纸上的 溶液电解,可见阳极与试纸接触处呈现
溶液电解,可见阳极与试纸接触处呈现___________ (填“红”或“蓝”)色圆点,电解 饱和溶液的实质是
饱和溶液的实质是___________ (用方程式表示)。当阴极产生 气体时,可加
气体时,可加___________ (填物质及物质的质量)使溶液恢复。
 试纸上的微型电解。
试纸上的微型电解。(1)如图,取一条广泛
 试纸,浸润了饱和
试纸,浸润了饱和 溶液后放置于玻璃片上,取两只回形针(铁制)夹住试纸两端,另取导线、鳄鱼夹、6V电池连接好电路。
溶液后放置于玻璃片上,取两只回形针(铁制)夹住试纸两端,另取导线、鳄鱼夹、6V电池连接好电路。 
当两根鳄鱼夹夹住回形针后,试纸上立刻出现以下现象:阳极回形针处很快出现大片红棕色;阴极附近迅速呈现大片蓝紫色,对照比色卡发现其
 约为13。
约为13。①如图,右端回形针为
②推测阳极回形针处出现的红棕色物质可能是
(2)小组同学另取两根铅笔芯作为电极,对
 试纸上的
试纸上的 溶液电解,可见阳极与试纸接触处呈现
溶液电解,可见阳极与试纸接触处呈现 饱和溶液的实质是
饱和溶液的实质是 气体时,可加
气体时,可加
您最近一年使用:0次



