1 . 甲烷是目前使用量非常大的一种清洁燃料。
(1)甲烷的电子式为_______ ,空间构型为_____ ,二氯甲烷的结构共有_____ 种。
(2)燃料电池是一种高效、环境友好的供电装置,如图是甲烷燃料电池原理示意图,回答下列问题:______  填“a”或“b”
填“a”或“b” ,该极的电极反应式是:
,该极的电极反应式是:_______ ,总反应式为_______ 。
(1)甲烷的电子式为
(2)燃料电池是一种高效、环境友好的供电装置,如图是甲烷燃料电池原理示意图,回答下列问题:
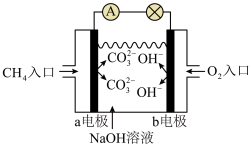
 填“a”或“b”
填“a”或“b” ,该极的电极反应式是:
,该极的电极反应式是:
您最近一年使用:0次
2 . 下列有关萃取、分液的说法中不正确的是
| A.分液操作中,应关闭分液漏斗上端的玻璃塞,防止有机试剂挥发,造成环境污染 |
| B.振荡分液漏斗中的溶液时,一只手压住口部,另一只手握住活塞部分倒转振荡 |
| C.萃取操作中,振荡分液漏斗中的溶液时应及时放气 |
| D.分液操作时,先将下层液体从下口放出,然后将上层液体从上口倒出 |
您最近一年使用:0次
3 . A、B、C、D、E、F六种元素,均位于周期表的前四周期,它们的核电荷数依次增加,A原子的L层p轨道中有2个电子,B元素在同周期元素中电负性最大,C与A原子的价电子数相同,D的最高价含氧酸酸性最强,E原子核外不成对电子数最多,F元素能形成的双原子分子,其单质在常温下呈液态。
(1)A的最高价含氧酸酸根离子的价层电子对数为_____ ,其 模型是
模型是_____ 。
(2)B、D、F简单氢化物沸点由高到低的顺序为_____ (填化学式),原因是_____ 。
(3)与E同族的第n周期元素核外电子排布不遵循洪特规则特例,则它的外围电子排布式为_____ 。
(4)与A相比,从电子云重叠方式的角度解释为什么C的原子间难以形成双键和叁键_____ 。
(1)A的最高价含氧酸酸根离子的价层电子对数为
 模型是
模型是(2)B、D、F简单氢化物沸点由高到低的顺序为
(3)与E同族的第n周期元素核外电子排布不遵循洪特规则特例,则它的外围电子排布式为
(4)与A相比,从电子云重叠方式的角度解释为什么C的原子间难以形成双键和叁键
您最近一年使用:0次
解题方法
4 . 完成下列小题
(1)胆矾的结构可表示如下:

则胆矾晶体中含有_____ (填序号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键 E.氢键
(2)向硫酸铜溶液里逐滴加入氨水至生成的蓝色沉淀溶解,得到深蓝色的透明溶液,蓝色沉淀溶解的离子方程式为_____ ,该配离子中的配体跟水分子相比,_____ 较容易跟铜离子形成配位键,原因是_____ 。
(3)配合物 中,配位原子是
中,配位原子是_____ ,该配合物的结构式为_____ (标出配位键)该配合物中, 键与Π键的个数比为
键与Π键的个数比为_____ 。
(1)胆矾的结构可表示如下:

则胆矾晶体中含有
A.配位键 B.离子键 C.极性共价键 D.非极性共价键 E.氢键
(2)向硫酸铜溶液里逐滴加入氨水至生成的蓝色沉淀溶解,得到深蓝色的透明溶液,蓝色沉淀溶解的离子方程式为
(3)配合物
 中,配位原子是
中,配位原子是 键与Π键的个数比为
键与Π键的个数比为
您最近一年使用:0次
名校
5 . 硫酸酸化的高锰酸钾溶液与草酸发生化学反应,反应如下:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O,某化学兴趣小组为了测定草酸浓度,主要做了如下实验。用0.1000mol/L酸性高锰酸钾溶液滴定未知浓度的H2C2O4溶液。实验中测得的数据记录如下:
请回答:
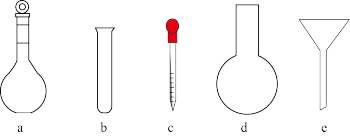
(1)配制KMnO4标准溶液时,使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要图中的______ (填字母代号)。
(2)用配制好的高锰酸钾滴定草酸时,高锰酸钾溶液应盛装于_______ (如图,填“甲”或“乙”)滴定管。滴定时,眼睛应注视______________________ 。

(3)该实验中未使用指示剂就可判断终点,到达终点的判断标志是____________ 。
(4)根据表中数据,计算H2C2O4溶液的浓度______________ 。
(5)下列造成H2C2O4溶液的浓度偏高的是_________________________________。
| 滴定次数 | H2C2O4体积 | 滴定前KMnO4体积 | 终点时KMnO4体积 |
1 | 25.00mL | 0.00mL | 21.41mL |
2 | 25.00mL | 0.02mL | 21.44mL |
3 | 25.00mL | 1.04mL | 22.47mL |
4 | 25.00mL | 0.04mL | 24.46 mL |
(1)配制KMnO4标准溶液时,使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要图中的

(2)用配制好的高锰酸钾滴定草酸时,高锰酸钾溶液应盛装于

(3)该实验中未使用指示剂就可判断终点,到达终点的判断标志是
(4)根据表中数据,计算H2C2O4溶液的浓度
(5)下列造成H2C2O4溶液的浓度偏高的是_________________________________。
| A.滴定终点读数时俯视 | B.滴定前有气泡,滴定后气泡消失 |
| C.润洗锥形瓶 | D.滴定过程中加入少量蒸馏水冲洗瓶壁 |
您最近一年使用:0次
2022-12-13更新
|
113次组卷
|
2卷引用:内蒙古赤峰市第四中学分校2021-2022学年高二上学期期中考试化学试题
解题方法
6 . Ⅰ.实验室常用以下几种方法制备氯气。
(1)二氧化锰和浓盐酸反应制氯气,写出其反应的离子方程式:_______
(2)高锰酸钾和浓盐酸反应制氯气,写出其反应的化学方程式:_______
(3)氯酸钾和浓盐酸反应制氯气,该反应中氧化产物与还原产物的物质的量之比:_______
II.图中装置用于二氧化锰和浓盐酸在加热条件下反应制取纯净、干燥的氯气。

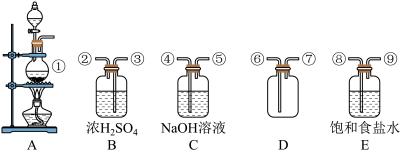
(4)在装置A~E中,有①~⑨ 9个接口,用编号表示仪器的导气管连接顺序依次为_______
(5)B瓶中浓H2SO4的作用是_______ ,E瓶盛有的饱和食盐水的作用是_______ ,C瓶中盛有NaOH溶液的作用是_______ ,此装置收集氯气的方法为_______ 。
(6)写出此实验装置制氯气的化学方程式_______ ,工业用氯气制漂白粉的化学方程式是_______ 。
(1)二氧化锰和浓盐酸反应制氯气,写出其反应的离子方程式:
(2)高锰酸钾和浓盐酸反应制氯气,写出其反应的化学方程式:
(3)氯酸钾和浓盐酸反应制氯气,该反应中氧化产物与还原产物的物质的量之比:
II.图中装置用于二氧化锰和浓盐酸在加热条件下反应制取纯净、干燥的氯气。


(4)在装置A~E中,有①~⑨ 9个接口,用编号表示仪器的导气管连接顺序依次为
(5)B瓶中浓H2SO4的作用是
(6)写出此实验装置制氯气的化学方程式
您最近一年使用:0次
7 . 有一包固体粉末试样,是由下列物质中的一种或多种组成:NaCl、CaCl2、CuSO4(无水)、Na2SO4、Na2CO3。为了要确定该粉末试样的成分,进行以下实验:
实验一:用烧杯取粉末试样,加足量蒸馏水,充分搅拌后形成无色的透明溶液X。
实验二:在溶液X中加了盐酸,观察到在溶液中陆续产生气泡,至溶液不再冒气泡,溶液仍为无色,得到无色透明溶液Y。
实验三:在无色透明的溶液Y中,滴加Ba(NO3)2溶液,即见白色沉淀。
实验四:继续滴加Ba(NO3)2溶液,至白色沉淀不再产生后,过滤分离出白色沉淀,得到透明的无色滤液Z。
实验五:在滤液Z中,滴入AgNO3溶液,则见白色沉淀,加入稀硝酸,沉淀不溶解。
(1)根据上述实验,原粉末中一定没有的物质是_________ ,一定含有的物质是_________ ,可能含有的物质是_________ 。
(2)按要求写出下列方程式:
①CaCl2的电离方程式:_________ 。
②写出实验二、实验三中发生的离子反应方程式:
实验二_________ 。
实验三_________ 。
实验一:用烧杯取粉末试样,加足量蒸馏水,充分搅拌后形成无色的透明溶液X。
实验二:在溶液X中加了盐酸,观察到在溶液中陆续产生气泡,至溶液不再冒气泡,溶液仍为无色,得到无色透明溶液Y。
实验三:在无色透明的溶液Y中,滴加Ba(NO3)2溶液,即见白色沉淀。
实验四:继续滴加Ba(NO3)2溶液,至白色沉淀不再产生后,过滤分离出白色沉淀,得到透明的无色滤液Z。
实验五:在滤液Z中,滴入AgNO3溶液,则见白色沉淀,加入稀硝酸,沉淀不溶解。
(1)根据上述实验,原粉末中一定没有的物质是
(2)按要求写出下列方程式:
①CaCl2的电离方程式:
②写出实验二、实验三中发生的离子反应方程式:
实验二
实验三
您最近一年使用:0次
解题方法
8 . 某研究性学习小组拟用如下装置设计实验,来探究纯净、干燥的氯气与氨气的反应。按要求回答下列问题:

(1)装置A中盛装浓盐酸的仪器名称是_______ ;装置D的作用是_______ ;装置E中饱和食盐水的作用是_______ ;
(2)导气管的正确连接顺序中,a与_______ 连接(填小写字母);
(3)装置F中发生8NH3+3Cl2=6NH4Cl+N2,该反应中氧化剂与还原剂的物质的量之比是_______ ,为使两种气体充分接触,明显地看到_______ 现象,则装置F中j与_______ 连接(填小写字母);
(4)装置B中所发生反应的化学方程式是_______ ;
(5)该学习小组研究发现,整套实验方案的主要缺陷是缺少_______ 装置。

(1)装置A中盛装浓盐酸的仪器名称是
(2)导气管的正确连接顺序中,a与
(3)装置F中发生8NH3+3Cl2=6NH4Cl+N2,该反应中氧化剂与还原剂的物质的量之比是
(4)装置B中所发生反应的化学方程式是
(5)该学习小组研究发现,整套实验方案的主要缺陷是缺少
您最近一年使用:0次
解题方法
9 . 下图中A~F均为中学化学中常见含金属元素的物质,其中A、D为单质,C为两性氧化物,B为红棕色粉末,它们之间有如下转化关系(反应过程中有些生成物已略去)。请按要求填空:
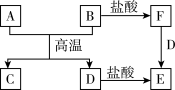
(1)B的化学式是_______ ;E中金属阳离子的符号是_______ ;
(2)A与B的反应是_______ 反应(填“吸热”或“放热”);
(3)向F中加入 溶液的现象是
溶液的现象是_______ ;
(4)D与水蒸气在高温下反应,生成固体物质的化学式是_______ ;
(5)工业上由C冶炼金属A的方法是_______ ;
(6)单质A与氢氧化钠溶液反应的化学方程式是_______ ;
(7)F与D反应的离子方程式是_______ 。

(1)B的化学式是
(2)A与B的反应是
(3)向F中加入
 溶液的现象是
溶液的现象是(4)D与水蒸气在高温下反应,生成固体物质的化学式是
(5)工业上由C冶炼金属A的方法是
(6)单质A与氢氧化钠溶液反应的化学方程式是
(7)F与D反应的离子方程式是
您最近一年使用:0次
解题方法
10 . 根据下表中各元素的信息,按要求填空:
(1)②的元素符号是_______ ,其原子结构示意图是_______ ;
(2)①和⑧两种元素组成化合物的电子式是_______ ;
(3)表中所列8种元素中,原子半径最大的是_______ (写元素名称),其单质与水反应的化学方程式是_______ ;
(4)⑥和⑦两种元素最高价氧化物对应的水化物相互反应的离子方程式是_______ ;
(5)下列对于元素⑧有关推断正确的是_______ 。
A.其最高化合价为+7
B.其气态氢化物的稳定性比元素⑦的强
C.其氧化物对应的水化物一定属于强酸
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(2)①和⑧两种元素组成化合物的电子式是
(3)表中所列8种元素中,原子半径最大的是
(4)⑥和⑦两种元素最高价氧化物对应的水化物相互反应的离子方程式是
(5)下列对于元素⑧有关推断正确的是
A.其最高化合价为+7
B.其气态氢化物的稳定性比元素⑦的强
C.其氧化物对应的水化物一定属于强酸
您最近一年使用:0次



