解题方法
1 . 回答下列问题。
(1)基态N原子的电子排布式为___________ 。基态P原子中,电子占据的最高能级原子轨道形状为___________ 。
(2)H2O中心原子杂化轨道类型为___________ ,说明H2O沸点大于H2S的原因___________ 。
(3)基态Ca原子价层电子由4s2状态变化为4s14p1状态所得原子光谱为___________ (填“发射”或“吸收”)光谱。
(4)下列氧原子电子排布图表示的状态中,能量最高的是___________ (填标号,下同),能量最低的是___________ 。
A.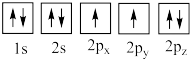 B.
B.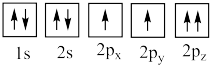
C. D.
D.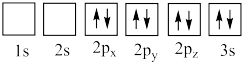
(1)基态N原子的电子排布式为
(2)H2O中心原子杂化轨道类型为
(3)基态Ca原子价层电子由4s2状态变化为4s14p1状态所得原子光谱为
(4)下列氧原子电子排布图表示的状态中,能量最高的是
A.
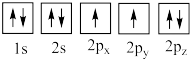 B.
B.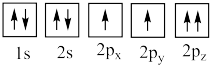
C.
 D.
D.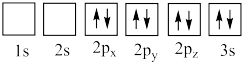
您最近一年使用:0次
2024-03-22更新
|
486次组卷
|
2卷引用:海南中学白沙学校2022-2023学年高二下学期期末考试化学试题
2 . NA代表阿伏加德罗常数的值。下列说法正确的是
| A.2.4g镁条在空气中充分燃烧,转移的电子数目为0.2NA |
B.5.6g铁粉与足量 溶液充分反应,产生的气体分子数目为0.05NA 溶液充分反应,产生的气体分子数目为0.05NA |
C.标准状况下,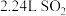 与 与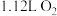 充分反应,生成的 充分反应,生成的 分子数目为0.1NA 分子数目为0.1NA |
D. 完全溶于 完全溶于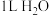 所得溶液会发生可逆反应,此时 所得溶液会发生可逆反应,此时 微粒数目为0.1NA 微粒数目为0.1NA |
您最近一年使用:0次
解题方法
3 . 根据如图所示装置(部分仪器已略去)回答下列有关问题。
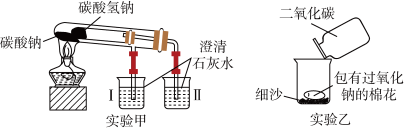
(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是_______ (填“I”或“II”),实验甲中该反应烧杯中发生反应的离子方程式是_______ 。
(2)通过实验甲可证明_______ (填“ ”或“
”或“ ”)更稳定。
”)更稳定。
(3)实验乙用来探究 与
与 的反应,观察到的实验现象为包有
的反应,观察到的实验现象为包有 的棉花着火。写出
的棉花着火。写出 与
与 反应的化学方程式:
反应的化学方程式:_______ ,棉花着火说明该反应的特点是_______ (填“放热反应”、“吸热反应”)。
(4)取10g碳酸钠和碳酸氢钠的混合物充分加热,将生成的 气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为
气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为_______ 。

(1)实验甲在加热过程中能观察到产生白色沉淀的烧杯是
(2)通过实验甲可证明
 ”或“
”或“ ”)更稳定。
”)更稳定。(3)实验乙用来探究
 与
与 的反应,观察到的实验现象为包有
的反应,观察到的实验现象为包有 的棉花着火。写出
的棉花着火。写出 与
与 反应的化学方程式:
反应的化学方程式:(4)取10g碳酸钠和碳酸氢钠的混合物充分加热,将生成的
 气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为
气体通入足量的澄清石灰水中,测得生成沉淀的质量为4.0g。则原混合物中碳酸钠的质量分数为
您最近一年使用:0次
解题方法
4 . 以黄铁矿(主要成分 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。

回答问题:
(1)写出黄铁矿煅烧的化学方程式_______ 。
(2)由炉渣制备还原铁粉的化学方程式为_______ 。
(3)欲得到更纯的 ,反应①应通入
,反应①应通入_______ (填“过量”或“不足量”)的 气体。
气体。
(4)因为 具有
具有_______ 性,导致商品 中不可避免地存在
中不可避免地存在 检验其中含有
检验其中含有 的方法是
的方法是_______ 。
 )为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
)为原料生产硫酸,应将产出的炉渣和尾气进行资源化综合利用,减轻对环境的污染。其中一种流程如下图所示。
回答问题:
(1)写出黄铁矿煅烧的化学方程式
(2)由炉渣制备还原铁粉的化学方程式为
(3)欲得到更纯的
 ,反应①应通入
,反应①应通入 气体。
气体。(4)因为
 具有
具有 中不可避免地存在
中不可避免地存在 检验其中含有
检验其中含有 的方法是
的方法是
您最近一年使用:0次
解题方法
5 . 下列叙述中,正确的是
A. 固体不导电,所以 固体不导电,所以 不是电解质 不是电解质 |
B. 、 、 在水溶液中均能导电,所以它们都是电解质 在水溶液中均能导电,所以它们都是电解质 |
C.熔融的 能导电,所以 能导电,所以 是电解质 是电解质 |
D. 溶于水,在通电条件下才能发生电离 溶于水,在通电条件下才能发生电离 |
您最近一年使用:0次
解题方法
6 . 无水 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和
常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水 。已知:氯化亚砜(
。已知:氯化亚砜( )熔点-101℃,沸点76℃,易水解。
)熔点-101℃,沸点76℃,易水解。
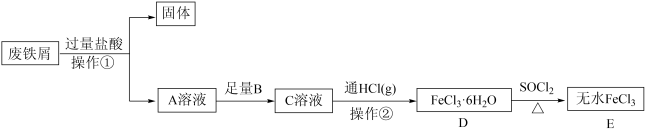
回答问题:
(1)操作①是_______ ,固体是_______ 。
(2)为避免引入新的杂质,试剂B可以选用_______ (填编号)。
a. 溶液 b.
溶液 b. 水 c.
水 c. 水 d.
水 d. 溶液
溶液
(3)操作②是蒸发结晶,加热的同时通入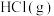 的目的是
的目的是_______ 。
(4)检验D晶体溶液中的阳离子,实验操作是_______ 。
(5)反应D→E的化学方程式为_______ 。
(6)由D转化成E的过程中可能产生少量亚铁盐,写出一种可能的还原剂_______ ,并设计实验检验是否存在
_______ 。
 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和
常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和 杂质)为原料制备无水
杂质)为原料制备无水 。已知:氯化亚砜(
。已知:氯化亚砜( )熔点-101℃,沸点76℃,易水解。
)熔点-101℃,沸点76℃,易水解。
回答问题:
(1)操作①是
(2)为避免引入新的杂质,试剂B可以选用
a.
 溶液 b.
溶液 b. 水 c.
水 c. 水 d.
水 d. 溶液
溶液(3)操作②是蒸发结晶,加热的同时通入
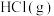 的目的是
的目的是(4)检验D晶体溶液中的阳离子,实验操作是
(5)反应D→E的化学方程式为
(6)由D转化成E的过程中可能产生少量亚铁盐,写出一种可能的还原剂

您最近一年使用:0次
7 . 完成下列问题。
(1)连二亚硫酸钠 ,俗称保险粉,易溶于水,常用于印染、纸张漂白等。回答下列问题:
,俗称保险粉,易溶于水,常用于印染、纸张漂白等。回答下列问题:
① 中S的化合价为
中S的化合价为_______ 。
②向锌粉的悬浮液中通入 ,制备
,制备 ,生成
,生成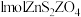 ,反应中转移的电子为
,反应中转移的电子为_______ mol。
(2)高铁酸盐具有极强的氧化性,可作水处理剂。其制备方法为低温下,在 溶液中加入
溶液中加入 浓溶液可析出
浓溶液可析出 。完成下列填空:
。完成下列填空:
①写出上述得到 的化学方程式
的化学方程式_______ 。
②实验室配制 溶液时,需加入少量稀硫酸,用离子方程式解释其原因
溶液时,需加入少量稀硫酸,用离子方程式解释其原因_______ 。
(1)连二亚硫酸钠
 ,俗称保险粉,易溶于水,常用于印染、纸张漂白等。回答下列问题:
,俗称保险粉,易溶于水,常用于印染、纸张漂白等。回答下列问题:①
 中S的化合价为
中S的化合价为②向锌粉的悬浮液中通入
 ,制备
,制备 ,生成
,生成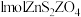 ,反应中转移的电子为
,反应中转移的电子为(2)高铁酸盐具有极强的氧化性,可作水处理剂。其制备方法为低温下,在
 溶液中加入
溶液中加入 浓溶液可析出
浓溶液可析出 。完成下列填空:
。完成下列填空:①写出上述得到
 的化学方程式
的化学方程式②实验室配制
 溶液时,需加入少量稀硫酸,用离子方程式解释其原因
溶液时,需加入少量稀硫酸,用离子方程式解释其原因
您最近一年使用:0次
解题方法
8 . 依据下列实验,预测的实验现象正确的是
| 选项 | 实验内容 | 预测的实验现象 |
| A |  溶液中滴加 溶液中滴加 溶液至过量 溶液至过量 | 产生白色沉淀后沉淀消失 |
| B |  溶液中滴加 溶液中滴加 溶液 溶液 | 溶液变血红色 |
| C |  悬浊液中滴加 悬浊液中滴加 溶液至过量 溶液至过量 | 黄色沉淀全部转化为白色沉淀 |
| D | 酸性 溶液中滴加乙醇至过量 溶液中滴加乙醇至过量 | 溶液紫红色褪去 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
9 . 金属的冶炼与生产、生活及国防军事等领域均密切相关。下列有关金属冶炼的原理错误的是
A.用电解法制取金属钠: |
B.用 作还原剂冶炼金属Ag: 作还原剂冶炼金属Ag: |
C.用 作还原剂冶炼金属V: 作还原剂冶炼金属V: |
D.用Mg活泼金属为还原剂冶炼Ti: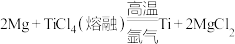 |
您最近一年使用:0次
解题方法
10 . 过氧化钠具有强氧化性,遇木炭、铝粉等还原性物质时可燃烧。下列有关说法不正确的是
A. 与 与 反应时, 反应时, 是氧化剂, 是氧化剂, 是还原剂 是还原剂 |
| B.熔融过氧化钠时不可使用石英坩埚 |
| C.过氧化钠与木炭、铝粉反应时,过氧化钠均表现出强氧化性 |
| D.过氧化钠与二氧化硫反应时可生成亚硫酸钠 |
您最近一年使用:0次



