解题方法
1 . 装置如图所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:___________ 极,C极的电极反应式为___________ ,一段时间后丁中X极附近的颜色逐渐___________ (填“变深”或“变浅”)。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为___________ 。
(3)现用丙装置给铜件镀银,则H应该是___________ (填“铜”或“银”),电镀液是___________ 溶液。常温下,当乙中溶液的c(OH-)=0.1mol·L-1时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为___________ g,甲中溶液的酸性___________ (填“变大”“变小”或“不变”)。

(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成,对应单质的物质的量之比为
(3)现用丙装置给铜件镀银,则H应该是
您最近一年使用:0次
2 . 某研究小组对铁生锈进行研究。
(1)甲同学设计了A、B、C一组实验(如图),探究铁生锈的条件。
①通过上述实验现象分析,可得出铁生锈的外部条件是___________ 。
②由于与金属接触的介质不同,金属腐蚀分成不同类型,本实验中铁生锈属于___________ ,正极电极反应式为___________ 。
③实验B所用的水要经过___________ 处理;植物油的作用是___________ 。
④实验C中碱石灰的作用是___________ 。
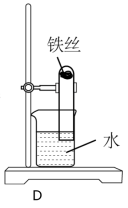
(2)乙同学为了达到同样目的,设计了实验D(如图),发现一段时间后,试管中的液面升高,其原因是___________ ,该实验___________ (填“能”或“不能”)说明水对铁钉生锈产生影响。
(1)甲同学设计了A、B、C一组实验(如图),探究铁生锈的条件。

①通过上述实验现象分析,可得出铁生锈的外部条件是
②由于与金属接触的介质不同,金属腐蚀分成不同类型,本实验中铁生锈属于
③实验B所用的水要经过
④实验C中碱石灰的作用是
(2)乙同学为了达到同样目的,设计了实验D(如图),发现一段时间后,试管中的液面升高,其原因是
您最近一年使用:0次
3 . 下列说法正确的是
①标准状况下,6.02×1023个分子所占的体积约是22.4 L
②0.5 mol H2所占体积为11.2 L
③标准状况下,1 mol H2O的体积为22.4 L
④常温常压下,28 g CO与N2的混合气体所含的原子数为2NA
⑤各种气体的气体摩尔体积都约为22.4 L·mol−1
⑥标准状况下,体积相同的气体的分子数相同
①标准状况下,6.02×1023个分子所占的体积约是22.4 L
②0.5 mol H2所占体积为11.2 L
③标准状况下,1 mol H2O的体积为22.4 L
④常温常压下,28 g CO与N2的混合气体所含的原子数为2NA
⑤各种气体的气体摩尔体积都约为22.4 L·mol−1
⑥标准状况下,体积相同的气体的分子数相同
| A.①③⑤ | B.④⑥ | C.③④⑥ | D.①④⑥ |
您最近一年使用:0次
名校
解题方法
4 . 下列关于物质性质的比较,正确的是
A.原子半径大小: | B.氢化物稳定性: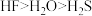 |
C.酸性强弱: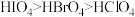 | D.碱性强弱: |
您最近一年使用:0次
2024-08-12更新
|
192次组卷
|
3卷引用:第四章 物质结构 元素周期律【单元测试B卷】
解题方法
5 . 氯化铁是常用的金属刻蚀剂。工业上用硫铁矿渣(主要成分为 、
、 、FeO)制备氯化铁溶液,流程如下。
、FeO)制备氯化铁溶液,流程如下。___________ 。
(2)反应釜中 与盐酸反应的化学方程式为
与盐酸反应的化学方程式为___________ 。
(3)下列说法正确的是___________ 。
a.加入反应釜中的盐酸可用稀硫酸代替
b.混合器中加入过氧化氢溶液的目的是将 氧化为
氧化为
(4)用氯化铁溶液刻蚀覆铜板可制作印刷电路板,在刻蚀过程中,氯化铁与铜反应生成氯化亚铁和氯化铜,该反应的离子方程式是___________ 。
 、
、 、FeO)制备氯化铁溶液,流程如下。
、FeO)制备氯化铁溶液,流程如下。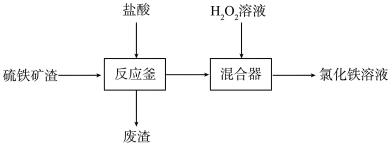
(2)反应釜中
 与盐酸反应的化学方程式为
与盐酸反应的化学方程式为(3)下列说法正确的是
a.加入反应釜中的盐酸可用稀硫酸代替
b.混合器中加入过氧化氢溶液的目的是将
 氧化为
氧化为
(4)用氯化铁溶液刻蚀覆铜板可制作印刷电路板,在刻蚀过程中,氯化铁与铜反应生成氯化亚铁和氯化铜,该反应的离子方程式是
您最近一年使用:0次
2024-08-12更新
|
551次组卷
|
4卷引用:第一章 物质及变化【单元测试B卷】
名校
解题方法
6 . 已知: ,
,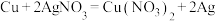 ,则下列判断正确的是
,则下列判断正确的是
 ,
,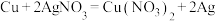 ,则下列判断正确的是
,则下列判断正确的是A.还原性: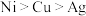 | B.氧化性: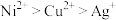 |
C.还原性: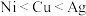 | D.氧化性: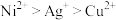 |
您最近一年使用:0次
2024-08-12更新
|
1213次组卷
|
3卷引用:第一章 物质及变化【单元测试A卷】
解题方法
7 . 下列关于金属铁及其化合物的说法错误的是
A. 能与 能与 反应生成 反应生成 ,故钢瓶不能用于保存液氯 ,故钢瓶不能用于保存液氯 |
| B.氯化铁溶液可腐蚀覆铜板,可用于印刷电路板 |
C. 在空气中较难保存 在空气中较难保存 |
D.用 溶液检验 溶液检验 是否变质 是否变质 |
您最近一年使用:0次
2024-08-12更新
|
273次组卷
|
3卷引用:第三章 铁 金属材料【单元测试B卷】
8 . 回答下列问题。
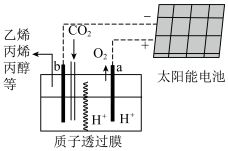
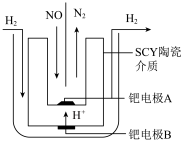
(1)据报道以二氧化碳为原料采用特殊的电极电解强酸性的二氧化碳水溶液可得到多种燃料,其原理如图所示。电解时其中b极上生成乙烯的电极反应式为___________ 。___________ 极,电极反应式为___________ 。___________ ,阳极产生气体的化学式为___________ 。
(1)据报道以二氧化碳为原料采用特殊的电极电解强酸性的二氧化碳水溶液可得到多种燃料,其原理如图所示。电解时其中b极上生成乙烯的电极反应式为
您最近一年使用:0次
2024高三·全国·专题练习
9 . 下列关于反应能量的说法正确的是
| A.若反应A(g)=B(g) ΔH<0,说明物质A(g)比物质B(g)稳定,分子内共价键键能A比B大 |
| B.若Mg(s)+CuSO4(aq)=MgSO4(aq)+Cu(s) ΔH=a kJ·mol-1,则a<0 |
C.101 kPa时,2H2(g)+O2(g)=2H2O(g) ΔH=-Q kJ·mol-1,则H2的燃烧热为 Q kJ·mol-1 Q kJ·mol-1 |
| D.H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1,则相同条件下含1 mol NaOH的氢氧化钠溶液与含0.5 mol H2SO4的浓硫酸混合后放出57.3 kJ的热量 |
您最近一年使用:0次
解题方法
10 . 到目前为止,由化学能转变的热能或电能仍然是人类使用的主要能源。
(1)从能量变化角度研究反应: 。下图能正确表示该反应中能量变化的是
。下图能正确表示该反应中能量变化的是_______ (填字母)。_______ (填“正”或“负”)极,可观察到Cu棒上有气泡生成,写出Cu棒上的电极反应式_______ 。若反应过程中Zn棒减少的质量为3.25 g,则生成的氢气在标准状况下的体积为_______ L。
②若电解质为硫酸铜溶液,则Cu棒上发生_______ (填“氧化”或“还原”)反应,Zn棒上发生的电极反应式为_______ 。
③若实验过程中发现Zn棒上产生了氢气,请说明原因_______ 。
(1)从能量变化角度研究反应:
 。下图能正确表示该反应中能量变化的是
。下图能正确表示该反应中能量变化的是

②若电解质为硫酸铜溶液,则Cu棒上发生
③若实验过程中发现Zn棒上产生了氢气,请说明原因
您最近一年使用:0次



