1 . 实验是学习化学、探究化学过程的重要途径。下列装置不能达到相应实验目的的是
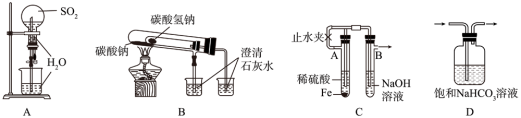

| A.进行喷泉实验 | B.比较 与 与 的热稳定性 的热稳定性 |
C.制备 沉淀 沉淀 | D.除去 中混有的 中混有的 气体 气体 |
您最近一年使用:0次
解题方法
2 . 氮及其化合物的价类二维图如下图所示。

回答下列问题:
(1)从氮元素化合价变化的角度分析,A、C、D、F中既有氧化性又有还原性的有____ (填化学式)。
(2)B分子中含有18个电子,其电子式为_______ ;A与NaClO溶液反应制备B的离子方程式为_______ 。
(3)将气体A充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入气体E(两端用夹子K1、K2夹好),在一定温度下按下图装置进行实验。

(4)工业上以A为原料生产G,反应路线为A→D→E→F→G,假设生产过程中氮的转化率为100%,则生产80kgG,共消耗标准状况下O2的体积为_______ m3。

回答下列问题:
(1)从氮元素化合价变化的角度分析,A、C、D、F中既有氧化性又有还原性的有
(2)B分子中含有18个电子,其电子式为
(3)将气体A充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入气体E(两端用夹子K1、K2夹好),在一定温度下按下图装置进行实验。

| 操作步骤 | 实验现象 | 解释原因 |
| 打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中 | ①Y管中 | ②C为产物之一,则反应的化学方程式为 |
| 将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝集 |
| 打开K2 | ③ | ④ |
您最近一年使用:0次
3 . 实验室有不纯的过氧化钠,欲用排水法测量其纯度,准确称量该样品8.0克装入C装置中。实验操作如下,请完成下列问题:
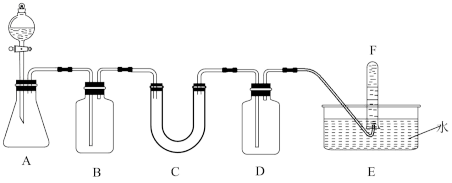
(1)A是实验室常见制备 的装置,锥形瓶内盛有某不溶于水的块状固体,锥形瓶上方盛装盐酸的仪器名称:
的装置,锥形瓶内盛有某不溶于水的块状固体,锥形瓶上方盛装盐酸的仪器名称:_______ , 锥形瓶内发生反应的离子方程式为_______ 。
(2)填写下表中的空白
(3)写出C装置中主要反应的化学方程式:_______ 。
(4)欲检验F中收集的气体,其具体操作步骤及现象:_______ 。
(5)缓缓通入过量的 后,收集到气体为1120.0mL(标准状况下),则过氧化钠的纯度为
后,收集到气体为1120.0mL(标准状况下),则过氧化钠的纯度为_______ %(三位有效数字)。

(1)A是实验室常见制备
 的装置,锥形瓶内盛有某不溶于水的块状固体,锥形瓶上方盛装盐酸的仪器名称:
的装置,锥形瓶内盛有某不溶于水的块状固体,锥形瓶上方盛装盐酸的仪器名称:(2)填写下表中的空白
| 装置编号 | 加入试剂 | 加入该试剂的目的 |
| B | ||
| D |
(4)欲检验F中收集的气体,其具体操作步骤及现象:
(5)缓缓通入过量的
 后,收集到气体为1120.0mL(标准状况下),则过氧化钠的纯度为
后,收集到气体为1120.0mL(标准状况下),则过氧化钠的纯度为
您最近一年使用:0次
2022-01-25更新
|
314次组卷
|
3卷引用:湖北省部分市州2021-2022学年高一上学期期末联合调研考试化学试题
湖北省部分市州2021-2022学年高一上学期期末联合调研考试化学试题(已下线)考点13 钠及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)河南省沈丘县长安高级中学2022-2023学年高一上学期期中考试化学试题
4 . 用下列操作或装置进行相应实验,能达到实验目的的是
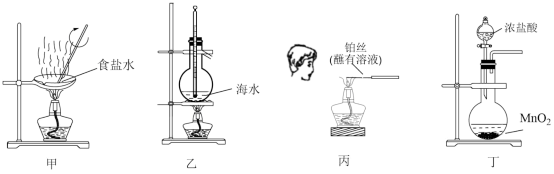

A.用装置甲获得 晶体 晶体 |
| B.用装置乙制取蒸馏水 |
C.用操作丙检验溶液中是否含有 |
| D.用装置丁制取氯气 |
您最近一年使用:0次
2022-01-24更新
|
264次组卷
|
2卷引用:江苏省常州市教育学会2021-2022学年高一上学期期末学业水平监测化学试题
名校
5 . 下列操作能达到相应实验目的的是
| 实验目的 | 操作 | |
| A | 检验 溶液是否变质 溶液是否变质 | 取少量加入到酸性 溶液中 溶液中 |
| B | 测定家用84消毒液的 | 用洁净的玻璃棒蘸取少许消毒液滴在 试纸上 试纸上 |
| C | 除去 中的少量 中的少量 | 将混合气体通过盛有饱和 溶液的洗气瓶 溶液的洗气瓶 |
| D | 实验室制备 胶体 胶体 | 向沸水中逐滴加入饱和 溶液,边加边搅拌 溶液,边加边搅拌 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-01-25更新
|
276次组卷
|
2卷引用:山东省威海市2021-2022学年高一上学期期末考试化学试题
6 . 实验是探究化学过程的重要途径。用下列实验装置进行实验,能达到相应实验目的的是
 | 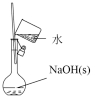 |  |  |
A.制备 胶体 胶体 | B.配制  溶液 溶液 | C.确定溶液中是否含有 元素 元素 | D.用 试纸测新制氯水的 试纸测新制氯水的 值 值 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
7 . Ⅰ.现有混有少量SO2杂质的CO2气体,请选用适当的实验装置,收集纯净干燥的CO2气体。
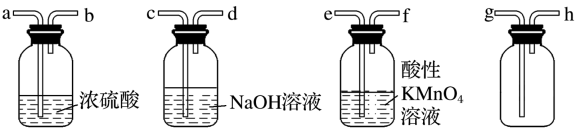
(1)要达到实验目的,按气流从左到右,各接口连接顺序正确的是_______ (填字母)。
(2)下列溶液或用品中:①澄清石灰水;②H2S溶液;③酸性KMnO4溶液;④溴水;⑤Ba(NO3)2溶液;⑥品红溶液;⑦湿润的蓝色石蕊试纸。不能区别SO2和CO2气体的是_______。
Ⅱ. 前几年我国多地发生了严重的雾霾天气,这种天气的形成与汽车尾气排放有关。汽车尾气中常含有CO、NOx等气体,为减轻污染,一般汽车都加装了“催化净化器”,可将汽车尾气中的有毒气体转化为无污染的气体。某化学兴趣小组在实验室模拟汽车尾气处理,设计了下图所示装置(部分夹持装置已略去)。

(3)装置(Ⅲ)的主要作用为_______ 。
(4)停止加热,打开活塞K,放入适量氧气时,装置(Ⅱ)中可观察到的现象是_______ 。
(5)该套装置的不完善之处是_______ 。
(6)汽车尾气中含有CO和NOx,消除它们对大气污染的方法是安装催化转化器,使它们发生反应生成两种无毒的气体,其中一种是单质,该反应的化学方程式为_______ 。
(7)工业上常用纯碱液来吸收NOx,有关反应的化学方程式为2NO2+Na2CO3=NaNO2+NaNO3+CO2、NO2+NO+Na2CO3=2NaNO2+CO2。现有标准状况下a L NO2和b L NO的混合气体恰好被200 mL Na2CO3溶液完全吸收,则a、b应满足的关系为_______ 。Na2CO3溶液的物质的量浓度为_______ mol·L-1。

(1)要达到实验目的,按气流从左到右,各接口连接顺序正确的是
(2)下列溶液或用品中:①澄清石灰水;②H2S溶液;③酸性KMnO4溶液;④溴水;⑤Ba(NO3)2溶液;⑥品红溶液;⑦湿润的蓝色石蕊试纸。不能区别SO2和CO2气体的是_______。
| A.①⑤⑦ | B.①⑤ | C.①⑦ | D.②③④⑤⑥ |
Ⅱ. 前几年我国多地发生了严重的雾霾天气,这种天气的形成与汽车尾气排放有关。汽车尾气中常含有CO、NOx等气体,为减轻污染,一般汽车都加装了“催化净化器”,可将汽车尾气中的有毒气体转化为无污染的气体。某化学兴趣小组在实验室模拟汽车尾气处理,设计了下图所示装置(部分夹持装置已略去)。

(3)装置(Ⅲ)的主要作用为
(4)停止加热,打开活塞K,放入适量氧气时,装置(Ⅱ)中可观察到的现象是
(5)该套装置的不完善之处是
(6)汽车尾气中含有CO和NOx,消除它们对大气污染的方法是安装催化转化器,使它们发生反应生成两种无毒的气体,其中一种是单质,该反应的化学方程式为
(7)工业上常用纯碱液来吸收NOx,有关反应的化学方程式为2NO2+Na2CO3=NaNO2+NaNO3+CO2、NO2+NO+Na2CO3=2NaNO2+CO2。现有标准状况下a L NO2和b L NO的混合气体恰好被200 mL Na2CO3溶液完全吸收,则a、b应满足的关系为
您最近一年使用:0次
8 . 下图所示实验方案无法 达到预期实验目的的是
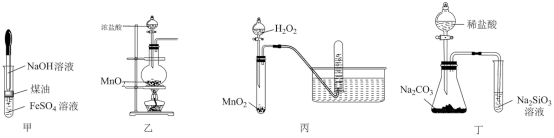
A.用甲制备少量 |
B.用乙制备少量 |
C.用丙制备并收集 |
| D.用丁比较Cl、C、Si的非金属性强弱 |
您最近一年使用:0次
2022-01-23更新
|
317次组卷
|
3卷引用: 浙江省衢州市2021-2022学年高一上学期期末教学质量检测化学试题
浙江省衢州市2021-2022学年高一上学期期末教学质量检测化学试题(已下线)【2023】【高一下】【期中考】【北斗联盟】【高中化学】【娄斌收集】浙江省淳安县汾口中学2023-2024学年高一上学期期末模拟(1月月考)化学试题
名校
解题方法
9 . SO2和焦亚硫酸钠(Na2S2O5)可用作食品添加剂。回答下列问题:
(1)实验室利用铜与浓硫酸制取SO2的化学方程式为___________ ,发生装置为___________ (填字母)。
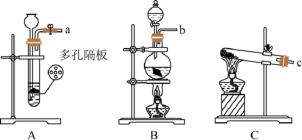
(2)焦亚硫酸钠易被氧化而变质,选用下列试剂设计实验方案,检验焦亚硫酸钠样品氧化变质的程度。
已知:2NaHSO3 Na2S2O5+H2O。
Na2S2O5+H2O。
试剂:稀盐酸、稀H2SO4、稀HNO3、BaCl2溶液、酸性KMnO4溶液、H2O2溶液
(3)某小组利用下列装置测定空气中SO2的含量。
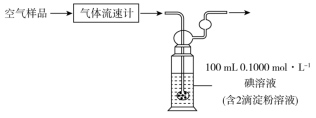
已知该反应的化学方程式为:SO2+I2+2H2O=H2SO4+2HI,若空气流速为a m3·min-1,当观察到___________ 时,结束计时,测定耗时t min。假定样品中的SO2可被溶液充分吸收,该空气样品中SO2的含量是___________ mg·m-3。
(1)实验室利用铜与浓硫酸制取SO2的化学方程式为

(2)焦亚硫酸钠易被氧化而变质,选用下列试剂设计实验方案,检验焦亚硫酸钠样品氧化变质的程度。
已知:2NaHSO3
 Na2S2O5+H2O。
Na2S2O5+H2O。试剂:稀盐酸、稀H2SO4、稀HNO3、BaCl2溶液、酸性KMnO4溶液、H2O2溶液
| 实验编号 | 实验步骤 | 现象 | 结论 |
| Ⅰ | 取少量样品,加入除氧蒸馏水 | 固体完全溶解得到无色溶液 | / |
| Ⅱ | 取实验I的溶液, | 样品已氧化变质 | |
| Ⅲ | 另取实验I的溶液, | 样品未完全氧化变质 |

已知该反应的化学方程式为:SO2+I2+2H2O=H2SO4+2HI,若空气流速为a m3·min-1,当观察到
您最近一年使用:0次
名校
解题方法
10 . 以二氧化锰和浓盐酸为主要原料制取氯气,并设计了如图所示装置(其中A是连有注射器针头的橡皮管,针头已插入并穿过橡皮塞)。
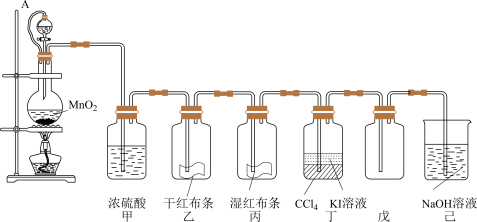
试回答下列问题:
(1)乙和丙中的现象分别是_____ ;由上述现象可得出结论:_____ (写化学式)具有漂白作用;
(2)圆底烧瓶内发生反应的化学方程式为_____ ;分液漏斗与烧瓶连接橡皮管的目的是_____ ;
(3)ClO2气体是一种新型高效含氯消毒剂。实验室可通过以下反应制2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O,试回答下列问题。若反应共产生了0.2mol气体,消耗还原剂的质量为_____ g。ClO2的有效氯含量为_____ (有效氯含量指每克含氯消毒剂的氧化能力相当于多少克Cl2的氧化能力)。
(4)用ClO2气体可去除地下水中Mn2+,生成难溶于水的MnO2,该反应的离子方程式为_____ 。

试回答下列问题:
(1)乙和丙中的现象分别是
(2)圆底烧瓶内发生反应的化学方程式为
(3)ClO2气体是一种新型高效含氯消毒剂。实验室可通过以下反应制2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O,试回答下列问题。若反应共产生了0.2mol气体,消耗还原剂的质量为
(4)用ClO2气体可去除地下水中Mn2+,生成难溶于水的MnO2,该反应的离子方程式为
您最近一年使用:0次



