名校
解题方法
1 . 下列实验过程可以达到实验目的的是
| 选项 | 实验目的 | 实验过程 |
| A | 配制 的NaOH溶液 的NaOH溶液 | 称取4.0g固体NaOH于烧杯中,加入少量蒸馏水溶解,转移至250mL容量瓶中定容 |
| B | 鉴别 和 和 | 分别将固体置于试管中加热,称量加热前后固体的质量 |
| C | 探究 的氧化性 的氧化性 | 向盛有2mL酸性 溶液的试管中滴入 溶液的试管中滴入 的溶液,观察溶液颜色变化 的溶液,观察溶液颜色变化 |
| D | 检验 样品是否变质 样品是否变质 | 将待测样品溶于水,加入硝酸酸化的氯化钡溶液,观察实验现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 高铁酸盐是优良的多功能水处理剂。K2FeO4为紫色固体,可溶于水,微溶于浓KOH溶液,难溶于有机物;在0~5℃、强碱性溶液中比较稳定,在酸性、中性溶液中易分解放出O2.某实验小组制备高铁酸钾(K2FeO4)并测定产品纯度。回答下列问题:
Ⅰ.制备K2FeO4
装置如下图所示,夹持、加热等装置略。
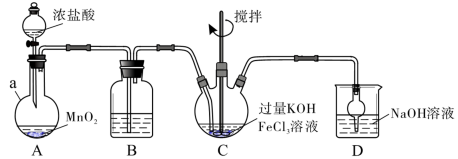
(1)仪器a的名称是___________ ,装置B中除杂质所用试剂是___________ ,装置D的作用是___________ 。
(2)A中发生反应的离子方程式为___________ 。
(3)C中反应为放热反应,而反应温度须控制在0~5℃,采用的控温方法为___________ ,反应中KOH必须过量的原因是___________ 。
(4)写出C中总反应的离子方程式:___________ 。C中混合物经重结晶、有机物洗涤纯化、真空干燥,得到高铁酸钾晶体。
Ⅱ.K2FeO4产品纯度的测定
准确称取1.00 g制得的晶体,配成250 mL溶液,准确量取25.00 mL K2FeO4溶液放入锥形瓶,加入足量CrCl3和NaOH溶液,振荡,再加入稀硫酸酸化后得Fe3+和Cr2O ,滴入几滴二苯胺磺酸钠作指示剂,用0.0500 mol/L(NH4)2Fe(SO4)2标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗(NH4)2Fe(SO4)2标准溶液28.00 mL。
,滴入几滴二苯胺磺酸钠作指示剂,用0.0500 mol/L(NH4)2Fe(SO4)2标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗(NH4)2Fe(SO4)2标准溶液28.00 mL。
(5)根据以上数据,样品中K2FeO4的质量分数为___________ 。若(NH4)2Fe(SO4)2标准溶液部分变质,会使测定结果___________ (填“偏高”“偏低”或“无影响”)。
Ⅰ.制备K2FeO4
装置如下图所示,夹持、加热等装置略。

(1)仪器a的名称是
(2)A中发生反应的离子方程式为
(3)C中反应为放热反应,而反应温度须控制在0~5℃,采用的控温方法为
(4)写出C中总反应的离子方程式:
Ⅱ.K2FeO4产品纯度的测定
准确称取1.00 g制得的晶体,配成250 mL溶液,准确量取25.00 mL K2FeO4溶液放入锥形瓶,加入足量CrCl3和NaOH溶液,振荡,再加入稀硫酸酸化后得Fe3+和Cr2O
 ,滴入几滴二苯胺磺酸钠作指示剂,用0.0500 mol/L(NH4)2Fe(SO4)2标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗(NH4)2Fe(SO4)2标准溶液28.00 mL。
,滴入几滴二苯胺磺酸钠作指示剂,用0.0500 mol/L(NH4)2Fe(SO4)2标准溶液滴定至终点(溶液显浅紫红色),平行测定三次,平均消耗(NH4)2Fe(SO4)2标准溶液28.00 mL。(5)根据以上数据,样品中K2FeO4的质量分数为
您最近一年使用:0次
2021-04-07更新
|
758次组卷
|
5卷引用:天津市红桥区2021届高三一模考试化学试题
天津市红桥区2021届高三一模考试化学试题天津市红桥区2020-2021学年高三下学期第一次教学质量调查(一模)化学试题新疆师范大学附属中学2021-2022学年高三9月月考化学试题(已下线)二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)湖南省长沙市雅礼中学2024届高三上学期月考试卷(一)化学试题
3 . 下列实验操作或设计与实验现象、结论均正确的是
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| A | 取少量某溶液于试管中,加入 浓溶液并加热,用湿润的红色石蕊试纸检验产生的气体 浓溶液并加热,用湿润的红色石蕊试纸检验产生的气体 | 湿润的红色石蕊试纸变蓝 | 溶液中一定含有 |
| B | 向 浓度为 浓度为 的 的 溶液中逐滴加入等浓度的 溶液中逐滴加入等浓度的 溶液 溶液 | 溶液褪色 |  漂白溶液,表现强氧化性 漂白溶液,表现强氧化性 |
| C | 取少量 固体样品溶于蒸馏水,加入足量稀盐酸,再加入适量 固体样品溶于蒸馏水,加入足量稀盐酸,再加入适量 溶液 溶液 | 白色沉淀产生 | 样品已经变质 |
| D | 室温下,用 试纸分别测定浓度均为 试纸分别测定浓度均为 的 的 溶液和 溶液和 溶液的 溶液的 | 溶液 : : 约为9, 约为9, 约为10 约为10 | 酸性: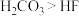 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-06更新
|
243次组卷
|
2卷引用:湖南省湖湘教育三新探索协作体2021-2022学年高三上学期期中联考化学试题
4 . 根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 室温下,用pH试纸测得:0.1mol·L-1 Na2SO3溶液的pH约为10;0.1mol·L-1 NaHSO3溶液的pH约为5。 |  结合H+的能力比 结合H+的能力比 的强 的强 |
B | 将FeCl2样品溶于试管中,加入氯水,继续滴加KSCN溶液,溶液变红 | FeCl2样品已经被氧化变质 |
C | 向2支盛有2 mL相同浓度银氨溶液的试管中分别加入2滴相同浓度的NaCl和NaI溶液,一支试管中产生黄色沉淀,另一支中无明显现象 | Ksp(AgCl) > Ksp(AgI) |
D | 向CuSO4溶液中加入铁粉,有红色固体析出 | Fe2+的氧化性强于Cu2+的氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
5 . 下列实验的现象描述和结论相匹配的是
| 实验操作 | 实验现象 | 实验结论 | |
| A | 用导线将铜片和锌片连接起来插入盛稀硫酸的烧杯中 | 锌片、铜片上都有大量气泡 | 锌片失去的部分电子通过导线流向铜片 |
| B | 将某气体通入酸性KMnO4溶液 | 溶液褪色 | 该气体一定是SO2 |
| C | 向含有SO2的BaCl2溶液中通气体X | 产生白色沉淀 | X一定表现氧化性 |
| D | 将亚硫酸钠样品溶于水,滴加稀盐酸酸化的Ba(NO3)2溶液 | 产生白色沉淀 | 亚硫酸钠样品已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 下列实验操作、现象和结论正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 将Fe(NO3)2样品溶于稀硫酸,滴加KSCN溶液 | 溶液变红 | Fe(NO3)2样品已变质 |
| B | 向Na2S溶液中滴加足量稀盐酸 | 有气泡生成 | 非金属性:Cl>S |
| C | 向稀硫酸酸化的H2O2溶液中滴入FeCl2溶液 | 溶液变黄色 | 氧化性:H2O2>Fe3+ |
| D | 溶有SO2的BaCl2溶液中通入气体X | 有白色沉淀生成 | X一定是 Cl2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-12-02更新
|
335次组卷
|
3卷引用:新疆乌鲁木齐市第八中学2020-2021学年高二上学期期末考试化学试题
名校
解题方法
7 . 过氧化钠常用作漂白剂、杀菌剂、消毒剂,能与水和二氧化碳等物质发生反应,保存不当时容易变质。某实验小组以过氧化钠为研究对象进行了如下实验。
(1)探究一包 样品是否已经变质:取少量样品,将其溶解,加入
样品是否已经变质:取少量样品,将其溶解,加入____ 溶液,充分振荡后有白色沉淀,证明 已经变质。
已经变质。
(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了mg样品,并设计如图所示装置来测定过氧化钠的质量分数。
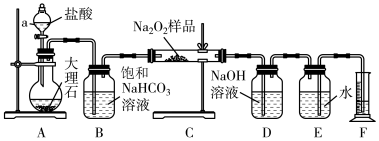
①装置中仪器a的名称是____ ,装置D的作用是____ 。
②将仪器连接好以后,必须进行的第一步操作是____ 。
③写出装置C中发生的主要反应的化学方程式:____ 。
④反应结束后,在读取实验中生成气体的体积时,你认为合理的是____ (填序号)。
A.读取气体体积前,需冷却到室温
B.调整量筒使E、F内液面高度相同
C.视线与凹液面的最低点相平时读取量筒中水的体积
⑤读出量筒内水的体积后,将其折算成氧气的质量为ng,则样品中过氧化钠的质量分数为____ ×100%。
⑥压强不变时在一个密闭容器中放入足量过氧化钠固体,然后充入等体积的 和
和 ,电火花引燃后充分反应,恢复至原温度,余下气体的体积为原体积的
,电火花引燃后充分反应,恢复至原温度,余下气体的体积为原体积的____ 。
(1)探究一包
 样品是否已经变质:取少量样品,将其溶解,加入
样品是否已经变质:取少量样品,将其溶解,加入 已经变质。
已经变质。(2)该实验小组为了粗略测定过氧化钠的质量分数,称取了mg样品,并设计如图所示装置来测定过氧化钠的质量分数。

①装置中仪器a的名称是
②将仪器连接好以后,必须进行的第一步操作是
③写出装置C中发生的主要反应的化学方程式:
④反应结束后,在读取实验中生成气体的体积时,你认为合理的是
A.读取气体体积前,需冷却到室温
B.调整量筒使E、F内液面高度相同
C.视线与凹液面的最低点相平时读取量筒中水的体积
⑤读出量筒内水的体积后,将其折算成氧气的质量为ng,则样品中过氧化钠的质量分数为
⑥压强不变时在一个密闭容器中放入足量过氧化钠固体,然后充入等体积的
 和
和 ,电火花引燃后充分反应,恢复至原温度,余下气体的体积为原体积的
,电火花引燃后充分反应,恢复至原温度,余下气体的体积为原体积的
您最近一年使用:0次
8 . 下列根据实验操作和实验现象所得出的结论正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将某气体通入淀粉KI溶液中 | 溶液变成蓝色 | 该气体一定是氯气 |
| B | 向AgNO3溶液中滴加过量氨水 | 得到澄清溶液 | Ag+和NH3 H2O可以大量共存 H2O可以大量共存 |
| C | 在某盐溶液中加Al,然后加入少量NaOH溶液,加热 | 产生的气体可使湿润的红色石蕊试纸变蓝色 | 该盐中含有NO |
| D | 将Fe(NO3)2样品溶于稀硫酸后,滴加KSCN溶液 | 溶液变血红色 | Fe(NO3)2样品已变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 为了测定某氯化钙样品中钙元素的含量,进行如下实验(实验步骤已打乱 ):
①将沉淀全部放入锥形瓶中,加入足量的10%H2SO4和适量的蒸馏水,使沉淀完全溶解,溶液呈酸性,加热至75℃,趁热用0.0500mol·L-1KMnO4溶液进行滴定,记录所用KMnO4溶液的体积。
②过滤并洗涤沉淀。
③准确称取氯化钙样品0.2400g,放入烧杯中,加入适量6mol·L-1的盐酸和适量蒸馏水使样品完全溶解,再滴加35.00mL0.2500mol·L-1(NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀。经检验,Ca2+已沉淀完全。
④再重复以上操作2次并进行数据处理。
完成下列各题:
(1)上面的实验步骤合理的顺序是___ (填序号)。
(2)写出步骤①中加入KMnO4溶液后发生反应的离子方程式___ 。
(3)滴定终点判断的依据是___ 。
(4)某次实验滴定结束时滴定管内的液面见图,则此时液面读数为___ mL。

(5)实验最终测得氯化钙样品中钙元素的质量分数38.00%(样品中不含其它含有钙元素的杂质),下列说法能合理解释该实验结果的是___ 。
A.酸性高锰酸钾溶液已部分变质
B.滴定过程中,用蒸馏水冲洗锥形瓶内壁上的KMnO4溶液
C.滴定时有部分高锰酸钾溶液滴在了实验台上
D.酸式滴定管用蒸馏水洗过后又用所要盛装的溶液润洗
①将沉淀全部放入锥形瓶中,加入足量的10%H2SO4和适量的蒸馏水,使沉淀完全溶解,溶液呈酸性,加热至75℃,趁热用0.0500mol·L-1KMnO4溶液进行滴定,记录所用KMnO4溶液的体积。
②过滤并洗涤沉淀。
③准确称取氯化钙样品0.2400g,放入烧杯中,加入适量6mol·L-1的盐酸和适量蒸馏水使样品完全溶解,再滴加35.00mL0.2500mol·L-1(NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀。经检验,Ca2+已沉淀完全。
④再重复以上操作2次并进行数据处理。
完成下列各题:
(1)上面的实验步骤合理的顺序是
(2)写出步骤①中加入KMnO4溶液后发生反应的离子方程式
(3)滴定终点判断的依据是
(4)某次实验滴定结束时滴定管内的液面见图,则此时液面读数为

(5)实验最终测得氯化钙样品中钙元素的质量分数38.00%(样品中不含其它含有钙元素的杂质),下列说法能合理解释该实验结果的是
A.酸性高锰酸钾溶液已部分变质
B.滴定过程中,用蒸馏水冲洗锥形瓶内壁上的KMnO4溶液
C.滴定时有部分高锰酸钾溶液滴在了实验台上
D.酸式滴定管用蒸馏水洗过后又用所要盛装的溶液润洗
您最近一年使用:0次
2021-01-29更新
|
229次组卷
|
3卷引用:浙江省嘉兴市2020-2021学年高二上学期期末测试化学试题
10 . 现有一瓶Na2O2因保管不善,部分变质转化为NaOH、Na2CO3.某小组设计实验,测定样品中Na2O2的纯度。
实验I:
连接好图1装置,检查气密性。在倒置量筒中充满水,准确称取10.0 g样品,加入锥形瓶中,并加入少量MnO2粉末,从分液漏斗中缓慢滴加水,至锥形瓶中无气泡产生,待整个装置冷却到室温,读取量筒内气体的数据。
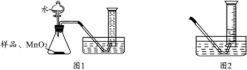
(1)实验中加MnO2的目的是___________ 。
(2)若冷却至室温后水槽的图示如图2,则应进行的操作是___________ 。
小红提出实验I的误差较大,设计完成了实验II。
实验II:
连接好图3装置,检查气密性。在碱式滴定管中加入适量水,准确称取10.0 g样品,加入锥形瓶中,并加入少量MnO2粉末。准确读取碱式滴定管读数V1 mL,从分液漏斗中缓慢滴加水,至锥形瓶中无气泡产生,待整个装置冷却到室温,读取碱式滴定管读数V2 mL。
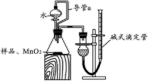
(3)导管a的作用:___________ 、___________ 。
(4)已知该实验条件下,气体摩尔体积为Vm L/mol,则样品中Na2O2的纯度为___________ 。
(5)下列操作导致测量样品纯度偏大的是___________ 。
a.实验前读数时,俯视刻度线读数
b.实验结束读数时,未冷却至室温
c.实验结束读数时,仰视刻度线读数
d.实验结束读数时,量气装置中右侧液面高于左侧液面
实验I:
连接好图1装置,检查气密性。在倒置量筒中充满水,准确称取10.0 g样品,加入锥形瓶中,并加入少量MnO2粉末,从分液漏斗中缓慢滴加水,至锥形瓶中无气泡产生,待整个装置冷却到室温,读取量筒内气体的数据。
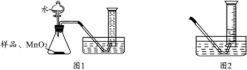
(1)实验中加MnO2的目的是
(2)若冷却至室温后水槽的图示如图2,则应进行的操作是
小红提出实验I的误差较大,设计完成了实验II。
实验II:
连接好图3装置,检查气密性。在碱式滴定管中加入适量水,准确称取10.0 g样品,加入锥形瓶中,并加入少量MnO2粉末。准确读取碱式滴定管读数V1 mL,从分液漏斗中缓慢滴加水,至锥形瓶中无气泡产生,待整个装置冷却到室温,读取碱式滴定管读数V2 mL。
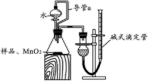
(3)导管a的作用:
(4)已知该实验条件下,气体摩尔体积为Vm L/mol,则样品中Na2O2的纯度为
(5)下列操作导致测量样品纯度偏大的是
a.实验前读数时,俯视刻度线读数
b.实验结束读数时,未冷却至室温
c.实验结束读数时,仰视刻度线读数
d.实验结束读数时,量气装置中右侧液面高于左侧液面
您最近一年使用:0次



