解题方法
1 . X、Y、Z、W、R是短周期元素,原子序数依次增大。X原子核外各层电子数之比为 ,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:
,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:
(1)元素X的最高价氧化物的电子式为___________ ;元素Z的离子结构示意图为___________ 。
(2)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为___________ 。
(3)元素W位于周期表的第___________ 族,其非金属性比R弱,用原子结构的知识解释原因:___________ 。
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液做该氧化物的吸收剂,写出吸收剂与足量该氧化物反应的离子方程式:___________ 。
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为 ,则该反应的化学方程式为
,则该反应的化学方程式为___________ 。
 ,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:
,Y原子和Z原子的核外电子数之和为20,W和R是同周期相邻元素,Y的氧化物和R的氧化物均能形成酸雨。请回答下列问题:(1)元素X的最高价氧化物的电子式为
(2)单质铜和元素Y的最高价氧化物对应水化物的稀溶液发生反应的化学方程式为
(3)元素W位于周期表的第
(4)R的一种氧化物能使品红溶液褪色,工业上用Y的气态氢化物的水溶液做该氧化物的吸收剂,写出吸收剂与足量该氧化物反应的离子方程式:
(5)Y和Z组成的化合物ZY,被大量用于制造电子元件。工业上用Z的氧化物、X单质和Y单质在高温下制备ZY,其中Z的氧化物和X单质的物质的量之比为
 ,则该反应的化学方程式为
,则该反应的化学方程式为
您最近一年使用:0次
解题方法
2 . 下列化学用语使用正确的是
| A.在氮原子中,质子数为7而中子数不一定为7 |
| B.106g的乙醇和丙醇混合液完全燃烧生成的CO2为112L (标准状况) |
C.Na2O2的电子式为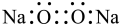 |
D. 的结构示意图为 的结构示意图为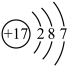 |
您最近一年使用:0次
3 . 下列说法正确的是
A. 电子式: 电子式: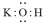 |
B. 电离: 电离: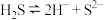 |
C. 中P原子最外层达8电子稳定结构 中P原子最外层达8电子稳定结构 |
D. 第一步水解: 第一步水解: |
您最近一年使用:0次
解题方法
4 . 下列化学用语或图示不正确的是
| A.甲醛和乙酸的实验式均为CH2O |
B.空间填充模型(比例模型) 既可以表示甲烷分子,也可以表示四氟化碳分子 既可以表示甲烷分子,也可以表示四氟化碳分子 |
C.反-2-丁烯分子的球棍模型: |
D.用电子式表示Na2S的形成过程: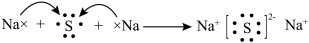 |
您最近一年使用:0次
名校
解题方法
5 . 臭氧广泛用于水处理、空气净化、医药等领域,其治理含氰废水的原理为
 。下列说法错误的是
。下列说法错误的是

 。下列说法错误的是
。下列说法错误的是A. 和 和 互为同位素 互为同位素 | B.中子数为8的氧原子: |
C. 的电子式为 的电子式为 | D. 是强电解质 是强电解质 |
您最近一年使用:0次
名校
解题方法
6 . 一种用于合成治疗免疫疾病药的物质,其结构如图所示,其中X、Y、Z、Q、W为1~20号元素且原子序数依次增大,Z与Q同主族,Q和W的简单离子具有相同的电子层结构。下列叙述正确的是
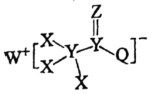

| A.非金属性:Z>Y>Q |
| B.简单氢化物的沸点:Q>Z |
| C.WZX与WXQ均是强电解质,水溶液之间可以发生复分解反应 |
| D.原子序数为82的元素与Q位于同一主族 |
您最近一年使用:0次
名校
7 . 钼的常见价态为+4、+5、+6,钼钢是制火箭发动机的重要材料,钼酸钠晶体(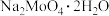 )是一种重要的金属缓蚀剂。某工厂利用钼钢(主要成分
)是一种重要的金属缓蚀剂。某工厂利用钼钢(主要成分 )为原料制备金属钼和钼酸钠晶体的流程如下:
)为原料制备金属钼和钼酸钠晶体的流程如下:___________ ,“锻烧”尾气为 ,“锻烧”的化学方程式为
,“锻烧”的化学方程式为___________ 。
(2)NaClO的电子式为___________ 。
(3)采用NaClO氧化精钼矿的方法是将矿石中的钼浸出,该反应放热,产物中有 存在写出该反应的离子方程式
存在写出该反应的离子方程式___________ 。操作II所得的钼酸要水洗,检验钼酸是否洗涤干净的方法是___________ 。
(4)钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如图2___________ 。
②当浓硫酸浓度大于90%,腐蚀速率几乎为0,原因是___________ 。
③分析随着盐酸和硫酸浓度的增大,碳素钢在两者中腐蚀速率产生明显差异的主要原因是 有利于碳钢的腐蚀,
有利于碳钢的腐蚀, 不利于碳钢的腐蚀
不利于碳钢的腐蚀
(5)某温度下,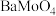 。在水中的沉淀溶解平衡曲线如图所示,要使溶液中钼酸根离子完全沉淀(浓度小于
。在水中的沉淀溶解平衡曲线如图所示,要使溶液中钼酸根离子完全沉淀(浓度小于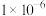 mol/L),溶液中
mol/L),溶液中 的浓度应大于
的浓度应大于___________ mol/L。
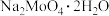 )是一种重要的金属缓蚀剂。某工厂利用钼钢(主要成分
)是一种重要的金属缓蚀剂。某工厂利用钼钢(主要成分 )为原料制备金属钼和钼酸钠晶体的流程如下:
)为原料制备金属钼和钼酸钠晶体的流程如下: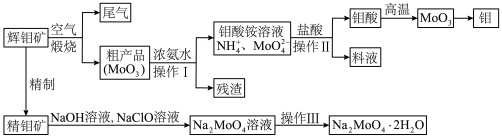
 ,“锻烧”的化学方程式为
,“锻烧”的化学方程式为(2)NaClO的电子式为
(3)采用NaClO氧化精钼矿的方法是将矿石中的钼浸出,该反应放热,产物中有
 存在写出该反应的离子方程式
存在写出该反应的离子方程式(4)钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂。常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如图2
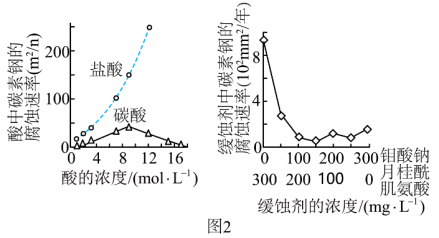
②当浓硫酸浓度大于90%,腐蚀速率几乎为0,原因是
③分析随着盐酸和硫酸浓度的增大,碳素钢在两者中腐蚀速率产生明显差异的主要原因是
 有利于碳钢的腐蚀,
有利于碳钢的腐蚀, 不利于碳钢的腐蚀
不利于碳钢的腐蚀(5)某温度下,
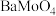 。在水中的沉淀溶解平衡曲线如图所示,要使溶液中钼酸根离子完全沉淀(浓度小于
。在水中的沉淀溶解平衡曲线如图所示,要使溶液中钼酸根离子完全沉淀(浓度小于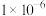 mol/L),溶液中
mol/L),溶液中 的浓度应大于
的浓度应大于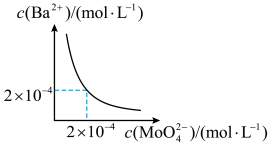
您最近一年使用:0次
解题方法
8 . 下列化学用语或图示表达错误的 是
A. 的电子式: 的电子式: 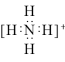 | B. 的球棍模型: 的球棍模型: |
C.苯的比例模型: | D. 的离子结构示意图: 的离子结构示意图: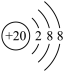 |
您最近一年使用:0次
名校
9 . 纳米银粒是一种杀菌剂,对沙眼衣原体等数十种致病微生物都有强烈的抑制和杀灭作用,而且不会产生耐药性。可通过肼(N2H4)还原银氨溶液制备纳米颗粒。具体步骤如下:
Ⅰ.在洁净的试管中加入2%AgNO3溶液10mL,逐滴加入2%稀氨水,边滴边振荡至沉淀恰好完全溶解。
Ⅱ.取10mLN2H4溶液于大烧杯中并加入5g分散剂混合均匀,加热至55~60℃。
Ⅲ.将Ⅰ中所得溶液滴加到Ⅱ中所得的分散系中,反应15min。
Ⅳ.冷却、分离、洗涤、干燥得纳米银粉。
已知:AgOH是白色难溶于水的物质,常温下极不稳定,分解生成棕色微溶于水的Ag2O。
回答下列问题:
(1)N2H4是一种常用还原剂,写出N2H4的电子式:___________ 。
(2)步骤Ⅲ发生反应的离子方程式为___________ ;验证纳米银颗粒生成的方法是___________ 。
(3)下列有关说法错误的是___________(填字母)。
(4)步骤I使用的AgNO3溶液需用HNO3酸化,其主要目的是___________ 。
(5)若用AgNO3溶液与维生素C以及明胶在一定条件下也可制得纳米银颗粒。
①该体系中维生素C的作用为___________ 。
②已知明胶可与溶液中Ag+形成如下配合物,[Ag(明胶)]+得电子后,明胶继续吸附在银核表面。
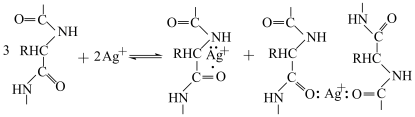
明胶在该体系中充当___________ 。
Ⅰ.在洁净的试管中加入2%AgNO3溶液10mL,逐滴加入2%稀氨水,边滴边振荡至沉淀恰好完全溶解。
Ⅱ.取10mLN2H4溶液于大烧杯中并加入5g分散剂混合均匀,加热至55~60℃。
Ⅲ.将Ⅰ中所得溶液滴加到Ⅱ中所得的分散系中,反应15min。
Ⅳ.冷却、分离、洗涤、干燥得纳米银粉。
已知:AgOH是白色难溶于水的物质,常温下极不稳定,分解生成棕色微溶于水的Ag2O。
回答下列问题:
(1)N2H4是一种常用还原剂,写出N2H4的电子式:
(2)步骤Ⅲ发生反应的离子方程式为
(3)下列有关说法错误的是___________(填字母)。
| A.步骤Ⅰ,银氨溶液也可用AgCl与氨水反应制得 |
| B.步骤Ⅱ,可采用水浴加热 |
| C.步骤Ⅲ,为了加快反应速度,可以一次性加入银氨溶液 |
| D.步骤Ⅳ,洗涤时可先水洗,再用乙醇洗涤 |
(4)步骤I使用的AgNO3溶液需用HNO3酸化,其主要目的是
(5)若用AgNO3溶液与维生素C以及明胶在一定条件下也可制得纳米银颗粒。
①该体系中维生素C的作用为
②已知明胶可与溶液中Ag+形成如下配合物,[Ag(明胶)]+得电子后,明胶继续吸附在银核表面。

明胶在该体系中充当
您最近一年使用:0次
名校
解题方法
10 . 下列化学用语表述正确的是
A. 的分子结构模型: 的分子结构模型: |
| B.HClO的结构式:H-Cl-O |
C.中子数为18的S原子: |
D. 的电子式: 的电子式: |
您最近一年使用:0次
2024-01-02更新
|
184次组卷
|
2卷引用:陕西省商洛市部分学校2023-2024学年高三上学期11月联考化学试题



