1 . nesteretal A是一种从某菌体中提取出来的笼状聚半缩酮,在2021年,化学家Yuichiro Kawamoto等人提出了nesteretal A的一种全合成路线。下面展示了该全合成路线的部分反应。
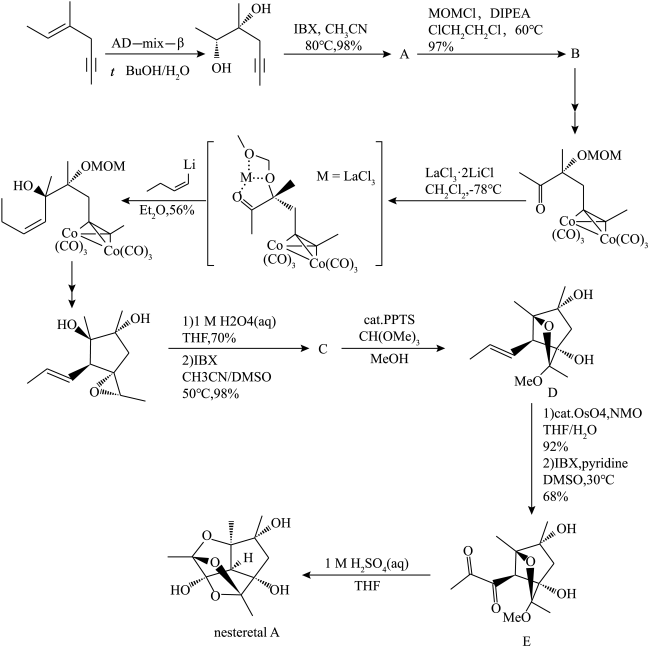
(1)已知IBX是一种氧化剂,可以将醇氧化为酮;环氧乙烷在酸性水溶液中会水解为乙二醇。请画出A、C的键线式______ 、______ 。
(2)根据前后反应,写出MOMCl的键线式______ ,并说明A到B的反应类型______ 。
(3)加入反应物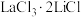 的目的是什么
的目的是什么______ ?
(4)试画出D到E的第一步反应产物的键线式______ 。(不要求立体构型)
(5)请写出nesteretal A的分子式_______ 。

(1)已知IBX是一种氧化剂,可以将醇氧化为酮;环氧乙烷在酸性水溶液中会水解为乙二醇。请画出A、C的键线式
(2)根据前后反应,写出MOMCl的键线式
(3)加入反应物
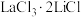 的目的是什么
的目的是什么(4)试画出D到E的第一步反应产物的键线式
(5)请写出nesteretal A的分子式
您最近半年使用:0次
解题方法
2 . 第三代半导体材料氮化镓(GaN)有多种制备方法:
方法Ⅰ: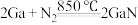
方法Ⅱ: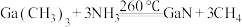
方法Ⅲ: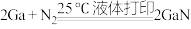
(1)基态 的核外电子排布式为
的核外电子排布式为___________ 。
(2)氨气、甲烷中心原子的杂化方式是___________ ,分子构型分别为___________ 、___________ 。氨气熔沸点高于甲烷,是因为固体、液态氨气分子中存在氢键。在固体氨中每个氨气分子与6个氨气形成氢键,请画出其氢键___________ 。
(3)方法Ⅰ比方法Ⅱ温度高的主要原因是(从结构上解释)___________ 。
(4)方法Ⅲ中,通电氮气流中存在N、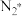 、
、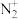 活化粒子,常温下就能与液体镓反应(如图所示)。
活化粒子,常温下就能与液体镓反应(如图所示)。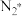 、
、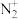 电子式分别为
电子式分别为___________ 、___________ ,1mol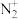 完全反应得到
完全反应得到___________ mol 。
。
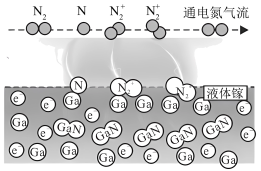
(5)对高温GaN熔液慢速降温,至2950K时形成结晶。科学家展示了从中截取厚度为1.5个原子厚度的微观结构截面图(如下所示):

区域1、区域2分别为氮化镓___________ 、___________ (填“结构A”或“结构B”)的结构。
方法Ⅰ:
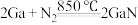
方法Ⅱ:
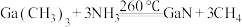
方法Ⅲ:
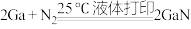
(1)基态
 的核外电子排布式为
的核外电子排布式为(2)氨气、甲烷中心原子的杂化方式是
(3)方法Ⅰ比方法Ⅱ温度高的主要原因是(从结构上解释)
(4)方法Ⅲ中,通电氮气流中存在N、
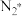 、
、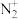 活化粒子,常温下就能与液体镓反应(如图所示)。
活化粒子,常温下就能与液体镓反应(如图所示)。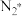 、
、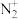 电子式分别为
电子式分别为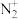 完全反应得到
完全反应得到 。
。
(5)对高温GaN熔液慢速降温,至2950K时形成结晶。科学家展示了从中截取厚度为1.5个原子厚度的微观结构截面图(如下所示):

区域1、区域2分别为氮化镓
您最近半年使用:0次
名校
解题方法
3 . 某钾盐X由四种元素组成,某小组按如下流程进行实验。请回答:
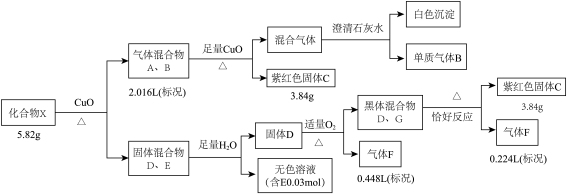
已知:相同条件下,A、B为中学常见气体且密度相同。D、E均为二元化合物,气体F能使品红溶液褪色且通入无色溶液E中,有淡黄色沉淀生成。
(1)气体B的电子式是___________ ,C的化学式是___________ 。
(2)写出固体混合物D、G共热所发生的化学反应方程式___________ 。
(3)无色溶液E中滴加盐酸观察到气泡。收集少量气体通入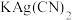 溶液,观察到黑色沉淀生成。写出生成沉淀的离子反应方程式(发生非氧化还原反应)
溶液,观察到黑色沉淀生成。写出生成沉淀的离子反应方程式(发生非氧化还原反应)___________ 。
(4)将G溶于氨水得到一无色溶液,设计实验检验无色溶液中主要离子___________ 。

已知:相同条件下,A、B为中学常见气体且密度相同。D、E均为二元化合物,气体F能使品红溶液褪色且通入无色溶液E中,有淡黄色沉淀生成。
(1)气体B的电子式是
(2)写出固体混合物D、G共热所发生的化学反应方程式
(3)无色溶液E中滴加盐酸观察到气泡。收集少量气体通入
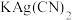 溶液,观察到黑色沉淀生成。写出生成沉淀的离子反应方程式(发生非氧化还原反应)
溶液,观察到黑色沉淀生成。写出生成沉淀的离子反应方程式(发生非氧化还原反应)(4)将G溶于氨水得到一无色溶液,设计实验检验无色溶液中主要离子
您最近半年使用:0次
2023-04-14更新
|
773次组卷
|
3卷引用:浙江省绍兴市2023届高三二模考试化学试题
名校
4 . 芝麻酚又名3, 亚甲二氧基苯酚,是芝麻油重要的香气成分,也是芝麻油重要的品质稳定剂。一种制备芝麻酚H的路线如下:
亚甲二氧基苯酚,是芝麻油重要的香气成分,也是芝麻油重要的品质稳定剂。一种制备芝麻酚H的路线如下:
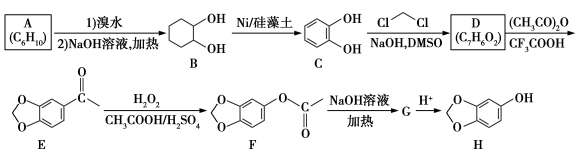
回答下列问题:
(1)A中官能团的名称为___________ ,A的结构简式为___________ 。
(2)B中官能团的电子式是___________ ,B生成C的反应类型为___________ 。
(3)D的结构简式为___________ 。
(4)写出 中第2步反应的化学方程式
中第2步反应的化学方程式___________ 。
(5)写出2种满足下列条件的化合物E的同分异构体的结构简式:___________ 、___________ 。
①苯环上一氯代物只有1种;
②能发生银镜反应,且羟基直接连接苯环上;
③核磁共振氢谱图显示有4组峰,且个数比为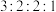 。
。
(6)请结合以上流程及已学知识,写出以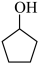 为原料,制备
为原料,制备 的合成路线流程图
的合成路线流程图___________ 。
 亚甲二氧基苯酚,是芝麻油重要的香气成分,也是芝麻油重要的品质稳定剂。一种制备芝麻酚H的路线如下:
亚甲二氧基苯酚,是芝麻油重要的香气成分,也是芝麻油重要的品质稳定剂。一种制备芝麻酚H的路线如下:
回答下列问题:
(1)A中官能团的名称为
(2)B中官能团的电子式是
(3)D的结构简式为
(4)写出
 中第2步反应的化学方程式
中第2步反应的化学方程式(5)写出2种满足下列条件的化合物E的同分异构体的结构简式:
①苯环上一氯代物只有1种;
②能发生银镜反应,且羟基直接连接苯环上;
③核磁共振氢谱图显示有4组峰,且个数比为
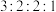 。
。(6)请结合以上流程及已学知识,写出以
 为原料,制备
为原料,制备 的合成路线流程图
的合成路线流程图
您最近半年使用:0次
解题方法
5 . 饱和多元醇A,含碳39.13%,碳氧原子个数比为1:1,A的名称为_______ 。A与等摩尔的醋酸酐反应,得到的化合物结构简式为_______ 。A的水溶液在碱存在下可溶解Cu(OH)2,使溶液变蓝,溶液中的蓝色物质结构为_______ 。
您最近半年使用:0次
6 . (1)Tropinone是一个茛菪烷类生物碱,是合成药物阿托品硫酸盐的中间体。它的合成在有机合成史上具有里程碑意义,开启了多组分反应的研究。Tropinone的许多衍生物具有很好的生理活性,从而可以进行各种衍生化反应。在研究tropinone和溴苄的反应中发现:
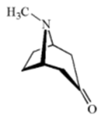
 A+B
A+B
此反应的两个产物A和B可以在碱性条件下相互转换。因此,纯净的A或B在碱性条件下均会变成A和B的混合物。画出A、B以及二者在碱性条件下相互转换的中间体的结构简式_____ 。
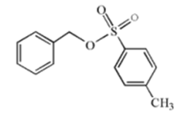
(2)高效绿色合成一直是有机化学家追求的目标,用有机化合物替代金属氧化剂是重要的研究方向之一、硝基甲烷负离子是一种温和的有机氧化剂。画出硝基甲烷负离子的共振式____ (氮原子的形式电荷为正),并完成图中反应______ (写出所有产物):
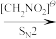 [ ]→
[ ]→

 A+B
A+B此反应的两个产物A和B可以在碱性条件下相互转换。因此,纯净的A或B在碱性条件下均会变成A和B的混合物。画出A、B以及二者在碱性条件下相互转换的中间体的结构简式
(2)高效绿色合成一直是有机化学家追求的目标,用有机化合物替代金属氧化剂是重要的研究方向之一、硝基甲烷负离子是一种温和的有机氧化剂。画出硝基甲烷负离子的共振式

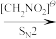 [ ]→
[ ]→
您最近半年使用:0次
7 . X、Y、Z、Q、R是五种短周期元素,原子序数依次增大。X、Y两元素最高正价与最低负价之和均为0;Q与X同主族;Z、R分别是地壳中含量最高的非金属元素和金属元素。
请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号)_______________________ 。
(2)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质(写分子式)____________________ 。
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A B (在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式:
B (在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式:________ ;D的电子式:________ 。
①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为________________ ;由A转化为B的离子方程式为______________________ 。
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因:_________________________________ 。A、B浓度均为0.1mol/L的混合溶液中,离子浓度由大到小的顺序是_________________ ;常温下,在该溶液中滴加稀盐酸至中性时,溶质的主要成分有___________ 。
请回答下列问题:
(1)五种元素原子半径由大到小的顺序是(写元素符号)
(2)X与Y能形成多种化合物,其中既含极性键又含非极性键,且相对分子质量最小的物质(写分子式)
(3)由以上某些元素组成的化合物A、B、C、D有如下转化关系:A
 B (在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式:
B (在水溶液中进行),其中,C是溶于水显酸性的气体;D是淡黄色固体。写出C的结构式:①如果A、B均由三种元素组成,B为两性不溶物,则A的化学式为
②如果A由三种元素组成,B由四种元素组成,A、B溶液均显碱性。用离子方程式表示A溶液显碱性的原因:
您最近半年使用:0次
2019-01-30更新
|
2062次组卷
|
6卷引用:2013年全国普通高等学校招生统一考试理科综合能力测试化学(天津卷)
2013年全国普通高等学校招生统一考试理科综合能力测试化学(天津卷)(已下线)2014高考化学二轮专题突破 专题六物质结构和元素周期律练习卷(已下线)2014届高考化学二轮复习必做训练 物质结构、元素周期律练习卷2016届陕西省西安市第七十中学高三上学期10月月考化学试卷四川省广安市第二中学2019届高三上学期第一次月考化学试题百所名校联考-物质结构 元素周期律
8 . 下表为周期表的一部分,表中所列的字母分别代表一种化学元素。
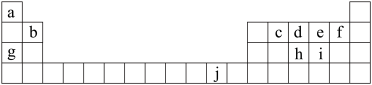
用化学用语回答下列问题:
(1)写出元素f的基态原子核外电子排布式______________ ;
(2)在C6a6分子中,元素c为______________ 杂化,该分子是___________ 分子(填“极性”或“非极性”)。
(3)ci2分子的电子式为_____________ ,ci2与ce2比较,沸点较高的是______________ (写分子式);
(4)第一电离能:h_________ i;电负性:g___________ b(填“>”、“<”或“=”)。
(5)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述正确的是___________ ;
(6)将氨水滴入到j的硫酸盐溶液中,先产生蓝色沉淀,然后沉淀逐渐溶解并得到深蓝色溶液,显深蓝色的离子是_____________ ,写出蓝色沉淀溶解在氨水中的离子方程式______________ ;

用化学用语回答下列问题:
(1)写出元素f的基态原子核外电子排布式
(2)在C6a6分子中,元素c为
(3)ci2分子的电子式为
(4)第一电离能:h
(5)下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙述正确的是
| A.j位于元素周期表中第四周期、IB族,属于ds区元素 |
| B.d的基态原子中,2p能级为半充满,属于p区元素 |
| C.最外层电子排布式为4s1,一定属于IA族 |
| D.最外层电子排布式为ns2np1,该元素可能是ⅢA族或ⅢB族 |
您最近半年使用:0次
解题方法
9 . 有四种化合物W、X、Y、Z,它们都是由短周期元素A、B、C、D、E中的两种元素组成的。已知:
(a)A、B、C、D、E五种元素的原子序数依次增大,且A、D同主族,C、E同主族,B、C同周期。
(b)W由B、C组成,分子中原子个数比为B∶C=1∶2,固体易升华。
(c)X由A、C组成,分子中原子个数比为A∶C=1∶1。
(d)Y由C、D形成的离子化合物,且Y中相应元素的微粒之比为:C∶D=1∶1。
(e)Z是由D、E形成的离子化合物,其中阳离子比阴离子少一个电子层,阴、阳离子数之比为1:2。
试回答下列各小题:
(1)各元素符号:A_______ B________ C________ D________ E_______
(2)W的电子式:___________ 。(3)X的结构式:___________ 。
(4)Y的电子式:___________ 。(5)Z的化学式:____________ 。
(6)写出Y与水反应的化学方程式_______________________ :
(a)A、B、C、D、E五种元素的原子序数依次增大,且A、D同主族,C、E同主族,B、C同周期。
(b)W由B、C组成,分子中原子个数比为B∶C=1∶2,固体易升华。
(c)X由A、C组成,分子中原子个数比为A∶C=1∶1。
(d)Y由C、D形成的离子化合物,且Y中相应元素的微粒之比为:C∶D=1∶1。
(e)Z是由D、E形成的离子化合物,其中阳离子比阴离子少一个电子层,阴、阳离子数之比为1:2。
试回答下列各小题:
(1)各元素符号:A
(2)W的电子式:
(4)Y的电子式:
(6)写出Y与水反应的化学方程式
您最近半年使用:0次
2016-12-09更新
|
1278次组卷
|
4卷引用:2014-2015学年云南省玉溪市第一中学高一下期末化学试卷
10 . A、B、C、D、E五种短周期元素,它们的原子序数依次增大;A原子核内无中子;B元素的最高价氧化物对应水化物与其氢化物能反应生成盐F;D与A同主族,且与E同周期;E元素原子的最外层电子数是其次外层电子数的3/4,A、B、D、E这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。请回答下列问题:
(1)C元素在元素周期表中的位置是_______ ;C、D、E三种元素简单离子半径由大到小的顺序为________ (用离子符号表示)。
(2)写出分别由A、D与C形成的原子个数比为1:1的化合物的电子式_________ 、_________ 。
(3)A与C、E间分别形成甲、乙两种共价化合物,且甲有10个电子,乙有18个电子,则沸点较高的是(填化学式)_________ 。
(4)F含有的化学键类型是_________ 、_________ 。
(5)D和C形成的一种化合物能与A和C形成的一种化合物反应产生C单质,该反应的离子方程式为____________ 。
(6)用电子式表示A、B形成化合物的过程:______________ 。
(1)C元素在元素周期表中的位置是
(2)写出分别由A、D与C形成的原子个数比为1:1的化合物的电子式
(3)A与C、E间分别形成甲、乙两种共价化合物,且甲有10个电子,乙有18个电子,则沸点较高的是(填化学式)
(4)F含有的化学键类型是
(5)D和C形成的一种化合物能与A和C形成的一种化合物反应产生C单质,该反应的离子方程式为
(6)用电子式表示A、B形成化合物的过程:
您最近半年使用:0次



