解题方法
1 . 下表为元素周期表的一部分,请根据元素①~⑧所处的位置回答下列问题:
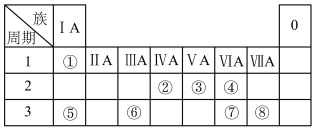
(1)元素④⑤⑧的离子半径由大到小的顺序为_______ (用离子符号表示)。
(2)元素⑦的原子结构示意图为_______ ,元素④⑦的最简单氢化物的稳定性关系为_______ (用化学式表示)。
(3)由元素④⑤组成原子个数比为1:1的化合物中含_______ (填“离子键”、“共价键”或“离子键和共价键”),将78g该化合物投入98g水中,所得溶液的质量分数为_______ 。
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是_______ (填化学式),该酸与元素⑥的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(5)由元素①③组成的含 和
和 的分子的电子式分别是
的分子的电子式分别是_______ 、_______ 。

(1)元素④⑤⑧的离子半径由大到小的顺序为
(2)元素⑦的原子结构示意图为
(3)由元素④⑤组成原子个数比为1:1的化合物中含
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是
(5)由元素①③组成的含
 和
和 的分子的电子式分别是
的分子的电子式分别是
您最近一年使用:0次
解题方法
2 . 1—20号元素中的A、B、C、D、E五种元素,它们的原子序数按E、C、D、A、B依次增大,E原子最外层有4个电子;A-与B+的核外电子排布相同;D的气态氢化物的化学式为H2D,最高价氧化物中D的质量分数为40%,且D原子核内质子数和中子数相等;C的原子序数比D少9,比B少12。
(1)写元素符号:A_____ ,B_____ ,C_______ ,D_______ ,E_______ 。
(2)画出A-、B+的结构示意图:_______ ,_______ 。
(3)D最高价氧化物对应的水化物化学式为____ ,C的气态氢化物的化学式为______ 。
(4)D、C最高价氧化物对应的水化物相互反应的离子方程式:_______ 。
(1)写元素符号:A
(2)画出A-、B+的结构示意图:
(3)D最高价氧化物对应的水化物化学式为
(4)D、C最高价氧化物对应的水化物相互反应的离子方程式:
您最近一年使用:0次
名校
3 . X、Y、Z、W、R是短周期原子序数依次增大的五种主族元素,X是宇宙中含量最多的元素,Y、Z、W同周期且相邻,Y的原子序数等于W原子的最外层电子数。X、Y、Z、W、R组成的M是一种温和的还原剂,其结构如图所示。下列说法正确的是
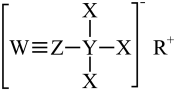
| A.简单离子半径:R>W |
| B.最高价氧化物对应水化物的酸性:W>Z |
| C.最简单氢化物的沸点:Z>W |
| D.M属于共价化合物 |
您最近一年使用:0次
名校
4 . 氢是宇宙中含量最高的元素,占宇宙总质量的75%,应用前景十分广阔。
(1)H可与N形成多种分子,其中某分子含18个e-、6个原子,则该分子的结构式为___________ 。
(2)工业上用C和H2O制取H2。已知:
①C(s) + H2O(g) = H2(g) + CO(g) ΔH1
②C(s) + 2H2O(g) = 2H2(g) + CO2(g) ΔH2
则CO(s) + H2O(g) = H2(g) + CO2(g) ΔH =___________ (用ΔH1、ΔH2表示)。
(3)NaBH4是一种重要的储氢载体。
①B在元素周期表中的位置为___________ 。
②NaBH4(s)与H2O (l)反应生成NaBO2(s)和一种气体,在25℃,101kPa下,已知每消耗3.8g NaBH4放热21.6kJ,则该反应的热化学方程式为___________ ;反应前后B的化合价不变,则反应消耗1molNaBH4时转移的电子数目为___________ 。
(1)H可与N形成多种分子,其中某分子含18个e-、6个原子,则该分子的结构式为
(2)工业上用C和H2O制取H2。已知:
①C(s) + H2O(g) = H2(g) + CO(g) ΔH1
②C(s) + 2H2O(g) = 2H2(g) + CO2(g) ΔH2
则CO(s) + H2O(g) = H2(g) + CO2(g) ΔH =
(3)NaBH4是一种重要的储氢载体。
①B在元素周期表中的位置为
②NaBH4(s)与H2O (l)反应生成NaBO2(s)和一种气体,在25℃,101kPa下,已知每消耗3.8g NaBH4放热21.6kJ,则该反应的热化学方程式为
您最近一年使用:0次
名校
5 . A、B、C、D、E、F、G均为短周期元素,原子序数依次递增。A元素原子核内无中子,B元素原子最外层电子数是次外层电子数的2倍,D是地壳中含量最多的元素,E的化合物焰色反应是黄色,F与G位置相邻,G是同周期元素中原子半径最小的元素。
请用化学用语回答:
(1)B的最高价氧化物的电子式是___________ 。
(2)用电子式表示E2F的形成过程___________ 。
(3)E、F、G三种元素所形成的简单离子,半径由大到小的顺序是___________ 。(用离子符号表示)
(4)下列实验操作对应的实验现象中,不正确的是___________ (填字母)。
(5)写出A与C形成的10电子分子中的化学键有___________ ,该物质的水溶液常用于检验输送G的单质的管道是否漏气,若漏气就会产生白烟,发生反应的化学方程式为___________ 。
请用化学用语回答:
(1)B的最高价氧化物的电子式是
(2)用电子式表示E2F的形成过程
(3)E、F、G三种元素所形成的简单离子,半径由大到小的顺序是
(4)下列实验操作对应的实验现象中,不正确的是
| 选项 | 实验操作 | 实验现象 |
| a | 将E单质投入到CuSO4溶液中 | 生成大量红色固体 |
| b | 向AlCl3溶液中通入过量C的气态氢化物 | 先生成白色沉淀,然后沉淀溶解 |
| c | 将G的单质通入到NaBr溶液中充分反应后,加入四氯化碳,振荡,静置 | 分两层,下层溶液变为橙红色 |
| d | 将B的最高价氧化物通入到Na2SiO3溶液中 | 生成白色沉淀 |
您最近一年使用:0次
名校
解题方法
6 . 下列说法错误的是
| A.烷烃的通式为CnH2n+2,随n值的增大,碳元素的质量分数逐渐减小 |
| B.分子式为C2H6和分子式为C5H12的烷烃的一氯代物的数目可能相同 |
C.丙烷的球棍模型为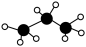 |
D.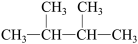 和 和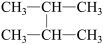 属于同种物质 属于同种物质 |
您最近一年使用:0次
名校
7 . 按照要求回答问题。
(1) 的电子式为
的电子式为_______ ,写出其用于呼吸面具做供氧剂的化学方程式:_______ 。
(2)实验室用NaOH浓溶液配制0.1 mol·L NaOH溶液500 mL,需量取密度为1.4 g·cm
NaOH溶液500 mL,需量取密度为1.4 g·cm 质量分数为40%的NaOH溶液
质量分数为40%的NaOH溶液_______ mL(保留一位小数),该实验所需的玻璃仪器除玻璃棒、量筒、胶头滴管、烧杯之外,还有_______ 。
(3)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的 ,则C→D的化学方程式:
,则C→D的化学方程式:_______ 。
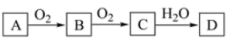
(4)盛放NaOH溶液的试剂瓶不能用玻璃塞,其原因是(用离子方程式表示):_______ 。
(5)高铁酸钠( )是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用
)是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用 的反应原理来制备高铁酸钠,若制备1 mol
的反应原理来制备高铁酸钠,若制备1 mol  ,则该反应转移的电子为
,则该反应转移的电子为_______ mol。
(1)
 的电子式为
的电子式为(2)实验室用NaOH浓溶液配制0.1 mol·L
 NaOH溶液500 mL,需量取密度为1.4 g·cm
NaOH溶液500 mL,需量取密度为1.4 g·cm 质量分数为40%的NaOH溶液
质量分数为40%的NaOH溶液(3)非金属单质A经如图所示的过程转化为含氧酸D,已知D为强酸,若A在常温下为气体单质,将装满气体C的试管倒扣在水槽中,溶液最终充满试管容积的
 ,则C→D的化学方程式:
,则C→D的化学方程式:
(4)盛放NaOH溶液的试剂瓶不能用玻璃塞,其原因是(用离子方程式表示):
(5)高铁酸钠(
 )是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用
)是一种绿色杀菌消毒剂,可用于饮用水处理。某实验小组利用 的反应原理来制备高铁酸钠,若制备1 mol
的反应原理来制备高铁酸钠,若制备1 mol  ,则该反应转移的电子为
,则该反应转移的电子为
您最近一年使用:0次
解题方法
8 . 我国化学家侯德榜改革国外的纯碱生产工艺,生产流程示意简图如下:
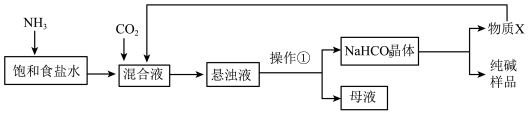
(1)物质X的电子式为_______ ;
(2)上述转化过程可证明热稳定性:NaHCO3_______ Na2CO3(填“>”、“=”或“<”);如图装置也可比较二者的稳定性,则Z为_______ (填物质名称),烧杯_______ (填“I”或“II”)中溶液变浑浊。
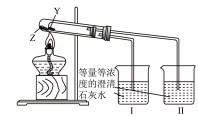
(3)“操作①”得到的NaHCO3晶体中会含有少量NaCl杂质。
①检验含有该杂质的操作为_______ 。
②采用如下方法进行NaHCO3晶体纯度测定:

该试样中NaHCO3的质量分数为_______ %(精确到0.1)。

(1)物质X的电子式为
(2)上述转化过程可证明热稳定性:NaHCO3

(3)“操作①”得到的NaHCO3晶体中会含有少量NaCl杂质。
①检验含有该杂质的操作为
②采用如下方法进行NaHCO3晶体纯度测定:

该试样中NaHCO3的质量分数为
您最近一年使用:0次
2023-02-14更新
|
325次组卷
|
3卷引用:山东省聊城市2022-2023学年高一上学期期末教学质量抽测化学试题
山东省聊城市2022-2023学年高一上学期期末教学质量抽测化学试题山东省聊城市2022-2023学年高一上学期期末考试化学试题(已下线)专题04 钠、氯及其化合物-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
9 . 家中的食品、调味品、洗涤剂和药品等都含有化学物质,以下是胃药和加碘食盐的标签,请回答下列问题。
(1)标签中涉及到的金属元素有___________  ,非金属元素有
,非金属元素有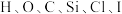 ;
; 在元素周期表中的位置是
在元素周期表中的位置是___________ , 的结构示意图为
的结构示意图为___________ 。
(2)写出由 两种元素组成的常见温室气体的电子式
两种元素组成的常见温室气体的电子式___________ 。
(3)比较下列性质,用“>”、“=”或“<”填空。
①酸性:
___________ 
②还原性:
___________ 
③离子半径: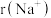
___________ 
(4)用以下对比实验探究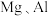 的金属性强弱以及
的金属性强弱以及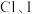 的非金属性强弱。
的非金属性强弱。
| 铝镁咀嚼片 【药品名】铝镁咀嚼片 【成分】氢氧化镁、氢氧化铝、二甲基硅油 【适应症】胃酸过多引起的胃痛、烧心等胃胀气的治疗 | 食用盐 【配料表】精制盐、碘酸钾 【碘含量(以I计)】21mg/kg~39mg/kg 【保质期】36个月 |
 ,非金属元素有
,非金属元素有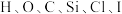 ;
; 在元素周期表中的位置是
在元素周期表中的位置是 的结构示意图为
的结构示意图为(2)写出由
 两种元素组成的常见温室气体的电子式
两种元素组成的常见温室气体的电子式(3)比较下列性质,用“>”、“=”或“<”填空。
①酸性:


②还原性:


③离子半径:
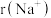

(4)用以下对比实验探究
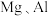 的金属性强弱以及
的金属性强弱以及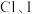 的非金属性强弱。
的非金属性强弱。| 比较Mg、Al金属性强弱 | 比较Cl、I非金属性强弱 |
选择的试剂: 溶液、 溶液、 溶液、氨水、 溶液、氨水、 溶液 溶液 | 选择的试剂:新制氯水、 溶液 溶液 |
操作:向两支试管中分别加入少许 溶液和 溶液和 溶液,然后滴加氨水,直到不再产生白色沉淀 溶液,然后滴加氨水,直到不再产生白色沉淀 和白色沉淀 和白色沉淀 为止,再向两支试管中分别加入 为止,再向两支试管中分别加入 溶液,边加边振荡,观察现象。 溶液,边加边振荡,观察现象。 | 操作:向盛有 溶液的试管中加入 溶液的试管中加入 新制氯水,振荡 新制氯水,振荡 |
| 现象: | 现象:溶液由无色变为棕黄色 化学方程式: |
结论:金属性 强于 强于 | 结论:非金属性Cl强于I |
您最近一年使用:0次
解题方法
10 . 如图为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
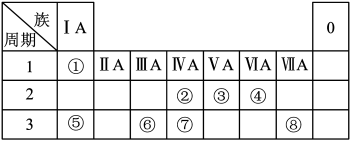
(1)地壳中含量居于第二位的元素在周期表中的位置是___________ 。
(2)②的最高价氧化物的分子式为___________ ;⑦的最高价氧化物对应水化物的分子式为___________ 。
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:___________ 、___________ 。
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___________(填字母)。
(5)半径大小比较:③___________ ④;金属性强弱比较:⑤___________ ⑥(填“>”、“<”或“=”)。
(6)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为___________ 。

(1)地壳中含量居于第二位的元素在周期表中的位置是
(2)②的最高价氧化物的分子式为
(3)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式:
(4)W是第四周期与④同主族的元素。据此推测W不可能具有的性质是___________(填字母)。
| A.最高正化合价为+6 | B.气态氢化物比 稳定 稳定 |
| C.最高价氧化物对应水化物的酸性比硫酸弱 | D.单质在常温下可与氢气化合 |
(5)半径大小比较:③
(6)已知X为第IIA族元素(第一到第四周期),其原子序数为a,Y与X位于同一周期,且为第IIIA族元素,则Y的原子序数b与a所有可能的关系式为
您最近一年使用:0次



