1 . 医用生理盐水是质量分数为0.9%的NaCl水溶液。下列有关表示错误的是
A.钠离子的结构示意图: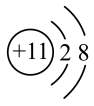 |
B.质子数为11、中子数为12的钠原子: |
C. 、 、 、 、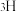 互称为同素异形体 互称为同素异形体 |
D.NaCl的电离方程式: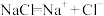 |
您最近一年使用:0次
名校
2 . 亚硝酰氯NOCl常用于合成洗涤剂、触媒及用作中间体,是一种红褐色液体或黄色气体,其熔点-64.5℃,沸点-5.5℃,遇水易水解。某学习小组在实验室用Cl2与NO制备NOCl并测定其纯度。
(1)若用KClO3和浓盐酸制取Cl2反应的离子方程式为___________ 。
(2)NOCl分子中各原子均满足8电子稳定结构,则NOCl的结构式为___________ 。
(3)利用制得的NO和Cl2制备NOCl,装置如图所示(夹持装置略去):

①装置连接顺序为a→___________ (按气流自左向右方向,用小写字母表示)。
②装置I、II除可进一步干燥NO、Cl2外,另一个作用是___________ 。
③装置VI在实验时可观察到的现象是___________ 。
④若不用装置IV中的干燥管对实验有何影响___________ (用化学方程式表示)。
(4)亚硝酰氯NOCl纯度的测定(假设杂质不参与反应):取VI中所得液体100g溶于NaOH溶液中,然后加入一定量稀硫酸和KI,并通入足量N2,将NO全部赶出,最后将溶液稀释至250.00mL;取出25.00mL样品溶于锥形瓶中,用淀粉作指示剂,用cmol·L-1Na2S2O3标准溶液滴定至终点,最终消耗标准溶液的体积为20.00mL。
已知:2 +4H++2I-=2NO+I2+2H2O;I2+2
+4H++2I-=2NO+I2+2H2O;I2+2 =
= +2I-
+2I-
①滴定终点的现象:当滴入最后半滴标准溶液后,___________ 。
②亚硝酰氯(NOCl)的质量分数为___________ %。(用含c的代数式表示)
(1)若用KClO3和浓盐酸制取Cl2反应的离子方程式为
(2)NOCl分子中各原子均满足8电子稳定结构,则NOCl的结构式为
(3)利用制得的NO和Cl2制备NOCl,装置如图所示(夹持装置略去):

①装置连接顺序为a→
②装置I、II除可进一步干燥NO、Cl2外,另一个作用是
③装置VI在实验时可观察到的现象是
④若不用装置IV中的干燥管对实验有何影响
(4)亚硝酰氯NOCl纯度的测定(假设杂质不参与反应):取VI中所得液体100g溶于NaOH溶液中,然后加入一定量稀硫酸和KI,并通入足量N2,将NO全部赶出,最后将溶液稀释至250.00mL;取出25.00mL样品溶于锥形瓶中,用淀粉作指示剂,用cmol·L-1Na2S2O3标准溶液滴定至终点,最终消耗标准溶液的体积为20.00mL。
已知:2
 +4H++2I-=2NO+I2+2H2O;I2+2
+4H++2I-=2NO+I2+2H2O;I2+2 =
= +2I-
+2I-①滴定终点的现象:当滴入最后半滴标准溶液后,
②亚硝酰氯(NOCl)的质量分数为
您最近一年使用:0次
名校
解题方法
3 . Ⅰ.以硫铁矿(主要成分 )为原料生产硫酸及尾气处理的一种流程如下图。回答下列问题:
)为原料生产硫酸及尾气处理的一种流程如下图。回答下列问题:

(1)硫铁矿主要成分 中阴离子电子式
中阴离子电子式___________ ,其煅烧的化学反应方程式为___________ 。
(2)制酸尾气用纯碱吸收生成 离子方程式
离子方程式___________ 。
(3)焦亚硫酸钠( )是常用的食品抗氧化剂,常用于葡萄酒、果脯等食品中,其在空气中久置会与氧气反应生成
)是常用的食品抗氧化剂,常用于葡萄酒、果脯等食品中,其在空气中久置会与氧气反应生成 ,写出该反应的化学方程式
,写出该反应的化学方程式___________ 。
Ⅱ.聚合硫酸铝铁(PFAS)是一种新型高效水处理剂。以粉煤灰(主要成分为 、
、 、FeO等)为铝源,利用炼铁炉渣(主要成分为
、FeO等)为铝源,利用炼铁炉渣(主要成分为 、FeO、
、FeO、 等)为铁源,制备PFAS的工艺流程如下:
等)为铁源,制备PFAS的工艺流程如下:

(4)“碱溶”时,粉煤灰发生反应的离子方程式为___________ ,获“酸溶Ⅱ”时,将炼铁炉渣粉碎的目的是___________ 。
(5)硫酸工业中,用98%的浓硫酸a吨吸收 ,制得含
,制得含 40%(质量分数)的发烟硫酸
40%(质量分数)的发烟硫酸___________ 吨。
(6)“氧化”时 的作用是
的作用是___________ ,此时用控制温度在50~57℃之间,其原因是___________ 。
 )为原料生产硫酸及尾气处理的一种流程如下图。回答下列问题:
)为原料生产硫酸及尾气处理的一种流程如下图。回答下列问题:
(1)硫铁矿主要成分
 中阴离子电子式
中阴离子电子式(2)制酸尾气用纯碱吸收生成
 离子方程式
离子方程式(3)焦亚硫酸钠(
 )是常用的食品抗氧化剂,常用于葡萄酒、果脯等食品中,其在空气中久置会与氧气反应生成
)是常用的食品抗氧化剂,常用于葡萄酒、果脯等食品中,其在空气中久置会与氧气反应生成 ,写出该反应的化学方程式
,写出该反应的化学方程式Ⅱ.聚合硫酸铝铁(PFAS)是一种新型高效水处理剂。以粉煤灰(主要成分为
 、
、 、FeO等)为铝源,利用炼铁炉渣(主要成分为
、FeO等)为铝源,利用炼铁炉渣(主要成分为 、FeO、
、FeO、 等)为铁源,制备PFAS的工艺流程如下:
等)为铁源,制备PFAS的工艺流程如下:
(4)“碱溶”时,粉煤灰发生反应的离子方程式为
(5)硫酸工业中,用98%的浓硫酸a吨吸收
 ,制得含
,制得含 40%(质量分数)的发烟硫酸
40%(质量分数)的发烟硫酸(6)“氧化”时
 的作用是
的作用是
您最近一年使用:0次
解题方法
4 . 金属镍广泛应用于制造记忆合金、储氢合金以及用作加氢反应的催化剂,是重要的战略物资,但资源匮乏。由镍矿渣[主要含 、NiS,还含锌、铁、钙的氧化物、
、NiS,还含锌、铁、钙的氧化物、 等]制备草酸镍晶体的流程如图:
等]制备草酸镍晶体的流程如图: 与萃取剂(用HA表示)存在:
与萃取剂(用HA表示)存在: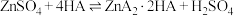
(1)“酸浸”过程中,生成了一中臭鸡蛋气味的气体,写出相应反应的离子方程式_______ ,滤渣1的主要成分是_______
(2)已知“除铁”时,NaClO的作用是将 氧化为
氧化为 并转化为
并转化为 沉淀而除去,若将氧化剂改为
沉淀而除去,若将氧化剂改为 ,写出
,写出 与
与 反应生成
反应生成 的化学方程式
的化学方程式_______
(3)“除钙”时,加入 溶液使钙离子转化为
溶液使钙离子转化为 沉淀,写出
沉淀,写出 的电子式
的电子式_______
(4)若已知萃取剂的密度大于水的密度,则应保留_______ 液体。(填“上层”或“下层”)在完成“萃取”操作后,后续操作依次为_______ 、_______
(5)某化学实验小组同学模拟上述工艺流程,称取了11.8g“镍矿渣”,在实验室制备草酸镍晶体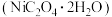 。若“沉镍”操作获得的草酸镍晶体经洗涤、干燥后,称量其质量为3.66g,则镍矿渣中镍元素的质量分数为
。若“沉镍”操作获得的草酸镍晶体经洗涤、干燥后,称量其质量为3.66g,则镍矿渣中镍元素的质量分数为_______ 。
 、NiS,还含锌、铁、钙的氧化物、
、NiS,还含锌、铁、钙的氧化物、 等]制备草酸镍晶体的流程如图:
等]制备草酸镍晶体的流程如图:
 与萃取剂(用HA表示)存在:
与萃取剂(用HA表示)存在: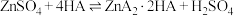
(1)“酸浸”过程中,生成了一中臭鸡蛋气味的气体,写出相应反应的离子方程式
(2)已知“除铁”时,NaClO的作用是将
 氧化为
氧化为 并转化为
并转化为 沉淀而除去,若将氧化剂改为
沉淀而除去,若将氧化剂改为 ,写出
,写出 与
与 反应生成
反应生成 的化学方程式
的化学方程式(3)“除钙”时,加入
 溶液使钙离子转化为
溶液使钙离子转化为 沉淀,写出
沉淀,写出 的电子式
的电子式(4)若已知萃取剂的密度大于水的密度,则应保留
(5)某化学实验小组同学模拟上述工艺流程,称取了11.8g“镍矿渣”,在实验室制备草酸镍晶体
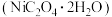 。若“沉镍”操作获得的草酸镍晶体经洗涤、干燥后,称量其质量为3.66g,则镍矿渣中镍元素的质量分数为
。若“沉镍”操作获得的草酸镍晶体经洗涤、干燥后,称量其质量为3.66g,则镍矿渣中镍元素的质量分数为
您最近一年使用:0次
2023-04-27更新
|
207次组卷
|
2卷引用:山东省德州市2022-2023学年高一下学期4月期中考试化学试题
名校
5 . 亚硝酰氯(NOCl)是有机物合成中的重要试剂,是一种红褐色液体或黄色气体,遇水易水解。某化学小组利用NO和 在实验室中制备NOCl,装置如图。
在实验室中制备NOCl,装置如图。

已知:沸点 为-34℃、NO为-152℃、NOCl为-6℃。NOCl易水解,能与
为-34℃、NO为-152℃、NOCl为-6℃。NOCl易水解,能与 反应。
反应。
回答下列问题:
(1)NOCl分子中各原子均满足8电子的稳定结构,则NOCl的电子式为_______ 。
(2)仪器a的名称:_______ 。
(3)NO和氯气混合前,先关闭 ,打开
,打开 、
、 ,操作的目的为
,操作的目的为_______ 。
(4)装置D中的温度区间应控制在_______ 。
(5)上述实验装置有一处不足,请指出不足之处:_______ 。
(6)亚硝酰氯(NOCl)纯度的测定。取D中所得液体20g溶于适量的NaOH溶液中,配制成250mL溶液;取出25.00mL样品溶液于锥形瓶中,滴加适量试剂X,用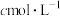
 标准溶液滴定至终点,消耗标准溶液的体积为20.00mL。
标准溶液滴定至终点,消耗标准溶液的体积为20.00mL。
①亚硝酰氯(NOCl)与NaOH溶液反应的方程式为_______ 。
②已知:
试剂X为_______ 。
A.NaBr B.NaI C. D.
D.
③亚硝酰氯(NOCl)的质量分数为_______ 。
 在实验室中制备NOCl,装置如图。
在实验室中制备NOCl,装置如图。
已知:沸点
 为-34℃、NO为-152℃、NOCl为-6℃。NOCl易水解,能与
为-34℃、NO为-152℃、NOCl为-6℃。NOCl易水解,能与 反应。
反应。回答下列问题:
(1)NOCl分子中各原子均满足8电子的稳定结构,则NOCl的电子式为
(2)仪器a的名称:
(3)NO和氯气混合前,先关闭
 ,打开
,打开 、
、 ,操作的目的为
,操作的目的为(4)装置D中的温度区间应控制在
(5)上述实验装置有一处不足,请指出不足之处:
(6)亚硝酰氯(NOCl)纯度的测定。取D中所得液体20g溶于适量的NaOH溶液中,配制成250mL溶液;取出25.00mL样品溶液于锥形瓶中,滴加适量试剂X,用
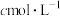
 标准溶液滴定至终点,消耗标准溶液的体积为20.00mL。
标准溶液滴定至终点,消耗标准溶液的体积为20.00mL。①亚硝酰氯(NOCl)与NaOH溶液反应的方程式为
②已知:
| 物质 | AgCl | AgBr | AgI |  | AgSCN |  |
 |  |  | 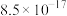 | 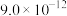 |  | 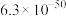 |
| 颜色 | 白色 | 淡黄色 | 黄色 | 砖红色 | 白色 | 灰黑色 |
A.NaBr B.NaI C.
 D.
D.
③亚硝酰氯(NOCl)的质量分数为
您最近一年使用:0次
名校
解题方法
6 . 近日,西湖大学理学院何睿华课题组发现了世界首例具有本征相于性的光阴极量子材料——钛酸锶。某小组以钛铁矿为原料制备钛酸锶的流程图如下:

已知几种物质的主要成分如表所示。
回答下列问题:
(1)“气体”分子的电子式为_______ 。
(2)为了提高“焙烧”速率,宜采取的措施有_______ 答一条合理措施即可)。从“滤渣2”中提纯铁粉的物理方法是_______ 。
(3)“滤液2”和“滤液3”中浓度有明显变化的离子为_______ (填离子符号)。设计简单实验检验滤液4含有Fe2+:_______ 。
(4)“热解”中主要反应的离子方程式为_______ 。用“热水”而不用常温水,其目的是_______ 。
(5)在“灼烧”中盛装H2TiO3的仪器是_______ (填名称)。
(6)某钛铁矿中含钛元素的质量分数为ω,100kg该钛铁矿经上述流程最终制得mg钛酸锶,则钛的收率为_______ %(提示:钛的收率等于实际钛产量与理论钛产量之比)。

已知几种物质的主要成分如表所示。
| 物质 | 成分 |
| 钛铁矿 | 主要成分是FeTiO3,含少量SiO2、Fe3O4等 |
| 浸液1 | Fe3+、Fe2+、TiO2+、H+、 |
| 滤液2 | Fe2+、TiO2+、H+、 |
| 滤液3 | Fe2+、TiO2+、H+、 |
(1)“气体”分子的电子式为
(2)为了提高“焙烧”速率,宜采取的措施有
(3)“滤液2”和“滤液3”中浓度有明显变化的离子为
(4)“热解”中主要反应的离子方程式为
(5)在“灼烧”中盛装H2TiO3的仪器是
(6)某钛铁矿中含钛元素的质量分数为ω,100kg该钛铁矿经上述流程最终制得mg钛酸锶,则钛的收率为
您最近一年使用:0次
2023-05-01更新
|
237次组卷
|
2卷引用:江西省2023届高三下学期二模考试理综化学试题
名校
7 . 氢气是一种理想的绿色清洁能源,氢气的制取是氢能源利用领域的研究热点。
(1)碱金属氢化物制氢。以一种制氢储氢材料氢化钠(NaH)在室温下结合 制氢为例,反应为
制氢为例,反应为 。
。
①NaH的电子式为___________ ;
②在化学方程式上标出该反应中电子转移的方向与数目___________ 。
(2)甲烷重整制氢。主要反应为: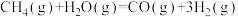 ;
;
① 中氢元素的质量分数为
中氢元素的质量分数为___________ ,是含氢量最高的有机物;甲烷重整制氢是我国目前最主要的制氢来源。
②碳元素在周期表中的位置为___________ ;当1个碳原子与其他4个原子连接时,这个碳原子将采取___________ (填“空间构型”)取向与之成键形成稳定结构,使得烷烃性质稳定。
③汽油的辛烷值的测定是以异辛烷和正庚烷为标准燃料进行的,它们互为___________ ;该异辛烷的结构简式为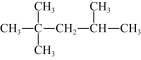 ,用系统命名法命名该有机物
,用系统命名法命名该有机物___________ ;写出同时满足下列条件的正庚烷的一种同分异构体的结构简式:___________ (a.一个支链,b.该物质在光照下与氯气取代的一氯代物有3种)。
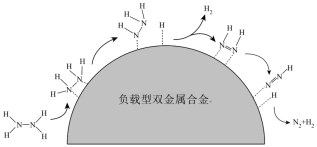
(3)肼催化分解制氢。在温和条件下,负载型双金属合金催化肼( )迅速分解,并且制氢选择性可达100%,可能机理如图所示,(图上“虚线”表示吸附在催化剂上)
)迅速分解,并且制氢选择性可达100%,可能机理如图所示,(图上“虚线”表示吸附在催化剂上)  催化分解制氢的总反应方程式为
催化分解制氢的总反应方程式为___________ 。
(1)碱金属氢化物制氢。以一种制氢储氢材料氢化钠(NaH)在室温下结合
 制氢为例,反应为
制氢为例,反应为 。
。①NaH的电子式为
②在化学方程式上标出该反应中电子转移的方向与数目
(2)甲烷重整制氢。主要反应为:
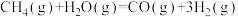 ;
;
①
 中氢元素的质量分数为
中氢元素的质量分数为②碳元素在周期表中的位置为
③汽油的辛烷值的测定是以异辛烷和正庚烷为标准燃料进行的,它们互为
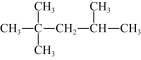 ,用系统命名法命名该有机物
,用系统命名法命名该有机物(3)肼催化分解制氢。在温和条件下,负载型双金属合金催化肼(
 )迅速分解,并且制氢选择性可达100%,可能机理如图所示,(图上“虚线”表示吸附在催化剂上)
)迅速分解,并且制氢选择性可达100%,可能机理如图所示,(图上“虚线”表示吸附在催化剂上)  催化分解制氢的总反应方程式为
催化分解制氢的总反应方程式为
您最近一年使用:0次
2023-04-22更新
|
195次组卷
|
2卷引用:江苏省黄埭中学2022-2023学年高一下学期期中调研测试化学试题
名校
8 . 下列说法正确的是
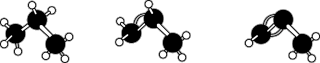

| A.丙烷、丙烯、丙炔的球棍模型分别为如图 |
| B.有机物中碳的质量分数最高的物质是乙炔 |
| C.卤代烃均难溶于水,且密度比水大 |
| D.利用溴水可以区分乙醇、己烯、四氯化碳、己烷 |
您最近一年使用:0次
解题方法
9 . 我国化学家侯德榜改革国外的纯碱生产工艺,生产流程示意简图如下:
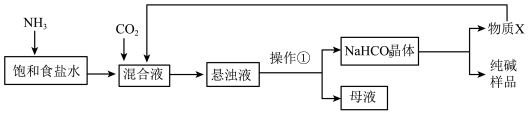
(1)物质X的电子式为_______ ;
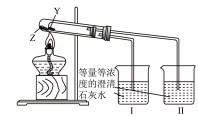
(2)上述转化过程可证明热稳定性:NaHCO3_______ Na2CO3(填“>”、“=”或“<”);如图装置也可比较二者的稳定性,则Z为_______ (填物质名称),烧杯_______ (填“I”或“II”)中溶液变浑浊。
(3)“操作①”得到的NaHCO3晶体中会含有少量NaCl杂质。
①检验含有该杂质的操作为_______ 。
②采用如下方法进行NaHCO3晶体纯度测定:

该试样中NaHCO3的质量分数为_______ %(精确到0.1)。

(1)物质X的电子式为
(2)上述转化过程可证明热稳定性:NaHCO3

(3)“操作①”得到的NaHCO3晶体中会含有少量NaCl杂质。
①检验含有该杂质的操作为
②采用如下方法进行NaHCO3晶体纯度测定:

该试样中NaHCO3的质量分数为
您最近一年使用:0次
2023-02-14更新
|
325次组卷
|
3卷引用:山东省聊城市2022-2023学年高一上学期期末教学质量抽测化学试题
山东省聊城市2022-2023学年高一上学期期末教学质量抽测化学试题山东省聊城市2022-2023学年高一上学期期末考试化学试题(已下线)专题04 钠、氯及其化合物-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)
名校
10 . X、Y、Z、W、R是短周期原子序数依次增大的五种主族元素,X是宇宙中含量最多的元素,Y、Z、W同周期且相邻,Y的原子序数等于W原子的最外层电子数。X、Y、Z、W、R组成的M是一种温和的还原剂,其结构如图所示。下列说法正确的是
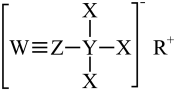
| A.简单离子半径:R>W |
| B.最高价氧化物对应水化物的酸性:W>Z |
| C.最简单氢化物的沸点:Z>W |
| D.M属于共价化合物 |
您最近一年使用:0次



