1 . 针对表中10种元素及由这些元素形成的单质和化合物,用元素符号或者化学式填写以下空格。
(1)最活泼的金属元素是___________ ,最活泼的非金属元素是___________ ,最不活泼的元素是___________ 。
(2)碱性最强的最高价氧化物对应水化物是___________ ,酸性最强的最高价氧化物对应水化物是___________ ,最稳定的气态氢化物是___________ 。
(3)在④与⑤中,还原性较强的是___________ ,在⑧与⑨的单质中,氧化性较强的是___________ 。
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:___________ ;用电子式表示④和⑧形成的化合物的形成过程___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)碱性最强的最高价氧化物对应水化物是
(3)在④与⑤中,还原性较强的是
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:
您最近一年使用:0次
2 . 现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第4周期元素,它们的原子序数依次增大。请根据下列相关信息回答问题。
(1)B元素基态原子具有___________ 种运动状态不同的电子,能量最高的电子,其电子云在空间有___________ 个伸 展方向。
(2)根据上述信息,画出C元素基态原子的轨道表示式___________ 。
(3)F在元素周期表中属于___________ 区元素。
(4)写出DA3的电子式:___________ (用元素符号表示)。
| 元素 | 相关信息 |
| A | 元素的原子核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p电子数比s电子数少1 |
| C | 元素的第一至第四电离能分别是I1=738 kJ/mol、I2=1451 kJ/mol、I3= 7733 kJ/mol、I4= 10540 kJ/mol |
| D | 原子核外填充电子的所有p轨道全满或半满 |
| E | 元素的主族序数与周期序数的差为3 |
| F | 在元素周期表的第6列 |
(2)根据上述信息,画出C元素基态原子的轨道表示式
(3)F在元素周期表中属于
(4)写出DA3的电子式:
您最近一年使用:0次
名校
3 . 如图是元素周期表中合并的短周期部分,表中字母分别表示一种元素。请回答下列问题:
(1)g元素在周期表中的位置是第 ___________ 。
(2)所给元素中c和d两种元素氢化物的稳定性更强的是___________ (填物质的化学式)。
(3)图中所给元素中d、e、f、g所对应的简单离子半径大小顺序为___________ (填离子符号)。
(4)图中所给元素中b、g、h最高氧化物对应水化物酸性大小顺序为___________ (填化学式)。
(5)用电子式表示a原子与g原子形成常见化合物的过程:___________ 。
| a | |||||||
| b | c | d | |||||
| e | f | g | h | k | |||
(2)所给元素中c和d两种元素氢化物的稳定性更强的是
(3)图中所给元素中d、e、f、g所对应的简单离子半径大小顺序为
(4)图中所给元素中b、g、h最高氧化物对应水化物酸性大小顺序为
(5)用电子式表示a原子与g原子形成常见化合物的过程:
您最近一年使用:0次
名校
4 . 如表为元素周期表的一部分,用化学用语回答下列问题:
(1)⑧的原子结构示意图为________ 。
(2)③⑧⑩的最高价氧化物对应的水化物,酸性最强的是________ (填化学式)。
(3)③的气态氢化物与③的最高价氧化物对应的水化物反应生成的盐是________ (填化学式)。
(4)①④⑩三种元素的原子能形成原子数目比为1:1:1的共价化合物,它的电子式为________ 。②④两种元素形成的原子数目比为1:2的共价化合物的结构式为________ 。
(5)⑤的最高价氧化物的水化物与⑦的最高价氧化物反应的离子方程式为________ 。
主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)⑧的原子结构示意图为
(2)③⑧⑩的最高价氧化物对应的水化物,酸性最强的是
(3)③的气态氢化物与③的最高价氧化物对应的水化物反应生成的盐是
(4)①④⑩三种元素的原子能形成原子数目比为1:1:1的共价化合物,它的电子式为
(5)⑤的最高价氧化物的水化物与⑦的最高价氧化物反应的离子方程式为
您最近一年使用:0次
名校
解题方法
5 . 已知A、B、C、D、E、F是分属三个短周期的六种主族元素,且原子序数依次增大,D元素焰色试验时火焰呈黄色。①B是植物生长三要素之一,它能形成多种氧化物,某些氧化物会造成光化学污染。②C和D能形成电子总数为30和38的两种化合物。③E与C同主族。请回答下列问题:
(1)元素F在元素周期表中的位置是___________ 。
(2)C、D、E三种元素形成的简单离子的离子半径由小到大的顺序是___________ (用离子符号表示)。
(3)C和D形成电子总数为38的化合物中化学键类型有___________ (填“离子键”“极性共价键”或“非极性共价键”)。
(4)写出D的最高价氧化物对应的水化物的电子式:___________ 。
(5)E、F两种元素形成的氢化物中还原性较强的是___________ (填化学式);用电子式表示该化合物的形成过程:___________ 。
(1)元素F在元素周期表中的位置是
(2)C、D、E三种元素形成的简单离子的离子半径由小到大的顺序是
(3)C和D形成电子总数为38的化合物中化学键类型有
(4)写出D的最高价氧化物对应的水化物的电子式:
(5)E、F两种元素形成的氢化物中还原性较强的是
您最近一年使用:0次
名校
解题方法
6 . 部分短周期主族元素的原子半径和主要化合价的关系如图所示,其中E、G、T位于同一周期。回答下列问题:

(1)B位于第_______ 周期第______ 族。
(2)FDB的电子式为_______ ;T的原子结构示意图为_______ 。
(3)设计简单实验证明D的非金属性比C的强:________ 。
(4)A和D的简单氢化物相遇产生“白烟”,其生成物的化学式是_______ 。
(5)在上述元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式,下同),碱性最强的是_______ ;上述非金属元素的简单氢化物中,沸点最高的是_______ ,还原性最强的是_______ 。
(6)G、D的最高价氧化物对应的水化物之间发生反应的化学方程式为_______ 。

(1)B位于第
(2)FDB的电子式为
(3)设计简单实验证明D的非金属性比C的强:
(4)A和D的简单氢化物相遇产生“白烟”,其生成物的化学式是
(5)在上述元素的最高价氧化物对应的水化物中,酸性最强的是
(6)G、D的最高价氧化物对应的水化物之间发生反应的化学方程式为
您最近一年使用:0次
2023-10-27更新
|
174次组卷
|
2卷引用:新疆乌鲁木齐市实验学校2023-2024学年高一上学期1月期末化学试题
7 . A、B、C、D、E是五种原子序数逐渐增大的短周期元素,A是周期表中原子半径最小的元素,其中B、C同周期,A与D、B与E同主族,E原子核内质子数等于B、C原子电子数之和,E的单质是应用最为广泛的半导体材料。试回答:
(1)E在元素周期表中的位置是___________ 。
(2)A与B形成的含有18个电子的物质甲的结构式是___________ ,C与D形成的原子个数比为1∶1的化合物乙的电子式是___________ ,化合物乙中含有___________ (填“极性键”或“非极性键”)。
(3)常温下B的最简单氢化物与氯气反应生成两种气态物质的化学方程式为___________ 。
(4)A和B形成的化合物中,丙是一种重要的基本化工原料,其产量可以用来衡量一个国家的石油化工发展水平,写出由丙制得高聚物的反应方程式:___________ ,该反应类型是___________ 。
(5)工业上利用E的氧化物与B的单质在高温条件下反应制备新型陶瓷材料EB,同时生成B的二元化合物,写出制备新型陶瓷材料EB的化学方程式:___________ 。
(1)E在元素周期表中的位置是
(2)A与B形成的含有18个电子的物质甲的结构式是
(3)常温下B的最简单氢化物与氯气反应生成两种气态物质的化学方程式为
(4)A和B形成的化合物中,丙是一种重要的基本化工原料,其产量可以用来衡量一个国家的石油化工发展水平,写出由丙制得高聚物的反应方程式:
(5)工业上利用E的氧化物与B的单质在高温条件下反应制备新型陶瓷材料EB,同时生成B的二元化合物,写出制备新型陶瓷材料EB的化学方程式:
您最近一年使用:0次
8 . 下图为元素周期表的一部分,根据元素①~⑧在表中的位置回答下列问题。

(1)这8种元素中,原子半径最大的是:___________ (填元素符号),最高价氧化物对应的水化物碱性最强的是:___________ (填化学式,下同),最高价氧化物对应的水化物酸性最强的是:___________ 。
(2)写出元素①与③形成的化合物的电子式为:___________ 。
(3)用电子式表示元素⑤与⑧形成化合物的过程:___________ 。
(4)元素⑥的单质与⑤的最高价氧化物对应水化物反应的化学方程式:___________ 。
(5)⑤元素的单质与④的最简单氢化物反应的离子方程式为:___________ 。

(1)这8种元素中,原子半径最大的是:
(2)写出元素①与③形成的化合物的电子式为:
(3)用电子式表示元素⑤与⑧形成化合物的过程:
(4)元素⑥的单质与⑤的最高价氧化物对应水化物反应的化学方程式:
(5)⑤元素的单质与④的最简单氢化物反应的离子方程式为:
您最近一年使用:0次
名校
解题方法
9 . 如图是元素周期表的一部分,针对表中①~⑧元素,填写下列空白:
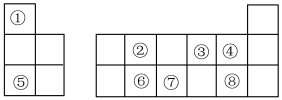
(1)⑥原子的结构示意图为___________ ,元素⑦在周期表中的位置为___________ 。
(2)图中8种元素最高价氧化物对应的水化物中,酸性最强的是___________ (填化学式,下同),碱性最强的是___________ 。
(3)写出由①③元素构成的化合物对应的电子式:___________ (写一种即可)。用电子式表示⑤和⑧形成化合物的过程:___________ 。
(4)④、⑤和⑧三种元素的离子半径由大到小的顺序是___________ (用离子符号和“>”表示)。
(5)据元素周期律,推测⑥的最高价氧化物属于___________ (填“酸性”或“碱性”)氧化物,写出得出该结论的化学方程式:___________ 。

(1)⑥原子的结构示意图为
(2)图中8种元素最高价氧化物对应的水化物中,酸性最强的是
(3)写出由①③元素构成的化合物对应的电子式:
(4)④、⑤和⑧三种元素的离子半径由大到小的顺序是
(5)据元素周期律,推测⑥的最高价氧化物属于
您最近一年使用:0次
名校
10 . 从樟科植物枝叶提取的精油中含有甲、乙两种成分,由甲转化为乙的过程如下(已略去无关产物),回答相关问题。

(1)写出物质甲中含氧官能团的电子式___________ 。
(2)反应Ⅱ的试剂和条件是___________ 。
(3)请选用提供的试剂检验物质乙中含有碳碳双键。提供的试剂:a.稀盐酸、b.稀硫酸、c.新制的氢氧化铜是浊液、d.酸性 溶液、e.NaOH溶液,所选试剂为
溶液、e.NaOH溶液,所选试剂为___________ (填字母)。
(4)写出乙与新制 悬浊液反应的化学方程式
悬浊液反应的化学方程式___________ 。
Ⅱ.有机分离提纯常常利用物质的酸碱性分离混合液。某一混合液含苯酚、苯甲醇,其分离方案如图:

已知:常温下,苯酚和苯甲醇微溶于水。
(5)试剂A可选择_______ ,写出水层中通入CO2的化学方程式_______ 。
(6)填写操作名称:操作Ⅱ_______ 。

(1)写出物质甲中含氧官能团的电子式
(2)反应Ⅱ的试剂和条件是
(3)请选用提供的试剂检验物质乙中含有碳碳双键。提供的试剂:a.稀盐酸、b.稀硫酸、c.新制的氢氧化铜是浊液、d.酸性
 溶液、e.NaOH溶液,所选试剂为
溶液、e.NaOH溶液,所选试剂为(4)写出乙与新制
 悬浊液反应的化学方程式
悬浊液反应的化学方程式Ⅱ.有机分离提纯常常利用物质的酸碱性分离混合液。某一混合液含苯酚、苯甲醇,其分离方案如图:

已知:常温下,苯酚和苯甲醇微溶于水。
(5)试剂A可选择
(6)填写操作名称:操作Ⅱ
您最近一年使用:0次



