名校
1 . 完成下列小题
(1)现有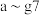 种短周期元素,它们在周期表中的位置如图,请据此回答下列问题:
种短周期元素,它们在周期表中的位置如图,请据此回答下列问题:
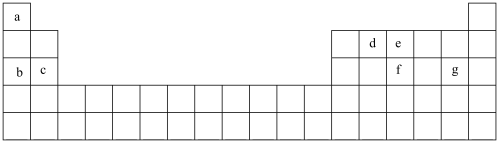
①元素 和f在周期表中的位置
和f在周期表中的位置_____ ,_____ 。
②用电子式表示由 与
与 元素组成化合物的形成过程:
元素组成化合物的形成过程:_____ 。
③元素的原子间反应最容易形成离子键的是_____ 。
A.c和f B.b和g C.d和g D.b和
④ 与
与 元素形成的分子中所有原子
元素形成的分子中所有原子_____ (填“是”或“不是”)都满足最外层为8电子结构
(2) 和
和 代表原子序数依次增大的四种短周期元素,它们满足以下条件:
代表原子序数依次增大的四种短周期元素,它们满足以下条件:
①元素周期表中, 与
与 相邻,
相邻, 与
与 也相邻;②
也相邻;② 、
、 和
和 三种元素的原子最外层电子数之和为17.请填空:
三种元素的原子最外层电子数之和为17.请填空:
①下列元素的符号:
_____ 、
_____ 、
_____ 。
② 和
和 可组成一化合物,其原子个数之比为
可组成一化合物,其原子个数之比为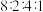 。写出该化合物的化学式
。写出该化合物的化学式_____ 。
(1)现有
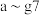 种短周期元素,它们在周期表中的位置如图,请据此回答下列问题:
种短周期元素,它们在周期表中的位置如图,请据此回答下列问题:
①元素
 和f在周期表中的位置
和f在周期表中的位置②用电子式表示由
 与
与 元素组成化合物的形成过程:
元素组成化合物的形成过程:③元素的原子间反应最容易形成离子键的是
A.c和f B.b和g C.d和g D.b和

④
 与
与 元素形成的分子中所有原子
元素形成的分子中所有原子(2)
 和
和 代表原子序数依次增大的四种短周期元素,它们满足以下条件:
代表原子序数依次增大的四种短周期元素,它们满足以下条件:①元素周期表中,
 与
与 相邻,
相邻, 与
与 也相邻;②
也相邻;② 、
、 和
和 三种元素的原子最外层电子数之和为17.请填空:
三种元素的原子最外层电子数之和为17.请填空:①下列元素的符号:



②
 和
和 可组成一化合物,其原子个数之比为
可组成一化合物,其原子个数之比为 。写出该化合物的化学式
。写出该化合物的化学式
您最近一年使用:0次
名校
解题方法
2 . 1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经一百多年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
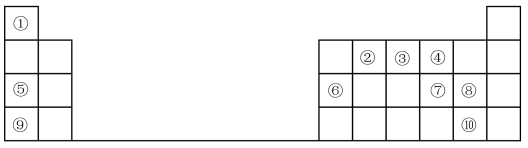
(1)元素②在周期表中的位置___________
(2)元素⑤和⑨的最高价氧化物的水化物中,碱性较强的是___________ (填化学式)。
(3)元素①与⑦可形成18电子分子,请用电子式表示该分子的形成过程:___________ 。
(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是___________ (用离子符号表示),
(5)元素⑨的最高价氧化物的水化物与元素⑥的单质反应的化学方程式为:___________ 。
(6)元素的非金属性⑩___________ ⑧(填“>”或“<”);下列事实不能 证明上述结论的是___________ 。
A.元素⑧的单质与⑩的气态氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的气态氢化物的水溶液的酸性比元素⑩的弱
C.元素⑧和⑩的气态氢化物受热分解,前者的分解温度高
D.元素⑧的最高价氧化物的水化物的酸性比元素⑩的强
E.元素⑧的气态氢化物的还原性比元素⑩的弱

(1)元素②在周期表中的位置
(2)元素⑤和⑨的最高价氧化物的水化物中,碱性较强的是
(3)元素①与⑦可形成18电子分子,请用电子式表示该分子的形成过程:
(4)元素⑦⑧⑨的简单离子半径由大到小的顺序是
(5)元素⑨的最高价氧化物的水化物与元素⑥的单质反应的化学方程式为:
(6)元素的非金属性⑩
A.元素⑧的单质与⑩的气态氢化物的水溶液反应,溶液变为橙黄色
B.元素⑧的气态氢化物的水溶液的酸性比元素⑩的弱
C.元素⑧和⑩的气态氢化物受热分解,前者的分解温度高
D.元素⑧的最高价氧化物的水化物的酸性比元素⑩的强
E.元素⑧的气态氢化物的还原性比元素⑩的弱
您最近一年使用:0次
2024-02-13更新
|
146次组卷
|
2卷引用:天津市重点校2023-2024学年高一上学期期末联考化学试题
2024·云南·模拟预测
名校
3 . 亚硝酰氯(NOCl)可用于合成清洁剂,可由氯气与一氧化氮在常温常压下合成。熔点:-64.5℃,沸点:-5.5℃;常温下是黄色的有毒气体,遇水易水解。已知NO不与NaOH溶液反应。请按要求回答下列问题。
(1)过量铁屑和稀硝酸充分反应制备NO的离子方程式为___________ 。
(2)制备NOCl的装置如下图所示,仪器B的名称为:___________ 。___________ 。NOCl分子中各原子均满足8电子稳定结构,则它的电子式为___________ 。
②若实验中没有安装装置B,其后果是___________ 。
③实验开始应先在装置中通入 ,至装置A中充满黄绿色气体时,再将NO缓缓通入,此操作的目的是
,至装置A中充满黄绿色气体时,再将NO缓缓通入,此操作的目的是___________ 。
(3)工业生产过程中NO尾气处理方法有多种,其中间接电化学法,其原理如图所示:阴极的电极反应式为___________ 。
(1)过量铁屑和稀硝酸充分反应制备NO的离子方程式为
(2)制备NOCl的装置如下图所示,仪器B的名称为:

②若实验中没有安装装置B,其后果是
③实验开始应先在装置中通入
 ,至装置A中充满黄绿色气体时,再将NO缓缓通入,此操作的目的是
,至装置A中充满黄绿色气体时,再将NO缓缓通入,此操作的目的是(3)工业生产过程中NO尾气处理方法有多种,其中间接电化学法,其原理如图所示:阴极的电极反应式为

您最近一年使用:0次
23-24高一上·天津·期末
解题方法
4 . 下表列出了A−R共9种元素在周期表中的位置(填元素符号)
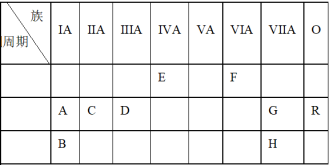
(1)这9种元素,其中化学性质最不活泼的是___________ (填化学式)
(2)A、D元素的最高价氧化物对应水化物反应的离子方程式是_______ 。
(3)A、C、D三种元素按原子半径由大到小的顺序排列为_______ 。
(4)F元素氢化物的化学式是_______ ,该氢化物在常温下跟B发生反应的化学方程式是___________ ,所得溶液的pH_______ 7。(填“>”、“=”或“<”)
(5)H元素跟A元素形成化合物的电子式是________ ,高温灼烧该化合物时,火焰呈_______ 色。

(1)这9种元素,其中化学性质最不活泼的是
(2)A、D元素的最高价氧化物对应水化物反应的离子方程式是
(3)A、C、D三种元素按原子半径由大到小的顺序排列为
(4)F元素氢化物的化学式是
(5)H元素跟A元素形成化合物的电子式是
您最近一年使用:0次
5 . 下列表格是元素周期表的一部分,请按要求填空。
(1)写出④⑤⑦的原子半径由大到小的顺序为___________ 。
(2)元素③和⑩形成的化合物中存在的化学键类型为___________ 。
(3)写出由①和⑥形成的化合物的电子式___________ 。
(4)元素⑪在周期表中的位置________ ,其基态原子的核外电子排布式为___________ 。
(5)写出⑧⑫的最高价氧化物的水化物发生反应的化学方程式___________ 。
(6)写出元素②基态原子的核外电子占据的能量最高的原子轨道的形状为___________ ,该基态原子的价层电子轨道表示式为___________ 。
(7)元素④的气态氢化物的VSEPR模型为___________ ,分子的空间结构为___________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ||||||||||||||
| ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||||||||||||
| ⑪ | ⑫ | ||||||||||||||||
(2)元素③和⑩形成的化合物中存在的化学键类型为
(3)写出由①和⑥形成的化合物的电子式
(4)元素⑪在周期表中的位置
(5)写出⑧⑫的最高价氧化物的水化物发生反应的化学方程式
(6)写出元素②基态原子的核外电子占据的能量最高的原子轨道的形状为
(7)元素④的气态氢化物的VSEPR模型为
您最近一年使用:0次
6 . 氮及其化合物的相互转化对生命、生产生活意义重大。 是重要的化工原料,可发生如下转化:
是重要的化工原料,可发生如下转化:

(1)写出氮元素在周期表的位置_________ ,写出氯元素的原子结构示意图________ 。
(2)写出 的电子式
的电子式___________ , 的结构式
的结构式___________ 。
(3)下列说法正确的是___________ (填序号)。
a.实验室可用浓氨水和生石灰反应,快速制取少量氨气
b. 分子中所有原子在同一平面上
分子中所有原子在同一平面上
c.用 处理硝酸工业排放的尾气
处理硝酸工业排放的尾气 ,利用了
,利用了 的还原性
的还原性
(4)写出过量 发生转化Ⅰ的化学反应方程式
发生转化Ⅰ的化学反应方程式___________
(5)反应Ⅱ在碱性条件下恰好完全反应,还原产物的阴离子是___________ ,检验该阴离子的方实验方法是___________
(6)反应Ⅲ中 与
与 的物质的量相等,产物A既是氧化产物又是还原产物,且A中不含氧元素,则A的化学式
的物质的量相等,产物A既是氧化产物又是还原产物,且A中不含氧元素,则A的化学式___________ 。
 是重要的化工原料,可发生如下转化:
是重要的化工原料,可发生如下转化:
(1)写出氮元素在周期表的位置
(2)写出
 的电子式
的电子式 的结构式
的结构式(3)下列说法正确的是
a.实验室可用浓氨水和生石灰反应,快速制取少量氨气
b.
 分子中所有原子在同一平面上
分子中所有原子在同一平面上c.用
 处理硝酸工业排放的尾气
处理硝酸工业排放的尾气 ,利用了
,利用了 的还原性
的还原性(4)写出过量
 发生转化Ⅰ的化学反应方程式
发生转化Ⅰ的化学反应方程式(5)反应Ⅱ在碱性条件下恰好完全反应,还原产物的阴离子是
(6)反应Ⅲ中
 与
与 的物质的量相等,产物A既是氧化产物又是还原产物,且A中不含氧元素,则A的化学式
的物质的量相等,产物A既是氧化产物又是还原产物,且A中不含氧元素,则A的化学式
您最近一年使用:0次
解题方法
7 . 下表列出了A−R6种元素在周期表中的位置,请回答:
(1)这6种元素,其中化学性质最不活泼的是_____ (填化学式)。
(2)F元素氢化物的化学式是_____ 。
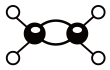
(3)下图为某有机物的球棍模型(其中 代表氢原子,
代表氢原子, 代表E原子),该有机物中E元素与氢元素的质量比
代表E原子),该有机物中E元素与氢元素的质量比
_____ 。
(4)A元素的最高价氧化物对应水化物的电子式是_____ ,高温灼烧该化合物时,火焰呈_____ 色;化合物溶于水所得溶液的pH_____ 7.(填“>”、“=”或“<”)。
(5)B、D元素的最高价氧化物对应水化物反应的离子方程式是_____ 。
(6)实验室用固体烧碱配制480mL0.1 AOH溶液。
AOH溶液。
①配制上述溶液时需称量AOH固体的质量为_____ g(保留小数点后两位)。
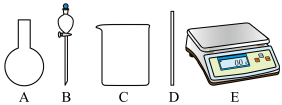
②配制过程中需要在图中挑选仪器,其中玻璃仪器除了500mL的容量瓶,还缺少_____ (填仪器名称)。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | E | F | ||||||
| 3 | A | D | R | |||||
| 4 | B |
(2)F元素氢化物的化学式是
(3)下图为某有机物的球棍模型(其中
 代表氢原子,
代表氢原子, 代表E原子),该有机物中E元素与氢元素的质量比
代表E原子),该有机物中E元素与氢元素的质量比

(4)A元素的最高价氧化物对应水化物的电子式是
(5)B、D元素的最高价氧化物对应水化物反应的离子方程式是
(6)实验室用固体烧碱配制480mL0.1
 AOH溶液。
AOH溶液。①配制上述溶液时需称量AOH固体的质量为
②配制过程中需要在图中挑选仪器,其中玻璃仪器除了500mL的容量瓶,还缺少

您最近一年使用:0次
8 . 下表列出了①~⑥六种元素在周期表中的位置:

请按要求回答下列问题:
(1)写出下列标号元素的元素符号:①___________ 、⑤___________ 。
(2)④和⑥两种元素形成的化合物的电子式是___________ 。
(3)元素②形成的最简单有机物的空间构型为___________ 。
(4)元素③的气态氢化物的分子式为___________ ,最高价氧化物对应水化物的分子式为___________ 。
(5)画出元素⑤的原子结构示意图___________ 。
(6)元素④的单质在氧气中燃烧的化学方程式是___________ 。

请按要求回答下列问题:
(1)写出下列标号元素的元素符号:①
(2)④和⑥两种元素形成的化合物的电子式是
(3)元素②形成的最简单有机物的空间构型为
(4)元素③的气态氢化物的分子式为
(5)画出元素⑤的原子结构示意图
(6)元素④的单质在氧气中燃烧的化学方程式是
您最近一年使用:0次
解题方法
9 . 下表是元素周期表的一部分,针对编号①-⑫元素,回答下列有关问题:
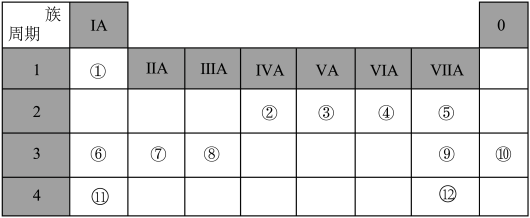
(1)在这些元素中,非金属性最强的元素是_____ (填元素符号,下同),最不活泼的元素是_____ 。
(2)写出元素③对应气态氢化物的电子式:_____ 。
(3)在元素⑥和⑪中,单质与水反应较剧烈的是_____ (填元素符号),它与水反应的化学方程式是_____ 。这是因为同主族元素,随原子序数逐渐增大,原子的电子层数逐渐增大,原子半径逐渐_____ ,元素的金属性逐渐_____ 。
(4)在元素⑥、⑦与⑧的最高价氧化物对应的水化物中,碱性由强到弱的顺序是_____ (填化学式)。
(5)能证明⑨和⑫单质氧化性强弱的实验事实(用离子方程式表示)是_____ 。
(6)①、②、④三种元素形成的有机物的分子结构模型如图所示,写出该有机物的结构简式:_____ ;
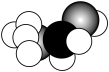
①与②所形成的最简单的烯烃与溴的四氯化碳溶液反应的化学方程式:_____ 。

(1)在这些元素中,非金属性最强的元素是
(2)写出元素③对应气态氢化物的电子式:
(3)在元素⑥和⑪中,单质与水反应较剧烈的是
(4)在元素⑥、⑦与⑧的最高价氧化物对应的水化物中,碱性由强到弱的顺序是
(5)能证明⑨和⑫单质氧化性强弱的实验事实(用离子方程式表示)是
(6)①、②、④三种元素形成的有机物的分子结构模型如图所示,写出该有机物的结构简式:

①与②所形成的最简单的烯烃与溴的四氯化碳溶液反应的化学方程式:
您最近一年使用:0次
名校
10 . 现有下列短周期元素性质的有关数据:
(1)根据元素周期律确定a至h8种元素在周期表中的位置,将它们的元素编号填入如表相应的空格内_______ 。
(2)上述元素形成的氢化物中,分子间存在氢键的有_______ (填氢化物的化学式)。
(3)氢化铝锂(LiAlH4)是一种易燃易爆具有极强还原性的物质,它在有机合成上应用广泛。在125℃时氢化铝锂分解为氢气、金属铝及氢化锂(LiH)。
①氢化铝锂易水解(与水反应),最初得三种产物,请写出其水解反应化学方程式:_______ 。
②与氢化铝锂性质相似但较为温和的还原剂由上述a、d、h三种元素组成,请画出这种还原剂的电子式:_______ ,写出该物质受热分解的反应方程式:_______ 。
| 元素编号 | a | b | c | d | e | f | g | h |
| 原子半径/nm | 0.037 | 0.071 | 0.075 | 0.082 | 0.102 | 0.143 | 0.152 | 0.186 |
| 最高化合价或最低 | +1 | -1 | -3 | +3 | -2 | +3 | +1 | +1 |
| Ⅰ族 | Ⅱ族 | Ⅲ族 | Ⅳ族 | Ⅴ族 | Ⅵ族 | Ⅶ族 | Ⅷ族 | |
| 第一周期 | _____ | |||||||
| 第二周期 | _____ | _____ | _____ | _____ | ||||
| 第三周期 | _____ | _____ | _____ |
(3)氢化铝锂(LiAlH4)是一种易燃易爆具有极强还原性的物质,它在有机合成上应用广泛。在125℃时氢化铝锂分解为氢气、金属铝及氢化锂(LiH)。
①氢化铝锂易水解(与水反应),最初得三种产物,请写出其水解反应化学方程式:
②与氢化铝锂性质相似但较为温和的还原剂由上述a、d、h三种元素组成,请画出这种还原剂的电子式:
您最近一年使用:0次



