名校
1 . 氯化氰 ,又名氯甲氰,熔点为
,又名氯甲氰,熔点为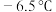 ,沸点为
,沸点为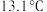 ,剧毒,可溶于水、乙醇、乙醚等,受热易分解,易与水发生剧烈反应。某小组制备氯化氰并探究其性质的实验装置如图所示。已知:
,剧毒,可溶于水、乙醇、乙醚等,受热易分解,易与水发生剧烈反应。某小组制备氯化氰并探究其性质的实验装置如图所示。已知: 具有较强的还原性。
具有较强的还原性。
(1)D装置中盛放 的仪器名称为
的仪器名称为_______ ,检验A装置气密性的方法是_______ 。
(2)A装置中发生反应生成 的离子方程式为
的离子方程式为_______ , 的作用是
的作用是_______ 。
(3)B、C装置中盛放的试剂相同,其作用是_______ 。F装置的作用是降低温度,其中干冰起作用的原因是_______ 。
(4)在 条件下,由
条件下,由 和
和 制备氯化氰的化学方程式为
制备氯化氰的化学方程式为_______ ,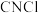 的电子式为
的电子式为_______ 。
(5)上述实验中, 完全反应时收集到
完全反应时收集到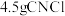 ,则产率为
,则产率为_______ %(保留2位小数)。
 ,又名氯甲氰,熔点为
,又名氯甲氰,熔点为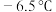 ,沸点为
,沸点为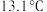 ,剧毒,可溶于水、乙醇、乙醚等,受热易分解,易与水发生剧烈反应。某小组制备氯化氰并探究其性质的实验装置如图所示。已知:
,剧毒,可溶于水、乙醇、乙醚等,受热易分解,易与水发生剧烈反应。某小组制备氯化氰并探究其性质的实验装置如图所示。已知: 具有较强的还原性。
具有较强的还原性。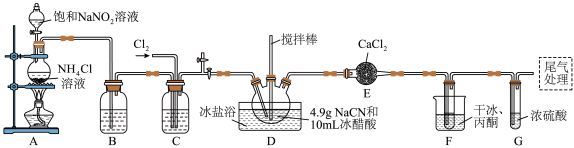
(1)D装置中盛放
 的仪器名称为
的仪器名称为(2)A装置中发生反应生成
 的离子方程式为
的离子方程式为 的作用是
的作用是(3)B、C装置中盛放的试剂相同,其作用是
(4)在
 条件下,由
条件下,由 和
和 制备氯化氰的化学方程式为
制备氯化氰的化学方程式为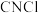 的电子式为
的电子式为(5)上述实验中,
 完全反应时收集到
完全反应时收集到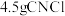 ,则产率为
,则产率为
您最近一年使用:0次
名校
2 . 到目前为止,我们学习了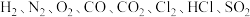 、
、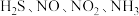 等气体.
等气体.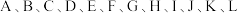 各代表以上气体中一种气体,它们具有如下性质:
各代表以上气体中一种气体,它们具有如下性质:
①A能使湿润的红色石蕊试纸变蓝,A和B相遇时,会产生大量白烟;
②将C和D分别通入品红溶液时,品红溶液都会褪色,但给褪色后的溶液加热时,通入D的溶液会重新变红,通入C的溶液不会重新变红;
③E和F相遇生成红棕色气体K;
④G有臭鸡蛋气味,G在足量F中燃烧生成D和 ;
;
⑤H在C中燃烧时,生成B,同时在集气瓶口会有白雾出现;
⑥D和I都能使澄清石灰水变浑浊;
⑦J在F中燃烧生成I.
⑧在加热及催化剂催化下,J和E反应生成I和L.
(1)实验室收集气体E的方法为_________ ,收集气体K的方法为_________ 。
(2)A的电子式为_________ 。
(3)①中生成白烟的成分为_______ (填名称)。
(4)④中发生反应的化学方程式为_________________ 。
(5)⑤中火焰颜色为________ .白雾成分为_________ (选填“ ”或“盐酸”)。
”或“盐酸”)。
(6)⑧中发生反应的化学方程式为_________________ 。
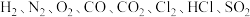 、
、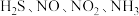 等气体.
等气体.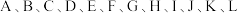 各代表以上气体中一种气体,它们具有如下性质:
各代表以上气体中一种气体,它们具有如下性质:①A能使湿润的红色石蕊试纸变蓝,A和B相遇时,会产生大量白烟;
②将C和D分别通入品红溶液时,品红溶液都会褪色,但给褪色后的溶液加热时,通入D的溶液会重新变红,通入C的溶液不会重新变红;
③E和F相遇生成红棕色气体K;
④G有臭鸡蛋气味,G在足量F中燃烧生成D和
 ;
;⑤H在C中燃烧时,生成B,同时在集气瓶口会有白雾出现;
⑥D和I都能使澄清石灰水变浑浊;
⑦J在F中燃烧生成I.
⑧在加热及催化剂催化下,J和E反应生成I和L.
(1)实验室收集气体E的方法为
(2)A的电子式为
(3)①中生成白烟的成分为
(4)④中发生反应的化学方程式为
(5)⑤中火焰颜色为
 ”或“盐酸”)。
”或“盐酸”)。(6)⑧中发生反应的化学方程式为
您最近一年使用:0次
3 . 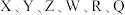 为原子序数依次增大的六种短周期主族元素。
为原子序数依次增大的六种短周期主族元素。 是原子半径最小的元素;
是原子半径最小的元素; 原子最外层电子数是核外电子层数的3倍;
原子最外层电子数是核外电子层数的3倍; 是短周期中金属性最强的元素;
是短周期中金属性最强的元素; 是地壳中含量最多的金属元素;
是地壳中含量最多的金属元素; 的最高正价与最低负价代数和为4。回答下列问题:
的最高正价与最低负价代数和为4。回答下列问题:
(1)用电子式表示
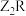 的形成过程:
的形成过程:(2)W在周期表中的位置是
(3)ZYX的电子式为
 中含有的化学键类型为
中含有的化学键类型为(4)
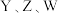 三种元素对应的简单离子半径由大到小的顺序是
三种元素对应的简单离子半径由大到小的顺序是(5)下列说法能证明非金属性
 强于
强于 的是
的是a.简单阴离子的还原性: b.简单氢化物热稳定性:
b.简单氢化物热稳定性:
c.氧化物对应的水化物的酸性: d.
d.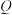 的单质能从
的单质能从 溶液中置换出
溶液中置换出 单质
单质
(6)
 的单质与
的单质与 的最高价氧化物对应的水化物反应的化学方程式为
的最高价氧化物对应的水化物反应的化学方程式为
您最近一年使用:0次
2024-03-29更新
|
159次组卷
|
2卷引用:山西省部分学校2023-2024学年高一上学期1月期末化学试题
名校
解题方法
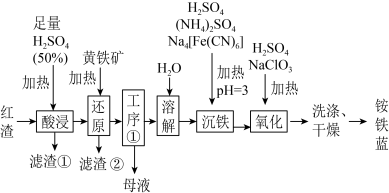
4 . 以焙烧黄铁矿FeS2(杂质为石英等)产生的红渣为原料生产制备铵铁蓝Fe(NH4)[Fe(CN)6]颜料的工艺流程如图:_______ (填化学式),滤渣①的主要成分是_______ (填化学式)。
(2)黄铁矿研细的目的是_______ 。
(3)工序①经过_______ 、过滤、洗涤得到一种含7个结晶水的晶体,该晶体为_______ (填化学式)。
(4)沉铁工序中生成一种白色沉淀为Fe(NH4)2[Fe(CN)6]。
①该物质的阴离子是由Fe2+和CN-结合形成的,CN-的电子式与氮气的电子式相似,请写出CN-的电子式:_______ 。
②该物质在酸性条件下加入NaClO3溶液,充分反应得到铵铁蓝,试补全下列离子方程式:_______ 。6Fe(NH4)2[Fe(CN)6]+ClO +_______=6FeNH4[Fe(CN)6]+ _______+_______NH
+_______=6FeNH4[Fe(CN)6]+ _______+_______NH +3H2O。
+3H2O。
(2)黄铁矿研细的目的是
(3)工序①经过
(4)沉铁工序中生成一种白色沉淀为Fe(NH4)2[Fe(CN)6]。
①该物质的阴离子是由Fe2+和CN-结合形成的,CN-的电子式与氮气的电子式相似,请写出CN-的电子式:
②该物质在酸性条件下加入NaClO3溶液,充分反应得到铵铁蓝,试补全下列离子方程式:
 +_______=6FeNH4[Fe(CN)6]+ _______+_______NH
+_______=6FeNH4[Fe(CN)6]+ _______+_______NH +3H2O。
+3H2O。
您最近一年使用:0次
2024-03-01更新
|
86次组卷
|
2卷引用:山西省运城市康杰中学2023-2024学年高一下学期化学试题
5 . 下表为元素周期表的一部分,表中序号分别代表某一元素。请回答下列问题:
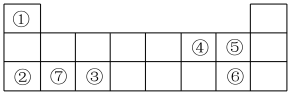
(1)⑥在元素周期表中的位置是___________ 。
(2)④的离子结构示意图为___________ 。
(3)②③④⑥四种元素的简单离子半径由小到大的顺序为___________ (用离子符号表示)。
(4)①④形成的既含极性键又含非极性键的共价化合物的电子式为___________ 。
(5)用电子式表示②④只含有离子键的化合物的形成过程___________ 。
(6)②③⑦最高价氧化物对应的水化物的碱性由强到弱的顺序为___________ (写化学式),⑤和⑥形成的气态氢化物,稳定性较弱的是___________ (写化学式)。
(7)单质②与元素④的简单氢化物反应的离子方程式为___________ 。

(1)⑥在元素周期表中的位置是
(2)④的离子结构示意图为
(3)②③④⑥四种元素的简单离子半径由小到大的顺序为
(4)①④形成的既含极性键又含非极性键的共价化合物的电子式为
(5)用电子式表示②④只含有离子键的化合物的形成过程
(6)②③⑦最高价氧化物对应的水化物的碱性由强到弱的顺序为
(7)单质②与元素④的简单氢化物反应的离子方程式为
您最近一年使用:0次
名校
解题方法
6 . W、X、Y、Z、R、V、Q是七种短周期元素,原子序数依次增大。X原子的最外层电子数是次外层的2倍,Z为地壳中含量最多的元素,V的周期数和主族序数相等,W和R同主族,且都能与Z形成A2Z、A2Z2(A可以表示W或R)型的两种化合物,Q的单质为黄绿色有毒气体。请回答下列问题:
(1)W为___________ (填元素名称),Y在元素周期表中的位置为___________ 。
(2)请写出XZ2的电子式___________ 。
(3)Z、R、V形成的简单离子的半径由大到小的顺序为___________ (填离子符号)。
(4)请写出V的最高价氧化物与R的最高价氧化物对应的水化物的溶液反应的离子方程式___________ 。
(5)请写出Q的单质与水反应的离子方程式___________ 。
(1)W为
(2)请写出XZ2的电子式
(3)Z、R、V形成的简单离子的半径由大到小的顺序为
(4)请写出V的最高价氧化物与R的最高价氧化物对应的水化物的溶液反应的离子方程式
(5)请写出Q的单质与水反应的离子方程式
您最近一年使用:0次
2023-12-31更新
|
196次组卷
|
3卷引用:山西省运城市盐湖区第五高级中学2023-2024学年高一上学期期末达标化学模拟考试卷
7 . 化学实验是研究物质及其变化的基本方法。
(1)过氧化氢和稀盐酸的混合溶液可以刻蚀含铜的电路板。请写出用过氧化氢和稀盐酸刻蚀电路板时发生反应的离子方程式:___________ 。当反应一段时间后,随着溶液变蓝,气泡产生的速率加快,其可能的原因是___________ 。
(2)含铜电路板也可以用 进行刻蚀,对刻蚀后的液体(
进行刻蚀,对刻蚀后的液体(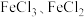 和
和 )进行处理后制备
)进行处理后制备 ,简易流程如图所示:
,简易流程如图所示:

①试剂a是___________ 。
②滤渣1的主要成分是___________ (填化学式)。
③往溶液A中逐滴加入氨水至过量时,可观察到的实验现象为___________ 。
(3) 和
和 是氮元素的两种重要的氢化物。
是氮元素的两种重要的氢化物。
① 常用作制冷剂的原因为
常用作制冷剂的原因为___________ 。
② 能使锅炉内壁的铁锈
能使锅炉内壁的铁锈 变成磁性氧化层,减缓锅炉锈蚀,且不产生污染物。
变成磁性氧化层,减缓锅炉锈蚀,且不产生污染物。 的结构式为
的结构式为___________ ;写出 与铁锈反应的化学方程式:
与铁锈反应的化学方程式:___________ 。
(1)过氧化氢和稀盐酸的混合溶液可以刻蚀含铜的电路板。请写出用过氧化氢和稀盐酸刻蚀电路板时发生反应的离子方程式:
(2)含铜电路板也可以用
 进行刻蚀,对刻蚀后的液体(
进行刻蚀,对刻蚀后的液体(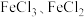 和
和 )进行处理后制备
)进行处理后制备 ,简易流程如图所示:
,简易流程如图所示:
①试剂a是
②滤渣1的主要成分是
③往溶液A中逐滴加入氨水至过量时,可观察到的实验现象为
(3)
 和
和 是氮元素的两种重要的氢化物。
是氮元素的两种重要的氢化物。①
 常用作制冷剂的原因为
常用作制冷剂的原因为②
 能使锅炉内壁的铁锈
能使锅炉内壁的铁锈 变成磁性氧化层,减缓锅炉锈蚀,且不产生污染物。
变成磁性氧化层,减缓锅炉锈蚀,且不产生污染物。 的结构式为
的结构式为 与铁锈反应的化学方程式:
与铁锈反应的化学方程式:
您最近一年使用:0次
名校
8 . 随着原子序数的递增,A~G七种短周期元素的最高正价或最低负价与原子序数的关系如图所示。
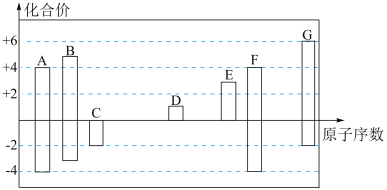
(1)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为___________ 。
(2) A、B、C三种元素的第一电离能由大到小的顺序是___________ (填元素名称)。
(3)F元素的最高价氧化物与氢氧化钠溶液反应的化学方程式是___________ 。
(4)元素A与C形成的电子总数为22的分子的结构式为___________ 。
(5)元素C与D按原子个数比1∶1形成的化合物的电子式为___________ ,其所含的化学键有___________ (填化学键类型)。

(1)在A、B、F、G四种元素中,非金属性最弱的元素在周期表中的位置为
(2) A、B、C三种元素的第一电离能由大到小的顺序是
(3)F元素的最高价氧化物与氢氧化钠溶液反应的化学方程式是
(4)元素A与C形成的电子总数为22的分子的结构式为
(5)元素C与D按原子个数比1∶1形成的化合物的电子式为
您最近一年使用:0次
9 . 常温常压下肼( )是一种易溶于水的无色油状液体,具有强还原性,在工业生产中应用非常广泛。
)是一种易溶于水的无色油状液体,具有强还原性,在工业生产中应用非常广泛。
(1)已知 中存在极性键和非极性键,写出
中存在极性键和非极性键,写出 的电子式:
的电子式:___________ 。
(2)发射卫星时可用肼作燃料,用 作氧化剂,当
作氧化剂,当 气态肼和
气态肼和 完全反应生成氮气和水蒸气时,放出
完全反应生成氮气和水蒸气时,放出 热量,该反应的化学方程式为
热量,该反应的化学方程式为___________ , 气态肼参与该反应,放出的热量为
气态肼参与该反应,放出的热量为___________ kJ。
(3)液态肼、空气、 溶液构成的燃料电池的装置如图1所示:
溶液构成的燃料电池的装置如图1所示:

①该电池的负极反应式为___________ 。
②该电池工作一段时间后,b电极附近溶液的
___________ 。(选填“增大”“减小”“不变”)
(4)向一体积为 的恒容密闭容器中加入
的恒容密闭容器中加入 ,在
,在 催化下发生反应:
催化下发生反应: 。测得容器中
。测得容器中 随时间的变化情况如图2所示。
随时间的变化情况如图2所示。

① 时,若改变反应条件使
时,若改变反应条件使 ,则平衡被打破,反应
,则平衡被打破,反应___________ (填“正”或“逆”)向进行。
② 内用氢气表示的平均反应速率为
内用氢气表示的平均反应速率为___________ 。
 )是一种易溶于水的无色油状液体,具有强还原性,在工业生产中应用非常广泛。
)是一种易溶于水的无色油状液体,具有强还原性,在工业生产中应用非常广泛。(1)已知
 中存在极性键和非极性键,写出
中存在极性键和非极性键,写出 的电子式:
的电子式:(2)发射卫星时可用肼作燃料,用
 作氧化剂,当
作氧化剂,当 气态肼和
气态肼和 完全反应生成氮气和水蒸气时,放出
完全反应生成氮气和水蒸气时,放出 热量,该反应的化学方程式为
热量,该反应的化学方程式为 气态肼参与该反应,放出的热量为
气态肼参与该反应,放出的热量为(3)液态肼、空气、
 溶液构成的燃料电池的装置如图1所示:
溶液构成的燃料电池的装置如图1所示:
①该电池的负极反应式为
②该电池工作一段时间后,b电极附近溶液的

(4)向一体积为
 的恒容密闭容器中加入
的恒容密闭容器中加入 ,在
,在 催化下发生反应:
催化下发生反应: 。测得容器中
。测得容器中 随时间的变化情况如图2所示。
随时间的变化情况如图2所示。
①
 时,若改变反应条件使
时,若改变反应条件使 ,则平衡被打破,反应
,则平衡被打破,反应②
 内用氢气表示的平均反应速率为
内用氢气表示的平均反应速率为
您最近一年使用:0次
解题方法
10 . 元素周期律的发现,对化学的发展有很大影响。作为元素周期律表现形式的元素周期表,反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表中的一部分,请参照以下五种元素在表中的位置,回答下列问题:
(1)写出M的原子结构示意图:__________ 。
(2)原子半径:X__________ Z(填“大于”或“小于”)。
(3)M与W形成化合物的电子式为__________ ,其中含有的化学键类型是__________ (填“离子键”或“共价键”);高温灼烧含M元素的化合物时,火焰呈__________ 。
(4)X、Y的最高价氧化物对应水化物的酸性:__________ >__________ (填化学式)。
族 周期 | IA | 0 | ||||||
1 | ⅡA | Ⅲ | ⅣA | VA | ⅥA | ⅦA | ||
2 | X | Y | Z | W | ||||
3 | M | |||||||
(2)原子半径:X
(3)M与W形成化合物的电子式为
(4)X、Y的最高价氧化物对应水化物的酸性:
您最近一年使用:0次



