2024高三下·全国·专题练习
解题方法
1 . 由硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、Al2O3和SiO2)得到绿矾(FeSO4·7H2O),然后制取透明氧化铁颜料的流程如下:

已知:①透明氧化铁又称纳米氧化铁,粒子直径微小(10~90nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
②Fe3+能将FeS2中的硫元素氧化为+6价。
回答下列问题:
(1)FeS2的电子式为___________ 。
(2)“滤渣”中的主要成分是___________ 。
(3)“还原”过程中涉及的离子方程式为___________ 。
(4)流程中“ ”环节的目的是
”环节的目的是___________ 。
(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到色泽纯正的氢氧化铁,而且还可以___________ 。

已知:①透明氧化铁又称纳米氧化铁,粒子直径微小(10~90nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
②Fe3+能将FeS2中的硫元素氧化为+6价。
回答下列问题:
(1)FeS2的电子式为
(2)“滤渣”中的主要成分是
(3)“还原”过程中涉及的离子方程式为
(4)流程中“
 ”环节的目的是
”环节的目的是(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到色泽纯正的氢氧化铁,而且还可以
您最近一年使用:0次
2024高三下·全国·专题练习
2 . 8月1日起,为了国家信息安全,我国禁止镓和锗的出口,锗是一种重要的半导体材料,工业上用精硫锗矿(主要成分为GeS2)制取高纯度锗的工艺流程如图所示:

(1)COCl2分子中各原子均达到8电子稳定结构,其结构式为___________ 。
(2)800℃升华时通入N2的目的是:___________ 、___________ 。
(3)酸浸时Ge、S元素均被氧化到最高价态,写出该反应的离子方程式:___________ ,酸浸时温度不能过高的原因是___________ 。
(4)GeCl4易水解生成GeCl4·n H2O,证明GeCl4·n H2O沉淀洗涤干净的方法是___________ 。

(1)COCl2分子中各原子均达到8电子稳定结构,其结构式为
(2)800℃升华时通入N2的目的是:
(3)酸浸时Ge、S元素均被氧化到最高价态,写出该反应的离子方程式:
(4)GeCl4易水解生成GeCl4·n H2O,证明GeCl4·n H2O沉淀洗涤干净的方法是
您最近一年使用:0次
3 . 现有A、B、C、D、E五种元素,均为前四周期元素、它们的原子序数依次增大。请根据下列相关信息,回答有关问题。
(1)写出下列元素的元素符号B:___________ ;C:___________ ;D___________ 。
(2)用元素符号表示 的电子式为
的电子式为___________ 。
(3)C在火焰上灼烧产生的黄光是一种(填字母)___________ 。
a.吸收光谱 b.发射光谱
(4)E元素在元素周期表的位置为:___________ ,属于___________ 区。
(5)E最高能层电子的电子云轮廓形状为___________ 。与其同周期的元素中,基态原子最外层电子数与其相同的全部元素的价电子排布式为___________ 。
(6)某主族元素X的前3级电离能如下表所示,则X位于___________ 族。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都低于同周期相邻元素 |
| C元素基态原子核外有11个不同运动状态的电子 |
| D元素位于元素周期表中的第八列,在地壳中的含量居前四位 |
| E元素基态原子的M层全充满,N层没有成对电子,只有1个未成对电子 |
(2)用元素符号表示
 的电子式为
的电子式为(3)C在火焰上灼烧产生的黄光是一种(填字母)
a.吸收光谱 b.发射光谱
(4)E元素在元素周期表的位置为:
(5)E最高能层电子的电子云轮廓形状为
(6)某主族元素X的前3级电离能如下表所示,则X位于
| 元素 | 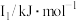 | 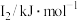 | 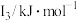 |
| X | 737.7 | 1450.7 | 7732.7 |
您最近一年使用:0次
2023-12-25更新
|
170次组卷
|
2卷引用:陕西省西安交通大学附属中学2023-2024学年高二上学期期中考试化学试题
2024·浙江温州·一模
4 . 2023年8月1日起,我国对镓(Ga)等相关物项实施出口管制。Ga与B、Al处于同一主族。请回答:
(1)基态Ga原子的价电子排布图:___________ ;
(2)①硼的氢化物叫硼烷( )。如
)。如 (乙硼烷-6)、
(乙硼烷-6)、 (丁硼烷-10)等。下列说法
(丁硼烷-10)等。下列说法不正确 的是___________ ;
A.B原子由 需吸收能量
需吸收能量
D. 与
与 反应生成
反应生成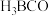 ,
,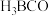 分子中
分子中 键与
键与 键数目之比为:
键数目之比为:
②氮和硼形成的化合的BN,与 互为等电子体,通常存在石墨型与金刚石型两种结构,可发生如下转化:
互为等电子体,通常存在石墨型与金刚石型两种结构,可发生如下转化: 。两类化合物中B原子的杂化方式分别为:
。两类化合物中B原子的杂化方式分别为:___________ ;金刚石型的BN的硬度大于金刚石,原因是___________ ;
③ 极易发生水解生成
极易发生水解生成 和
和 ,请写出反应的化学方程式:
,请写出反应的化学方程式:___________ ;
(3)Ga与N形成的化合物是一种重要的半导体材料,晶体的部分结构如图。___________ ;
②下列所示为图1所对应晶胞的是:___________ 。
(1)基态Ga原子的价电子排布图:
(2)①硼的氢化物叫硼烷(
 )。如
)。如 (乙硼烷-6)、
(乙硼烷-6)、 (丁硼烷-10)等。下列说法
(丁硼烷-10)等。下列说法A.B原子由
 需吸收能量
需吸收能量B. 的结构式:
的结构式:

D.
 与
与 反应生成
反应生成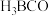 ,
,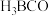 分子中
分子中 键与
键与 键数目之比为:
键数目之比为:
②氮和硼形成的化合的BN,与
 互为等电子体,通常存在石墨型与金刚石型两种结构,可发生如下转化:
互为等电子体,通常存在石墨型与金刚石型两种结构,可发生如下转化: 。两类化合物中B原子的杂化方式分别为:
。两类化合物中B原子的杂化方式分别为:③
 极易发生水解生成
极易发生水解生成 和
和 ,请写出反应的化学方程式:
,请写出反应的化学方程式:(3)Ga与N形成的化合物是一种重要的半导体材料,晶体的部分结构如图。
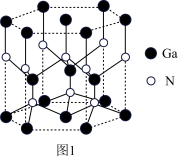
②下列所示为图1所对应晶胞的是:
A. B.
B. C.
C. D.
D.
您最近一年使用:0次
2023-11-10更新
|
796次组卷
|
4卷引用:热点25 物质结构与性质综合题
(已下线)热点25 物质结构与性质综合题浙江省温州市普通高中2024届高三上学期第一次适应性考试(一模)化学试题(已下线)专题04 物质结构与性质(2大题型)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)浙江省部分学校2024届高三下学期模拟考试化学试卷
2022高二·西藏·学业考试
5 . 乙烯的产量可以用来衡量一个国家的石油化工发展水平,A和B是生活中两种常见的有机物,C是一种具有香味的物质,且碳原子数是A的两倍。现以乙烯为主要原料合成C,其合成路线如图所示,请回答下列问题:
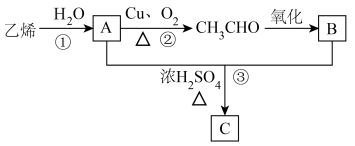
(1)乙烯的结构简式:______ 。
(2)A分子中含有的官能团名称为______ 。
(3)②的反应类型为______ ,③的反应类型为______ 。
(4)写出反应①的化学方程式_______ 。

(1)乙烯的结构简式:
(2)A分子中含有的官能团名称为
(3)②的反应类型为
(4)写出反应①的化学方程式
您最近一年使用:0次
2023高一·云南·学业考试
6 . 下表列出了①~⑩十种元素在元素周期表中的位置。

根据表中元素①~⑩,回答下列问题:
(1)位于短周期的元素共有___________ 种,含②的物质常用于新能源汽车电池的制造,该元素的名称为___________ 。
(2)⑤、⑥、⑦中原子半径最大的是___________ (填元素符号)。
(3)③、④的最高价氧化物对应的水化物的酸性:H3BO3___________ H2CO3(选填“>”或“<”)。
(4)⑩的元素符号为Kr,该原子的电子式为___________ 。
(5)⑧的固态氢化物CaH2与H2O反应生成Ca(OH)2和一种可燃性气体单质,写出CaH2与H2O反应的化学方程式___________ 。

根据表中元素①~⑩,回答下列问题:
(1)位于短周期的元素共有
(2)⑤、⑥、⑦中原子半径最大的是
(3)③、④的最高价氧化物对应的水化物的酸性:H3BO3
(4)⑩的元素符号为Kr,该原子的电子式为
(5)⑧的固态氢化物CaH2与H2O反应生成Ca(OH)2和一种可燃性气体单质,写出CaH2与H2O反应的化学方程式
您最近一年使用:0次
解题方法
7 . 下表列出了A−R6种元素在周期表中的位置,请回答:
(1)这6种元素,其中化学性质最不活泼的是_____ (填化学式)。
(2)F元素氢化物的化学式是_____ 。
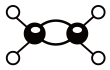
(3)下图为某有机物的球棍模型(其中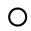 代表氢原子,
代表氢原子, 代表E原子),该有机物中E元素与氢元素的质量比
代表E原子),该有机物中E元素与氢元素的质量比
_____ 。
(4)A元素的最高价氧化物对应水化物的电子式是_____ ,高温灼烧该化合物时,火焰呈_____ 色;化合物溶于水所得溶液的pH_____ 7.(填“>”、“=”或“<”)。
(5)B、D元素的最高价氧化物对应水化物反应的离子方程式是_____ 。
(6)实验室用固体烧碱配制480mL0.1 AOH溶液。
AOH溶液。
①配制上述溶液时需称量AOH固体的质量为_____ g(保留小数点后两位)。
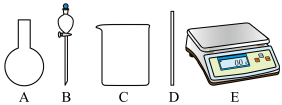
②配制过程中需要在图中挑选仪器,其中玻璃仪器除了500mL的容量瓶,还缺少_____ (填仪器名称)。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 2 | E | F | ||||||
| 3 | A | D | R | |||||
| 4 | B |
(2)F元素氢化物的化学式是
(3)下图为某有机物的球棍模型(其中
 代表氢原子,
代表氢原子, 代表E原子),该有机物中E元素与氢元素的质量比
代表E原子),该有机物中E元素与氢元素的质量比

(4)A元素的最高价氧化物对应水化物的电子式是
(5)B、D元素的最高价氧化物对应水化物反应的离子方程式是
(6)实验室用固体烧碱配制480mL0.1
 AOH溶液。
AOH溶液。①配制上述溶液时需称量AOH固体的质量为
②配制过程中需要在图中挑选仪器,其中玻璃仪器除了500mL的容量瓶,还缺少

您最近一年使用:0次
名校
解题方法
8 . 下表列出了①~⑩十种元素在周期表中的位置:
请按要求回答下列问题:
(1)上述元素中,金属性最强的是___________ (填元素名称),最高价氧化物对应水化物酸性最强的是___________ (写出酸的化学式)。
(2)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是:___________ 。(用离子符号表示)
(3)由元素③形成的单质的电子式为___________ ,由元素⑥和⑨形成化合物乙,请用电子式表示物质乙的形成过程___________ 。
(4)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为___________ 。
(5)请用一个化学方程式证明元素⑧和⑨的非金属性强弱关系___________ 。
(6)可以比较⑤、⑥两元素金属性强弱的实验是___________。
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ |
(1)上述元素中,金属性最强的是
(2)由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是:
(3)由元素③形成的单质的电子式为
(4)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为
(5)请用一个化学方程式证明元素⑧和⑨的非金属性强弱关系
(6)可以比较⑤、⑥两元素金属性强弱的实验是___________。
| A.比较这两种元素最高价氧化物对应的水化物的碱性 |
| B.将⑤的单质投入到⑥的盐溶液中 |
| C.将这两种元素的单质分别放入冷水中 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
您最近一年使用:0次
9 . X、Y、Z、W、R、Q为原子序数依次增大的六种短周期主族元素。X是原子半径最小的元素;Y原子最外层电子数是核外电子层数的3倍;Z是短周期中金属性最强的元素;W是地壳中含量最多的金属元素;R的最高正价与最低负价代数和为4,请回答下列问题:
(1)W在周期表中的位置是___________ 。
(2)写出化合物Z2R的电子式:___________ 。
(3)写出化合物X2Y2的结构式:___________ 。
(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是___________ (用元素的离子符号表示)。
(5)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是___________ 。
(6)X、Y、Z三种元素形成的化合物是___________ (填化学式),含有化学键的类型是___________ 。
(1)W在周期表中的位置是
(2)写出化合物Z2R的电子式:
(3)写出化合物X2Y2的结构式:
(4)Y、Z、W三种元素对应的简单离子半径由大到小的顺序是
(5)W的单质与Z的最高价氧化物对应的水化物反应的化学方程式是
(6)X、Y、Z三种元素形成的化合物是
您最近一年使用:0次
22-23高一上·江苏盐城·期末
解题方法
10 . 下图是元素周期表的一部分。按要求填写下列空白:
(1)元素⑤在周期表中的位置为___________ ;
(2)①~⑧元素的最高价氧化物中,具有两性的是___________ (填化学式);
(3)元素⑦的最简单气态氢化物的电子式是___________ ;
(4)④、⑤、⑥、⑦对应简单离子的半径最小的是___________ (填离子符号);
(5)⑤和⑥两种元素的最高价氧化物对应的水化物反应的离子方程式___________ ;
(6)下列方案中不能证明非金属性⑧比⑦强的是___________(填选项字母)。
| ① | |||||||||
| ② | ③ | ④ | |||||||
| ⑤ | ⑥ | ⑦ | ⑧ |
(2)①~⑧元素的最高价氧化物中,具有两性的是
(3)元素⑦的最简单气态氢化物的电子式是
(4)④、⑤、⑥、⑦对应简单离子的半径最小的是
(5)⑤和⑥两种元素的最高价氧化物对应的水化物反应的离子方程式
(6)下列方案中不能证明非金属性⑧比⑦强的是___________(填选项字母)。
| A.最高价氧化物对应水化物的酸性⑧比⑦的强 |
| B.单质与变价金属反应,产物的价态⑧比⑦的高 |
| C.简单气态氢化物对应水溶液的酸性⑧比⑦的强 |
| D.⑧的单质可将⑦的单质从其化合物中置换出来 |
您最近一年使用:0次



