名校
1 . 氯化氰 ,又名氯甲氰,熔点为
,又名氯甲氰,熔点为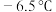 ,沸点为
,沸点为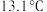 ,剧毒,可溶于水、乙醇、乙醚等,受热易分解,易与水发生剧烈反应。某小组制备氯化氰并探究其性质的实验装置如图所示。已知:
,剧毒,可溶于水、乙醇、乙醚等,受热易分解,易与水发生剧烈反应。某小组制备氯化氰并探究其性质的实验装置如图所示。已知: 具有较强的还原性。
具有较强的还原性。
(1)D装置中盛放 的仪器名称为
的仪器名称为_______ ,检验A装置气密性的方法是_______ 。
(2)A装置中发生反应生成 的离子方程式为
的离子方程式为_______ , 的作用是
的作用是_______ 。
(3)B、C装置中盛放的试剂相同,其作用是_______ 。F装置的作用是降低温度,其中干冰起作用的原因是_______ 。
(4)在 条件下,由
条件下,由 和
和 制备氯化氰的化学方程式为
制备氯化氰的化学方程式为_______ ,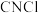 的电子式为
的电子式为_______ 。
(5)上述实验中, 完全反应时收集到
完全反应时收集到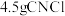 ,则产率为
,则产率为_______ %(保留2位小数)。
 ,又名氯甲氰,熔点为
,又名氯甲氰,熔点为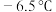 ,沸点为
,沸点为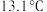 ,剧毒,可溶于水、乙醇、乙醚等,受热易分解,易与水发生剧烈反应。某小组制备氯化氰并探究其性质的实验装置如图所示。已知:
,剧毒,可溶于水、乙醇、乙醚等,受热易分解,易与水发生剧烈反应。某小组制备氯化氰并探究其性质的实验装置如图所示。已知: 具有较强的还原性。
具有较强的还原性。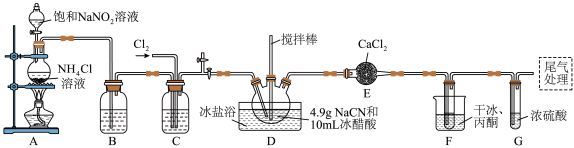
(1)D装置中盛放
 的仪器名称为
的仪器名称为(2)A装置中发生反应生成
 的离子方程式为
的离子方程式为 的作用是
的作用是(3)B、C装置中盛放的试剂相同,其作用是
(4)在
 条件下,由
条件下,由 和
和 制备氯化氰的化学方程式为
制备氯化氰的化学方程式为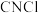 的电子式为
的电子式为(5)上述实验中,
 完全反应时收集到
完全反应时收集到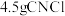 ,则产率为
,则产率为
您最近半年使用:0次
解题方法
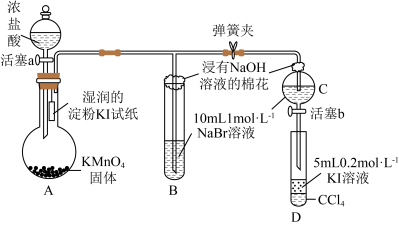
2 . 为证明卤族元素的非金属性强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检查)。
已知:①溴水呈黄色,而且颜色随浓度增大而加深。
② 容易从水中转移到
容易从水中转移到 中,导致下层(
中,导致下层( 层)因溶有
层)因溶有 显紫色。
显紫色。
实验过程:
①打开弹簧夹,打开活塞a,滴加浓盐酸。
②当B和C中的溶液都变为黄色时,夹紧弹簧夹。
③当B中溶液黄色加深时关闭活塞a。
④……
(1)NaOH的电子式为___________ 。
(2)A装置中制备氯气的离子方程式为___________ ,HCl的作用是做___________ 。
(3)B装置中主要反应的化学方程式为___________ 。
(4)为验证溴的氧化性强于碘,过程④的操作和现象分别是___________ 。
(5)过程③的实验目的是___________ 。
(6)结合元素周期表,从原子结构的角度解释氯、溴、碘单质的氧化性逐渐减弱的原因:___________ 。
(7)下列事实能说明元素Y的非金属性比硫元素强的是___________ 。
a.Y单质通入 溶液中,溶液出现淡黄色浑浊
溶液中,溶液出现淡黄色浑浊
b.与 反应时,1mol Y单质得到的电子比1mol S多
反应时,1mol Y单质得到的电子比1mol S多
c.Y和S的简单氢化物受热时,前者的分解温度较高
d.Y元素的氧化物对应水化物的酸性比S强
已知:①溴水呈黄色,而且颜色随浓度增大而加深。
②
 容易从水中转移到
容易从水中转移到 中,导致下层(
中,导致下层( 层)因溶有
层)因溶有 显紫色。
显紫色。实验过程:
①打开弹簧夹,打开活塞a,滴加浓盐酸。
②当B和C中的溶液都变为黄色时,夹紧弹簧夹。
③当B中溶液黄色加深时关闭活塞a。
④……
(1)NaOH的电子式为
(2)A装置中制备氯气的离子方程式为
(3)B装置中主要反应的化学方程式为
(4)为验证溴的氧化性强于碘,过程④的操作和现象分别是
(5)过程③的实验目的是
(6)结合元素周期表,从原子结构的角度解释氯、溴、碘单质的氧化性逐渐减弱的原因:
(7)下列事实能说明元素Y的非金属性比硫元素强的是
a.Y单质通入
 溶液中,溶液出现淡黄色浑浊
溶液中,溶液出现淡黄色浑浊b.与
 反应时,1mol Y单质得到的电子比1mol S多
反应时,1mol Y单质得到的电子比1mol S多c.Y和S的简单氢化物受热时,前者的分解温度较高
d.Y元素的氧化物对应水化物的酸性比S强
您最近半年使用:0次
解题方法
3 . 下表为元素周期表的一部分,针对表中①~⑧元素,回答下列问题:_____ ,M层有___ 个电子。写出③的原子结构示意图_____ 。
(2)元素②在周期表中的位置是_____ ,③元素在周期表中的位置是第2周期_____ 族。
(3)写出②的最高价氧化物_______ ,写出⑥的最高价氧化物_____ 。
(4)⑤和⑥两种元素的最高价氧化物对应水化物中碱性较强的是______ (填化学式)。
(5)⑤的单质在③中燃烧,产物是______ 。

(2)元素②在周期表中的位置是
(3)写出②的最高价氧化物
(4)⑤和⑥两种元素的最高价氧化物对应水化物中碱性较强的是
(5)⑤的单质在③中燃烧,产物是
您最近半年使用:0次
解题方法
4 . 现有8种元素的性质、数据如下表所列,它们属于第二或第三周期。
回答下列问题:
(1)③的元素符号是_____ ,④的元素名称是_____ 。①在元素周期表中的位置是(周期、族)_____ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_____ ;名称是_____ ;碱性最强的化合物的电子式是:_____ ,其含有的化学键的名称为_____ 。
(3)比较④和⑦的氢化物的稳定性(用化学式表示)_____ 。
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:_____ 。
(5)写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:_____ 。
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | |
| -2 | -3 | -1 | -3 |
(1)③的元素符号是
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是
(3)比较④和⑦的氢化物的稳定性(用化学式表示)
(4)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:
(5)写出②最高价氧化物对应水化物跟⑤的氢化物水溶液反应的离子方程式:
您最近半年使用:0次
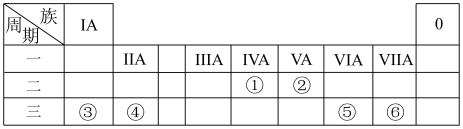
5 . 下表列出了①~⑥六种元素在元素周期表中的位置:
(1)元素②的单质的化学式是_______ ,元素⑥的单质的化学式是______ 。
(2)元素⑤与⑥的简单气态氢化物的热稳定性比较:_____ (填化学式)。
(3)这六种元素中,位于第三周期且原子半径最小的元素的原子结构示意图为_____ 。
(4)这六种元素中,能与氧结合,生成物可做耐火材料的是_____ (填元素符号)。
(5)在盛有水的小烧杯中加入元素③的单质,发生反应的化学方程式为_____ ;向上述反应后的溶液中再通入元素⑥的单质,发生反应的化学方程式为_____ 。
(1)元素②的单质的化学式是
(2)元素⑤与⑥的简单气态氢化物的热稳定性比较:
(3)这六种元素中,位于第三周期且原子半径最小的元素的原子结构示意图为
(4)这六种元素中,能与氧结合,生成物可做耐火材料的是
(5)在盛有水的小烧杯中加入元素③的单质,发生反应的化学方程式为
您最近半年使用:0次
名校
解题方法
6 . I 亚硝酰氯(NOCl)是有机药物制备的重要试剂,可按以下流程合成和利用。
(1)NOCl的电子式为___________ ,化合物X的结构简式为___________ 。
(2)下列说法正确的是___________。
(3)已知浓盐酸和浓硝酸混合配制王水时会产生亚硝酰氯,写出该反应的化学方程式___________ 。
Ⅱ 请回答下列问题:
(4)由磷原子核形成的三种微粒:a. 、b.
、b. 、c.
、c. ,半径由大到小的顺序为
,半径由大到小的顺序为___________ (填标号,下同);再失去一个电子所需最低能量由大到小的顺序为___________ 。
(5)比较H-O-H键角大小;H3O+___________ H2O(填“>”、“<”或“=”)。
(6)C为有机材料的主角,Si为无机材料的主角,SiC结构类似金刚石,下图为SiC的晶胞图,其中两个正方体中心重合、各面分别平行,其中心为Si原子(用•表示),试在小立方体画出相应C原子(用 表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。
表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。___________

(1)NOCl的电子式为
(2)下列说法正确的是___________。
| A.NOCl中的氮元素呈正价 |
| B.NOCl分子的空间结构为直线形 |
C.化合物X的沸点低于氯乙酰胺(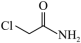 ) ) |
| D.工业上可以用蒸馏水吸收多余的NOCl,防止污染环境 |
(3)已知浓盐酸和浓硝酸混合配制王水时会产生亚硝酰氯,写出该反应的化学方程式
Ⅱ 请回答下列问题:
(4)由磷原子核形成的三种微粒:a.
 、b.
、b. 、c.
、c. ,半径由大到小的顺序为
,半径由大到小的顺序为(5)比较H-O-H键角大小;H3O+
(6)C为有机材料的主角,Si为无机材料的主角,SiC结构类似金刚石,下图为SiC的晶胞图,其中两个正方体中心重合、各面分别平行,其中心为Si原子(用•表示),试在小立方体画出相应C原子(用
 表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。
表示)的位置,在大正方体画出相应Si原子(用•表示)的位置。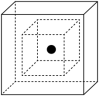
您最近半年使用:0次
解题方法
7 . 下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白(涉及表中元素一律用对应化学符号表示):
(1)在这些元素中,化学性质最不活泼的是:_____________ (填具体元素符号,下同),原子结构示意图为_____________ 。元素⑩名称为_____________ ,在周期表中的位置_________________ 。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是_________________ ,碱性最强的化合物的电子式是:_________________________ 。
(3)用电子式表示元素②的常见单质_____________ 其结构式为_________________ 。
(4)表示①与⑦的化合物的电子式为_________________ ,该化合物是由_____________ (填“极性”、“非极性”)键形成的。
(5)③、⑥、⑦三种元素形成的简单离子,离子半径由大到小的顺序是_________ 。
(6)元素③的简单氢化物的结构式为_____________________ ;该氢化物常温下和元素⑦的单质反应的化学方程式为 _____________________ 。
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)用电子式表示元素②的常见单质
(4)表示①与⑦的化合物的电子式为
(5)③、⑥、⑦三种元素形成的简单离子,离子半径由大到小的顺序是
(6)元素③的简单氢化物的结构式为
您最近半年使用:0次
8 . A、B、C、D、E四种元素,它们原子的核电荷数均小于18,且依次递增,A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子的最外层电子数之和与C原子的最外层电子数相等;D的最外层电子数是次外层电子数的3倍;E的单质是用途最广泛的半导体材料。试推断它们各是什么元素并回答下列问题:
(1)写出下列元素符号:A________ ,C________ ,E________ 。
(2)B、C、D的气态氢化物的稳定性由大到小的顺序为_____________ (用化学式表示)
(3)画出D的离子结构示意图______________ 。
(4)用一个化学方程式证明B、E的非金属性的强弱________________ 。
(5)写出E的最高价氧化物的一种用途:_______________ 。
(1)写出下列元素符号:A
(2)B、C、D的气态氢化物的稳定性由大到小的顺序为
(3)画出D的离子结构示意图
(4)用一个化学方程式证明B、E的非金属性的强弱
(5)写出E的最高价氧化物的一种用途:
您最近半年使用:0次
9 . 在研究前18号元素时发现,随原子序数递增可以将它们排成如图所示的蜗牛形状。图中每个点代表一种元素,其中①代表氢元素。___________ 键(填“离子”或“共价”);
(2)写出由元素①、②、③形成的化合物的电子式___________ 。
(3)Li和元素③在同一族,现代航天工业中选择用 做供氧剂的原因是
做供氧剂的原因是___________ 。
(4)元素④在元素周期表中的位置是___________ 。
(5)自然界磷元素只存在一种稳定的核素 。约里奧-居里夫妇在核反应中用α粒子轰击
。约里奧-居里夫妇在核反应中用α粒子轰击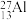 ,得到另一种核素
,得到另一种核素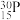 。
。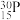 与
与 的关系是
的关系是___________ 。
(6)请设计实验验证元素④的非金属性弱于元素⑤的非金属性___________ (用离子方程式表示)。
(7)向由元素②、③、⑤按原子个数比1∶1∶1组成的化合物水溶液中滴入石蕊试液,溶液变成蓝色,一段时间后溶液颜色褪去,请解释原因___________ 。

(2)写出由元素①、②、③形成的化合物的电子式
(3)Li和元素③在同一族,现代航天工业中选择用
 做供氧剂的原因是
做供氧剂的原因是(4)元素④在元素周期表中的位置是
(5)自然界磷元素只存在一种稳定的核素
 。约里奧-居里夫妇在核反应中用α粒子轰击
。约里奧-居里夫妇在核反应中用α粒子轰击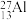 ,得到另一种核素
,得到另一种核素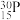 。
。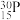 与
与 的关系是
的关系是(6)请设计实验验证元素④的非金属性弱于元素⑤的非金属性
(7)向由元素②、③、⑤按原子个数比1∶1∶1组成的化合物水溶液中滴入石蕊试液,溶液变成蓝色,一段时间后溶液颜色褪去,请解释原因
您最近半年使用:0次
解题方法
10 . 153年前门捷列夫制得世界上第一张元素周期表,它反映了元素之间的内在联系,是对元素的一种很好的自然分类。下图为现代元素周期表的一部分,请回答下列问题(以下问题均用相应的化学符号表达):________________
(2)元素①的简单气态氢化物的电子式为_________________ ;
用电子式表示②与⑨形成 化合物的过程:
化合物的过程:______________
(3) 是弱酸,它的浓溶液与软锰矿的反应和⑧的氢化物与软锰矿的反应类似,请写出浓
是弱酸,它的浓溶液与软锰矿的反应和⑧的氢化物与软锰矿的反应类似,请写出浓 溶液和软锰矿在加热条件下反应的化学方程式:
溶液和软锰矿在加热条件下反应的化学方程式:____________ ;反应中断裂的化学键类型有_________ 、__________ 。
(4)比较元素⑦⑧形成的气态氢化物的稳定性:_________ >_______ 。

(2)元素①的简单气态氢化物的电子式为
用电子式表示②与⑨形成
 化合物的过程:
化合物的过程:(3)
 是弱酸,它的浓溶液与软锰矿的反应和⑧的氢化物与软锰矿的反应类似,请写出浓
是弱酸,它的浓溶液与软锰矿的反应和⑧的氢化物与软锰矿的反应类似,请写出浓 溶液和软锰矿在加热条件下反应的化学方程式:
溶液和软锰矿在加热条件下反应的化学方程式:(4)比较元素⑦⑧形成的气态氢化物的稳定性:
您最近半年使用:0次



