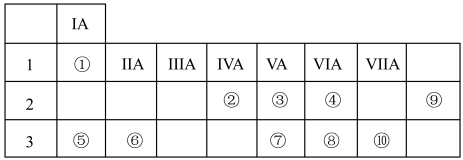
1 . 下表列出了①~⑨九种元素在周期表中的位置:
(1)元素④在周期表中所处位置_______ 。
(2)按气态氢化物的稳定性由强到弱的顺序排列,④⑦⑧的氢化物稳定性:_______ (写氢化物的化学式)。
(3)元素⑤、⑥最高价氧化物对应水化物的碱性强弱为_______ (填化学式)。
(4)元素⑧的原子结构示意图是_______ 。
(5)写出元素⑤形成的单质在氧气中燃烧的化学方程式_______ 。
(6)用电子式表示⑤与⑧反应得到的化合物的形成过程_______ 。
(1)元素④在周期表中所处位置
(2)按气态氢化物的稳定性由强到弱的顺序排列,④⑦⑧的氢化物稳定性:
(3)元素⑤、⑥最高价氧化物对应水化物的碱性强弱为
(4)元素⑧的原子结构示意图是
(5)写出元素⑤形成的单质在氧气中燃烧的化学方程式
(6)用电子式表示⑤与⑧反应得到的化合物的形成过程
您最近一年使用:0次
名校
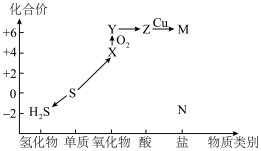
2 . 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系: 的电子式为
的电子式为________ ;将 与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为
与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为________ 。
(2)S粉与热的Z浓溶液反应可转化为________ ,反应的化学方程式为________ 。
(3)配平下列反应:_____
____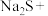 ____
____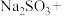 ____
____ ____
____ ____
____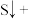 ____
____
(4)下列有关硫及其化合物的性质,说法正确的是
(5)某同学为探究Cu与浓硫酸的反应,用如图所示的装置进行有关实验。________ 。
②C的作用是________ ,装置D中试管口放置的棉花应浸有一种液体,这种液体是________ 。
 的电子式为
的电子式为 与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为
与X混合,可生成黄色固体,该反应氧化产物与还原产物的质量之比为(2)S粉与热的Z浓溶液反应可转化为
(3)配平下列反应:
____
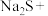 ____
____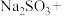 ____
____ ____
____ ____
____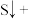 ____
____
(4)下列有关硫及其化合物的性质,说法正确的是
| A.X能使溴水褪色,证明X有漂白性 | B.将X通入 溶液中有白色沉淀生成 溶液中有白色沉淀生成 |
C.硫在过量的 中燃烧可以生成Y 中燃烧可以生成Y | D.若N为钠盐,则N与Z的稀溶液反应可生成 |
(5)某同学为探究Cu与浓硫酸的反应,用如图所示的装置进行有关实验。

②C的作用是
您最近一年使用:0次
名校
3 . 根据①~⑩号元素所在周期表中的位置,回答下列问题:

(1)⑨形成的简单离子结构示意图为___________ 。
(2)用电子式表示⑤和⑩形成原子数目比为1:2的化合物的形成过程___________ 。
(3)②③④三种元素分别形成简单离子的离子半径由大到小的顺序是_________ (填离子符号)。
(4)①和⑧构成的化合物能和水剧烈反应产生氢气,该反应的化学方程式为___________ 。
(5)⑥的单质与④的最高价氧化物对应水化物反应的离子方程式为___________ 。
(6)②和⑦相比非金属性较强的是___________ (填元素符号),下列能证明这一事实的有___________ (填序号)。
A.⑦的简单氢化物稳定性强于②的简单氢化物
B.⑦的简单氢化物酸性强于②的简单氢化物
C.⑦单质与氢气反应比②单质与氢气反应更加剧烈
D.⑦单质的熔点比②单质的低
(7)运用元素周期律推测陌生元素的性质,下列推断错误的是___________(填序号)

(1)⑨形成的简单离子结构示意图为
(2)用电子式表示⑤和⑩形成原子数目比为1:2的化合物的形成过程
(3)②③④三种元素分别形成简单离子的离子半径由大到小的顺序是
(4)①和⑧构成的化合物能和水剧烈反应产生氢气,该反应的化学方程式为
(5)⑥的单质与④的最高价氧化物对应水化物反应的离子方程式为
(6)②和⑦相比非金属性较强的是
A.⑦的简单氢化物稳定性强于②的简单氢化物
B.⑦的简单氢化物酸性强于②的简单氢化物
C.⑦单质与氢气反应比②单质与氢气反应更加剧烈
D.⑦单质的熔点比②单质的低
(7)运用元素周期律推测陌生元素的性质,下列推断错误的是___________(填序号)
| A.铊(Tl)单质既能与盐酸作用产生氢气,又能与NaOH溶液反应放出氢气 |
| B.砹(At)单质为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀硝酸 |
C.锂(Li)单质在氧气中剧烈燃烧,产物是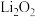 |
D.硫酸锶( )是难溶于水的白色固体 )是难溶于水的白色固体 |
您最近一年使用:0次
解题方法
4 . 如图是元素周期表的一部分。回答下列问题:

(1)世界上绝大部分卤素都存在于海洋中,海洋是卤素的资源宝库。
① 的离子结构示意图为
的离子结构示意图为________ 。
②表中几种元素的最高价氧化物对应水化物酸性最强的是________ (填化学式);写出该物质在水溶液中的电离方程式:________ 。
③用电子式表示短周期元素中,原子半径最大的元素与氯形成的简单化合物的形成过程:________ 。
④氰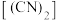 是一种无色、可燃气体,剧毒、有苦杏仁味,与卤素单质的性质相似,试写出氰与NaOH溶液在常温下反应的离子方程式:
是一种无色、可燃气体,剧毒、有苦杏仁味,与卤素单质的性质相似,试写出氰与NaOH溶液在常温下反应的离子方程式:________ 。
(2)硒是人体必需的微量元素,起到抗氧化的作用。
①写出Se在周期表中的位置:________ 。
② 溶于水生成
溶于水生成 ,向所得溶液中通入
,向所得溶液中通入 气体发生反应,生成Se和
气体发生反应,生成Se和 。写出
。写出 与
与 反应的化学方程式:
反应的化学方程式:________ 。
(3)下列说法正确的是________ (填字母)。
a.原子半径: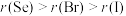
b. 中存在的化学键为非极性共价键
中存在的化学键为非极性共价键
c.非金属性:Cl>Se>Br

(1)世界上绝大部分卤素都存在于海洋中,海洋是卤素的资源宝库。
①
 的离子结构示意图为
的离子结构示意图为②表中几种元素的最高价氧化物对应水化物酸性最强的是
③用电子式表示短周期元素中,原子半径最大的元素与氯形成的简单化合物的形成过程:
④氰
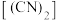 是一种无色、可燃气体,剧毒、有苦杏仁味,与卤素单质的性质相似,试写出氰与NaOH溶液在常温下反应的离子方程式:
是一种无色、可燃气体,剧毒、有苦杏仁味,与卤素单质的性质相似,试写出氰与NaOH溶液在常温下反应的离子方程式:(2)硒是人体必需的微量元素,起到抗氧化的作用。
①写出Se在周期表中的位置:
②
 溶于水生成
溶于水生成 ,向所得溶液中通入
,向所得溶液中通入 气体发生反应,生成Se和
气体发生反应,生成Se和 。写出
。写出 与
与 反应的化学方程式:
反应的化学方程式:(3)下列说法正确的是
a.原子半径:
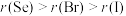
b.
 中存在的化学键为非极性共价键
中存在的化学键为非极性共价键c.非金属性:Cl>Se>Br
您最近一年使用:0次
解题方法
5 . 四氯化钛( )是制取航天工业材料——钛合金的重要原料。实验室以
)是制取航天工业材料——钛合金的重要原料。实验室以 和
和 为原料制取液态
为原料制取液态 的装置如图所示(部分夹持装置省略)。
的装置如图所示(部分夹持装置省略)。
①反应原理: 。
。
②反应条件:无水、无氧,加热。
回答下列问题:
(1)所装稀硫酸的仪器名称为___________ 。装置C处用热水浴的目的是___________ 。
(2)若没有装置F,则装置E中产生白雾的原因是___________ 。
(3)实验开始时,缓慢滴入稀硫酸,能证明 已排尽装置中的空气的实验现象是
已排尽装置中的空气的实验现象是___________ 。
(4)从E处产物中分离出 的实验方法是
的实验方法是___________ 。
(5) 的电子式为
的电子式为___________ 。
(6) 还可由
还可由 、焦炭和氯气在加热条件下制得,生成体积比为2:1的
、焦炭和氯气在加热条件下制得,生成体积比为2:1的 和
和 混合气体,反应中氧化剂与还原剂的物质的量之比为4:3,反应的化学方程式为
混合气体,反应中氧化剂与还原剂的物质的量之比为4:3,反应的化学方程式为___________ 。
 )是制取航天工业材料——钛合金的重要原料。实验室以
)是制取航天工业材料——钛合金的重要原料。实验室以 和
和 为原料制取液态
为原料制取液态 的装置如图所示(部分夹持装置省略)。
的装置如图所示(部分夹持装置省略)。①反应原理:
 。
。②反应条件:无水、无氧,加热。

| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
 | -23 | 76 | 与 互溶 互溶 |
 | -25 | 136 | 遇潮湿空气产生白雾,在550℃时能被氧气氧化 |
(1)所装稀硫酸的仪器名称为
(2)若没有装置F,则装置E中产生白雾的原因是
(3)实验开始时,缓慢滴入稀硫酸,能证明
 已排尽装置中的空气的实验现象是
已排尽装置中的空气的实验现象是(4)从E处产物中分离出
 的实验方法是
的实验方法是(5)
 的电子式为
的电子式为(6)
 还可由
还可由 、焦炭和氯气在加热条件下制得,生成体积比为2:1的
、焦炭和氯气在加热条件下制得,生成体积比为2:1的 和
和 混合气体,反应中氧化剂与还原剂的物质的量之比为4:3,反应的化学方程式为
混合气体,反应中氧化剂与还原剂的物质的量之比为4:3,反应的化学方程式为
您最近一年使用:0次
2024-01-10更新
|
55次组卷
|
2卷引用:甘肃省天水市第三中学、天水九中、新梦想高考复读学校2023-2024学年高三上学期12月份大联考化学试题
名校
解题方法
6 . a、b、c、d为四种由短周期元素构成的中性粒子,它们都有14个电子,且除a外都是共价型分子。回答下列问题:
(1)a是单核粒子,a单质可用作半导体材料,a所形成的晶体类型为___________ 晶体。
(2)b是双核化合物,常温下为无色无味气体,则b的化学式为___________ 。
(3)c是双核单质,写出其电子式:___________ 。c分子中所含共价键的类型为___________ (填“极性键”或“非极性键”)。物质c与氢气反应所生成的氢化物易溶于水的原因是___________ (写一条即可)。
(4)d是四核化合物,其结构式为___________ ;d分子内所含共价键 键与
键与 键个数比为
键个数比为___________ ;d分子的空间结构为___________ 。
(1)a是单核粒子,a单质可用作半导体材料,a所形成的晶体类型为
(2)b是双核化合物,常温下为无色无味气体,则b的化学式为
(3)c是双核单质,写出其电子式:
(4)d是四核化合物,其结构式为
 键与
键与 键个数比为
键个数比为
您最近一年使用:0次
名校
解题方法
7 . 某磁铁矿石A的主要成分是磁性氧化铁(Fe3O4),还含少量的Al2O3、Cu2O。某工厂利用此矿石进行有关物质的回收利用,其中F为常见的补铁剂,工艺流程如图(已知Cu2O不溶于水和碱,但溶于强酸:Cu2O+2H+=Cu+Cu2++H2O)。根据流程回答下列问题:_____ ,铝离子的结构示意图为_____ 。
(2)溶液D与过量试剂X反应的离子方程式是_____ 、_____ 。
(3)在溶液F中滴加NaOH溶液的现象是_____ 。
(4)操作1的名称为_____ 。
(5)已知E为红色固体,写出证明E中无Cu2O的方法:_____ (写出实验操作与现象)。
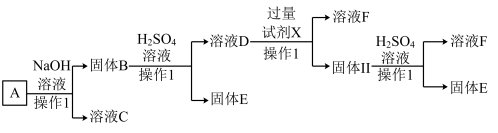
(2)溶液D与过量试剂X反应的离子方程式是
(3)在溶液F中滴加NaOH溶液的现象是
(4)操作1的名称为
(5)已知E为红色固体,写出证明E中无Cu2O的方法:
您最近一年使用:0次
2023-04-15更新
|
594次组卷
|
5卷引用:甘肃省武威市民勤县第一中学2023-2024学年高一下学期开学考试化学试题
甘肃省武威市民勤县第一中学2023-2024学年高一下学期开学考试化学试题(已下线)广东省深圳中学2022-2023学年高一上学期期末考试化学试题(已下线)专项02 离子反应和氧化还原反应的应用-【好题汇编】备战2023-2024学年高一化学上学期期末真题分类汇编(人教版2019必修第一册)广东省深圳市南头中学2023-2024学年高一上学期期末调研考试(模拟)化学试题新疆生产建设兵团第三师图木舒克市第二中学2023-2024学年高一下学期开学考试化学试题
名校
解题方法
8 . 下图是元素周期表的一部分。按要求填写下列空白:
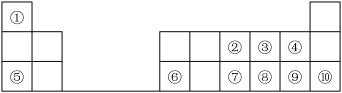
(1)元素⑦在周期表中的位置可表示为_______ 。
(2)④、⑧、⑨的简单离子半径的大小顺序为_______ (填离子符号)。
(3)①-⑩元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式)。
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是_______ (用化学式表示)。
(5)⑤的最高价氧化物对应的水化物的电子式为_______ ;⑧的气态氢化物的结构式为_______ ;已知①③⑨可形成一种常见的一元弱酸,用电子式表示其形成过程:_______ 。
(6)已知元素在周期表中的位置,反映了元素的原子结构和性质。运用元素周期律,可以推测陌生元素的性质,分析下面的推断错误的是_______ (填序号)。
①铊(Tl)单质既能与盐酸作用产生氢气,又能与NaOH溶液反应放出氢气
②砹(At)单质为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀硝酸
③锂(Li)单质在氧气中剧烈燃烧,产物是Li2O2
④硫酸锶(SrSO4)是难溶于水的白色固体
⑤硒化氢(H2Se)比H2S稳定

(1)元素⑦在周期表中的位置可表示为
(2)④、⑧、⑨的简单离子半径的大小顺序为
(3)①-⑩元素的最高价氧化物对应的水化物中,酸性最强的是
(4)④⑧⑨三种元素形成的气态氢化物稳定性由大到小的顺序是
(5)⑤的最高价氧化物对应的水化物的电子式为
(6)已知元素在周期表中的位置,反映了元素的原子结构和性质。运用元素周期律,可以推测陌生元素的性质,分析下面的推断错误的是
①铊(Tl)单质既能与盐酸作用产生氢气,又能与NaOH溶液反应放出氢气
②砹(At)单质为有色固体,HAt不稳定,AgAt不溶于水也不溶于稀硝酸
③锂(Li)单质在氧气中剧烈燃烧,产物是Li2O2
④硫酸锶(SrSO4)是难溶于水的白色固体
⑤硒化氢(H2Se)比H2S稳定
您最近一年使用:0次
名校
9 . 下表是元素周期表的一部分,表中所列的数字分别代表某一种元素。
请回答下列问题:
(1)属于卤族元素的有_______ (填元素符号,下同);属于碱金属元素的有_______ 。
(2)②③原子结构的相同点是_______ 。
(3)画出元素④的原子结构示意图:_______ ;元素④与⑤同属于_______ 族;预测它们单质的化学性质的相似性是_______ 。
(4)元素⑥与⑦的原子最外层电子数都为_______ ;单质的氧化性:⑥_______ (填“>”或“<”)⑦,其依据是_______ 。
(5)写出一种由上述九种元素中的三种不同主族元素组成的离子化合物的化学式:_______ (任写一种)。
| 周期 | IA | 0 | ||||||
| 一 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 二 | ⑥ | |||||||
| 三 | ② | ④ | ⑦ | ⑧ | ||||
| 四 | ③ | ⑤ | ⑨ |
(1)属于卤族元素的有
(2)②③原子结构的相同点是
(3)画出元素④的原子结构示意图:
(4)元素⑥与⑦的原子最外层电子数都为
(5)写出一种由上述九种元素中的三种不同主族元素组成的离子化合物的化学式:
您最近一年使用:0次
10 . 下表列出了①~⑧八种元素在周期表中的位置:
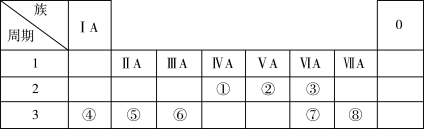
请回答下列问题:
(1)①、②、③三种元素中非金属性最强的是_______ (用元素符号表示)。
(2)写出④、⑥两种元素的最高价氧化物对应水化物在溶液中相互反应的离子方程式:_______ 。
(3)画出⑤的原子结构示意图_______ 。
(4)⑦、⑧两种元素原子半径大小比较_______ (用元素符号表示)。
(5)画出⑧的氢化物的电子式_______ 。
(6)写出②、⑧氢化物反应的化学方程式_______ 。

请回答下列问题:
(1)①、②、③三种元素中非金属性最强的是
(2)写出④、⑥两种元素的最高价氧化物对应水化物在溶液中相互反应的离子方程式:
(3)画出⑤的原子结构示意图
(4)⑦、⑧两种元素原子半径大小比较
(5)画出⑧的氢化物的电子式
(6)写出②、⑧氢化物反应的化学方程式
您最近一年使用:0次



