名校
1 . Ⅰ.A、B、C、D、E五种元素的核电荷数均小于18,且依次增大。A原子核内仅有一个质子;B原子的电子总数与D原子的最外层电子数相等;A原子与B原子最外层电子数之和与C原子的最外层电子数相等;D原子最外层电子数是次外层电子数的3倍,E的最高价氧化物对应水化物的碱性在短周期元素中最强。
(1)B元素原子的结构示意图:_______ 。
(2)甲、乙、丙、丁是由以上部分元素组成的10电子微粒。阳离子甲和阴离子乙在加热条件下生成的丙和丁,请写出该反应的离子方程式_______ 。
(3)化合物W是由元素D和E组成的淡黄色固体,则W的电子式为_______ 。
(4)由元素A、C、D组成的盐M,其中含有的化学键类型有_______ ,属于_______ (共价化合物或离子化合物)。
Ⅱ.最近,德国科学家实现了Rb原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知Rb的原子序数为37,相对原子质量是85。
(5)Rb在元素周期表中的位置为_______ 。下列关于Rb的说法中不正确的是_______ 。
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(1)B元素原子的结构示意图:
(2)甲、乙、丙、丁是由以上部分元素组成的10电子微粒。阳离子甲和阴离子乙在加热条件下生成的丙和丁,请写出该反应的离子方程式
(3)化合物W是由元素D和E组成的淡黄色固体,则W的电子式为
(4)由元素A、C、D组成的盐M,其中含有的化学键类型有
Ⅱ.最近,德国科学家实现了Rb原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知Rb的原子序数为37,相对原子质量是85。
(5)Rb在元素周期表中的位置为
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
您最近一年使用:0次
名校
2 . Ⅰ.下列8种化学符号: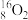 、
、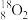 、
、 、
、 、
、 、
、 、
、 、
、
(1)表示核素的符号共_______ 种。
(2)互为同位素的是_______ 。
(3)质量相同的H216O和D216O所含中子数之比为_______ 。
请回答下列问题:
(4)Y在元素周期表中的位置是_______ 。
(5)X、Z两种元素的气态氢化物稳定性由强到弱的顺序为:_______ 。(化学式表示)
(6)Z、W两种元素的最高价氧化物对应水化物的酸性由强到弱的的顺序为:_______ (用化学式表示)
(7)下列说法能比较出Y与同族的短周期元素Q非金属性强弱的是:_______。
(8)P是W的同族元素,其最高价氧化物可用于制造光导纤维,写出P最高价氧化物与NaOH溶液反应的离子方程式:_______ 。
(9)用电子式表示WY2的形成过程:_______ 。
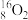 、
、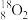 、
、 、
、 、
、 、
、 、
、 、
、
(1)表示核素的符号共
(2)互为同位素的是
(3)质量相同的H216O和D216O所含中子数之比为
Ⅱ.短周期元素X、Y、Z、W在周期表中的相对位置如下图所示,其中W元素的原子结构示意图为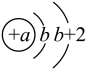 。
。
W | X | Y |
Z |
请回答下列问题:
(4)Y在元素周期表中的位置是
(5)X、Z两种元素的气态氢化物稳定性由强到弱的顺序为:
(6)Z、W两种元素的最高价氧化物对应水化物的酸性由强到弱的的顺序为:
(7)下列说法能比较出Y与同族的短周期元素Q非金属性强弱的是:_______。
| A.Y单质与Q单质发生置换反应 |
| B.Y与Q最高价氧化物对应的水化物的酸性 |
| C.Y、Q形成的化合物中两元素的化合价 |
| D.Y、Q的最简单气态氢化物的沸点 |
(8)P是W的同族元素,其最高价氧化物可用于制造光导纤维,写出P最高价氧化物与NaOH溶液反应的离子方程式:
(9)用电子式表示WY2的形成过程:
您最近一年使用:0次
名校
3 . X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:①元素周期表中,Z与Y相邻,Z与W相邻;②X分别与Y、Z、W可组成化学式为YX3,X2Z和X2W三种共价化合物;③Y的最简氢化物可与其最高价含氧酸反应。
(1)W在元素周期表中的位置是___________ 。
(2)X2W的结构式是___________ 。
(3)X、Y和Z组成的一种化合物是强酸,写出该酸的稀溶液与铜反应的离子方程式:___________ 。
(4)Y的最简氢化物与其最高价含氧酸反应产物为___________ (填化学式),写出检验其阳离子的办法___________ 。
(5)由X、Z元素构成既有极性键又有非极性键的化合物的电子式是___________ 。
(1)W在元素周期表中的位置是
(2)X2W的结构式是
(3)X、Y和Z组成的一种化合物是强酸,写出该酸的稀溶液与铜反应的离子方程式:
(4)Y的最简氢化物与其最高价含氧酸反应产物为
(5)由X、Z元素构成既有极性键又有非极性键的化合物的电子式是
您最近一年使用:0次
名校
4 . 已知A、B、C、D、E、F、G、H为原子序数依次增大的主族元素,其中D与G同族,且D为短周期主族元素中原子半径最大的元素,常见的F的单质为有色气体。A、B、C、E、F、H在元素周期表中的相对位置如图,请回答下列问题:
(1)已知元素H的一种核素的中子数为45,请用原子符号表示该核素:___________ 。
(2)请用电子式表示D和E的原子形成化合物(该化合物含有三个原子核)的过程:___________ 。
(3)元素D和C可组成淡黄色固体,该化合物所含的化学键类型有___________ (填“离子键”、“极性键”或“非极性键”)。
(4)C和E的最简单氢化物中稳定性较强的是___________ (填化学式)。
(5)为确定 中是否含有
中是否含有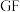 ,可使用的鉴别方法为
,可使用的鉴别方法为___________ 。
(6)比较元素E和F的非金属性强弱:在E的氢化物的水溶液中通入少量F的单质,可观察到的实验现象是___________ ,写出发生反应的化学方程式:___________ 。
(7)请从原子结构的角度解释C的非金属性强与E的原因___________ 。
| A | B | C | |
| E | F | ||
| H |
(2)请用电子式表示D和E的原子形成化合物(该化合物含有三个原子核)的过程:
(3)元素D和C可组成淡黄色固体,该化合物所含的化学键类型有
(4)C和E的最简单氢化物中稳定性较强的是
(5)为确定
 中是否含有
中是否含有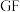 ,可使用的鉴别方法为
,可使用的鉴别方法为(6)比较元素E和F的非金属性强弱:在E的氢化物的水溶液中通入少量F的单质,可观察到的实验现象是
(7)请从原子结构的角度解释C的非金属性强与E的原因
您最近一年使用:0次
名校
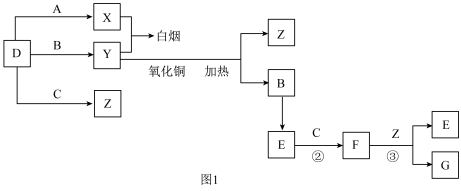
5 . A、B、C、D是四种常见气体单质。E的相对分子质量比F小16,且F为红棕色。有关的转化关系如图1所示(反应条件与部分反应的生成物略去)。
(1)D的化学式为_______ ,Y的电子式为_______ 。
(2)Y与氧化铜反应,每生成1molB消耗3mol氧化铜,该反应的化学方程式为________ 。
(3)Y与E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为_______ 。
(4)气体F和气体 在通常条件下同时通入盛有
在通常条件下同时通入盛有 溶液的洗气瓶中(如图2所示),洗气瓶中是否有沉淀生成?
溶液的洗气瓶中(如图2所示),洗气瓶中是否有沉淀生成?______ (填“是”或“否”),理由是_______ 。 ②(体积比)
②(体积比) ③
③ 充满干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,假设烧瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度由大到小的顺序为
充满干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,假设烧瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度由大到小的顺序为_______ (用①②③表示)。
(1)D的化学式为
(2)Y与氧化铜反应,每生成1molB消耗3mol氧化铜,该反应的化学方程式为
(3)Y与E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为
(4)气体F和气体
 在通常条件下同时通入盛有
在通常条件下同时通入盛有 溶液的洗气瓶中(如图2所示),洗气瓶中是否有沉淀生成?
溶液的洗气瓶中(如图2所示),洗气瓶中是否有沉淀生成?
 ②(体积比)
②(体积比) ③
③ 充满干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,假设烧瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度由大到小的顺序为
充满干燥烧瓶,将烧瓶倒置于水中,瓶内液面逐渐上升,假设烧瓶内溶液不扩散,则最终该溶液中溶质的物质的量浓度由大到小的顺序为
您最近一年使用:0次
名校
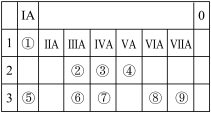
6 . 下图是元素周期表的一部分,针对表中①~⑦元素,填写下列空白:
(1)对⑧⑨元素说法正确的是 。
(2)下列说法正确的是 。
(3)下列比较正确的是 。
(4)下列说法正确的是 。
(5)对各种元素的实验室制法或工业制法错误的是 。
| 族 周期 | IA | 0 | ||||||
| 1 | ⑧ | IIA | IIIA | IVA | VA | VIA | VIIA | ⑨ |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ |
| A.⑧单质通常是双原子分子,⑨单质是单原子分子 |
| B.3H质量数是3,中子数是1 |
| C.⑧属于IA主族元素,是碱金属 |
| D.⑧单质是最轻的气体,有三种同位素 |
| A.②元素的最低价氢化物的化学式为NH3 | B.⑦的氢化物属于共价化合物 |
C.②元素的原子结构示意图为 | D.F的最高价为+7价 |
| A.②和⑥两种元素的原子半径大小为:②<⑥ |
| B.④和⑤两种元素的金属性强弱顺序为:④>⑤ |
| C.②③⑦的氢化物稳定性比较:②<③ ③>⑦ |
| D.最高价氧化物的水化物碱性比较:④>⑤ |
| A.元素④与⑦形成的化合物只含离子键,属于离子化合物。 |
| B.⑤的单质,最高价氧化物,最高价氧化物的水化物都能和盐酸反应,也能和NaOH溶液反应 |
| C.③的氢化物水溶液是弱酸,不能刻蚀玻璃 |
| D.②的氢化物不能制取化肥,但可以做制冷剂 |
| A.④单质的制法是电解熔融的氯化物 | B.⑤单质的制法是电解熔融的氧化物 |
| C.⑧单质的制法:可用Zn与盐酸反应 | D.⑦单质可用MnO2与稀盐酸加热制取 |
您最近一年使用:0次
名校
解题方法
7 . (1)A、B、C、D、E五种短周期元素,原子序数依次递增,A原子形成的阳离子是一个质子,B原子的最外层电子数是次外层的2倍,C原子的最外层电子数与B原子的核外电子总数相等,D在同周期元素中原子半径最大,而E在同周期元素中原子半径最小。A、C、D三种元素可形成化合物甲,B、C、D三种元素可形成化合物乙,甲和乙均为中学化学常见物质。请回答:
①甲的电子式为___________ ,其中所含化学键类型为___________ 。
②A的单质与C的单质燃烧产物的类型___________ (从化学键角度分类) 。
③A与C、D与C可形成化合物A2C、A2C2、D2C、D2C2,说出D2C2的一种用途___________ ;写出D2C2与E的氢化物的水溶液反应的离子方程式___________ 。
(2)某元素的同位素X,它的氯化物XCl 1.49 g溶于水制成溶液后,加入1mol·L-1的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,试通过计算确定:
①X元素在周期表中的位置___________ ;
②把一小粒X的单质放入水中,写出反应的离子方程式___________ 。
(3)选择适宜的材料和试剂设计一个原电池,以便完成下列反应:2Fe3++Fe=3Fe3+。画出原电池的示意图标注电极名称___________ 。
①甲的电子式为
②A的单质与C的单质燃烧产物的类型
③A与C、D与C可形成化合物A2C、A2C2、D2C、D2C2,说出D2C2的一种用途
(2)某元素的同位素X,它的氯化物XCl 1.49 g溶于水制成溶液后,加入1mol·L-1的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,试通过计算确定:
①X元素在周期表中的位置
②把一小粒X的单质放入水中,写出反应的离子方程式
(3)选择适宜的材料和试剂设计一个原电池,以便完成下列反应:2Fe3++Fe=3Fe3+。画出原电池的示意图标注电极名称
您最近一年使用:0次
名校
8 . 元素周期律的发现和元素周期表的诞生,开创了化学科学的新纪元。
Ⅰ.2019年是门捷列夫提出元素周期表150周年。下表为元素周期表的一部分,回答下列问题。 分子,用电子式表示该分子的形成过程:
分子,用电子式表示该分子的形成过程:______ 。
(2)⑤⑥⑧⑨中形成简单离子半径由大到小的顺序是______ (用离子符号表示)。
(3)用一个化学反应证明元素③比元素⑦的得电子能力强,该反应的离子方程式为______
Ⅱ.短周期元素X、Y、Z原子序数依次增大,其中Y元素的一种同位素可用于文物年代的断定,且其最外层电子数等于X、Z最外层电子总和的一半。Y、Z可形成 型化合物且分子中每个原子均满足8电子稳定结构。关于三种元素的价类二维图如下所示:
型化合物且分子中每个原子均满足8电子稳定结构。关于三种元素的价类二维图如下所示:
(4) 的化学式为
的化学式为______ 。X在空气中燃烧可获得 ,与X相邻的同主族金属元素Q在空气中燃烧可获得
,与X相邻的同主族金属元素Q在空气中燃烧可获得______ (填化学式);由此可判断,X、Q金属性较强的是______ (填元素符号)。
(5)用合适的方程式证明⑤的酸性强于⑥______ ,依据该事实______ (填“能”或“不能”)判断出Y、Z的非金属性强弱,理由是____________ 。
Ⅰ.2019年是门捷列夫提出元素周期表150周年。下表为元素周期表的一部分,回答下列问题。
 分子,用电子式表示该分子的形成过程:
分子,用电子式表示该分子的形成过程:(2)⑤⑥⑧⑨中形成简单离子半径由大到小的顺序是
(3)用一个化学反应证明元素③比元素⑦的得电子能力强,该反应的离子方程式为
Ⅱ.短周期元素X、Y、Z原子序数依次增大,其中Y元素的一种同位素可用于文物年代的断定,且其最外层电子数等于X、Z最外层电子总和的一半。Y、Z可形成
 型化合物且分子中每个原子均满足8电子稳定结构。关于三种元素的价类二维图如下所示:
型化合物且分子中每个原子均满足8电子稳定结构。关于三种元素的价类二维图如下所示: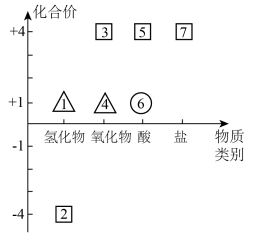
(4)
 的化学式为
的化学式为 ,与X相邻的同主族金属元素Q在空气中燃烧可获得
,与X相邻的同主族金属元素Q在空气中燃烧可获得(5)用合适的方程式证明⑤的酸性强于⑥
您最近一年使用:0次
名校
解题方法
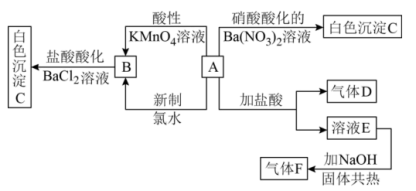
9 . 一种白色晶体A极易溶于水,将A配成溶液进行如下框图所示的实验,实验现象及转化关系如下列框图所示。其中A为正盐,气体D能使品红溶液褪色,气体F能使湿润的红色石蕊试纸变蓝。
(1)写出下列物质化学式:A___________ ;C___________ ;
(2)写出F的电子式:___________ ;
(3)写出溶液E与 共热反应的离子方程式:
共热反应的离子方程式:___________ ;
(4)写出A和新制氯水反应的离子方程式:___________ 。
(1)写出下列物质化学式:A
(2)写出F的电子式:
(3)写出溶液E与
 共热反应的离子方程式:
共热反应的离子方程式:(4)写出A和新制氯水反应的离子方程式:
您最近一年使用:0次
10 . 下表为元素周期表的一部分,回答下列问题。
(1)写出单质⑥与强碱水溶液反应的离子方程式:__________________ 。
(2)关于⑩所在主族的单质及化合物的叙述错误的是________(填字母)
(3)⑤与⑨可以形成________ (填“共价”或“离子”)化合物,用电子式表示其形成过程为________ 。
(4)为了探究元素②、③、⑦的非金属性强弱,该兴趣小组又设计如下装置, 、稀盐酸、碳酸钙、
、稀盐酸、碳酸钙、 溶液、饱和
溶液、饱和 溶液,
溶液,
已知 不溶于水。据此回答以下问题。
不溶于水。据此回答以下问题。
分液漏斗内装入的试剂为________ ,B中装入的试剂为________ ,烧杯C中发生反应的离子方程式为________________________________ 。(已知硅酸钠溶液足量)
ⅠA | 0 | |||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)关于⑩所在主族的单质及化合物的叙述错误的是________(填字母)
| A.从上到下,单质颜色越来越深,熔、沸点越来越高 |
| B.单质均可与水发生反应生成两种酸 |
C.单质均具有强氧化性,能将Fe氧化成 |
| D.氢化物均易溶于水,且均为强酸 |
(4)为了探究元素②、③、⑦的非金属性强弱,该兴趣小组又设计如下装置,

 、稀盐酸、碳酸钙、
、稀盐酸、碳酸钙、 溶液、饱和
溶液、饱和 溶液,
溶液,已知
 不溶于水。据此回答以下问题。
不溶于水。据此回答以下问题。分液漏斗内装入的试剂为
您最近一年使用:0次



