解题方法
1 . 下表是元素周期表的一部分,针对表中的元素①~⑩,请用化学用语回答下列问题:
(1)在元素①~⑨中,原子半径最小的元素是___________ (填元素符号或化学式,下同),最高价氧化物对应水化物碱性最强的是___________ ;
(2)①③⑤⑨对应的简单离子中,离子半径最小的金属离子是___________ (填离子符号)。
(3)元素⑦、⑧对应的最简氢化物的稳定性由大到小顺序为___________ ;元素①做焰色试验时的颜色为___________ ;
(4)写出元素①的单质与元素⑧的单质在加热条件下反应生成的化合物的电子式:___________ 。
(5)元素⑤的最高价氧化物与元素①的最高价氧化物对应的水化物反应的离子方程式为___________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ⑧ | |||||
| 3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
| 4 | ② | ④ |
(2)①③⑤⑨对应的简单离子中,离子半径最小的金属离子是
(3)元素⑦、⑧对应的最简氢化物的稳定性由大到小顺序为
(4)写出元素①的单质与元素⑧的单质在加热条件下反应生成的化合物的电子式:
(5)元素⑤的最高价氧化物与元素①的最高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
2 . 针对表中10种元素及由这些元素形成的单质和化合物,用元素符号或者化学式填写以下空格。
(1)最活泼的金属元素是___________ ,最活泼的非金属元素是___________ ,最不活泼的元素是___________ 。
(2)碱性最强的最高价氧化物对应水化物是___________ ,酸性最强的最高价氧化物对应水化物是___________ ,最稳定的气态氢化物是___________ 。
(3)在④与⑤中,还原性较强的是___________ ,在⑧与⑨的单质中,氧化性较强的是___________ 。
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:___________ ;用电子式表示④和⑧形成的化合物的形成过程___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 4 | ⑩ |
(2)碱性最强的最高价氧化物对应水化物是
(3)在④与⑤中,还原性较强的是
(4)④的最高价氧化物对应的水化物和⑥的最高价氧化物对应的水化物相互反应的化学方程式为:
您最近一年使用:0次
名校
3 . 无机物 均为短周期元素组成的物质,且均含有同种元素,其中
均为短周期元素组成的物质,且均含有同种元素,其中 是最简单氢化物、
是最简单氢化物、 是单质:上述物质在一定条件下可以发生如下转化。
是单质:上述物质在一定条件下可以发生如下转化。 为强碱,则
为强碱,则 的电子式为
的电子式为___________ 。
(2)若 为二元弱酸,则
为二元弱酸,则 的化学式为
的化学式为___________ 。
(3)若 为强酸,
为强酸, 在标准状况下是白色固体,则:
在标准状况下是白色固体,则:
① 的浓溶液与炭反应的化学方程式
的浓溶液与炭反应的化学方程式___________ 。
② 溶于水显酸性的原因(化学原理)是
溶于水显酸性的原因(化学原理)是___________ 。
(4)若 为强酸,且
为强酸,且 和
和 可以发生反应生成一种盐
可以发生反应生成一种盐 ,则:
,则:
① 的催化氧化是工业上制备硝酸的基础,其化学方程式
的催化氧化是工业上制备硝酸的基础,其化学方程式___________ 。
②实验室检验 中阳离子的离子方程式为
中阳离子的离子方程式为___________ 。
 均为短周期元素组成的物质,且均含有同种元素,其中
均为短周期元素组成的物质,且均含有同种元素,其中 是最简单氢化物、
是最简单氢化物、 是单质:上述物质在一定条件下可以发生如下转化。
是单质:上述物质在一定条件下可以发生如下转化。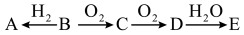
 为强碱,则
为强碱,则 的电子式为
的电子式为(2)若
 为二元弱酸,则
为二元弱酸,则 的化学式为
的化学式为(3)若
 为强酸,
为强酸, 在标准状况下是白色固体,则:
在标准状况下是白色固体,则:①
 的浓溶液与炭反应的化学方程式
的浓溶液与炭反应的化学方程式②
 溶于水显酸性的原因(化学原理)是
溶于水显酸性的原因(化学原理)是(4)若
 为强酸,且
为强酸,且 和
和 可以发生反应生成一种盐
可以发生反应生成一种盐 ,则:
,则:①
 的催化氧化是工业上制备硝酸的基础,其化学方程式
的催化氧化是工业上制备硝酸的基础,其化学方程式②实验室检验
 中阳离子的离子方程式为
中阳离子的离子方程式为
您最近一年使用:0次
名校
解题方法
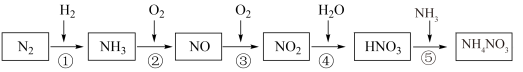
4 . 氮元素及其化合物的转化关系如图所示:___________ ,写出 的电子式
的电子式___________ 。
(2)浓、稀 的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:
的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:___________ 。
(3)氮氧化物 是大气污染物之一,处理
是大气污染物之一,处理 对于环境保护具有重要的意义。在一定条件下
对于环境保护具有重要的意义。在一定条件下 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。 ,反应的化学方程式为
,反应的化学方程式为___________ ;装置B内的试剂是___________ 。
②在装置 中
中 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中  和
和 的物质的量之比为
的物质的量之比为___________ 。
③工厂里常采用 溶液吸收
溶液吸收 的混合气体,使其转化为化工产品
的混合气体,使其转化为化工产品 ,试写出其化学方程式:
,试写出其化学方程式:___________ 。
④用不同浓度的 溶液吸收
溶液吸收 含量不同的尾气,关系如图:(
含量不同的尾气,关系如图:( 表示尾气里
表示尾气里 中
中 的含量)
的含量) 含量越大,氮氧化物的吸收率越大,当
含量越大,氮氧化物的吸收率越大,当 小于
小于 时,加入
时,加入  能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是___________ 。
(4) 是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:
是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:___________ (写出操作步骤、现象和结论)。
 的电子式
的电子式(2)浓、稀
 的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:
的性质既相似又有差别,写出足量的铁与稀硝酸反应的离子方程式:(3)氮氧化物
 是大气污染物之一,处理
是大气污染物之一,处理 对于环境保护具有重要的意义。在一定条件下
对于环境保护具有重要的意义。在一定条件下 可将
可将 还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。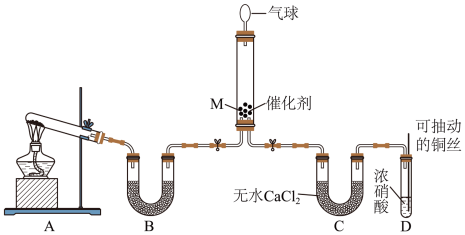
 ,反应的化学方程式为
,反应的化学方程式为②在装置
 中
中 和
和 充分反应,生成两种对环境友好的物质,该反应中
充分反应,生成两种对环境友好的物质,该反应中  和
和 的物质的量之比为
的物质的量之比为③工厂里常采用
 溶液吸收
溶液吸收 的混合气体,使其转化为化工产品
的混合气体,使其转化为化工产品 ,试写出其化学方程式:
,试写出其化学方程式:④用不同浓度的
 溶液吸收
溶液吸收 含量不同的尾气,关系如图:(
含量不同的尾气,关系如图:( 表示尾气里
表示尾气里 中
中 的含量)
的含量)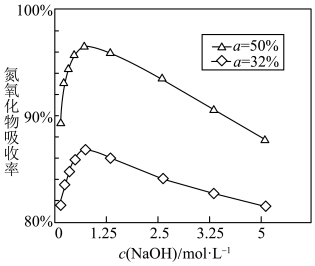
 含量越大,氮氧化物的吸收率越大,当
含量越大,氮氧化物的吸收率越大,当 小于
小于 时,加入
时,加入  能提升氮氧化物的吸收率,原因是
能提升氮氧化物的吸收率,原因是(4)
 是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:
是农业生产中常用的一种氮肥。实验室中检验某种化肥是铵态氮肥的方法是:
您最近一年使用:0次
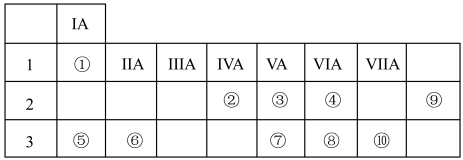
5 . 下表列出了①~⑨九种元素在周期表中的位置:
(1)元素④在周期表中所处位置_______ 。
(2)按气态氢化物的稳定性由强到弱的顺序排列,④⑦⑧的氢化物稳定性:_______ (写氢化物的化学式)。
(3)元素⑤、⑥最高价氧化物对应水化物的碱性强弱为_______ (填化学式)。
(4)元素⑧的原子结构示意图是_______ 。
(5)写出元素⑤形成的单质在氧气中燃烧的化学方程式_______ 。
(6)用电子式表示⑤与⑧反应得到的化合物的形成过程_______ 。
(1)元素④在周期表中所处位置
(2)按气态氢化物的稳定性由强到弱的顺序排列,④⑦⑧的氢化物稳定性:
(3)元素⑤、⑥最高价氧化物对应水化物的碱性强弱为
(4)元素⑧的原子结构示意图是
(5)写出元素⑤形成的单质在氧气中燃烧的化学方程式
(6)用电子式表示⑤与⑧反应得到的化合物的形成过程
您最近一年使用:0次
名校
6 . 下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。 和
和 形成的
形成的 分子的结构式是
分子的结构式是___________ ,分子中含有___________ (填“极性”或“非极性”)键。
(2)元素 的最简单气态氢化物的电子式是
的最简单气态氢化物的电子式是___________ 。元素 和
和 中,最简单气态氢化物的沸点较高的是
中,最简单气态氢化物的沸点较高的是___________ (用化学式表示),原因是___________ 。
(3)元素 和
和 形成的最简单化合物分子的空间结构是
形成的最简单化合物分子的空间结构是___________ (用文字表述)。元素 、
、 、
、 中,简单离子半径从大到小的顺序是
中,简单离子半径从大到小的顺序是___________ (用离子符号表示)。
(4)元素 的外围电子轨道表示式是
的外围电子轨道表示式是___________ 。元素 、
、 、
、 中,第一电离能从大到小的顺序是
中,第一电离能从大到小的顺序是___________ (用元素符号表示)。
(5)元素 的最简单气态氢化物和最高价氧化物对应的水化物可以发生反应,该反应的化学方程式是
的最简单气态氢化物和最高价氧化物对应的水化物可以发生反应,该反应的化学方程式是___________ 。元素 和
和 的最高价氧化物对应的水化物可以发生反应,该反应的离子方程式是
的最高价氧化物对应的水化物可以发生反应,该反应的离子方程式是___________ 。

 和
和 形成的
形成的 分子的结构式是
分子的结构式是(2)元素
 的最简单气态氢化物的电子式是
的最简单气态氢化物的电子式是 和
和 中,最简单气态氢化物的沸点较高的是
中,最简单气态氢化物的沸点较高的是(3)元素
 和
和 形成的最简单化合物分子的空间结构是
形成的最简单化合物分子的空间结构是 、
、 、
、 中,简单离子半径从大到小的顺序是
中,简单离子半径从大到小的顺序是(4)元素
 的外围电子轨道表示式是
的外围电子轨道表示式是 、
、 、
、 中,第一电离能从大到小的顺序是
中,第一电离能从大到小的顺序是(5)元素
 的最简单气态氢化物和最高价氧化物对应的水化物可以发生反应,该反应的化学方程式是
的最简单气态氢化物和最高价氧化物对应的水化物可以发生反应,该反应的化学方程式是 和
和 的最高价氧化物对应的水化物可以发生反应,该反应的离子方程式是
的最高价氧化物对应的水化物可以发生反应,该反应的离子方程式是
您最近一年使用:0次
名校
7 . X、Y、Z、P、Q、W、R、T是元素周期表短期中最常见的主族元素,且原子序数依次增大,其相关信息如下表:
(1)W元素位于周期表______ ;T离子的结构示意图为______ 。
(2)将Q、Z、R的简单离子的半径从大到小排序______ (用离子符号表示);R、T两种元素的最高价氧化物对应水化物的酸(或碱)性由强到弱的顺序为______ (用化学式表示)。
(3)X、Y、Z三种元素的简单氢化物中,稳定性最强的化合物的电子式为______ ,化合物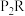 溶液在空气中长期放置,会和氧气反应生成与过氧化钠的结构相似的物质
溶液在空气中长期放置,会和氧气反应生成与过氧化钠的结构相似的物质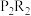 ,其溶液显黄色,则
,其溶液显黄色,则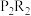 的电子式为
的电子式为______ 。
(4)Q的单质能与X、Z形成的某种化合物反应,写出其化学方程式:______ 。
(5)Z、P、R与H元素可以形成两种强电解质,二者反应可以生成一种有刺激性气味的气体,写出该反应的离子方程式______ 。
元素 | 相关信息 |
X | 其某一种同位素,被用作相对原子质量的标准 |
Y | 其最高价氧化物对应水化物能与其气态氢化物发生化合反应 |
P | 是短周期中(除稀有气体外)原子半径最大的元素 |
Q | 存在质量数为25、中子数为13的核素 |
W | 位于周期表第13列 |
R | 与Z同族,且最高价氧化物对应水化物的浓溶液常温下与W单质会出现钝化现象 |
(2)将Q、Z、R的简单离子的半径从大到小排序
(3)X、Y、Z三种元素的简单氢化物中,稳定性最强的化合物的电子式为
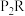 溶液在空气中长期放置,会和氧气反应生成与过氧化钠的结构相似的物质
溶液在空气中长期放置,会和氧气反应生成与过氧化钠的结构相似的物质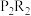 ,其溶液显黄色,则
,其溶液显黄色,则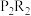 的电子式为
的电子式为(4)Q的单质能与X、Z形成的某种化合物反应,写出其化学方程式:
(5)Z、P、R与H元素可以形成两种强电解质,二者反应可以生成一种有刺激性气味的气体,写出该反应的离子方程式
您最近一年使用:0次
名校
8 . 氮是自然界中生物体生命活动不可缺少的重要元素,其化合物种类丰富。
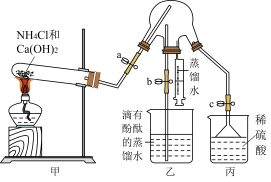
Ⅰ.氨是重要的化工原料,某同学设计如图装置制备氨气并进行氨气的性质检验,部分夹持装置己省略,请回答下列问题: 的电子式为
的电子式为___________ 。
(2)试管内发生反应的化学方程式为___________ 。
(3)①实验之前先检验装置的气密性,然后放入试剂,打开止水夹a、c,关闭止水夹b,再点燃酒精灯,实验过程中丙装置的作用是___________ 。
②一段时间后, 充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为
充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为___________ 。
③为提高乙装置中实验的成功率,将盛放有___________ 的干燥管连接在甲、乙装置之间。
Ⅱ.研究氮的循环和转化对生产、生活有重要的价值,某工厂制硝酸的流程如图所示。___________ (填“ⅰ”“ⅱ”或“ⅲ”)。
(5)写出“氧化炉”中反应的化学方程式___________ 。
(6)“吸收塔”排出的尾气中会含有NO、 等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与
等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与 反应的化学方程式补充完整:
反应的化学方程式补充完整:______ 。
 ___________
___________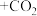 。
。
Ⅰ.氨是重要的化工原料,某同学设计如图装置制备氨气并进行氨气的性质检验,部分夹持装置己省略,请回答下列问题:
 的电子式为
的电子式为(2)试管内发生反应的化学方程式为
(3)①实验之前先检验装置的气密性,然后放入试剂,打开止水夹a、c,关闭止水夹b,再点燃酒精灯,实验过程中丙装置的作用是
②一段时间后,
 充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为
充满三颈烧瓶,关闭止水夹a、c,打开止水夹b,将注射器内的蒸馏水注入三颈烧瓶中,片刻后三颈烧瓶内可以观察到的现象为③为提高乙装置中实验的成功率,将盛放有
Ⅱ.研究氮的循环和转化对生产、生活有重要的价值,某工厂制硝酸的流程如图所示。
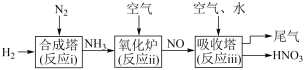
(5)写出“氧化炉”中反应的化学方程式
(6)“吸收塔”排出的尾气中会含有NO、
 等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与
等氮氧化物,为消除它们对环境的影响,通常用纯碱(Na2CO3)溶液吸收法。请将纯碱溶液与 反应的化学方程式补充完整:
反应的化学方程式补充完整: ___________
___________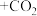 。
。
您最近一年使用:0次
名校
9 . 用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2 2Cl2+2H2O
2Cl2+2H2O
已知:i.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。___________ 。
(2)反应A的热化学方程式是___________ (注意:不写条件)。
(3)断开1 mol H-O键与断开1 mol H-Cl键所需能量相差为___________ kJ,H2O中H-O键比HCl中H-Cl键(填“强”或“弱”)___________ 。
(4)请回答:
H2(g)+Br2(l)=2HBr(g) ΔH=-72 kJ·mol-1,蒸发1mol Br2(1)需要吸收的能量为30kJ,则上表中a的数值为:___________ 。
(5)已知甲烷的燃烧热为890.3kJ·mol-1,H2O(g)=H2O(l) ΔH=-44.0kJ·mol-1,N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol-1,则甲烷脱硝反应:CH4(g)+2NO(g)+O2(g)=CO2(g)+N2(g)+2H2O(g) ΔH=___________ 。
(6)二氧化碳经催化氢化可转化成绿色能源乙醇(CH3CH2OH)。已知:
①2H2(g)+O2(g)=2H2O(g) = -483.6 kJ·mol-1
= -483.6 kJ·mol-1
②CH3CH2OH(l)+3O2(g)=2CO2(g)+3H2O(l) =-1366.8kJ·mol-1
=-1366.8kJ·mol-1
③H2O(l)=H2O(g) =+44.0kJ·mol-1
=+44.0kJ·mol-1
则二氧化碳与氢气转化成CH3CH2OH(l)和液态水的热化学方程式为:___________ 。
反应A:4HCl+O2
 2Cl2+2H2O
2Cl2+2H2O已知:i.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ii.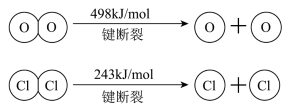
(2)反应A的热化学方程式是
(3)断开1 mol H-O键与断开1 mol H-Cl键所需能量相差为
(4)请回答:
| 参加反应的物质及状态 |  |  | 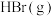 |
| 1mol分子中的化学键断裂时需要吸收的能量 | 436 | a | 369 |
(5)已知甲烷的燃烧热为890.3kJ·mol-1,H2O(g)=H2O(l) ΔH=-44.0kJ·mol-1,N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol-1,则甲烷脱硝反应:CH4(g)+2NO(g)+O2(g)=CO2(g)+N2(g)+2H2O(g) ΔH=
(6)二氧化碳经催化氢化可转化成绿色能源乙醇(CH3CH2OH)。已知:
①2H2(g)+O2(g)=2H2O(g)
 = -483.6 kJ·mol-1
= -483.6 kJ·mol-1②CH3CH2OH(l)+3O2(g)=2CO2(g)+3H2O(l)
 =-1366.8kJ·mol-1
=-1366.8kJ·mol-1③H2O(l)=H2O(g)
 =+44.0kJ·mol-1
=+44.0kJ·mol-1则二氧化碳与氢气转化成CH3CH2OH(l)和液态水的热化学方程式为:
您最近一年使用:0次
10 . 现有六种元素,其中A、B、C、D、E为短周期主族元素,F为第4周期元素,它们的原子序数依次增大。请根据下列相关信息回答问题。
(1)B元素基态原子具有___________ 种运动状态不同的电子,能量最高的电子,其电子云在空间有___________ 个伸 展方向。
(2)根据上述信息,画出C元素基态原子的轨道表示式___________ 。
(3)F在元素周期表中属于___________ 区元素。
(4)写出DA3的电子式:___________ (用元素符号表示)。
| 元素 | 相关信息 |
| A | 元素的原子核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 元素原子的核外p电子数比s电子数少1 |
| C | 元素的第一至第四电离能分别是I1=738 kJ/mol、I2=1451 kJ/mol、I3= 7733 kJ/mol、I4= 10540 kJ/mol |
| D | 原子核外填充电子的所有p轨道全满或半满 |
| E | 元素的主族序数与周期序数的差为3 |
| F | 在元素周期表的第6列 |
(2)根据上述信息,画出C元素基态原子的轨道表示式
(3)F在元素周期表中属于
(4)写出DA3的电子式:
您最近一年使用:0次



