1 . 电解重水( )是制取氘气(
)是制取氘气( )的一种方法。设
)的一种方法。设 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是
 )是制取氘气(
)是制取氘气( )的一种方法。设
)的一种方法。设 为阿伏加德罗常数的值。下列说法错误的是
为阿伏加德罗常数的值。下列说法错误的是A. 分子间存在氢键 分子间存在氢键 | B. 的熔、沸点比 的熔、沸点比 高 高 |
C.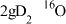 含中子数目为 含中子数目为 | D.制取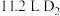 转移的电子数目为 转移的电子数目为 |
您最近一年使用:0次
名校
解题方法
2 . 碱式硫酸镁晶须 是一种无机镁盐晶须,将其添加到以橡胶、塑料为基体的复合材料中,能使该复合材料有良好的阻燃功效。一种以蛇纹石(主要含
是一种无机镁盐晶须,将其添加到以橡胶、塑料为基体的复合材料中,能使该复合材料有良好的阻燃功效。一种以蛇纹石(主要含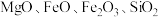 等)为原料制备碱式硫酸镁晶须的流程如图:
等)为原料制备碱式硫酸镁晶须的流程如图:
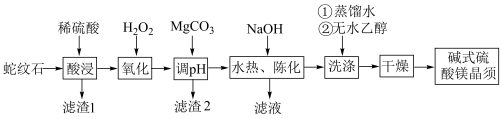
回答下列问题:
(1)酸浸时须将蛇纹石粉碎,其目的是_______ 。
(2)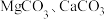 在高温下均易分解,但
在高温下均易分解,但 的分解温度比
的分解温度比 的低,试从结构角度解释其原因:
的低,试从结构角度解释其原因:_______ 。
(3)洗涤步骤中用无水乙醇洗涤的目的是_______ 。
(4)氧化的目的是_______ (用离子方程式表示),为检验溶液中的离子是否完全被氧化,可使用的试剂为_______ (填化学式)。
(5)将碱式硫酸镁晶须 进行热重分析测定其化学式,
进行热重分析测定其化学式,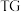 热重曲线[样品的固体残留率(
热重曲线[样品的固体残留率( )随温度变化]
)随温度变化] (微商热重曲线,表示质量的变化速率随温度的变化)如图1所示,第一次失重发生反应的化学方程式为
(微商热重曲线,表示质量的变化速率随温度的变化)如图1所示,第一次失重发生反应的化学方程式为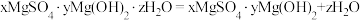 ,第三次失重后获得的晶体的晶胞结构如图2所示。
,第三次失重后获得的晶体的晶胞结构如图2所示。
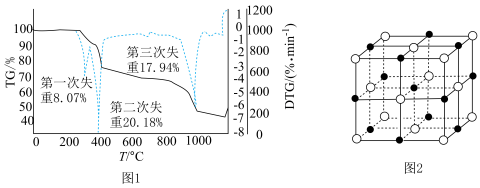
①x、y、z为最简整数比,则碱式硫酸镁晶须的化学式为_______ ;第二次失重发生反应的化学方程式为_______ 。
②图2中的晶胞参数为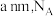 为阿伏加德罗常数的值,则晶胞中白球的配位数为
为阿伏加德罗常数的值,则晶胞中白球的配位数为_______ ,该晶体的密度为_______  。
。
 是一种无机镁盐晶须,将其添加到以橡胶、塑料为基体的复合材料中,能使该复合材料有良好的阻燃功效。一种以蛇纹石(主要含
是一种无机镁盐晶须,将其添加到以橡胶、塑料为基体的复合材料中,能使该复合材料有良好的阻燃功效。一种以蛇纹石(主要含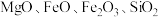 等)为原料制备碱式硫酸镁晶须的流程如图:
等)为原料制备碱式硫酸镁晶须的流程如图:
回答下列问题:
(1)酸浸时须将蛇纹石粉碎,其目的是
(2)
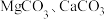 在高温下均易分解,但
在高温下均易分解,但 的分解温度比
的分解温度比 的低,试从结构角度解释其原因:
的低,试从结构角度解释其原因:(3)洗涤步骤中用无水乙醇洗涤的目的是
(4)氧化的目的是
(5)将碱式硫酸镁晶须
 进行热重分析测定其化学式,
进行热重分析测定其化学式,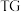 热重曲线[样品的固体残留率(
热重曲线[样品的固体残留率( )随温度变化]
)随温度变化] (微商热重曲线,表示质量的变化速率随温度的变化)如图1所示,第一次失重发生反应的化学方程式为
(微商热重曲线,表示质量的变化速率随温度的变化)如图1所示,第一次失重发生反应的化学方程式为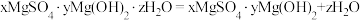 ,第三次失重后获得的晶体的晶胞结构如图2所示。
,第三次失重后获得的晶体的晶胞结构如图2所示。
①x、y、z为最简整数比,则碱式硫酸镁晶须的化学式为
②图2中的晶胞参数为
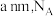 为阿伏加德罗常数的值,则晶胞中白球的配位数为
为阿伏加德罗常数的值,则晶胞中白球的配位数为 。
。
您最近一年使用:0次
2024-01-22更新
|
266次组卷
|
4卷引用:T28-工业流程题
名校
解题方法
3 . 乙酰苯胺俗称退热冰,是常用的化工原料和重要的化学试剂。某实验小组拟用一定量的乙酸和苯胺制备一定量的乙酰苯胺,具体实验步骤如下:
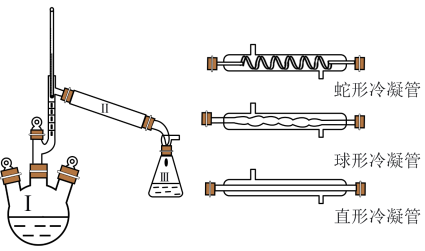
步骤1:安装装置,检查好气密性后向100mL三颈烧瓶中加入5.0mL苯胺、7.4mL乙酸(足量)和0.1g锌粉,加入沸石后,加热微沸回流,控制温度计温度为105C左右,反应40~60min。
步骤2:冷却后取下三颈烧瓶,搅拌下趁热倒入100mL冷水中,剧烈搅拌,冷却至室温,抽滤,压干。用5~10mL冷水洗涤,抽滤,压干,得到粗品。
步骤3:粗产品用150mL热水溶解,稍冷后,加入约0.2g活性炭,搅拌下加热煮沸1~2min,趁热抽滤,将滤液自然冷却至室温,晶体析出,抽滤,压干,干燥,称重。
已知:
回答下列问题
(1)Ⅱ处空白位置应选择的仪器为___________ (填“蛇形冷凝管”“球形冷凝管”或“直形冷凝管”);反应开始后发现忘加沸石,正确的操作为___________ 。
(2)步骤1中,发生反应的化学方程式是___________ ;温度计控温在105℃的原因是___________ 。
(3)步骤2中,用冷水进行洗涤的原因是___________ 。
(4)步骤3中,趁热抽滤的目的是___________ 。
(5)步骤3中,得到纯净乙酰苯胺6.3g,则实验产率为___________ (结果保留2位有效数字)。

步骤1:安装装置,检查好气密性后向100mL三颈烧瓶中加入5.0mL苯胺、7.4mL乙酸(足量)和0.1g锌粉,加入沸石后,加热微沸回流,控制温度计温度为105C左右,反应40~60min。
步骤2:冷却后取下三颈烧瓶,搅拌下趁热倒入100mL冷水中,剧烈搅拌,冷却至室温,抽滤,压干。用5~10mL冷水洗涤,抽滤,压干,得到粗品。
步骤3:粗产品用150mL热水溶解,稍冷后,加入约0.2g活性炭,搅拌下加热煮沸1~2min,趁热抽滤,将滤液自然冷却至室温,晶体析出,抽滤,压干,干燥,称重。
已知:
| 相对分子质量 | 熔点/℃ | 沸点/℃ | 密度/(g/mL) | 溶解性 | |
| 乙酸 | 60 | 16.6 | 117.9 | 1.05 | 能溶于水、乙醇、乙醚 |
| 苯胺 | 93 | -6 | 184 | 1.022 | 微溶于水,易溶于乙醇、乙醚 |
| 乙酰苯胺 | 135 | 114 | 304 | 1.12 | 微溶于冷水,能溶于热水 |
(1)Ⅱ处空白位置应选择的仪器为
(2)步骤1中,发生反应的化学方程式是
(3)步骤2中,用冷水进行洗涤的原因是
(4)步骤3中,趁热抽滤的目的是
(5)步骤3中,得到纯净乙酰苯胺6.3g,则实验产率为
您最近一年使用:0次
4 . 配合物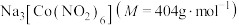 在分析化学中用于
在分析化学中用于 的鉴定,其制备装置示意图(夹持装置等略)及步骤如下:
的鉴定,其制备装置示意图(夹持装置等略)及步骤如下: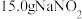 和
和 热蒸馏水,搅拌溶解。
热蒸馏水,搅拌溶解。
②磁力搅拌下加入 ,从仪器a加入50%醋酸
,从仪器a加入50%醋酸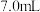 。冷却至室温后,再从仪器b缓慢滴入30%双氧水
。冷却至室温后,再从仪器b缓慢滴入30%双氧水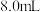 。待反应结束,滤去固体。
。待反应结束,滤去固体。
③在滤液中加入95%乙醇,静置40分钟。固液分离后,依次用乙醇、乙醚洗涤固体产品,称重。
已知:i.乙醇、乙醚的沸点分别是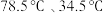 ;
;
ii. 的溶解度数据如下表。
的溶解度数据如下表。
回答下列问题:
(1)仪器a的名称是_______ ,使用前应_______ 。
(2)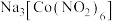 中钴的化合价是
中钴的化合价是_______ ,制备该配合物的化学方程式为_______ 。
(3)步骤①中,用热蒸馏水的目的是_______ 。
(4)步骤③中,用乙醚洗涤固体产品的作用是_______ 。
(5)已知: (亮黄色)足量
(亮黄色)足量 与
与 产品反应生成
产品反应生成 亮黄色沉淀,产品纯度为
亮黄色沉淀,产品纯度为_______ %。
(6)实验室检验样品中钾元素的常用方法是:将铂丝用盐酸洗净后,在外焰上灼烧至与原来的火焰颜色相同时,用铂丝蘸取样品在外焰上灼烧,_______ 。
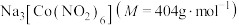 在分析化学中用于
在分析化学中用于 的鉴定,其制备装置示意图(夹持装置等略)及步骤如下:
的鉴定,其制备装置示意图(夹持装置等略)及步骤如下:
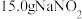 和
和 热蒸馏水,搅拌溶解。
热蒸馏水,搅拌溶解。②磁力搅拌下加入
 ,从仪器a加入50%醋酸
,从仪器a加入50%醋酸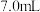 。冷却至室温后,再从仪器b缓慢滴入30%双氧水
。冷却至室温后,再从仪器b缓慢滴入30%双氧水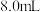 。待反应结束,滤去固体。
。待反应结束,滤去固体。③在滤液中加入95%乙醇,静置40分钟。固液分离后,依次用乙醇、乙醚洗涤固体产品,称重。
已知:i.乙醇、乙醚的沸点分别是
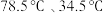 ;
;ii.
 的溶解度数据如下表。
的溶解度数据如下表。| 温度/℃ | 20 | 30 | 40 | 50 |
溶解度/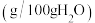 | 84.5 | 91.6 | 98.4 | 104.1 |
(1)仪器a的名称是
(2)
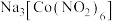 中钴的化合价是
中钴的化合价是(3)步骤①中,用热蒸馏水的目的是
(4)步骤③中,用乙醚洗涤固体产品的作用是
(5)已知:
 (亮黄色)足量
(亮黄色)足量 与
与 产品反应生成
产品反应生成 亮黄色沉淀,产品纯度为
亮黄色沉淀,产品纯度为(6)实验室检验样品中钾元素的常用方法是:将铂丝用盐酸洗净后,在外焰上灼烧至与原来的火焰颜色相同时,用铂丝蘸取样品在外焰上灼烧,
您最近一年使用:0次
2023-11-29更新
|
4124次组卷
|
5卷引用:题型17 化学实验综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
(已下线)题型17 化学实验综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)T15-实验综合题山东省潍坊市昌乐二中2023-2024学年高三上学期12月月考化学试题2023年河北省高考化学试卷福建省福州第三中学2023-2024学年高三下学期第十六次检测(三模)化学试题
2023高三·全国·专题练习
5 . 在N2气氛中,FeSO4·7H2O的脱水热分解过程如图所示:
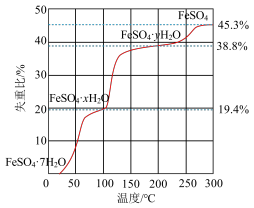
根据上述实验结果,可知
___________ ,
___________ 。

根据上述实验结果,可知


您最近一年使用:0次
名校
6 . 回答下列问题。
(1)相同质量的 和
和 所含硫原子的个数之比为
所含硫原子的个数之比为___________ 。
(2)已知CO、 的混合气体质量共14.8g,标准状况下体积为8.96L,则可推知该混合气体平均相对分子质量为
的混合气体质量共14.8g,标准状况下体积为8.96L,则可推知该混合气体平均相对分子质量为___________ ,CO的物质的量为___________ 。
(3)将 的
的 溶液由amL稀释至bmL,稀释后溶液中
溶液由amL稀释至bmL,稀释后溶液中 的物质的量浓度是
的物质的量浓度是___________  (用含a、b的代数式表示)。
(用含a、b的代数式表示)。
(4)质量比为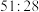 的
的 和CO,其所含的质子数之比为
和CO,其所含的质子数之比为___________ 。
(5)中和浓度为4mol/L,体积为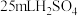 溶液,需要NaOH的质量为
溶液,需要NaOH的质量为___________ 。
(1)相同质量的
 和
和 所含硫原子的个数之比为
所含硫原子的个数之比为(2)已知CO、
 的混合气体质量共14.8g,标准状况下体积为8.96L,则可推知该混合气体平均相对分子质量为
的混合气体质量共14.8g,标准状况下体积为8.96L,则可推知该混合气体平均相对分子质量为(3)将
 的
的 溶液由amL稀释至bmL,稀释后溶液中
溶液由amL稀释至bmL,稀释后溶液中 的物质的量浓度是
的物质的量浓度是 (用含a、b的代数式表示)。
(用含a、b的代数式表示)。(4)质量比为
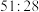 的
的 和CO,其所含的质子数之比为
和CO,其所含的质子数之比为(5)中和浓度为4mol/L,体积为
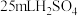 溶液,需要NaOH的质量为
溶液,需要NaOH的质量为
您最近一年使用:0次
解题方法
7 . 已知: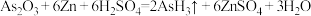 ,阿伏伽德罗常数的值为NA。若反应物中H2SO4消耗了3mol,则下列说法错误的是
,阿伏伽德罗常数的值为NA。若反应物中H2SO4消耗了3mol,则下列说法错误的是
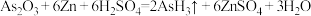 ,阿伏伽德罗常数的值为NA。若反应物中H2SO4消耗了3mol,则下列说法错误的是
,阿伏伽德罗常数的值为NA。若反应物中H2SO4消耗了3mol,则下列说法错误的是| A.转移电子的数目为6NA | B.标准状况下,生成H2O27g |
| C.生成还原产物的分子数为1NA | D.产物AsH3为平面三角形 |
您最近一年使用:0次
8 . 磷酸奥司他韦常用于甲型或乙型流感的治疗。设 为阿伏加德罗常数的值,则1mol磷酸(
为阿伏加德罗常数的值,则1mol磷酸( )所含氧原子数目为
)所含氧原子数目为
 为阿伏加德罗常数的值,则1mol磷酸(
为阿伏加德罗常数的值,则1mol磷酸( )所含氧原子数目为
)所含氧原子数目为A. | B.3 | C.4 | D.8 |
您最近一年使用:0次
2023-09-20更新
|
285次组卷
|
4卷引用:合格考真题汇编3物质的量
(已下线)合格考真题汇编3物质的量(已下线)合格考真题汇编3物质的量云南省2023年春季学期期末普通高中学业水平考试化学试题安徽省蚌埠市固镇县毛钽厂实验中学2023-2024学年高一上学期期末考试化学试题
9 . 1mol任何粒子的粒子数叫做阿伏加德罗常数符号为NA。1mol Cl2含有的原子数为
| A.0.5NA | B.NA | C.1.5NA | D.2NA |
您最近一年使用:0次
2023-08-31更新
|
796次组卷
|
7卷引用:合格考汇编9物质的量
(已下线)合格考汇编9物质的量(已下线)合格考真题汇编3物质的量(已下线)合格考真题汇编3物质的量(已下线)专题四 化学计量及应用2023年7月黑龙江省普通高中学业水平合格性考试化学试题(已下线)【精品卷】2.3.1 物质的量的单位—摩尔课堂例题-人教版2023-2024学年必修第一册四川省眉山市仁寿第一中学校(北校区)2023-2024学年高一上学期10月月考化学试题
2023高三·全国·专题练习
10 . 1mol乙烷和1 mol乙烯中,化学键数相同。( )
您最近一年使用:0次



