名校
解题方法
1 . 在实验室里,常用如下所示装置制取并收集氨气,反应方程式:
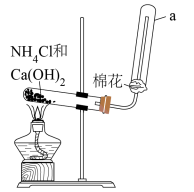
(1)该收集氨气的方法为向___________ (填“上”或“下”)排空气法;
(2)上图装置中仪器a的名称为___________ ;
(3)实验进行一段时间后,若用湿润的红色石蕊试纸靠近塞有棉花的试管口,观察到试纸变___________ (填“蓝”或“白”);
(4)为防止多余的氨气逸出而污染环境,在装置中的棉花事先浸有___________ (填“稀硫酸”或“NaOH溶液”);
(5)实验室欲制取4.48L (标准状况),至少需要
(标准状况),至少需要 的质量为
的质量为___________ g。


(1)该收集氨气的方法为向
(2)上图装置中仪器a的名称为
(3)实验进行一段时间后,若用湿润的红色石蕊试纸靠近塞有棉花的试管口,观察到试纸变
(4)为防止多余的氨气逸出而污染环境,在装置中的棉花事先浸有
(5)实验室欲制取4.48L
 (标准状况),至少需要
(标准状况),至少需要 的质量为
的质量为
您最近一年使用:0次
2023高三·全国·专题练习
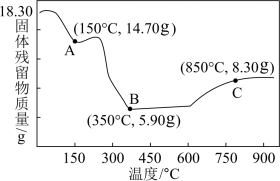
2 .  热分解的质量变化过程如图所示,其中
热分解的质量变化过程如图所示,其中 之前是隔绝空气加热,
之前是隔绝空气加热, 之后是在空气中加热,A、B、C三点时的产物均为纯净物。用化学方程式表示从A点到B点的物质转化:
之后是在空气中加热,A、B、C三点时的产物均为纯净物。用化学方程式表示从A点到B点的物质转化:_______ ,C点时产物的化学式是_______ 。
 热分解的质量变化过程如图所示,其中
热分解的质量变化过程如图所示,其中 之前是隔绝空气加热,
之前是隔绝空气加热, 之后是在空气中加热,A、B、C三点时的产物均为纯净物。用化学方程式表示从A点到B点的物质转化:
之后是在空气中加热,A、B、C三点时的产物均为纯净物。用化学方程式表示从A点到B点的物质转化:
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
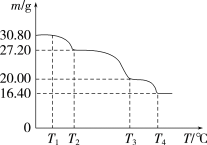
3 . 过硼酸钠晶体(NaBO3·4H2O)可用作洗衣业的无氯漂白剂、清洗材料和牙齿增白剂,在70 ℃以上加热会逐步失去结晶水。实验测得过硼酸钠晶体的质量随温度变化的情况如下图所示,则T2℃时所得晶体的化学式为_______ 。

您最近一年使用:0次
解题方法
4 . 设 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是A.1 mol Cu和Na分别与足量硫粉反应时,转移的电子数均为 |
B.铅蓄电池放电时,正极质量增加9.6 g,电路中通过的电子数目为 |
C.标准状况下4.48 L  溶于水得到的溶液中, 溶于水得到的溶液中, 和 和 的总数小于 的总数小于 |
D.金刚石晶体密度为 ,则晶体中碳原子的最小间距为 ,则晶体中碳原子的最小间距为 pm pm |
您最近一年使用:0次
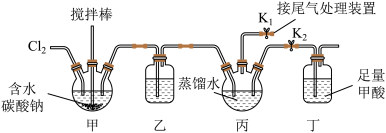
5 . 用如图装置制备次氯酸并验证其氧化性。 可以与含水碳酸钠反应得到
可以与含水碳酸钠反应得到 气体和
气体和 。下列说法错误的是
。下列说法错误的是
 可以与含水碳酸钠反应得到
可以与含水碳酸钠反应得到 气体和
气体和 。下列说法错误的是
。下列说法错误的是
A.装置甲中每生成16.8g碳酸氢钠同时生成标准状况下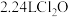 |
| B.装置乙中盛装的是浓硫酸 |
C.将装置丙中次氯酸溶液转移到装置丁中的具体操作是打开 关闭 关闭 |
| D.装置丁中溶液酸性显著增强可证明次氯酸的氧化性 |
您最近一年使用:0次
解题方法
6 . 工业上以铬铁矿(FeCr2O4质量分数为a%,含Al2O3、SiO2等杂质)为主要原料制备红矾钠(Na2Cr2O7•2H2O)的工艺流程图如图,回答下列问题:
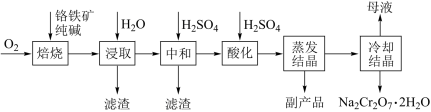
(1)焙烧的目的是将FeCr2O4转化为Na2CrO4,写出转化过程中生成可溶性含铝组分的化学方程式:______ 。
(2)下列有关说法不正确 的是______ 。
(3)蒸发结晶,盛放样品的容器名称是_______ 。
(4)酸化的目的是(结合离子方程式说明)______ 。
(5)利用氧化还原滴定法测定Na2Cr2O7•2H2O产品的纯度,从下列选项中选择合适的仪器和操作,补全如下步骤[“_______”上填写一件最关键仪器,“(_______)”内填写一种操作 ,均用字母表示]。用______ (称量产品2.50g)→在烧杯中__________ →用容量瓶__________ →用移液管(取25.00mL所配溶液于锥形瓶中)→加入足量碘化钠溶液→加入3滴淀粉指示剂→用______ (用0.1200mol•L-1Na2S2O3标准溶液滴定)→_________ 并且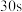 内不恢复原来的颜色,消耗标准溶液40.00mL
内不恢复原来的颜色,消耗标准溶液40.00mL
仪器:a.碱式滴定管;b.酸式滴定管;c.电子天平;d.托盘天平;
操作:e.加硫酸溶解;f.加盐酸溶解;g.配制250mL溶液;h.观察到溶液蓝色褪去:i.观察到溶液变成蓝色
(6)若以铬铁矿为原料制备mkg硼化铬(CrB),在工艺流程中Cr损失b%,则至少需要铬铁矿的质量为______ kg(用含字母的计算式表示)。

(1)焙烧的目的是将FeCr2O4转化为Na2CrO4,写出转化过程中生成可溶性含铝组分的化学方程式:
(2)下列有关说法
| A.蒸发结晶时如果长时间蒸发,有利于提高Na2Cr2O7•2H2O的产率 |
| B.除了Na2Cr2O7外,在上述工艺流程中可循环利用的物质还有H2SO4 |
| C.含铁元素的化合物可在中和过程中被除去 |
| D.焙烧时气流与矿料逆流而行,其目的是增大反应物接触面积,提高反应速率 |
(4)酸化的目的是(结合离子方程式说明)
(5)利用氧化还原滴定法测定Na2Cr2O7•2H2O产品的纯度,从下列选项中选择合适的仪器和操作,补全如下步骤[“_______”上填写一件最关键仪器,“(_______)”内填写
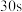 内不恢复原来的颜色,消耗标准溶液40.00mL
内不恢复原来的颜色,消耗标准溶液40.00mL仪器:a.碱式滴定管;b.酸式滴定管;c.电子天平;d.托盘天平;
操作:e.加硫酸溶解;f.加盐酸溶解;g.配制250mL溶液;h.观察到溶液蓝色褪去:i.观察到溶液变成蓝色
(6)若以铬铁矿为原料制备mkg硼化铬(CrB),在工艺流程中Cr损失b%,则至少需要铬铁矿的质量为
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
7 . Kistiakowsky曾研究了NOCl光化学分解反应,在一定频率(ν)光的照射下机理为:NOCl+hν→NOCl*,NOCl+NOCl*→2NO+Cl2;其中hν表示一个光子能量,NOCl*表示NOCl的激发态。可知,分解1 mol的NOCl需要吸收_______ mol的光子
您最近一年使用:0次
8 . 王水具有强氧化性,可以溶解金、铂等不活泼金属。王水中的硝酸会与盐酸发生反应:HNO3+3HCl=NOCl+Cl2↑+2H2O。设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.100 mL8 mol·L-1 HNO3溶液中含有的氧原子数目为2. 4NA |
| B.20 g 3H 37Cl中含有的中子数目为11 NA |
| C.11.2 L Cl2中含有的共价键数目为0. 5 NA |
| D.每生成65. 5 g NOCl,转移的电子数为NA |
您最近一年使用:0次
2023-05-04更新
|
881次组卷
|
6卷引用:T5-阿伏伽德罗常数
(已下线)T5-阿伏伽德罗常数(已下线)专题03 阿伏加德罗常数与化学计算 -2023年高考化学真题题源解密(新高考专用)江西省赣州市2023届高三下学期4月联考理科综合化学试题广东省四校2024届高三第一次联考化学试题广东省揭阳市惠来县第一中学2023-2024学年高三上学期第二次月考化学试题吉林省通化市梅河口市第五中学2023-2024学年高一下学期4月月考化学试题
名校
解题方法
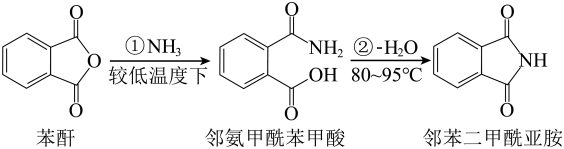
9 . 邻苯二甲酰亚胺广泛用于染料、农药医药橡胶、香料等行业,是许多重要有机精细化学品的中间体。反应原理为
制备邻苯二甲酰亚胺的实验装置如图所示。
向装置甲的三颈烧瓶中加入14.8000g苯酐(相对分子质量为148),然后再加入15.0mL氨水(过量),加热至冷凝管中有部分液体回流时开启搅拌,控制温度为80~95°C,待苯酐固体完全反应后,改为蒸馏装置乙,继续加热,将装置中的水蒸出,体系温度逐渐升高至固体熔化。保温反应60min后,冷却至室温,洗涤、抽滤、烘干,进一步提纯得固体邻苯二甲酰亚胺(相对分子质量为147)14.1120g。
请回答下列问题:
(1)仪器M的名称是___________ 。
(2)仪器Y中冷水由___________ (填“a”或“b”)口流出,装置甲中仪器X一般不用装置乙中仪器Y代替的原因是___________ 。
(3)装置甲中温度控制在80~95°C,若温度过低导致的结果是___________ 。
(4)反应①中除了生成邻氨甲酰苯甲酸,还可能生成的副产物是___________ (写一种物质的结构简式)。
(5)蒸馏时,需要及时将装置中的水蒸出,目的是___________ 。
(6)该固体产品的产率是___________ 。
(7)邻苯二甲酰亚胺还可以用邻二甲苯与氨气、空气在加热条件下催化反应一步制得,写出该反应的化学方程式:___________ 。
| 物质 | 熔点/°C | 沸点/°C | 溶解性 |
| 苯酐 | 131~134 | 284 | 不溶于冷水,微溶于热水 |
| 邻氨甲酰苯甲酸 | 140~143 | 394.2 | 稍溶于热水 |
| 邻苯二甲酰亚胺 | 232~235 | 366 | 微溶于水,易溶于碱溶液 |

向装置甲的三颈烧瓶中加入14.8000g苯酐(相对分子质量为148),然后再加入15.0mL氨水(过量),加热至冷凝管中有部分液体回流时开启搅拌,控制温度为80~95°C,待苯酐固体完全反应后,改为蒸馏装置乙,继续加热,将装置中的水蒸出,体系温度逐渐升高至固体熔化。保温反应60min后,冷却至室温,洗涤、抽滤、烘干,进一步提纯得固体邻苯二甲酰亚胺(相对分子质量为147)14.1120g。
请回答下列问题:
(1)仪器M的名称是
(2)仪器Y中冷水由
(3)装置甲中温度控制在80~95°C,若温度过低导致的结果是
(4)反应①中除了生成邻氨甲酰苯甲酸,还可能生成的副产物是
(5)蒸馏时,需要及时将装置中的水蒸出,目的是
(6)该固体产品的产率是
(7)邻苯二甲酰亚胺还可以用邻二甲苯与氨气、空气在加热条件下催化反应一步制得,写出该反应的化学方程式:
您最近一年使用:0次
2023-04-26更新
|
1359次组卷
|
4卷引用:专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)
(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)题型17 化学实验综合-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)河南省名校大联考2023届高三下学期三模考试理综化学试题江西省宜春市上高二中2023-2024学年高二下学期3月月考化学试题
10 . 硫氰化钾(KSCN)的用途非常广泛,如用KSCN溶液检验 。实验室可用如下装置制取KSCN。
。实验室可用如下装置制取KSCN。
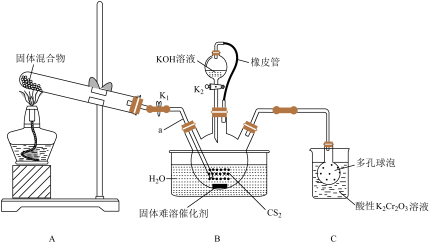
请回答下列问题:
(1)橡皮管的作用是_______ 。
(2)A装置是氨气发生装置,试管中的固体混合物为_______ (填化学式)。
(3)导管a插入 中的目的是
中的目的是_______ 。
(4)水浴加热B装置,三颈烧瓶中的反应除了生成 外,还生成了另一种酸式盐,其反应方程式为
外,还生成了另一种酸式盐,其反应方程式为_______ 。
(5)当三颈烧瓶中的液体不出现分层时,熄灭酒精灯,关闭 ,继续水浴加热(保持100℃),待酸式盐完全分解(保持100℃),再打开
,继续水浴加热(保持100℃),待酸式盐完全分解(保持100℃),再打开 ,继续水浴加热,就可以得到KSCN溶液。若要制取KSCN晶体,需进行的操作是:先将三颈烧瓶中的混合物进行
,继续水浴加热,就可以得到KSCN溶液。若要制取KSCN晶体,需进行的操作是:先将三颈烧瓶中的混合物进行_______ 、再将滤液蒸发浓缩、冷却结晶、过滤、_______ 、干燥。
(6)装置C中酸性 溶液的作用是
溶液的作用是_______ ;若三颈烧瓶中挥发出来的含硫物质恰好与200mL 2.0mol/L的 溶液反应,其中50%的硫元素转化为+6价硫,其余都转化为零价硫,理论上可制得KSCN质量为
溶液反应,其中50%的硫元素转化为+6价硫,其余都转化为零价硫,理论上可制得KSCN质量为_______ g。
 。实验室可用如下装置制取KSCN。
。实验室可用如下装置制取KSCN。
请回答下列问题:
(1)橡皮管的作用是
(2)A装置是氨气发生装置,试管中的固体混合物为
(3)导管a插入
 中的目的是
中的目的是(4)水浴加热B装置,三颈烧瓶中的反应除了生成
 外,还生成了另一种酸式盐,其反应方程式为
外,还生成了另一种酸式盐,其反应方程式为(5)当三颈烧瓶中的液体不出现分层时,熄灭酒精灯,关闭
 ,继续水浴加热(保持100℃),待酸式盐完全分解(保持100℃),再打开
,继续水浴加热(保持100℃),待酸式盐完全分解(保持100℃),再打开 ,继续水浴加热,就可以得到KSCN溶液。若要制取KSCN晶体,需进行的操作是:先将三颈烧瓶中的混合物进行
,继续水浴加热,就可以得到KSCN溶液。若要制取KSCN晶体,需进行的操作是:先将三颈烧瓶中的混合物进行(6)装置C中酸性
 溶液的作用是
溶液的作用是 溶液反应,其中50%的硫元素转化为+6价硫,其余都转化为零价硫,理论上可制得KSCN质量为
溶液反应,其中50%的硫元素转化为+6价硫,其余都转化为零价硫,理论上可制得KSCN质量为
您最近一年使用:0次



