1 . 如图是某研究性学习小组设计制取氯气并以氯气为反应物进行特定反应的装置

(1)①请写出装置A中发生反应的化学方程式______________________________________
②实验时,通常采用密度为1.19g/cm3、浓度为36.5%的浓盐酸。该浓盐酸的物质的量浓度_______ 。
③标准状况下,上述反应每生成4.48L氯气,转移电子的物质的量为________ mol。
(2)要将C装置接入B和D之间,正确的接法是:a→________ →________ →d 。
(3)实验开始先点燃A处的酒精灯,打开活塞K,让Cl2充满整个装置,再点燃D处的酒精灯。Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为__________________________________________ 。为了使C装置发挥更好的作用,可向烧杯中加入浓硫酸,加入浓硫酸的作用是_______________________________ 。
(4) D处反应完毕后,关闭弹簧夹K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是______________________________ ,B的作用是________________________
(5)A、B、C、D、E装置中有一处需要改进,请画出改进后的装置图________________________ 。

(1)①请写出装置A中发生反应的化学方程式
②实验时,通常采用密度为1.19g/cm3、浓度为36.5%的浓盐酸。该浓盐酸的物质的量浓度
③标准状况下,上述反应每生成4.48L氯气,转移电子的物质的量为
(2)要将C装置接入B和D之间,正确的接法是:a→
(3)实验开始先点燃A处的酒精灯,打开活塞K,让Cl2充满整个装置,再点燃D处的酒精灯。Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为
(4) D处反应完毕后,关闭弹簧夹K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是
(5)A、B、C、D、E装置中有一处需要改进,请画出改进后的装置图
您最近一年使用:0次
11-12高一上·陕西西安·期中
名校
解题方法
2 . 有下列化学仪器:①托盘天平;②玻璃棒;③药匙;④烧杯;⑤量筒;⑥容量瓶;⑦胶头滴管。
(1)现需要配制500 mL 1 mol/L硫酸溶液,需用质量分数为98%、密度为1.84 g/cm3的浓硫酸________ mL。
(2)从上述仪器中,按实验使用的先后顺序,其编号排列是_______ 。
(3)容量瓶使用前检验漏水的方法是_______ 。
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”)
①未经冷却趁热将溶液注入容量瓶中,_______________ ;
②摇匀后发现液面低于刻度线再加水,_____________ ;
③容量瓶中原有少量蒸馏水,_______________ ;
④定容时观察液面俯视,_____________ ;
⑤未将洗涤液注入容量瓶中,_______________ 。
(1)现需要配制500 mL 1 mol/L硫酸溶液,需用质量分数为98%、密度为1.84 g/cm3的浓硫酸
(2)从上述仪器中,按实验使用的先后顺序,其编号排列是
(3)容量瓶使用前检验漏水的方法是
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”)
①未经冷却趁热将溶液注入容量瓶中,
②摇匀后发现液面低于刻度线再加水,
③容量瓶中原有少量蒸馏水,
④定容时观察液面俯视,
⑤未将洗涤液注入容量瓶中,
您最近一年使用:0次
2020-02-01更新
|
416次组卷
|
4卷引用:2011-2012学年陕西省长安一中高一上学期期中考试化学试卷
(已下线)2011-2012学年陕西省长安一中高一上学期期中考试化学试卷云南省楚雄市紫溪中学2018-2019学年高一上学期期中考试化学试题湖北省荆州市沙市区沙市中学2019-2020学年高一化学过关训练9《化学计量在实验中的应用》云南省昭通市昭阳区第一中学2020-2021学年高一上学期期中考试化学试题
名校
解题方法
3 . 三氧化二铟(In2O3)是一种透明的导电材料,可运用于接触屏、液晶显示器等高科技领域;铟产业被称为“信息时代的朝阳产业”。利用水铟矿[主要成分In(OH)3,常温下Ksp[In(OH)3]=l.41×10-33]制备In2O3的工艺流程如下:

(1)写出水铟矿被硫酸酸浸的离子方程式___________________ 。
(2)从硫酸铟溶液中制备硫酸铟晶体的实验步骤:____ 、_____ 、过滤、洗涤、干燥。
(3)某研究机构用硫酸提取铟时,酸度(每升溶液中含硫酸的质量)与浸出率关系如图

①当酸度为196时,硫酸物质的量浓度为___________ 。
②请选择适宜的酸度值:_______ ,并说明选择的理由______________________________ 。

(1)写出水铟矿被硫酸酸浸的离子方程式
(2)从硫酸铟溶液中制备硫酸铟晶体的实验步骤:
(3)某研究机构用硫酸提取铟时,酸度(每升溶液中含硫酸的质量)与浸出率关系如图

①当酸度为196时,硫酸物质的量浓度为
②请选择适宜的酸度值:
您最近一年使用:0次
名校
4 . 已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:
(1)该“84消毒液”的物质的量浓度约___ mol·L-1(小数点后保留一位)。
(2)某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=___ mol·L-1。
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。需要称量NaClO固体的质量为__ g。下列为打乱了的操作示意图,其正确排序为____ 。

(4)配制过程中下列各项操作对消毒液物质的量浓度有和影响(填“偏小”、“偏大”或“无影响”)
A.用托盘天平称量NaClO固体时,砝码生锈___ 。
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水____ 。
C.定容时,俯视容量瓶刻度线进行定容____ 。
| 84消毒液 【有效成分】NaClO 【规格】1000mL 【质量分数】25% 【密度】1.19g·cm-3 |
(2)某同学取100mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480mL含NaClO质量分数为25%的消毒液。需要称量NaClO固体的质量为

(4)配制过程中下列各项操作对消毒液物质的量浓度有和影响(填“偏小”、“偏大”或“无影响”)
A.用托盘天平称量NaClO固体时,砝码生锈
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
C.定容时,俯视容量瓶刻度线进行定容
您最近一年使用:0次
2019-11-15更新
|
484次组卷
|
2卷引用:陕西省西安中学2019-2020学年高一上学期期中考试化学试题
名校
5 . 为验证氧化性Cl2>Fe3+>SO2,某小组用如图所示装置进行实验(夹持仪器和A中加热装置已略,气密性已检验)。
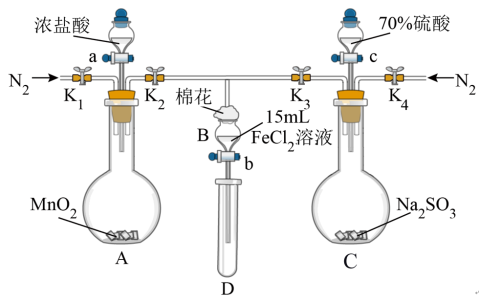
实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开K3和活塞c,加入70%的硫酸,一段时间后关闭K。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是__________________________ 。
(2)实验室在保存FeCl2溶液时为了防止FeCl2溶液变质,经常向其中加入铁粉,其原因是__________________________ 。
(3)若向第III步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的化学方程式__________________________ 。
(4)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的离子方程式为__________________________ 。
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示.他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是_____ (填“甲”、“乙”或“丙”)。
(6)将B中的FeCl2溶液换成100mLFeBr2溶液并向其中通入2.24LCl2(标准状况下),若溶液中有1/2的Br﹣被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为____ 。

实验过程:
Ⅰ.打开弹簧夹K1~K4,通入一段时间N2,再将T型导管插入B中,继续通入N2,然后关闭K1、K3、K4。
Ⅱ.打开活塞a,滴加一定量的浓盐酸,给A加热。
Ⅲ.当B中溶液变黄时,停止加热,关闭K2。
Ⅳ.打开活塞b,使约2mL的溶液流入D试管中,检验其中的离子。
Ⅴ.打开K3和活塞c,加入70%的硫酸,一段时间后关闭K。
Ⅵ.更新试管D,重复过程Ⅳ,检验B溶液中的离子。
(1)过程Ⅰ的目的是
(2)实验室在保存FeCl2溶液时为了防止FeCl2溶液变质,经常向其中加入铁粉,其原因是
(3)若向第III步B中的黄色溶液中通入H2S气体,会观察到有淡黄色沉淀生成,写出该反应的化学方程式
(4)若将制取的SO2通入硫酸酸化的高锰酸钾溶液可使溶液褪色,其反应的离子方程式为
(5)甲、乙、丙三位同学分别完成了上述实验,结论如下表所示.他们的检测结果一定能够证明氧化性Cl2>Fe3+>SO2的是
| 过程Ⅳ,B溶液中含有的离子 | 过程Ⅵ,B溶液中含有的离子 | |
| 甲 | 有Fe3+无Fe2+ | 有Fe2+ |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42﹣ |
| 丙 | 有Fe3+无Fe2+ | 有SO42﹣ |
您最近一年使用:0次
2019-02-12更新
|
571次组卷
|
2卷引用:【全国百强校】陕西省西安市长安区第一中学2018-2019学年高一上学期期末考试化学试题
名校
6 . 化学与人类社会可持续发展密切相关,能源、环境、材料以及日常生活等都离不开化学。
(1)硅是无机非金属材料的主角。请举出一种含硅元素的材料名称:__________ 。
(2)可以用浓氨水来检验氯气管道是否漏气,用此方法检查观察到的现象是___________ 。
(3)某校环保兴趣小组在处理污水样品时,需将质量分数为37%的浓盐酸(密度为1.19g·cm-3)配制成250mL0.1mol·L-1的盐酸。

①在上图所示仪器中,配制上述溶原不需要的是________ (填字母)。除图中已有仪器外,配制上述溶液还需要的玻璃仪器是_______________ 。
②若配制时其他操作均正确,烧杯没有洗涤,则所配溶液的物质的量浓度_________ (填“偏高”,“偏低”或“无影响”,下同);定容时俯视,则所配溶液的物质的量浓度_______ 。
(4)铝制品表面因有一层氧化铝薄膜而经久耐用,但该氧化膜易被酸、碱破坏。若将氧化铝与氢氧化钠的溶液作用,反应的离子方程式为______________________ 。
(5)工业上用铝土矿(含SiO2等杂质)生产铝。从Na2SiO3和NaAlO2混合溶液中制得Al(OH)3,需要从下列试剂中选择两种,最好选用的试剂组合是__________ (填字母)。
a.NaOH溶液 b.氨水 c.CO2 d.盐酸
(1)硅是无机非金属材料的主角。请举出一种含硅元素的材料名称:
(2)可以用浓氨水来检验氯气管道是否漏气,用此方法检查观察到的现象是
(3)某校环保兴趣小组在处理污水样品时,需将质量分数为37%的浓盐酸(密度为1.19g·cm-3)配制成250mL0.1mol·L-1的盐酸。

①在上图所示仪器中,配制上述溶原不需要的是
②若配制时其他操作均正确,烧杯没有洗涤,则所配溶液的物质的量浓度
(4)铝制品表面因有一层氧化铝薄膜而经久耐用,但该氧化膜易被酸、碱破坏。若将氧化铝与氢氧化钠的溶液作用,反应的离子方程式为
(5)工业上用铝土矿(含SiO2等杂质)生产铝。从Na2SiO3和NaAlO2混合溶液中制得Al(OH)3,需要从下列试剂中选择两种,最好选用的试剂组合是
a.NaOH溶液 b.氨水 c.CO2 d.盐酸
您最近一年使用:0次
2018-03-09更新
|
135次组卷
|
2卷引用:陕西省咸阳市2017-2018学年高一上学期期末考试化学试题
名校
7 . I.实验室用NaOH固体配制1.0mol/L的NaOH溶液450mL,回答下列问题:
(1)实验步骤:
①计算所需称量的NaOH的质量为________ g。
②用托盘天平称量NaOH固体。称量时应该将NaOH放于_____ 中且放置在天平左盘称量。
③将称得的固体放于烧杯中,并加水溶解。
④检查容量瓶是否漏水,用玻璃棒引流将溶解液立即转移进_______ mL容量瓶中。
⑤用少量水洗涤______________ 2-3次;并将洗涤液转移进容量瓶。
⑥定容操作为_________________ 。
⑦翻转摇匀后转入试剂瓶中储存。
Ⅱ.若配制1mol/L的稀硫酸溶液500 mL
(1)则需要质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为_______ mL(计算结果保留一位小数)。如果实验室有10mL、25mL、50mL量筒,就选用______ mL规格的量筒最好。
(2)下面操作造成所配稀硫酸浓度偏高的是______ (填序号)
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
(1)实验步骤:
①计算所需称量的NaOH的质量为
②用托盘天平称量NaOH固体。称量时应该将NaOH放于
③将称得的固体放于烧杯中,并加水溶解。
④检查容量瓶是否漏水,用玻璃棒引流将溶解液立即转移进
⑤用少量水洗涤
⑥定容操作为
⑦翻转摇匀后转入试剂瓶中储存。
Ⅱ.若配制1mol/L的稀硫酸溶液500 mL
(1)则需要质量分数为98%、密度为1.84 g/cm3的浓硫酸的体积为
(2)下面操作造成所配稀硫酸浓度偏高的是
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线
您最近一年使用:0次
2017-11-14更新
|
386次组卷
|
5卷引用:陕西省西安市第三十八中学2023-2024学年高一上学期第二次月考化学试卷
8 . 下图为实验室某浓硫酸试剂瓶的标签,试根据标签上的有关数据回答下列问题:
(1)该浓硫酸中H2SO4的物质的量浓度为_________ 。
(2)某学生欲用上述浓硫酸和蒸馏水配制100mL物质的量浓度为0.8 mol·L-1的稀硫酸,该学生需要量取_________ mL上述浓硫酸进行配制。
(3)为配制(2)中的稀硫酸,除了量筒、烧杯、胶头滴管外,还缺少的玻璃仪器是_________ 。
(4)在配制过程中,下列实验操作可能导致配制的硫酸溶液浓度偏高的是_________ (填序号)。
a.定容时俯视观察
b.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.容量瓶未干燥即用来配制溶液
e.往容量瓶转移时,有少量液体溅出;
f.未洗涤稀释浓硫酸的烧杯;
| 硫酸 分子式:H2SO4 相对分子质量:98 密度:1.84g/mL H2SO4的质量分数:98% |
(1)该浓硫酸中H2SO4的物质的量浓度为
(2)某学生欲用上述浓硫酸和蒸馏水配制100mL物质的量浓度为0.8 mol·L-1的稀硫酸,该学生需要量取
(3)为配制(2)中的稀硫酸,除了量筒、烧杯、胶头滴管外,还缺少的玻璃仪器是
(4)在配制过程中,下列实验操作可能导致配制的硫酸溶液浓度偏高的是
a.定容时俯视观察
b.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.容量瓶未干燥即用来配制溶液
e.往容量瓶转移时,有少量液体溅出;
f.未洗涤稀释浓硫酸的烧杯;
您最近一年使用:0次
名校
解题方法
9 . 在一定温度下,某饱和氢氧化钠溶液体积为V mL,溶液密度为d g·cm-3,质量分数为w,物质的量浓度为c mol·L-1,溶液中含氢氧化钠的质量为m g,该温度下NaOH的溶解度为S。请回答下列问题:
(1)用w来表示该温度下氢氧化钠的溶解度(S)为_______ 。
(2)用m、V表示溶液中溶质的物质的量浓度(c)为_______ 。
(3)用w、d表示溶液中溶质的物质的量浓度(c)为_______ 。
(4)用c、d表示溶液中溶质的质量分数(w)为_______ 。
(5)用S、d表示溶液中溶质的物质的量浓度(c)为_______ 。
已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(6)该“84消毒液”的物质的量浓度约为_______ mol·L-1。(保留小数点后一位)
(7)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=_______ mol·L-1。
(8)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下列说法正确的是_______(填字母)。
(9)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制2 L 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为_______ mol·L-1。
②需用浓硫酸的体积为_______ mL。
(1)用w来表示该温度下氢氧化钠的溶解度(S)为
(2)用m、V表示溶液中溶质的物质的量浓度(c)为
(3)用w、d表示溶液中溶质的物质的量浓度(c)为
(4)用c、d表示溶液中溶质的质量分数(w)为
(5)用S、d表示溶液中溶质的物质的量浓度(c)为
已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(6)该“84消毒液”的物质的量浓度约为
(7)某同学取100 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=
(8)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。下列说法正确的是_______(填字母)。
| A.容量瓶用蒸馏水洗净后,应烘干后才能用于溶液配制 |
| B.配制过程中,未用蒸馏水洗涤烧杯和玻璃棒可能导致结果偏低 |
| C.需要称量NaClO固体的质量为143.0 g |
①所配制的稀硫酸中,H+的物质的量浓度为
②需用浓硫酸的体积为
您最近一年使用:0次
名校
解题方法
10 . 用Na2CO3·10H2O晶体,配制0.2mol/L的Na2CO3溶液480mL
(1)应称取Na2CO3·10H2O晶体的质量为__________ 。
(2)根据下列操作对所配溶液的浓度产生的影响,完成下列要求:
①Na2CO3·10H2O晶体失去了部分结晶水;
②用“左物右码”的称量方法称量晶体(使用游码);
③碳酸钠晶体不纯,其中混有氯化钠;
④称量碳酸钠晶体时所用砝码生锈;
⑤容量瓶未经干燥使用;
其中引起所配溶液浓度偏高的有________ (填序号,下同),偏低的有_________ ,无影响的有__________ 。
(3)下列操作中,容量瓶所不具备的功能有__________________。
(4)为完成实验所需要的玻璃仪器有:_____________________ 。
(1)应称取Na2CO3·10H2O晶体的质量为
(2)根据下列操作对所配溶液的浓度产生的影响,完成下列要求:
①Na2CO3·10H2O晶体失去了部分结晶水;
②用“左物右码”的称量方法称量晶体(使用游码);
③碳酸钠晶体不纯,其中混有氯化钠;
④称量碳酸钠晶体时所用砝码生锈;
⑤容量瓶未经干燥使用;
其中引起所配溶液浓度偏高的有
(3)下列操作中,容量瓶所不具备的功能有__________________。
| A.配制一定体积准确浓度的标准溶液 |
| B.贮存溶液 |
| C.测量容量瓶规格以下的任意体积的液体 |
| D.准确稀释某一浓度的溶液 |
| E.用来加热溶解固体溶质 |
(4)为完成实验所需要的玻璃仪器有:
您最近一年使用:0次
2017-02-17更新
|
177次组卷
|
2卷引用:2016-2017学年陕西省宝鸡中学高一上期中化学卷



